基于慢吐气方法选择急性呼吸窘迫综合征模型呼气末正压的可行性
王玉妹 王 岩 周益民 徐珊珊 杨燕琳 张琳琳 周建新
(首都医科大学附属北京天坛医院重症医学科,北京 100070)
急性呼吸窘迫综合征(acute respiratory distress syndrome,ARDS)是重症医学科常见的急性呼吸衰竭,以肺容积减少、肺顺应性下降及大量肺泡塌陷为主要的病理生理学特征[1]。肺保护性通气策略是治疗ARDS患者的一项重要措施,尤其是呼气末正压(positive end-expiratory pressure,PEEP)的选择是目前的难点和热点[2]。选择PEEP的方法有很多,如最大顺应性法[3]、氧合表法[4]、分层电阻抗成像(electrical impedance tomography,EIT)技术[5-6]等。如何选择一个较合适的PEEP水平还存在很大的争议[2]。考虑呼吸力学特征的同时,还需要考虑血流动力学等,使得选择PEEP更加困难[7]。简单的识别呼吸力学特征,再联合血流动力学可能是更有效的方法。因此,本研究模拟了ARDS模型,应用慢吐气(prolonged expiration)[8]的方法进行PEEP滴定,根据呼吸机常规监测的呼出潮气量(expired tidal volume,VTe)数据计算肺复张容积,更简单的选择合适的PEEP区间,并通过EIT技术进行验证,探讨应用慢吐气及呼吸机监测选择PEEP的可行性。
1 材料与方法
1.1 实验动物及实验前准备
健康雄性巴马猪6只,体质量(38~42)kg,由北京实创世纪小型猪养殖基地提供,实验动物使用许可证号:SYXK(京)2019-0031。本研究已经通过了北京市神经外科研究所动物福利伦理委员会的伦理审批(伦理审批号:201703001)。
使用氯氨酮和陆眠宁肌肉麻醉,麻醉成功后进行气管插管,呼吸机辅助呼吸,设定容量控制通气模式(volume control ventilation,VCV),潮气量(tidal volume,VT)为6 mL/kg,呼吸频率(respiratory rate,RR)为15~25次/分,维持二氧化碳分压(arterial partial pressure of carbon dioxide,PaCO2)在35~45 mmHg(1 mmHg=0.133 kPa),吸呼比(inspiratory/expiratory ratio,I ∶E)为1∶2,吸氧浓度(inspired oxygen fraction,FiO2)为50%,PEEP初始设置为5 cmH2O(1 cmH2O=0.098 kPa)。
实验前准备包括连接心电监护监测心率(heart rate,HR)、末梢氧饱和度(pulse oxygen saturation, SpO2)等;股动脉置管连续监测平均动脉压(mean arterial pressure,MAP);股静脉置管开放静脉通路;绑上EIT绑带,连接EIT设备,连续监测EIT数据并进行离线分析。整个实验过程中持续静脉泵入丙泊酚镇静、 芬太尼镇痛、罗库溴铵肌松保证完全消除自主呼吸。
在整个实验过程中以6 mL·kg-1·h-1的速度静脉输注0.9%(质量分数)氯化钠注射液(以下简称生理盐水)。如果出现低血压情况,先进行补液,若低血压仍持续存在,可通过静脉注射去甲肾上腺素(10 μg推注或以0.05~0.5 μg·kg-1·min-1持续输注)进行治疗,MAP维持在65 mmHg以上。
1.2 模型制备
应用盐酸气管滴入法建立ARDS模型:将0.1 mol/L盐酸按照4 mL/kg由气管内缓慢滴入,30 min内完成[9]。将PEEP设置为5 cmH2O,每10 min进行一次血气分析,当氧合指数(arterial partial pressure of carbon dioxide/inspired oxygen fraction, PaO2/FiO2)低于200 mmHg,并稳定维持30 min时,即模型建立成功[10]。
1.3 实验流程
模型建立成功之后,进行一次肺复张,肺复张后采用慢吐气的方法进行递减的PEEP滴定过程,PEEP从20 cmH2O逐渐递减至0 cmH2O,间隔为5 cmH2O,具体流程见图1。每个PEEP水平维持20 min,并进行3~5 s 的吸气末阻断和呼气末阻断获得呼吸力学参数。
图1 实验流程图Fig.1 Experimental flowchart△1 cmH2O=0.098 kPa; Paw: airway pressure; PEEP: positive end-expiratory pressure.
1.4 数据收集
每个PEEP水平通气结束后,分别记录以下数据再降低PEEP:
1)采集动脉血进行血气分析,记录氧分压(arterial partial pressure of oxygen,PaO2)和PaCO2。
2)记录血流动力学指标,如HR、MAP等。
3)通过呼吸机监测,记录降低PEEP前后一口气的VTe、平台压(plateau pressure,Pplat)、呼吸系统顺应性(compliance of respiratory system,Crs)、驱动压(driving pressure)等,计算每二个PEEP水平之间的复张容积(recruitment volume,Vrec):
复张容积=(低PEEP的VTe-高PEEP的VTe)-
最小预测复张容积=(低PEEP的VTe-
高PEEP的VTe)-低PEEP的Crs*ΔPEEP
4)实验过程中连续进行EIT监测,离线分析数据,将肺从腹侧到背侧均分为二个区域:非重力依赖区和重力依赖区,计算每个分区的VT和Crs[11],同时计算过度膨胀/萎陷(overdistention/collapse)的比例[12]及均一指数(the global inhomogeneity index,GI指数)[13]。
1.5 统计学方法
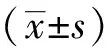
2 结果
2.1 模型的建立
所有的实验动物在造模后均达到了ARDS的标准,造模前的氧合指数为(412.6±65.6) mmHg,造模后氧合指数为(141.2±10.1) mmHg(t=10.016,P=0.000)。造模成功后Crs较基础值明显下降[造模前(74.5±13.0) mL/cmH2O,造模后(32.1±12.3) mL/cmH2O,t= 5.803,P=0.000],符合ARDS模型的生理学特点。在PEEP滴定过程中,在PEEP为15、20 cmH2O 的通气过程中时,实验动物均应用了一定剂量的去甲肾上腺素维持MAP在65 mmHg以上。
2.2 不同方法选择的较合适PEEP区间的比较
基于慢吐气方法计算的每两个PEEP水平间的Vrec与PEEP的关系如图2A, PEEP由10 cmH2O降至5 cmH2O时的Vrec最大,即较合适的PEEP区间在5~10 cmH2O。
由EIT计算的每个PEEP水平的过度膨胀/萎陷比例如图2B,在PEEP递减过程中,过度膨胀的比例越来越小,萎陷的比例越来越大,二者之和最小值在PEEP为5和10 cmH2O之间,即较合适的PEEP水平在5和10 cmH2O之间。
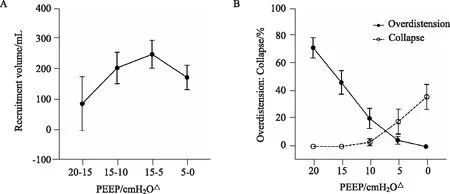
图2 不同方法选择的较合适PEEP的比较Fig.2 The comparison of optimal positive end-expiratory pressure (PEEP) selection by different methodsA: the change of recruitment volume with PEEP level using prolonged expiration; B: the percentage of overdistension and collapse at different PEEP level calculated by electrical impedance tomography (EIT). △1 cmH2O=0.098 kPa; PEEP: positive end-expiratory pressure.
2.3 不同PEEP水平之间其他参数的比较
在PEEP滴定过程中,不同PEEP水平之间血流动力学、呼吸力学及EIT参数之间的比较如图3。随着PEEP水平的降低,氧合指数逐渐降低,在PEEP 10、15和20 cmH2O三个水平时氧合指数大于300 mmHg。MAP和PaCO2在滴定过程中无明显变化,但在PEEP为15和20 cmH2O时,应用了血管活性药物维持血压。心率在实验中稍有波动,在PEEP为5 cmH2O时心率最低。整体的Crs在PEEP为10 cmH2O 时最高,此时驱动压也是最低的;非重力依赖区Crs在10 cmH2O时最高,而重力依赖区Crs在15 cmH2O时最高,有一定的差异。随着PEEP水平的降低,重力依赖区的VT越来越多,而非重力依赖区越来越少。GI指数在PEEP为10 cmH2O时最低,此时通气最均一。
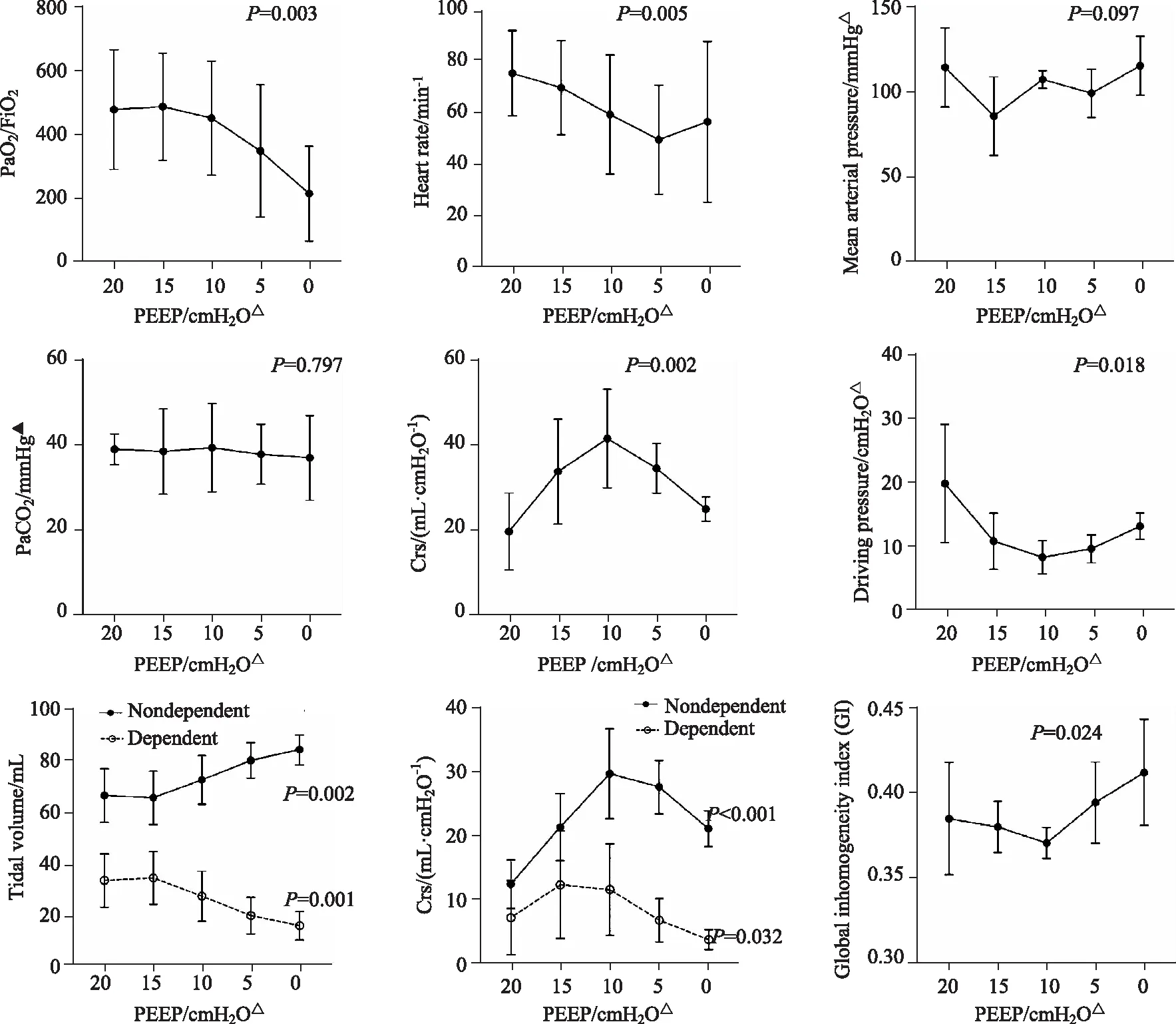
图3 不同PEEP水平之间各参数的比较Fig.3 Comparison of other parameters in different positive end-expiratory pressure (PEEP) levels PEEP: positive end-expiratory pressure; PaO2/FiO2: arterial partial pressure of oxygen/inspired oxygen fraction; PaCO2: arterial partial pressure of carbon dioxide; Crs: compliance of respiratory system; △1 cmH2O=0.098 kPa; ▲1 mmHg=0.133 kPa.
3 讨论
ARDS是重症医学科内比较常见的一种急性呼吸衰竭,机械通气是治疗ARDS的一项重要手段,其设置仍然是研究的重点,尤其是如何选择PEEP是重点和难点[14-15]。“最佳”的PEEP水平其实并不存在,临床医生需要一个比较合适的PEEP水平,该PEEP能够提供较好的顺应性、较高的氧合指数、比较低的无效腔量、更多的复张肺泡避免过度膨胀等[2],通过呼吸力学情况,可以选择一个比较合理的PEEP区间,然后根据血流动力学及其他指标进一步选择出更合适的PEEP水平。选择PEEP的方法有很多,大部分需要特殊的操作或复杂的工具,因此本研究提出通过慢吐气的方法结合呼吸机常规监测简单的选择一个PEEP区间,再通过血流动力学及其他指标选择合适的PEEP。
慢吐气是通过单次呼吸简化PEEP递减的过程,简单计算高PEEP降至低PEEP的去复张容积或Vrec[8]。在PEEP递减的同时,通过延长呼气时间,一般为6~9 s,利用高PEEP降至低PEEP的单口气计算Vrec。由于吸气的VT不变,呼气时间足够长,降低PEEP后单口气立即显示的呼出VT与改变PEEP前的呼出VT之间的差值就是PEEP水平改变导致的总肺容积的变化,即PEEP产生的容积变化。再计算出最小预测复张容积(minimal predicted volume,MPV)就能够计算出Vrec,当PEEP产生的容积变化大于MPV时,表示此次肺出现了复张[8];反之小于MPV时,过度膨胀占主导地位。因此,通过慢吐气的方法,结合呼吸机监测的呼出VT能够简单计算降低PEEP时的Vrec,Vrec最大的PEEP区间就认为是较合适的PEEP区间[16],再结合血流动力学及其他指标选择合理的PEEP水平。
比较合适的PEEP水平是在此PEEP水平下,最大程度的打开萎陷的肺泡,并且使得过度膨胀的肺泡最小化。计算萎陷和过度膨胀肺泡的方法,金标准是电子计算机断层扫描(computed tomography,CT),但是由于CT的复杂性、射线、转运风险等,目前CT很少用于临床评估复张和过度膨胀。本研究采用EIT的方法计算过度膨胀及萎陷肺泡的比例,从而评估该PEEP水平区间。EIT是一种无创、能够连续监测、床旁、直观的监测肺容积的方法[17],与CT具有很好的相关性,是目前比较常用的一种影像手段。EIT能够将肺通气的区域分成许多不同的像素点,通过计算每个像素点顺应性的变化,计算出过度膨胀和萎陷的肺泡比例[12]。这种方法也被用来选择合适的PEEP水平[5],选择过度膨胀和萎陷的比例之和最小时的PEEP水平即为较合适的PEEP水平。本研究通过EIT计算出过度膨胀及萎陷的肺泡比例,验证慢吐气方法选择的合适PEEP区间。慢吐气方法得到的较合适的PEEP区间是5~10 cmH2O,而EIT计算的过度膨胀和萎陷比例之和最小的位置也在5~10 cmH2O,二者是一致的。
通过慢吐气方法简单判断出合适的PEEP区间后,本研究也结合血流动力学及EIT提供的分区情况进行了一定程度上的验证。在PEEP为5和10 cmH2O时,氧合指数均在200 mmHg以上。虽然15和20 cmH2O 时氧合指数更高,但是此时MAP降低,并应用了血管活性药物,且驱动压比较高可能容易产生呼吸机相关性肺损伤,重力依赖区的潮气量很小,通气的均一性较差,此时的PEEP并不合适。PEEP低于5 cmH2O时,生理情况下肺即有3~5 cmH2O的PEEP,低于此水平是违背生理学的;此外,低于5 cmH2O 时,氧合指数也不算高,重力依赖区的萎陷程度非常严重,VT过小,通气均一性也较差。因此在5~10 cmH2O区间的PEEP水平是较合适的,这与慢吐气方法选择的PEEP区间是一致的。
本研究有一定的局限性,一是PEEP滴定过程中,PEEP水平的间隔为5 cmH2O较大,可以应用更小的间隔,如2 cmH2O,能够更缩短此区间的范围,更能准确地选择合适的PEEP水平。再者,本研究为动物研究,仍需要大型临床实验和数据进行支持和验证。
综上所述,应用慢吐气方法联合呼吸机常规监测选择合适的PEEP区间是简便易行的,具有可行性。选择出此PEEP区间后,再结合血流动力学及其他指标进一步选择更合适的PEEP水平也是至关重要的。

