介入联合仑伐替尼桥接治疗超米兰标准肝癌肝移植2例报道
鲁旭,李华,易述红,赵辉,朱曙光,李海波,杨扬,汪国营,2*
根据中国肝移植注册中心数据,近5年来,中国大陆肝癌肝移植例数占全球肝移植总例数的36.8%。米兰标准[1]是世界范围内最通用的移植标准即单发肿瘤直径≤5 cm,或肿瘤数目≤3个且每个肿瘤直径≤3 cm,无大血管侵犯或肝外转移。这些患者的5年生存率为75%。中国作为肝癌大国,病人在确诊时较多已处于中晚期阶段甚至伴有大血管的侵犯,单纯手术切除或者单一靶向、免疫治疗效果有限,肝移植是其为数不多的选择,这就要求我们进一步扩大肝移植的手术适应症,但随着肝癌肝移植指征的扩大[2-4],术后肿瘤复发率的增加不可避免[5],肝癌复发后受者中位生存期仅10.6~12.2个月[6,7],因此预防肿瘤复发、探索可行的术前降期或预防术后复发转移的可行方案尤为重要。
为了探究有效的桥接或者降期方案,我中心通过查阅国际文献,并未发现某种治疗是肝移植术前降期桥接的最佳方案[8],本中心曾提出针对肝癌的不同临床分期,需要选择不同的降期治疗方法,总的要求是能够减慢肿瘤生长速度,减低肿瘤扩散,使肿瘤直径减小,数目减少甚至消灭肿瘤从而减少术后肿瘤复发的概率、改善术后存活率。常用的治疗方法包括局部消融治疗、经皮穿刺肝动脉化疗栓塞(TACE)、选择性内放射治疗(selection internal radiation therapy,SIRT)等[9],以色列阿尔伯特·爱因斯坦医院的一项单中心、前瞻性、队列研究也表明超米兰标准的肿瘤患者在接受D⁃TACE降期治疗后,可以实现移植后5年生存与符合米兰标准的肝癌患者一样[10],由此说明术前的降期治疗是十分必要的。由于全球供肝的缺乏,活体供肝走入了我们的视野,但是活体肝移植相对于死者供体肝移植相比有更高的复发概率,并且其主要原因在于更少的局部治疗[11],因此活体供肝更要增加局部的治疗[12]。考虑到活体肝移植中局部治疗的使用效果较为可观,本中心建议超越米兰标准的肝癌患者采用仑伐替尼联合介入治疗进行降期桥接治疗,待肿瘤降期达到相关移植标准或部分缓解或疾病稳定后接受肝移植,评估仑伐替尼联合介入治疗实现肝癌降期和降低移植术后复发转移的疗效和安全性。本文报道了本中心2例病例,共同探讨移植术前介入联合仑伐替尼桥接治疗超米兰标准肝癌肝移植的安全性、有效性与预后。
1 临床资料
患者1,男,32岁,2020年1月2日因“间歇性右上腹痛1周”入院,入院后完善相关检查,我院CT提示:S4/8段肝癌,肝中静脉、门静脉S4分支不除外受侵,肝S6可疑子灶2枚(如下图1所示)。虑到患者多个病灶,可疑血管受侵,科室讨论后予仑伐替尼+介入治疗。2020年1月10日行介入治疗,术后复查肝功能未见明显波动,术后复查CT(如下图2),后于2020年2月19日行第二次介入治疗,期间病情稳定,肝功能无明显波动。后患者于2020年3月6日行同种异体原位肝移植术,术后病理回报:肿瘤下绝大部分坏死,仅周围见少许异形细胞团。(如下图3所示),患者规律随访,至2021年7月10日未见肿瘤复发,患者仍处于持续随访中。
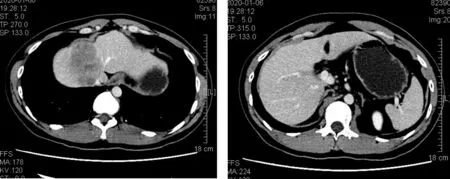
图1
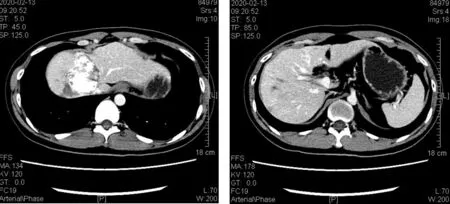
图2

图3
患者2,男,56岁,2020年4月1日因“右上腹痛伴乏力3月余”入院,入院后完善相关检查,AFP为56.6μg/L,我院CT提示:肝S5段、S8段肿物,考虑原发性肝癌可能性大,门静脉右前支及其远端分支癌栓形成,肝右静脉部分分支受侵犯(如下图4所示),考虑到患者多发肿瘤并血管侵犯,科室讨论后予仑伐替尼+介入治疗。2020年4月8日行介入治疗,术后复查肝功能未见明显波动。后患者病情稳定,于2020年5月3日行同种异体原位肝移植术,术后病理回报:镜下见绝大部分组织已坏死,仅见少量肿瘤细胞呈条索样、腺样排列(如下图5所示)。患者规律随访,至2021年7月10日未见肿瘤复发,患者仍处于持续随访中。
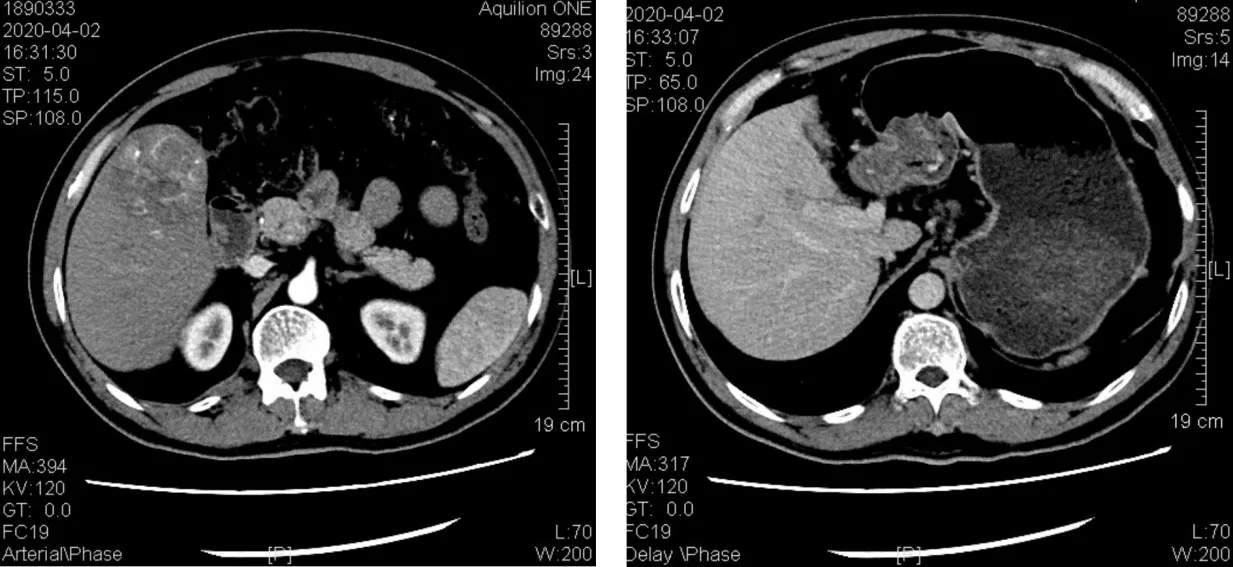
图4
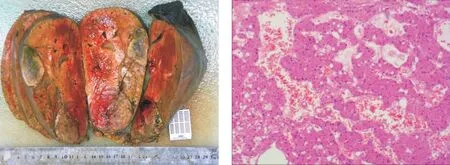
图5
2 讨论
肝移植是终末期肝癌有效的治疗手段,我国越来越多中晚期肝癌病人的出现使既往的米兰标准已无法满足临床的诊疗需要,急需一种新的治疗作为肝移植术前降期或者桥接的选择,使有大血管侵犯的晚期病人也可以实现肝移植治疗,同时保证病人的预后,预防肿瘤的复发,延长病人的无瘤生存期。
随着靶向药物的兴起,索拉菲尼进入我们的视野,但由于索拉菲尼的不良反应如手足皮肤反应、皮疹、高血压、腹泻以及脱发等[13],患者的耐受性较差,无法达到较好的依从性。仑伐替尼(Len⁃vatinib)是口服的多酶抑制剂,可抑制血管内皮生长因子受体VEGFR1、VEGFR2、VEGFR3,成纤维细胞生长因子受体FGFR1,2,3,4;血小板衍化生长因子受体α(PDGFRα),KIT及RET[14]。2015年由FDA批准用于治疗局部复发或转移、进展性、放射性碘难治性甲状腺癌。2016年5月获得批准与依维莫司联合治疗晚期的肾细胞癌[15]。继FDA于2018年批准用于无法切除的肝细胞肝癌的一线治疗后,国家药品监督管理局于同年9月批准仑伐替尼在国内上市,仑伐替尼至此进入我们的视野,在一项多中心Ⅲ期非劣效临床试验(REFLECT试验)中,仑伐替尼组患者的总体生存期稍优于索拉菲尼组(中位总生存期:仑伐替尼13.6月vs.索拉菲尼12.3月),但仑伐替尼比索拉菲尼表现出更长的疾病进展时间(8.9月vs.3.7月)、更长的无进展生存期(7.4月vs.3.7月)及更高的疾病控制率(24.1%vs.9.2%)[16]。仑伐替尼的主要不良反应为高血压(42%),腹泻(39%),食欲下降(34%)与体重下降(31%),3~4级的不良反应在仑伐替尼中更常见(57%vs.49%),其中高血压是最常见的3~4级不良反应,比例为23%。虽然也有报道显示仑伐替尼会导致呼吸系统和泌尿系统以及内分泌系统的不良反应,但是发生率较低,而且经过对应的治疗大部分可以缓解[17]。因此仑伐替尼是目前唯一一个在进展期肝癌中不亚于索拉菲尼的靶向药物、且在控制疾病进展中比索拉菲尼有一定的优势,因此EASL指南推荐仑伐替尼作为除索拉菲尼以外的进展期肝癌患者的一线治疗方式[18]。
TACE是肝癌综合治疗的常见手段,2005年AASLD指南推荐常规TACE(cTACE)作为不可切除肝癌/多灶肝癌的一线非根治性治疗手段[19];BRIDGE研究调查表明,cTACE已经成为我国、北美、欧洲和韩国在各期肝癌患者中最常用的治疗方案,约占29%~51%;而且,多项研究表明进展期肝癌患者同样能从cTACE中获益,cTACE可作为索拉菲尼外的可选治疗方式。虽然cTACE是治疗不可切除肝癌的有效措施,但也有一定的毒性和死亡率。约60%~80%的患者会出现栓塞后综合征,包括疼痛、恶心、发热等症状,但为自限性、持续约3~4天。大部分的病人在经过对症治疗后可好转,肝功能并无明显波动,在控住肿瘤的同时,最大限度的维持了患者肝功能的平稳。有文献表明,TACE和仑伐替尼联合治疗不能切除的肝癌,与TACE单一治疗相比,可显著改善临床结果,且安全性可控[20]。
综合上述研究进展,我中心提出了在移植术前介入联合仑伐替尼桥接治疗超米兰标准肝癌的临床研究方案,期待介入联合仑伐替尼可以实现肝移植患者术前的平稳过渡或更进一步实现降期,降低术后复发的风险,延长患者的无瘤生存,根据上诉2例病例报道分析,通过介入与靶向的联合治疗后,术后病理提示肿瘤处于大部分坏死状态,患者的短期预后较好,但鉴于2例患者分别随访16月与14月,随访时间较短,故而患者的长期预后仍需持续关注。同时应增加入组病例,通过统计学方法进一步验证临床获益,探究进一步的疗效评估。

