La2-xBixCuO4阴极材料的合成与电化学性质
庞姝彤 赵 辉
(黑龙江大学化学化工与材料学院,哈尔滨 150080)
类钙钛矿结构A2BO4型氧化物是一类同时具有电子导电和离子导电的混合导体材料,在氧透过性、热化学性能、电化学性能以及氧的扩散和表面交换能力等方面显示了明显的优势[1]。该材料具有层状结构,由单钙钛矿型的ABO3和岩盐型AO层交替堆积构成。其中A位通常由半径较大的碱土金属或稀土金属占据,配位数为9;B位被较小过渡金属离子占据,配位数为6[2-4]。与钙钛矿型材料相比,A2BO4型氧化物的AO岩盐层中非化学计量比的氧以间隙氧形式存在,因此具有较高的氧离子传导能力,对改善阴极材料的特性有很大贡献[5-6]。例如La2NiO4+δ通常是氧过量的,该材料具有较大的δ值,沿着ab平面表现出优异的氧传输性能[7-8]。通过A位掺杂Sr、Ba、Nd和Pr等元素,以及将B位的Ni用Co、Fe、Cu取代的方法,可以进一步改善La2NiO4+δ的电化学性能[9-12]。已有的研究表明对于B位元素为Mn、Fe、Co和Ni的A2BO4氧化物,材料体系存在大量的非化学计量氧(δ),即使A位掺杂Sr,这些氧化物也是氧过量的[13-17]。而当Cu作为B位元素时,δ相对较小。La2CuO4+δ的δ=0.01,因而一般而言这种材料的氧传输性能较差。通过在La位置掺入碱土金属(Ca、Sr、Ba),可以调节体系的氧含量以及过渡金属的平均氧化态[18-20]。Adnene等[21]研究了La2CuO4中Ca掺杂的影响,发现当 x≤0.165 时 La2-xCaxCuO4-δ氧化物的电导率以及氧空位浓度均随着钙掺杂而增大。在各种类型的掺杂元素中,Bi元素较少受到关注[22-25]。Bi3+可以2种方式影响材料的电化学性质:一是Bi掺杂促进氧空位形成,二是Bi3+具有6s孤对电子,是一种高度可极化的离子,能够提高氧空位迁移率。已有的研究表明,在钙钛矿结构的LaFeO3中,用Bi代替La能够明显改善材料的电化学性质[23-24]。最近 Zhu 等[25]报道了 Bi掺杂 La1.75Sr0.25NiO4+δ的电化学性能。他们发现Bi3+的6s孤对电子提高了氧的传输性能,这一点在Bi掺杂的La2Cu0.5Mn1.5O6中也有体现[26]。鉴于碱土离子掺杂的La2CuO4氧化物展现出良好的阴极性能,且铋掺杂La2CuO4材料的高温电化学性能研究还未见报道,我们采用甘氨酸-硝酸盐法制备La2-xBixCuO4,研究Bi的掺杂对于La2CuO4电化学性能的影响。
1 实验部分
1.1 阴极材料的合成
采用甘氨酸-硝酸盐法合成La2-xBixCuO4(x=0、0.05、0.10)材料。按照化学计量比准确移取硝酸镧、硝酸铋和硝酸铜的水溶液。再按甘氨酸与金属离子的化学计量比2∶1加入甘氨酸,快速加热搅拌混合液,直至剧烈燃烧产生粉末状的氧化物,将所得粉末氧化物进行研磨,在900℃烧结5 h,冷却至室温得到目标化合物,分别命名为LC、LBC0.05、LBC0.10。将合成的材料粉末在220 MPa下加压成型,再于950℃烧结12 h,得到致密陶瓷片。将陶瓷片切成长条形,用砂纸打磨平整四面、抛光,用于电导率测试和热膨胀测试。
1.2 电池的制备
将Sm0.2Ce0.8O1.9(SDC)粉末在220 MPa加压成型,1 200℃烧结12 h,1 400℃烧结24 h,得到SDC电解质圆片待测。
取适量LC、LBC0.05、LBC0.10粉末,分别加入含质量分数3%的乙基纤维素的松油醇,充分研磨制成阴极浆料。将所得浆料均匀对称涂在SDC电解质片两侧,在不同温度(800~950℃)下烧结2 h,制得两电极对称半电池,电极面积为0.5 cm×0.5 cm。电解质支撑单电池的制备过程如下:称取一定质量阳极粉末(质量比6∶4的NiO、SDC与质量分数5%的淀粉混合研磨均匀而成),加入适量含质量分数3%乙基纤维素的松油醇研磨得阳极浆料,将其均匀地涂在SDC电解质片的一侧,于1 350℃烧结4 h。再将阴极浆料均匀地涂在电解质片另一侧,于1 000℃烧结2 h,得到电解质支撑型单电池,阴极面积为0.6 cm×0.6 cm。
1.3 材料的测试与表征
粉体材料的物相采用Brunker D8-Advance型X射线粉末衍射仪(XRD)进行表征分析,射线管电压为40 kV,工作电流为40 mA,射线源为Cu靶Kα射线(λ=0.154 18 nm),测试角度范围2θ=10°~80°,扫描步长为0.02°,扫描速度为10(°)·min-1。
材料的电导率采用直流四探针法在空气气氛下进行测试,仪器为吉时利2700数字多用表(Keithley Model 2700),温度范围100~800 ℃。材料的热膨胀曲线采用SETARAM公司的SETSYS Evolution 16/18型多功能热分析仪进行测试,空气气氛,温度范围50~800℃,升温速率10℃·min-1。材料的氧程序升温脱附(O2-TPD)采用TPD/TPR多功能动态吸附仪(天津先权TP5076)进行测量,测量温度50~800℃,升温速率10℃·min-1,氦气流速20 mL·min-1。测试之前,样品在流动氧气(20 mL·min-1)中300℃预处理2 h。
电极的电化学性能使用AUTOLAB PGStat30电化学工作站进行研究,交流阻抗频率为10-2~106Hz,温度范围500~700℃,气氛为空气与氮气混合气。电解质支撑单电池的输出性能采用自制装置进行测试。加湿的氢气(含体积分数3%的H2O)为燃料气,空气中的氧为氧化剂,测试温度范围500~700℃。
2 结果与讨论
2.1 La2-xBixCuO4阴极材料的物相分析
图1a为La2-xBixCuO4材料在900℃烧结5 h后的XRD图。与标准XRD数据库对比可知,当x=0、0.05、0.10时,所有衍射峰均归属于类钙钛矿相La2CuO4,没有其他杂相生成,而当x=0.15时,在28°位置有不属于La2CuO4的杂相生成,经标准卡片对比可知其为Bi2O3。图1b为LBC0.10材料的Rietved精修图,表1为精修得到的晶胞参数数据。由图、表可知由于Bi的掺入,其空间群由正交晶系Fmmm变为四方晶系I4/mmm,且随着Bi掺杂量的增大,掺杂样品的晶胞体积逐渐增大。在K2NiF4型A2BO4结构中,A位原子为9配位,B位原子为6配位,Bi3+和La3+离子的有效半径分别为0.117和0.116 nm[27],由于Bi3+半径 略大于La3+,且Bi3+与Cu2+半径相差较大,因而Bi3+仅仅占据A位,导致晶胞体积增大。为了考察材料与电解质的高温化学相容性,将LBC0.10粉末与几种固体氧化物燃料电池(SOFC)的典型电解质材料按照质量比1∶1混合研磨均匀,在950℃空气气氛下烧结24 h。图1c为LBC0.10+SDC和LBC0.10+La0.9Sr0.1Ga0.8Mg0.2O2.85(LSGM)粉体的XRD图。由图可见,各个衍射峰分别归属为LBC0.10、SDC和LSGM的特征峰,没有杂相生成;图1d为LBC0.10+Ce0.9Gd0.1O1.95(CGO)以及 LBC0.10+Zr0.84Y0.16O1.92(YSZ)混合粉体的XRD图。与CGO、YSZ粉体的XRD图对比可知,混合粉体中CGO的衍射峰向低角度移动,这是因为La3+离子半径大于Ce4+,当LBC0.10中的La掺入到CGO中,导致CGO的晶胞体积增大,另外,图中出现了不属于LBC0.10和CGO的杂峰,可能是La3+从LBC0.10中扩散到CGO产生新的萤石型化合物(Ce,Gd,La)O2-δ,该化合物是一种电导率略低于CGO的氧化物离子导体,对阴极性能有影响;对于LBC0.1+YSZ体系,也出现了不属于LBC0.10和YSZ的杂峰,归属为La2Zr2O7烧绿石型化合物[28]。大量研究证实该物相阻挡氧离子的传输,因而会严重影响阴极性能;以上结果表明在950℃以内LBC0.10材料与电解质SDC和LSGM具有良好高温化学相容性。本工作中采用SDC作为电解质,进行后续研究。
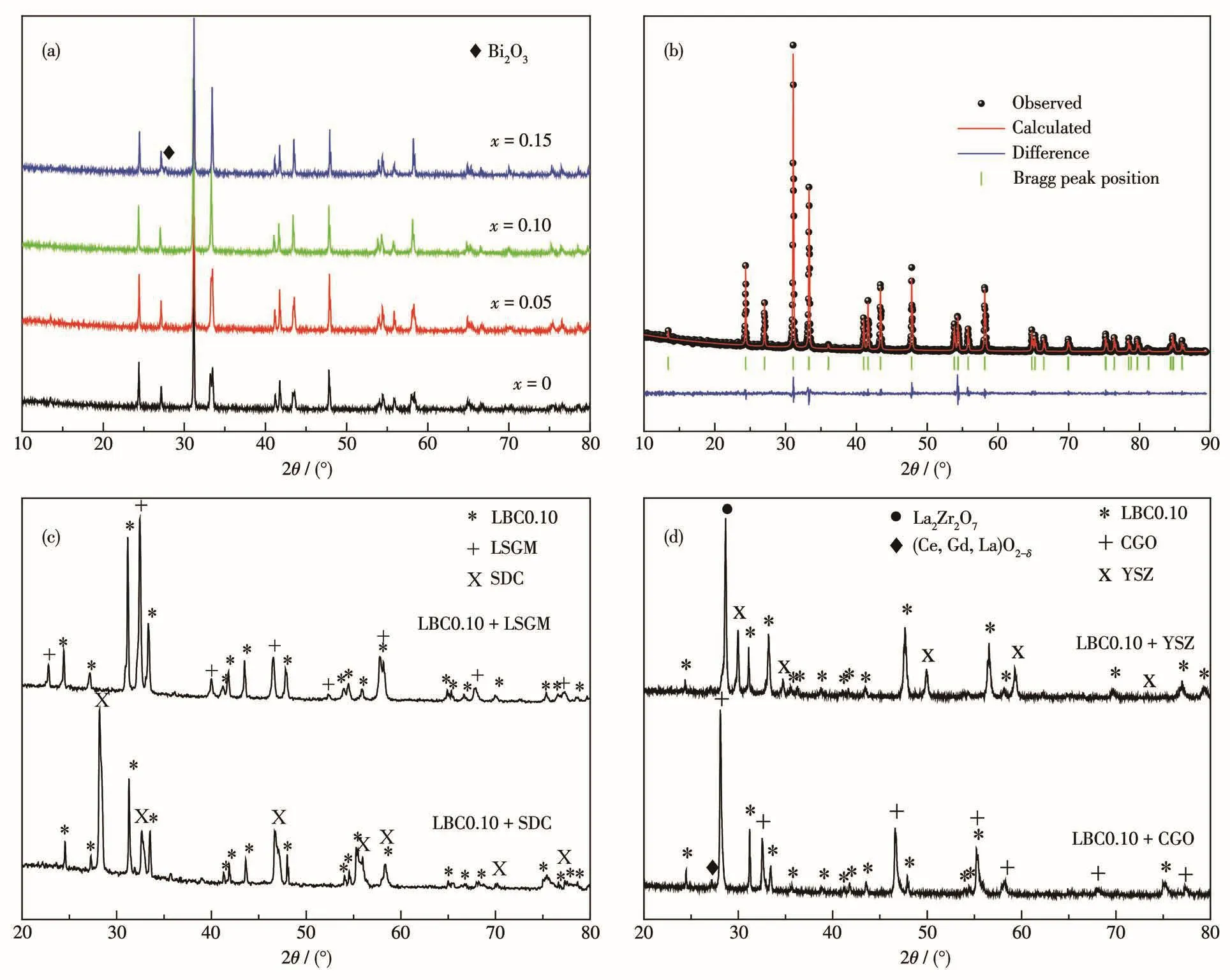
图1 (a)La2-xBixCuO4材料在900℃烧结5 h后的XRD图;(b)LBC0.10的XRD Rietved精修图;(c)LBC0.10+SDC、LBC0.10+LSGM以及(d)LBC0.10+CGO、LBC0.10+YSZ混合粉体在950℃空气气氛下烧结24 h的XRD图Fig.1 (a)XRD patterns of La2-xBixCuO4after sintering at 900℃for 5 h;(b)XRD Rietved refinement patterns of LBC0.10;XRD patterns of the mixed powder(c)LBC0.10+SDC,LBC0.10+LSGM and(d)LBC0.10+CGO,LBC0.10+YSZ that heated at 950℃in air for 24 h
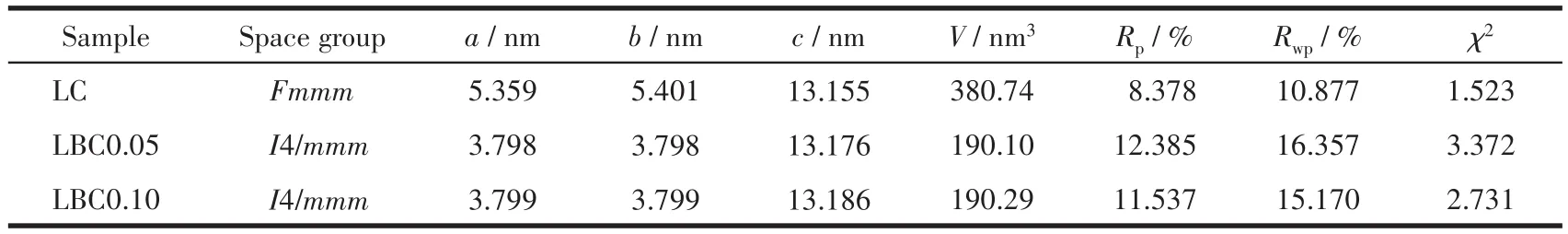
表1 La2-xBixCuO4材料的晶胞参数Table 1 Cell parameters of La2-xBixCuO4materials
2.2 La2-xBixCuO4的热膨胀以及电导率分析
作为SOFC的阴极材料,不仅要求其在工作温度范围内具有较高的电导率,而且还要求热膨胀系数尽量与其它组元相匹配。为此我们测试了系列材料的热膨胀曲线,如图2a所示。计算可知,La2-xBixCuO4系列材料的热膨胀系数(TEC)在1.210×10-5~1.302×10-5K-1范围内,而SDC电解质的热膨胀系数为1.23×10-5K-1,两者具有良好的热膨胀匹配性能。
电导率的高低是评价材料是否能作为SOFC阴极材料的一个重要指标。为此,我们采用四探针方法对La2-xBixCuO4材料进行高温电导率测试,结果如图2b所示。可见Bi的掺杂改变了La2CuO4的导电行为。La2CuO4的电导率随着测试温度的升高呈现增加的趋势,表现出半导体导电行为。而对于LBC0.05和LBC0.10,体系的电导率随着测试温度的升高,呈现出先增大后减小的趋势,在350℃出现拐点。这可能是掺Bi的材料在高温失去部分晶格氧造成的。另外,Bi的掺杂显著提升了La2CuO4的电导率。3种材料在测试温度范围内的最大电导率分别为6.64、55.31和90.30 S·cm-1。考虑到La2-xBixCuO4材料具有层状类钙钛矿结构,载流子主要在ab平面内通过金属—氧键进行传递,Bi3+进入体相取代La3+的位置,Bi元素的6s孤对电子在Cu—O平面内的电子传导中起到推动作用,因此材料的电导率随着Bi掺杂量的增加逐渐增大。
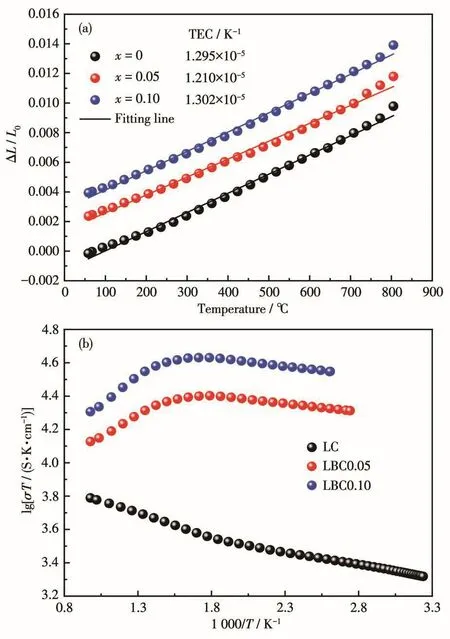
图2 La2-xBixCuO4材料的(a)热膨胀曲线和(b)电导率随温度变化图Fig.2 (a)Thermal expansion curves and(b)variation of conductivity versus temperature for La2-xBixCuO4 materials
2.3 La2-xBixCuO4材料的O2-TPD分析
为了研究材料的吸/放氧能力,进行O2-TPD测试,结果如图3所示。一般来说,在样品表面有α、β和γ三种活性氧物质,其中较低解吸附温度信号(小于400℃)对应表面的化学吸附氧,即α-氧物质;信号在较高温度(大于700℃)对应的晶格氧,称为γ-氧物质;信号位于400和700℃之间的为β-氧物质,这种氧物质与材料中存在的氧缺陷有关。图3显示在350~550℃之间3种材料均含有α-和β-氧物质。通过对谱图中的曲线进行分峰拟合,计算得到对应峰面积(表2)。可见随着Bi掺杂量的增加,α-和β-氧物质的含量均增大(峰面积增大)。这意味着Bi的掺杂使得材料中氧空位含量增加,同时表面吸附氧的能力增强。这些均有利于阴极催化氧还原反应。

图3 La2-xBixCuO4材料的TPD曲线Fig.3 TPD curves of La2-xBixCuO4materials
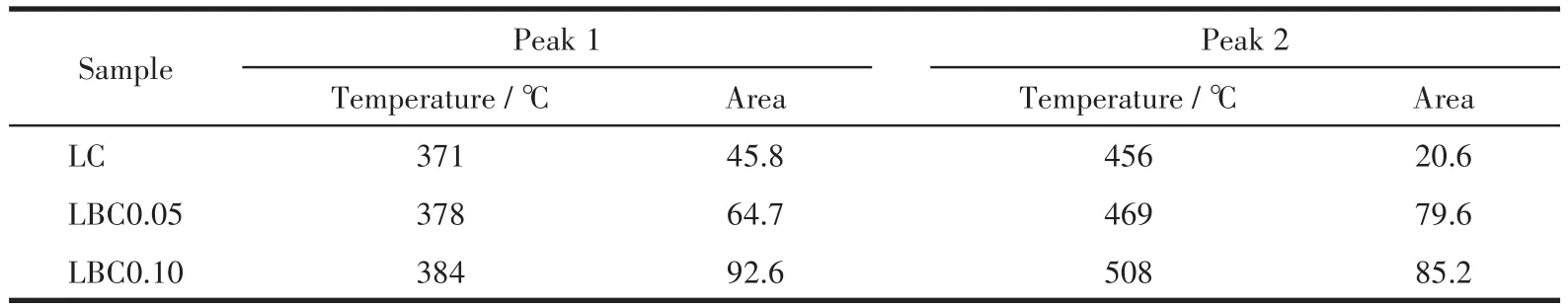
表2 La2-xBixCuO4的TPD曲线的分峰拟合值Table 2 Peak fitting values of TPD curves of La2-xBixCuO4
2.4 La2-xBixCuO4阴极的电化学性能
为了探究Bi的掺杂量对电极性能的影响,将不同材料在1 000℃烧结2 h制备成阴极,分别测试其在空气中700℃下的阻抗谱。如图4所示,阴极的交流阻抗图由一个压扁的不规则圆弧组成。从圆弧高频端以及低频端与实轴的交点数值差值中可以得到阴极极化电阻值(Rp)。可见随着Bi掺杂量的增大,极化电阻越来越小。当x=0.10时,极化电阻最小,在700℃时Rp=0.26 Ω·cm2。结合TPD测试结果可知,由于Bi的掺杂量增大,材料表面吸附氧的能力增强,体系中产生了更多的氧空位,提高了氧离子的传输性能,也为氧分子的还原反应提供了更多的活性位点。
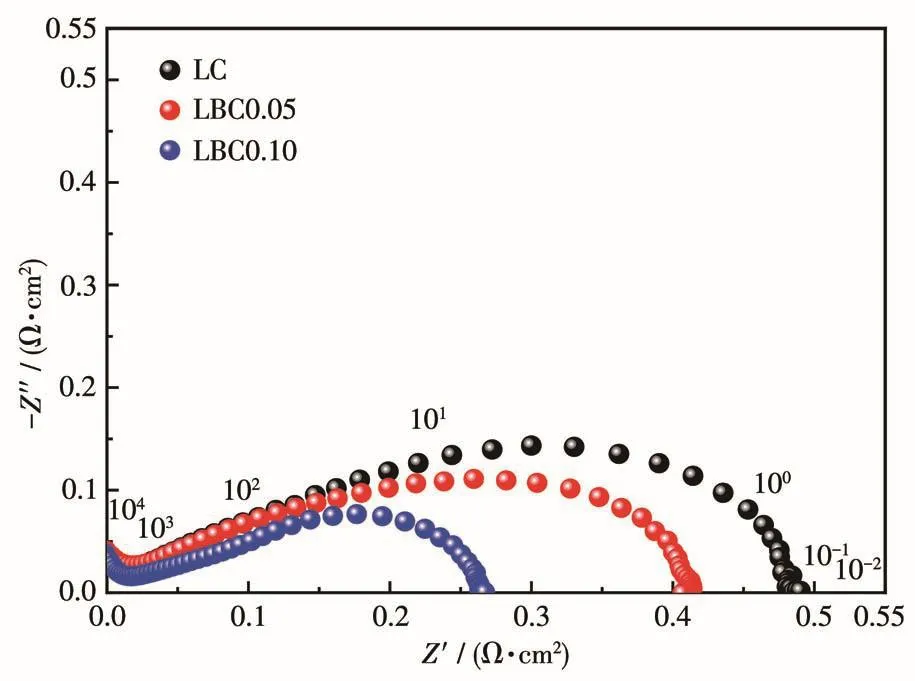
图4 La2-xBixCuO4材料在空气中700℃测试的阻抗谱图Fig.4 Impedance spectra of La2-xBixCuO4cathodes measured at 700℃in air
为了进一步明确电极反应速率控制步骤,以极化电阻最小的LBC0.10材料为研究对象,在700℃下测试了不同氧分压下的阻抗谱。如图5a所示,不同氧分压下的阻抗谱图均由高频和低频的2个扁平的圆弧组成。随着氧分压的降低,极化阻抗值相应增大,表明氧化还原反应过程受氧气浓度的影响。为了进一步讨论具体的反应速率控制步骤,采用等效电路R1-(RH-CPEH)-(RL-CPEL)对谱图进行拟合,其中R1代表SDC电解质以及测量导线的电阻,而RH和RL分别表示高频弧和低频弧的极化阻抗,CPEH和CPEL为对应弧的恒相位元。通过拟合分别得到高频弧、低频弧对应的极化电阻值。将其与氧分压进行作图,结果如图5b所示。根据文献报道[2-3],电极的极化电阻与氧分压的关系式可以描述为Rp=Rp0×(pO2)-n,其中 Rp0为指前因子,pO2表示氧分压,n为不同数值时代表电极上氧还原反应的不同过程:n=0代表氧离子由三相界面向电解质的扩散过程,n=0.25代表界面电荷转移过程,n=0.5代表吸附的氧原子在电极表面解离与扩散过程,n=1代表氧分子扩散并吸附在电极表面的过程。由图5b可知高频弧极化电阻对应的n值为0.2,接近0.25,表明高频弧对应界面电荷转移过程,而低频弧极化电阻对应的n值为0.75,介于0.5~1之间,意味着电极表面同时存在氧分子扩散以及吸附过程。根据分析结果可知,低频弧电阻总是大于高频弧电阻,因此确定电极上的速率控制步骤为氧分子的扩散与吸附过程。
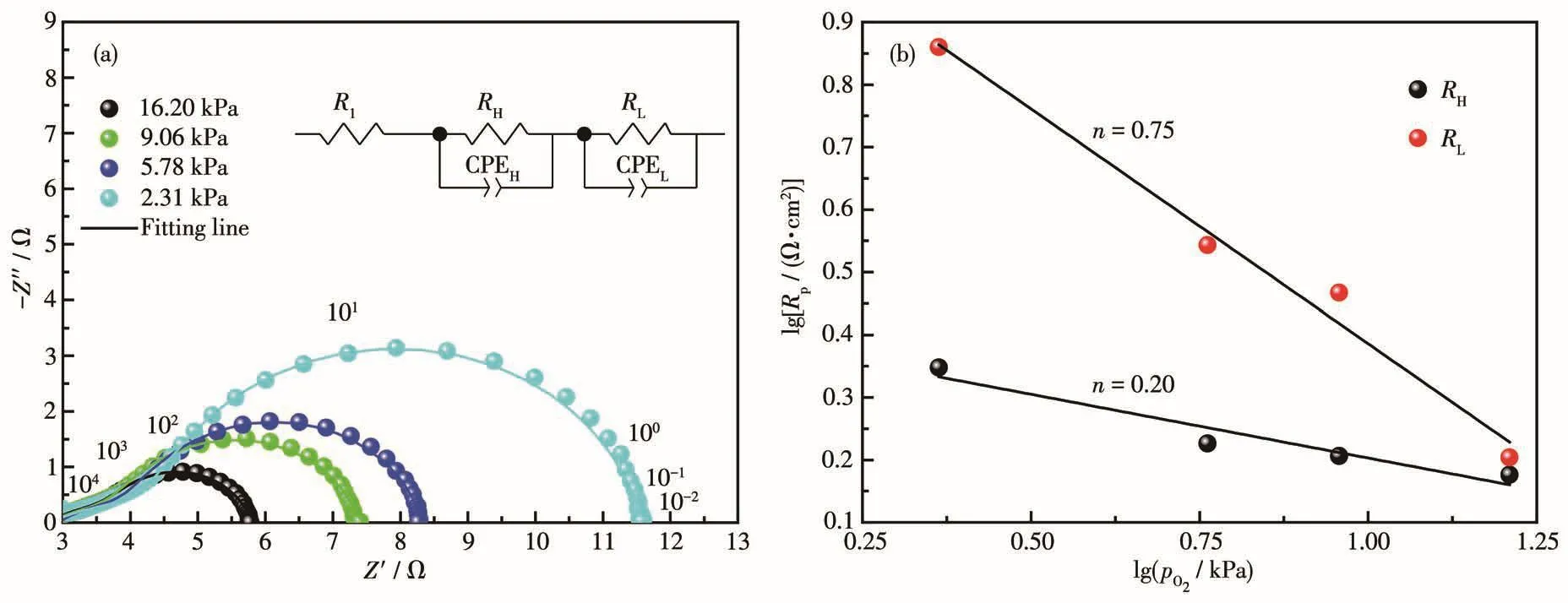
图5 LBC0.10阴极700℃下不同氧分压下的交流阻抗谱(a)及极化阻抗值随氧分压变化曲线(b)Fig.5 AC impedance spectrum(a)and polarization impedance curves(b)of LBC0.10 cathode at 700℃under different oxygen partial pressures
2.5 LBC0.10阴极的单电池性能测试
以湿氢(97% H2+3% H2O)为燃料,空气中的氧为氧化剂,测试电解质支撑NiO-SDC/SDC/LBC0.10单电池在不同温度的功率输出曲线(图6a)。可见单电池的开路电压(OCV)随着测试温度的升高而减小,700℃的OCV为0.84 V。这是由于SDC电解质在高温下发生铈的部分还原(有部分Ce4+还原生成Ce3+),SDC电解质内部产生导电电子,降低了电池的OCV。这个现象在其它以氧化铈作为电解质的SOFC体系中也有报道[28-29]。700℃下单电池的最大输出功率密度可以达到308 mW·cm-2(图6a),比La2CuO4(120 mW·cm-2)[30]提升了157%。SOFC器件的运行稳定性是衡量阴极材料性能的一个重要指标,因此我们进行了单体电池的稳定性测试(图6b)。结果表明,单体电池在700℃连续工作80 h后,输出功率从307.9 mW·cm-2降低到304.8 mW·cm-2,衰减了1.0%。结果表明LBC0.10阴极材料具有良好的氧还原催化活性和稳定性。

图6 (a)不同温度下NiO-SDC/SDC/LBC0.10单电池的电流密度-电压-功率密度曲线;(b)单电池在700℃、0.4 V负载下的长期稳定性测试曲线Fig.6 (a)Current density-voltage-power density curves of NiO-SDC/SDC/LBC0.10 single cell at different temperatures;(b)Long-term stability measurement of single cell with 0.4 V load at 700℃
3 结论
通过甘氨酸-硝酸盐法成功合成La2-xBixCuO4(x=0、0.05、0.10)系列阴极材料,系统地探究了Bi元素掺杂对材料的物相结构、高温化学相容性、导电性以及电化学性能的影响,具体结论如下:(1)XRD结果证明La2CuO4中Bi的掺杂量x最大为0.10,且掺杂使材料的晶体结构对称性发生改变,空间群由Fmmm变为I4/mmm。(2)LBC0.10氧化物与SDC粉体具有良好的高温化学相容性。(3)相比于文献报道的La2CuO4材料,La2-xBixCuO4系列材料表现出较高的电导率和改善的电化学性能。其中LBC0.10阴极在700 ℃的极化电阻为0.26 Ω·cm2,SDC电解质支撑单电池的最大功率密度为308 mW·cm-2。综上所述,Bi掺杂可有效地提高La2CuO4的电化学性能,La2-xBixCuO4是一类有潜力的中温固体氧化物燃料电池(IT-SOFCs)阴极材料。

