串联双柱固相萃取-原子吸收光谱法 检测葡萄酒中Fe、Cu和Mn的形态
李金梁,彭晶晶,杨洁,兰惠晶,张梦瑶,郭安鹊,2*
(1.西北农林科技大学葡萄酒学院,陕西杨凌 712100)(2.陕西省葡萄与葡萄酒工程技术研究中心,陕西杨凌 712100)
葡萄酒的适量氧化有利于其成熟(如利用橡木桶陈酿),但是过度氧化通常会导致褐变,严重影响葡萄酒的感官品质和营养价值[1]。葡萄酒的氧化主要表现为酚类物质(特别是邻羟基酚)的氧化,铁(Fe)离子在引发和延伸葡萄酒氧化反应中起着关键催化作用[1-3],共存的铜(Cu)、锰(Mn)离子具有氧化增效作用[4,5]。随着现代酿酒技术和设备的不断改进,葡萄酒中Fe、Cu、Mn等的含量已经大幅度降低[4,6]。然而,氧化褐变现象依然普遍存在[7,8],这与葡萄酒中上述金属的化学形态及其分布密切相关[9]。
元素形态是指某种元素在原子和分子结构水平上存在显著差异的各种存在形式,包括元素的价态、化合态和络合态等[10]。较之总浓度,葡萄酒中金属的形态不仅决定了金属的生物可利用性和毒性,也会对葡萄酒的氧化产生实质性影响[11-13]。在葡萄酒中,具有邻羟基结构的酚类物质(氧化底物)能够将Fe3+还原为Fe2+,促进氧化反应[14];酒石酸和苹果酸能够与Fe3+形成稳定络合物,一定程度上抑制酚类物质的氧化[15];pH变化会影响络合物的溶解性及其稳定性[16];氨基酸、多肽[17]、蛋白[12]、多糖[18]等也会影响金属的存在形态。因此,葡萄酒的氧化除了与金属的总量有关,更多地取决于其形态分布。然而,目前有关金属形态分析技术的报道很少,且多局限于价态的检测[19]。
葡萄酒成分复杂,金属元素形态分析面临基质干扰、形态转化等诸多挑战,利用高灵敏检测技术进行元素形态分析之前,从样品中分离出目标元素的各个形态已成为形态分析技术的关键[20]。当前常用的形态分离与富集方法主要包括液液萃取、固相萃取(SPE)、膜分离和共沉淀法等[21]。其中,SPE法由于选择性强、回收率高、有机溶剂使用少等诸多优势[22],已经成为一种现代高效的通用型样品前处理技术[20,22]。近年来,串联使用双柱SPE技术对样品进行预处理,结合火焰原子吸收法(FAAS)或电感耦合等离子体发射光谱法(ICP-OES)被成功用于葡萄酒中Fe、Cu等金属形态的测定[9,12]。然而,对于含有丰富多酚类物质的葡萄酒或其他饮料,传统的C18固相萃取柱主要萃取非极性的酚类物质,对强极性酚类物质(羟基苯甲酸、羟基肉桂酸及其衍生物)的吸附能力差、回收率低[21,23],而具有儿茶酚或没食子酰基结构的原儿茶酸、咖啡酸、没食子酸等能与金属离子(尤其是Fe3+)形成稳定络合物[25,26],C18柱并不适用于萃取葡萄酒中多种不同性质的酚类物质。与C18柱相比,以高聚物二乙烯基苯-乙烯吡咯烷酮为吸附剂的HLB固相萃取柱优势明显,更加适合保留样品中低含量的酚类物质[22,24]。
本实验通过利用HLB柱代替C18柱、优化双柱固相萃取条件,以及在模拟葡萄酒中考察pH值、有机酸对测定结果的影响,结合方法可靠性评价,构建一种快速准确、适用于葡萄酒中Fe、Cu、Mn形态分析的新技术,这对于明晰葡萄酒中Fe、Cu、Mn形态分布特征,深入研究葡萄酒氧化机制具有重要意义。
1 材料与方法
1.1 供试酒样
酒精水溶液(12%,V/V)、模拟酒;国产瓶装红葡萄酒(2017年赤霞珠干红,共5款)和白葡萄酒(4款霞多丽干白:2017年3款,2019年1款;2015年雷司令干白1款),来自甘肃紫轩酒业、宁夏御马酒庄、云南香格里拉酒业、新疆芳香庄园和丝路酒庄等企业,均为当地葡萄原料所酿商品葡萄酒。
酒精水溶液(12%,V/V):室温下制备,每100 mL溶液中含有12 mL无水乙醇。以此为溶剂,通过添加金属离子、单宁酸或有机酸,分别获得含金属离子、(单宁酸+金属离子)和有机酸的酒精水溶液,均现配现用。除非特别说明,上述溶液中的金属浓度为2000 μg/L Fe3+、500 μg/L Cu2+和2000 μg/L Mn2+,单宁酸浓度为500 mg/L。
模拟酒:参照郭安鹊等[27]的方法,配制含18 mmol/L (+)-酒石酸的酒精水溶液(12%,V/V),利用1 mol/L NaOH调节溶液的pH值为3.20。充氮气后于室温下避光放置。
1.2 仪器与试剂
Agilent AA 240Z石墨炉原子吸收光谱仪(GFAAS),美国Agilent公司;Milli-Q超纯水系统,美国Millipore公司;BT100FJ六通道数字分配型蠕动泵,保定创锐泵业有限公司;FHO-7023 12位固相萃取装置,广州菲罗门科学仪器有限公司。Polyclean X-HLB(反相固相萃取柱,500 mg/6 mL)和Superclean SCX(阳离子交换固相萃取柱,500 mg/6 mL),广州菲罗门科学仪器有限公司。标准品:1000 mg/L Fe3+、Cu2+(AAS级),1000 mg/L Mn2+、Zn2+、Al3+(ICP级),美国Sigma-Aldrich公司。L-酒石酸(99.5%)、L-酒石酸氢钾(99%)、L-苹果酸(99%)、柠檬酸(≥99.5%)、乳酸(≥85%)、琥珀酸(≥99.0%),分析纯,Sigma-Aldrich公司。乙酸,≥99.5%,分析纯,广东光华科技股份有限公司。浓硝酸,65%~68%(V/V),优级纯,洛阳昊华化学试剂有限公司;浓盐酸,36%~38%,优级纯,四川西陇科学有限公司;NaOH,≥98%,优级纯,天津市光复科技发展有限公司;无水乙醇,分析纯,四川西陇科学有限公司。实验用水均为超纯水(电阻率18.2 MΩ·cm)。
实验中所使用玻璃和塑料器材等均用10% HNO3(体积分数)浸泡过夜,再用超纯水冲洗干净,晾干后使用。
1.3 固相萃取柱活化
参照Polyclean X-HLB柱活化方法和Kontoudakis等[9]的研究报道,设置4种活化平衡方式:20 mL甲醇→30 mL水(方式1,“→”代表沿箭头方向顺序通过);20 mL甲醇→30 mL水→20 mL模拟酒(方式2);20 mL甲醇→30 mL水→10 mL 1 mol/L的盐酸→20 mL模拟酒(方式3);20 mL甲醇→30 mL水→10 mL1 mol/L的盐酸→30 mL水→20 mL模拟酒(方式4)。目前,SCX柱活化方法较为成熟、一致[9,28]。Superclean SCX柱的活化方式为:40 mL水→10 mL1 mol/L的盐酸→20 mL水→10 mL1 mol/L的NaOH→40 mL水。
借助固相萃取装置和真空泵,使各试剂以1~2 mL/min的流速依次通过小柱。过完试剂后,持续抽真空10 min左右去除SPE柱中残留的水分。
1.4 酒样中各金属形态的提取方法
抽取15 mL酒样,通过蠕动泵控制样品以1 mL/min流速首先通过Polyclean X-HLB柱:取5 mL流出液(馏分1)测定目标金属含量,疏水态含量就等于样品中金属总量减去馏分1中的金属含量[9];剩余的10 mL流出液随后以2 mL/min的流速通过Superclean SCX柱,获得残留态溶液(馏分2,用于测定酒样中目标金属的残留态含量)。最后,利用2 mol/L HNO3洗脱SCX柱,收集洗脱液(洗脱液1,用于测定金属的阳离子含量),也可通过馏分1和馏分2的差值进行比较验证。由上可知,金属总量=疏水态+阳离子+残留态。
1.5 原子吸收光谱测定条件
空白溶液:1% HNO3溶液。标准溶液:使用1% HNO3溶液将Fe3+、Cu2+、Mn2+标准溶液稀释,配制成200 μg/L的标准物质储备液。
标准曲线绘制:以1% HNO3溶液为参比,利用石墨炉原子吸收光谱仪(GFAAS)分别测定5个质量浓度梯度的Fe3+(0、20、40、100、160 μg/L)、Cu2+(0、20、40、60、100 μg/L)和Mn2+(0、20、40、100、140 μg/L)标准溶液。Fe的测定波长是372.0 nm,狭缝宽度0.2 nm,灯电流5.0 mA;Cu的分析波长是327.4 nm,狭缝宽度0.5 nm,灯电流4.0 mA;Mn的分析波长是403.1 nm,狭缝宽度0.2 nm,灯电流5.0 mA。以高纯氩气为保护气体,以峰高定量,进样体积为10 μL。仪器通过设定程序自动采集空白溶液和标准溶液系列,绘制标准曲线。GFAAS温度程序和气体流量如表1所示。
根据酒样中金属实际含量使用1% HNO3进行适当稀释后,直接进样测定,结果由标准曲线计算获得。
1.6 方法的灵敏度
通过检测限LOD(产生高于系统噪声水平可检测到响应的最低分析物浓度)和定量限LOQ(可准确和精确测量分析物的最低水平)评估方法的灵敏度[29]。
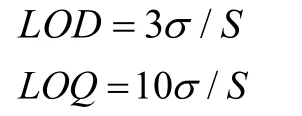
式中:
σ——空白样品多次测量值的标准差(n=9);
S——分析曲线斜率[30]。
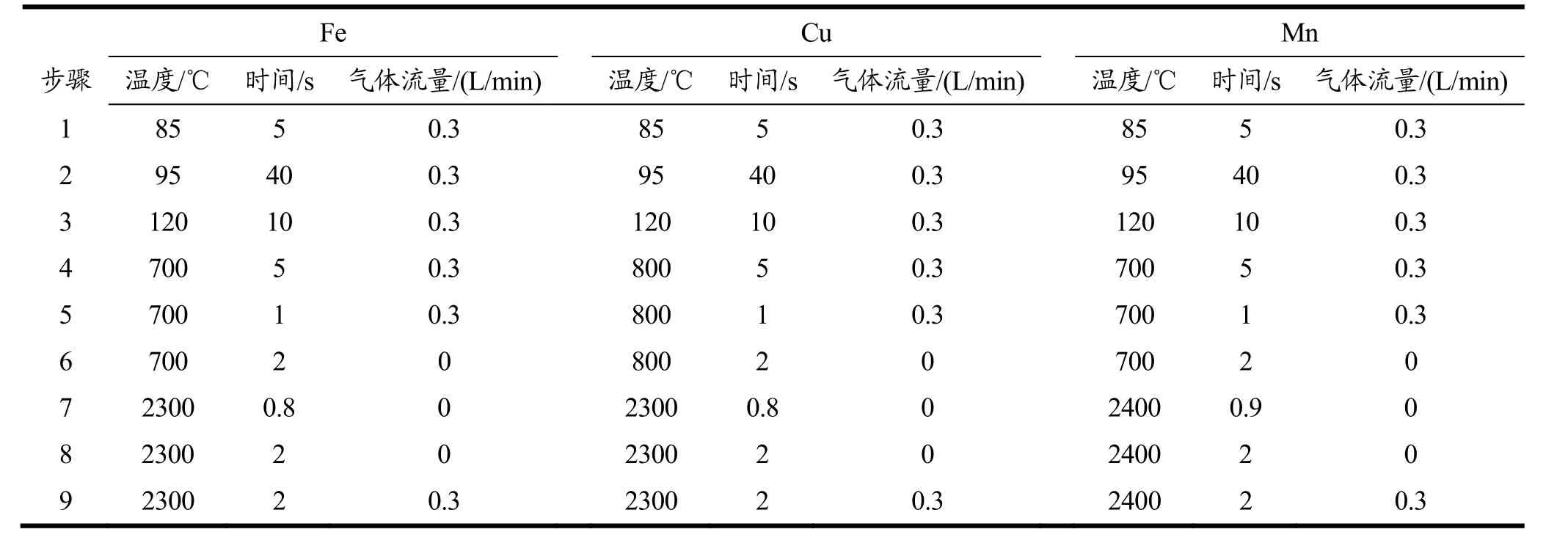
表1 测定Fe、Cu、Mn的石墨炉温度程序Table 1 Graphite furnace temperature program for determination of Fe, Cu and Mn

表2 活化方式对Polyclean X-HLB柱流出液中金属离子通过率的影响Table 2 Effects of activation methods on the throughput rates of metal ions in liquid effluents from the polyclean X-HLB column
1.7 方法的准确度和精密度
为了评价串联双柱固相萃取-原子吸收光谱法的准确性,对红葡萄酒、白葡萄酒及其馏分进行加标实验计算回收率。
回收率/%=100×(C1-C0)/C’
式中:
C1——加标后样品中金属的浓度,μg/L;
C0——加标之前样品中金属的浓度,μg/L;
C’——加到酒中的分析物的标准浓度[29],μg/L。
每种金属的加标浓度各设两个水平:低浓度Fe3+或Mn2+为500 μg/L,高浓度为2500 μg/L;低浓度Cu2+为20 μg/L,高浓度为500 μg/L。
选择白、红葡萄酒各一款,利用新建方法对原始酒样及其馏分中金属含量重复测定6次,计算相对标准偏差(% RSD),评估方法的精密度。
1.8 数据统计分析
借助数据处理软件DPS V6.50获得实验数据的ANOVA(Duncan新复极差法),每个处理重复3次,其结果以平均值±标准差表示。利用Microsoft excel 2010和Origin 2018进行图表绘制。
2 结果与分析
2.1 Polyclean X-HLB柱的活化
结果如表2所示,在仅含金属离子的酒精水溶液中,4种活化方式对HLB柱吸附Cu2+、Mn2+的影响很少,但是对Fe3+具有显著影响;活化方式4表现最佳,3种金属离子通过率(流出液中金属含量占金属总量的百分比)最高(均不低于93.71%)。由于单宁酸的邻酚结构可以与金属离子配合形成稳定的络合物[31],其加入后,3种金属的存在形态发生改变(Fe3+几乎全部被单宁酸络合),流出液中金属浓度均下降,但是不同活化方式之间的差异不显著。因此,选择方式4进行HLB柱的活化和平衡。
Pohl等[11-13]发现,在含单宁酸的酒精水溶液(pH 3.00~5.00)中:20%~85% Fe3+被Amberlite XAD-7HP柱保留,10%~35% Cu2+和9%~13% Mn2+被Amberlite XAD-16柱保留。相比Amberlite XAD系列固相萃取柱,在本实验条件下(pH=2.88),Polyclean X-HLB柱对上述金属离子的单宁酸络合物均具有更高的保留率,有效保证了葡萄酒中金属疏水态含量检测的准确性。
2.2 SPE柱流速对金属离子通过率的影响
样品分别以1、2、3 mL/min流速通过Polyclean X-HLB柱或Superclean SCX柱,结果如表3所示。含有金属离子的样品流经HLB柱后,流速仅对Fe3+产生了显著影响(随流速增加,流出液中Fe3+百分比浓度从93.71%降至79.43%);1 mL/min和2 mL/min处理之间的差异不显著,这与文献报道的结果一致[11-13];单宁酸加入后,流出液中Fe3+的浓度下降最大,且同一金属离子不同流速之间的差异并不显著(表3)。与酒精水溶液相比,葡萄酒成分更为复杂,所以选择1 mL/min作为HLB柱的最佳流速。
同样,由表3可知,仅含金属离子的样品流经SCX柱后,3种金属阳离子几乎全部被吸附,流速为2 mL/min的效果最好;加入的单宁酸由于与Fe3+形成稳定络合物,不能被SCX柱保留,所以通过率很高(≥75.77%)。考虑到萃取时间过长可能会造成金属形态转化问题,选择2 mL/min作为SCX柱的最佳流速,这与已有文献报道的1 mL/min略有不同[9,11-13,28]。
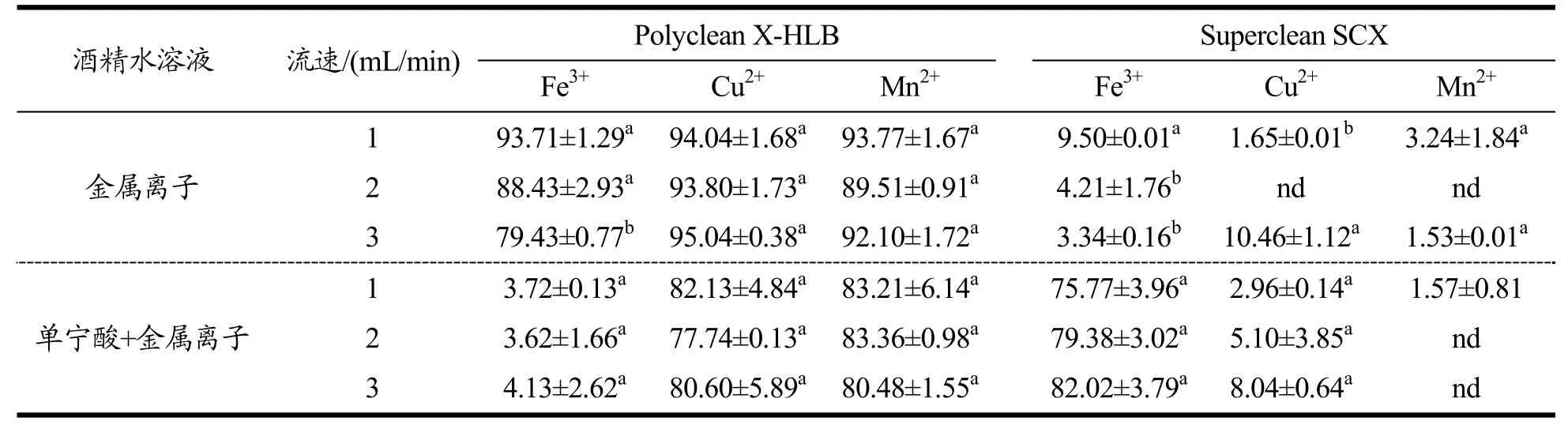
表3 流速对SPE柱流出液中金属离子通过率(%)的影响Table 3 Effects of different speeds on the throughput rates of metal ions in liquid effluents from SPE columns

表4 洗脱剂对SPE柱流出液中金属离子回收率(%)的影响Table 4 Effects of eluting agents on the recoveryof metal ions in liquid effluents from SPE columns

表5 共存Zn2+和Al3+对SPE柱流出液中金属离子通过率的影响Table 5 Effects of Zn2+ and Al3+on the throughput rates of metal ions in liquid effluents from SPE columns
2.3 SPE柱洗脱剂对金属离子回收率的影响
以1、2、3 mol/L盐酸或硝酸溶液为洗脱剂,分别对样品经过的Polyclean X-HLB柱和Superclean SCX柱进行洗脱,洗脱效果以回收率(洗脱液中金属离子含量与洗脱前SPE柱上吸附金属离子含量的比值)表示。结果显示(表4),对于Polyclean X-HLB柱,除了盐酸对Fe3+的洗脱结果(回收率≥98.27%)令人满意外,其他处理的洗脱效果均不理想。Pohl及其合作者也在相关研究中发现了同样的问题,所以建议采用差减法计算疏水态含量[11-13],即利用样品中的金属总量减去流出液中的含量就等于疏水态含量。
对于Superclean SCX柱,不同浓度的盐酸或硝酸洗脱后3种金属离子的回收率均令人满意,其中2 mol/L硝酸表现出最好的洗脱能力和稳定性,回收率为98.34%~99.29%(表4)。
2.4 共存Zn2+和Al3+对金属离子通过率的影响
有研究表明,K+、Na+、Ca2+、Mg2+和Fe3+、Cu2+、Mn2+同时通过固相萃取柱时不会对分离结果产生影响[12,13]。向只含金属离子的酒精水溶液中添加1 mg/L Zn2+和0.5 mg/L Al3+,在上述优化萃取条件下,依次通过Polyclean X-HLB和SupercleanSCX柱。测定结果表明(表5),共存Zn2+和Al3+没有对过柱后3种金属离子的分离结果产生显著影响。
2.5 葡萄酒中Fe、Cu、Mn含量检测方法的评价
2.5.1 标准曲线的线性
以Fe、Cu、Mn各自的质量浓度(μg/L)为横坐标、吸光度为纵坐标,得到铁标准曲线为y=0.0031x+0.0014,决定系数R2为0.9997;铜标准曲线为y=0.0056x+0.0391,R2为0.9919;锰标准曲线为y=0.0047x+0.0154,R2为0.9992。说明Fe、Cu和Mn在所设质量浓度范围内线性关系良好。
2.5.2 灵敏度
通过计算3倍多次空白的标准差σ除以分析曲线的斜率S可知,Fe、Cu、Mn的LOD值分别为1.56 μg/L、0.55 μg/L和0.39 μg/L,LOQ值分别为5.21 μg/L、1.83 μg/L和1.30 μg/L。说明方法的灵敏度高。
2.5.3 准确度和精密度
加标回收实验的结果显示(表6),白葡萄酒及其各馏分中Fe、Cu、Mn的加标回收率分别是92.49%~106.37%、96.68%~112.18%、94.03%~ 107.67%;红葡萄酒及其各馏分中Fe、Cu、Mn的加标回收率分别是92.04%~110.39%、90.53%~109.65%、101.94%~110.16%。表明方法的准确性良好。
对原始酒样及其馏分中金属含量重复测定6次的结果显示,Fe的相对标准偏差(%RSD)为1.59%~ 6.55%,Cu的相对标准偏差为3.55%~7.12%,Mn的相对标准偏差为0.89%~6.33%,说明方法的精密度良好。
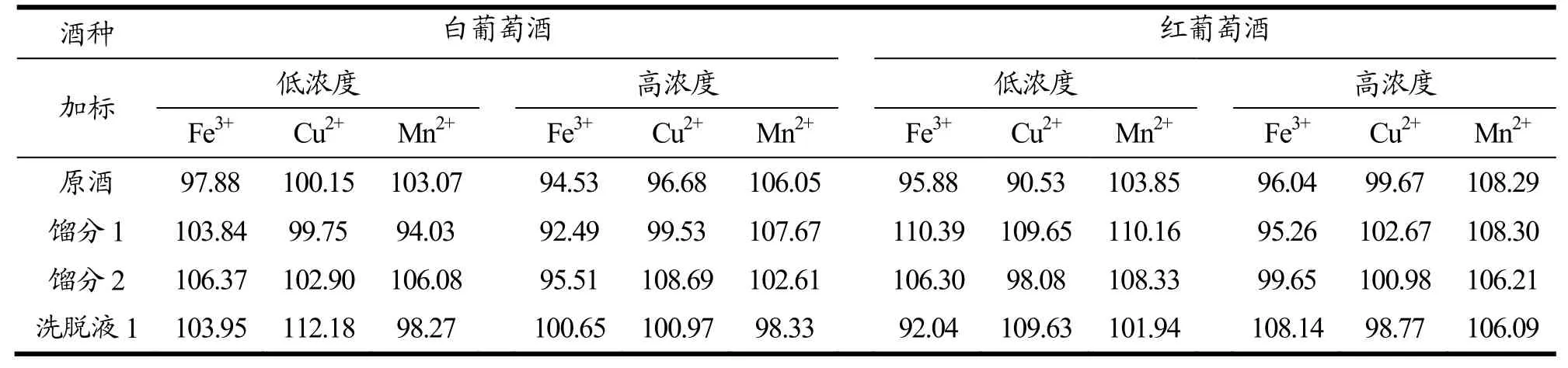
表6 白葡萄酒和红葡萄酒及其馏分、洗脱液在不同加标浓度下的回收率(%)Table 6 The recoveries (%) of white, red wine, their effluents and eluates in samples with two spiked levels
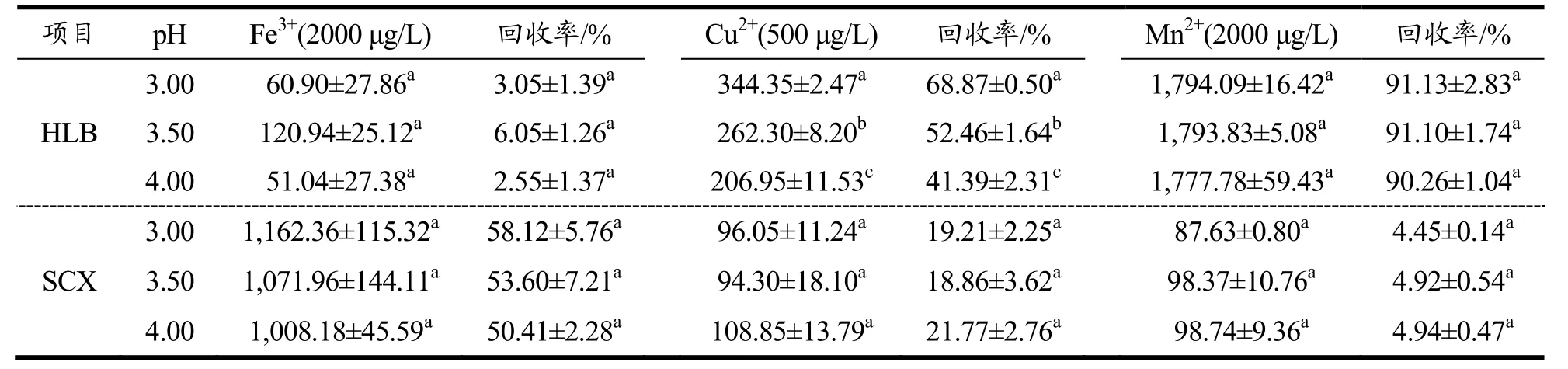
表7 pH对SPE柱流出液中金属离子回收率的影响Table 7 Effects of pH on the throughput rates of metal ions in liquid effluents from SPE columns
2.6 pH和有机酸对模拟葡萄酒中Fe、Cu、Mn形态测定的影响
2.6.1 pH的影响
为了解pH对Fe3+、Cu2+、Mn2+形态的影响,采用0.05 mol/L盐酸和0.05 mol/L NaOH调节12%(V/V)酒精水溶溶液的pH值为3.00、3.50和4.00(葡萄酒pH值范围);静置2 h后,各样品分别通过Polyclean X-HLB和Superclean SCX柱。
结果表明(表7),Fe3+对pH变化非常敏感,在实验pH条件下,93%以上被HLB柱吸附,仅有50%左右通过SCX柱;随着pH值增加,Cu2+通过HLB柱的百分比下降,约有20%左右通过SCX柱;Mn2+对pH变化不敏感,90%以上通过HLB柱,约有95%被SCX柱保留。pH变化对Fe、Cu形态的影响,很可能与Fe(OH)3等胶体的形成及后续沉淀有关[32,33]。水中的研究显示,当Fe3+浓度为5mg/L时,Fe3+在pH为3.36时就开始产生Fe(OH)3,pH为4.01时完全沉淀[34]。
2.6.2 有机酸的影响
葡萄酒中常见的有机酸(酒石酸、苹果酸、柠檬酸、琥珀酸、乳酸等),由于含有羟基官能团,能够和铁离子形成可溶性络合物[35,36],通过改变铁的形态分布而影响葡萄酒的氧化过程[37]。利用建立的串联双柱固相萃取-原子吸收光谱法,在酒精水溶液12%(V/V)中研究了不同pH条件下有机酸及其组合对酒样中Fe3+、Cu2+、Mn2+形态分布的影响。各有机酸浓度接近其在葡萄酒中的实际含量[15]。
结果表明(图1),有机酸种类、pH对Fe3+、Cu2+的存在形态具有显著影响,而对Mn2+的形态分布(以阳离子为主,平均占Mn总量的91.44%)影响很小。如图1所示,在模拟葡萄酒环境条件下,Fe3+因与酒石酸、苹果酸、柠檬酸络合主要以残留态存在(在pH 3.50~4.00时表现尤为明显),而由于与乳酸配合作用弱而以阳离子为主(虽然pH上升一定程度上提高了残留态的百分比);Cu2+形态对pH值变化非常敏感(酒石酸和柠檬酸表现最突出,其次是苹果酸,乳酸最弱):pH 3.00时主要是阳离子(≥86.48%),随着pH值增加,其百分比显著下降并伴随着残留态显著上升,至pH 4.00时酒石酸和柠檬酸溶液中的Cu2+以残留态为主,分别占到了60.44%和83.13%;与单一有机酸(主要是酒石酸、苹果酸和柠檬酸)相比,混合有机酸之间表现出对络合金属离子的竞争关系,很大程度上降低了阳离子的百分比而增加了疏水态的百分比(可能与其他酸加入后引起pH值下降有关)。
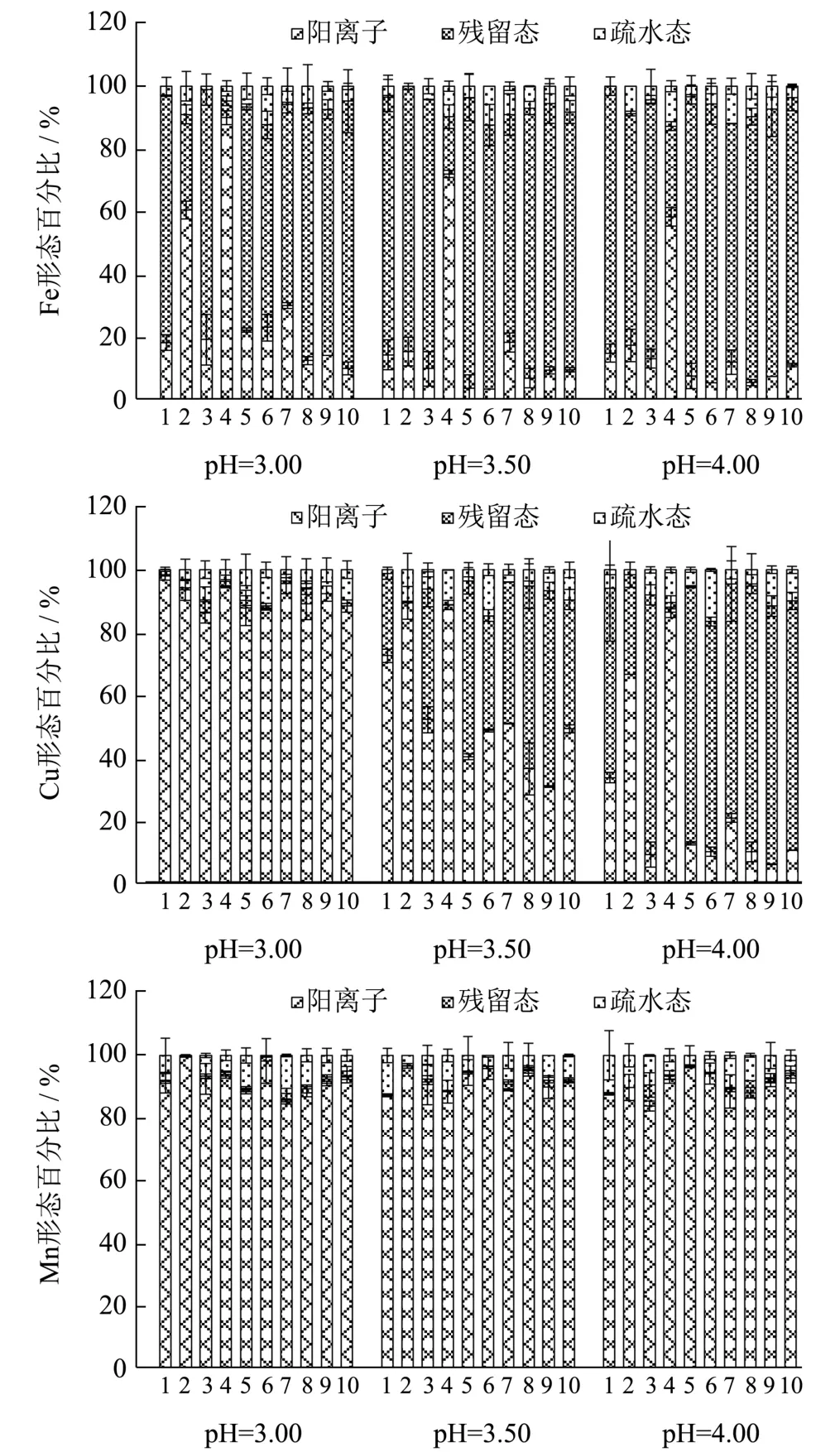
图1 不同pH条件下有机酸对酒精水溶液中Fe3+、Cu2+、Mn2+形态分布的影响Fig.1 Effects of organic acids on fraction distribution of ferric, cupric and Mn (II) ions in alcoholic solutions with different pH values
不同有机酸、pH对金属形态影响的差异,主要与它们在模拟葡萄酒中的离解程度、酸根离子与金属离子之间的相互作用强弱有关:相比于弱配体乳酸、琥珀酸和乙酸,酒石酸、苹果酸和柠檬酸与Fe3+络合作用更强,且混合有机酸之间存在相互竞争关系[15];通常情况下,有机酸络合作用依赖于pH值(金属离子和H+都要争夺配体),在葡萄酒pH条件下,苹果酸和酒石酸与Fe3+具有相似的络合能力[37],这与本实验的研究结果(pH 3.50~4.00)一致。另外,与上文“2.6.1 pH的影响”结果相比,由于有机酸与金属离子(如Fe3+和Cu2+)形成了稳定的可溶性络合物,改变了金属的形态分布(疏水态浓度降低),它们的加入提高了金属离子的溶解性[38]。
2.7 葡萄酒中Fe、Cu、Mn形态的测定
选择瓶装白、红葡萄酒各5款,利用串联双柱固相萃取-原子吸收光谱法,分析酒样中Fe、Cu、Mn的形态及其分布特征,结果如图2所示。就金属总量而言,不同酒样之间的差异比较大:红葡萄酒中Fe、Cu的平均含量(分别为2.23、0.15 mg/L)均比白葡萄酒中的(分别为0.88、0.09 mg/L)高,两种类型酒中Mn的含量非常接近(平均值分别为1.98、2.27 mg/L)。金属形态分析的结果表明(图2),酒样中同一金属的3种形态之间差异显著;相同类型葡萄酒中Fe或Mn的形态分布比较稳定(样品间差异小),而Cu的形态分布变化很大(样品间变化较大);酒样中Fe、Mn均主要以残留态存在(平均分别占金属总量的69.79%和58.05%),而Cu在白葡萄酒(以残留态为主,平均占45.62%)和红葡萄酒(以疏水态为主,平均占65.60%)中表现不同;Fe阳离子、Mn阳离子、Cu疏水态在白葡萄酒中排名其次,Fe疏水态、Cu残留态和Mn阳离子则在红葡萄酒中排名第二。
如前所述,酚类物质很容易与铁离子形成稳定络合物,所以与白葡萄酒相比,Fe在富含酚类物质的红葡萄酒中具有更多的疏水态;Cu在葡萄酒中具有较多的疏水态,这与Kontoudakis等[9]的研究结果相同。研究显示,葡萄酒中的铁离子主要以络合态存在[1],总体上白、红葡萄酒中的Fe应以残留态为主,这与本研究的结果一致。然而,Kontoudakis等[9]却发现白葡萄酒中铁的主要形态是阳离子。这可能与葡萄酒本身的化学成分和氧化还原状态有关:一方面,铁形态与有机酸种类、pH有关,如在低pH值苹果酸酒精水溶液中以阳离子为主;另一方面,葡萄酒的氧化还原状态决定了Fe2+/Fe3+比率[19],如酒石酸、苹果酸能够与Fe3+形成稳定络合物,但是与Fe2+的络合作用却很弱[37],最终影响了酒样中各种铁形态的分布。该团队也认为这可能与铁-有机酸络合物的解离和低pH条件有关[9]。目前,有关葡萄酒中Mn形态的研究还很少。然而,基于白、红葡萄酒中较高的Mn总量和阳离子比例,以及其在葡萄酒氧化反应中的重要作用,应当在今后研究中对Mn元素引起足够的重视。

图2 商品葡萄酒中Fe、Cu、Mn的形态分布Fig.2 Fraction distribution of Fe, Cu and Mn in commercial white (W) and red (R) wines
3 结论
3.1 构建出一种适用于葡萄酒中Fe、Cu、Mn形态检测的串联双柱固相萃取-原子吸收光谱技术,可有效测定金属的疏水态、阳离子和残留态。确定了Polyclean X-HLB最佳活化条件和最佳流速(1 mL/min),明晰了Superclean SCX的最佳流速(2 mL/min)和洗脱剂(2 mol/L硝酸);该法快速高效、准确可靠,也可用于其他酒精饮料中金属形态的检测。
3.2 在葡萄酒环境条件下,pH对Fe3+和Cu2+的形态具有显著影响,但是对Mn2+的形态影响很小;与单一有机酸相比,混合有机酸之间存在对金属离子的竞争络合关系,很大程度上提高了金属离子的溶解性。 3.3 白、红葡萄酒中Fe、Cu、Mn的形态分布特征不同,这与葡萄酒的成分和氧化还原状态密切相关。

