缺血后处理抑制内质网应激对肾缺血再灌注损伤的保护作用及机制
张天珍,谭晓华,吴翠娇
(青岛大学基础医学院,山东青岛 266071 1 人体解剖与组织胚胎学系; 2 病理学系)
肾缺血再灌注是指肾脏外科手术或肾实质性损伤会阻断肾脏血流造成缺血低氧,给予再灌注后,肾脏的血流和功能恢复。再灌注经常伴随着再氧化,会加重前期缺血低氧的组织损伤,造成再灌注损伤。在临床上,肾缺血再灌注损伤是导致急性肾损伤的主要原因之一[1-2]。急性肾损伤后近端小管持续的炎症状态等病理改变会导致肾脏纤维化的发生,从而增加慢性肾脏病和终末期肾病的风险[3]。缺血再灌注损伤的病理生理过程复杂,涉及肾微血管病变、线粒体功能障碍、自噬、炎症、内质网应激等多个方面[4-6]。其中内质网应激诱导细胞凋亡,是除了死亡受体和线粒体功能障碍凋亡途径外,新发现的第三种细胞凋亡途径,也是缺血再灌注所致肾损伤的细胞反应。已有研究结果证明,在肾缺血再灌注损伤后,内质网应激的强度增强,细胞凋亡增加,组织损伤加重[7-8]。减轻再灌注损伤后内质网应激强度或减少其持续时间,以降低器官组织结构损伤和功能障碍,成为研究热点。有研究通过给予肾脏缺血前处理(IPC)证明,IPC对缺血再灌注导致的肾损伤具有保护作用[9]。但由于器官缺血时间的不可预知性,IPC处理具有明显的临床局限。另研究表明,缺血后处理(IPO)可以减轻缺血再灌注器官(心、肝、肾、肠、胃)的损伤[10]。主要认为IPO 通过减轻炎症反应、氧化应激和细胞自噬等机制,来减轻缺血再灌注引发的肾损伤[11-13]。但是有关缺血再灌注损伤后IPO 影响内质网应激进而影响组织损伤的研究甚少。本实验通过建立动物模型,运用形态学、免疫组织化学、免疫荧光等技术,检测重要的内质网应激凋亡因子的表达,来进一步探讨IPO 如何影响内质网应激诱导的细胞凋亡,从而减轻缺血再灌注损伤。
1 材料与方法
1.1 实验材料
1.1.1 实验动物 健康雄性SD大鼠36只,体质量180~200 g,由青岛大学实验动物中心提供。
1.1.2 主要试剂 免疫显色试剂盒购自福州迈新生物技术开发公司;TUNEL 染色试剂盒购自德国曼海姆公司;抗体GRP78、CHOP、E-Cadherin均购自英国Abcam 公司;抗体Cleaved Caspase3购自美国Cell Signaling Technology公司;第二抗体购自索莱宝生物科技有限公司。
1.2 实验方法
1.2.1 动物分组及处理 将36只大鼠随机分为假手术组(Sham 组)、缺血再灌注组(IR 组)和IPO组,每组12只。IR 组参照TAN 等[14]的研究建立肾缺血再灌注模型。术前大鼠禁食12 h,可自由饮水。术时大鼠腹腔注射100 g/L 水合氯醛5 m L/kg,麻醉后仰卧位将大鼠固定于鼠台上,开腹暴露左、右肾,切除右肾,钝性分离左肾,暴露左肾动脉,用无创动脉夹夹住左肾动脉,观察肾脏颜色由鲜红色变为暗色即确认肾脏血流阻断,为缺血状态。夹闭45 min后松开动脉夹,观察肾脏颜色由暗红恢复成鲜红色即确认为血流恢复,缝合腹部切口。大鼠苏醒后放回鼠笼,予正常饮食,24 h后IR 模型制备成功。IPO 组在左肾动脉夹闭45 min后,松开动脉夹3 min,再夹闭左肾动脉30 s,松开30 s,共6次,其余操作同IR 组。Sham 组只行开腹并切除右肾,游离左肾,分离出左肾动脉不夹闭,切口用生理盐水纱布覆盖,45 min后关腹。建模24 h后,麻醉大鼠,开腹,用注射器采集下腔静脉血2 m L,置于EP 管中,放冰上暂存。然后摘取右肾,处死大鼠。
1.2.2 肾功能指标检测 将装有大鼠下腔静脉血的EP管在4℃下以4 000 r/min离心10 min,用加样器收集上层血清成分(不要吸到下层血细胞),将收集到的血清做好标记后置-80 ℃冰箱保存。最后送医院检验科使用半自动生化分析仪检测血清肌酐和尿素氮浓度。
1.2.3 肾组织形态学观察 以40 g/L的中性甲醛溶液固定肾组织48 h,常规石蜡包埋切片,苏木精-伊红(HE)染色,光学显微镜下观察组织形态。肾小管损伤评分[15]:切片HE染色后在病变严重处采用Paller法对肾小管损伤程度进行评分,即每个高倍视野随机选择10个有病变的肾小管区域按100个肾小管计分。计分标准:肾小管明显扩张、细胞扁平1分,刷状缘损伤或脱落1分或2分,管型2分,肾小管管腔内有脱落的、坏死的细胞以及未成管型或细胞碎片1分。
1.2.4 免疫组织化学方法检测肾组织中Cleaved Caspase3蛋白表达 石蜡切片经二甲苯脱蜡及乙醇梯度水化后,用微波炉进行抗原修复(柠檬酸钠,p H 值6.0),加Cleaved Caspase3抗体(1∶200)4℃过夜孵育。次日,室温复温40 min,以PBS洗片,加二抗(羊抗兔)37 ℃孵育1 h,以PBS 洗片后进行DAB染色,水洗终止染色后用苏木精复染12 s。最后采用乙醇梯度脱水,二甲苯透明,中性树胶封片,在光镜下观察。
1.2.5 Western blotting法检测肾组织中Cleaved Caspase3蛋白表达 制作肾组织匀浆后提取蛋白。分别制作100、120 g/L 的SDS-PAGE 分离胶和50 g/L的浓缩胶,在胶板上按照25μg的加样量上样,电泳1 h,然后电转50 min。电转转膜后以50 g/L脱脂奶粉封闭3 h,然后加Cleaved Caspase3抗体(1∶1 000)4 ℃过夜孵育。次日,以1×TBST 洗PVDF膜后,再加入二抗孵育2 h。以1×TBST 洗PVDF膜后,在膜上加显影液用显影仪显影。然后用Image J软件分析条带的灰度值,以β-actin为内参照,计算蛋白表达量。蛋白表达量=目的蛋白灰度值/β-actin蛋白灰度值。
1.2.6 TUNEL染色检测肾组织细胞凋亡 常规石蜡包埋制作肾组织切片(5μm),切片经二甲苯脱蜡及梯度乙醇水化后,用PBS洗涤3次,每次5 min。用滤纸小心吸去载玻片上组织周围的多余液体,立即在切片上加2滴Td T 酶缓冲液,室温放置5 min。用滤纸小心吸去切片周围的多余液体,立即在切片上滴加54μL Td T 酶反应液,置湿盒中于37 ℃反应1 h。将切片置于染色缸中,加入已预热到37 ℃的洗涤与终止反应缓冲液,于37 ℃保温30 min,每10 min将载玻片轻轻提起和放下1次,使液体轻微搅动。组织切片用PBS洗涤3次,每次5 min。直接在切片上滴加2滴过氧化物酶标记的抗地高辛抗体,于湿盒中室温反应30 min。用PBS洗3次,每次5 min。在组织切片上直接滴加新鲜配制的0.5 g/L的DAB 溶液,室温显色5 min。用蒸馏水洗4次,前3次每次1 min,最后1次5 min。于室温下用甲基绿复染10 min。用蒸馏水洗3次,前2次将载玻片提起放下10次,最后1次静置30 s。依同样方法再用正丁醇洗3次,用二甲苯脱水。封片、干燥后在光学显微镜下取5个不同的视野,分别计数总的细胞数和凋亡细胞数,计算细胞凋亡率(凋亡细胞数/总的细胞数)。
1.2.7 免疫荧光检测GRP78、CHOP和E-Cadherin蛋白表达 切片经二甲苯脱蜡及乙醇梯度水化后,用微波炉进行抗原修复(柠檬酸钠,p H 值6.0),加一抗4 ℃过夜孵育。次日,室温复温30 min,以PBS洗片后加荧光二抗孵育1 h(此后实验步骤避光操作),以DIPA 染色10 min,用防淬灭荧光剂封片,在激光共聚焦显微镜下观察并随机采集图片。
1.3 统计学处理
采用SPSS 25.0软件进行数据统计分析。计量资料数据以±s表示,多组比较采用单因素方差分析,组间两两比较采用LSD-t检验。以P<0.05表示差异有统计学意义。
2 结 果
2.1 各组肾功能生化指标比较
Sham 组血清肌酐和尿素氮浓度在正常范围内,IR 组的浓度明显高于Sham 组,IPO 组的浓度明显低于IR 组(F=202.726、496.013,P<0.05)。见表1。
表1 各组肾功能生化指标的比较(n=12,±s)

表1 各组肾功能生化指标的比较(n=12,±s)
各组血清肌酐和尿素氮比较,F=202.76、496.013,P<0.05。
组别肌酐(c/μmol·L-1)尿素氮(ρ/mg·L-1)Sham组71.60± 8.41 114.0±11.4 IR 组445.60±49.39 530.0±36.1 IPO 组200.00±12.73 164.0±14.1
2.2 肾组织的形态学观察
光镜下可见,Sham 组皮质迷路深部的肾小体较大,肾小体内的血管球呈现大量毛细血管切面,肾小囊包绕血管球外,中间有肾小囊腔相隔;近端小管切面多,管壁厚,管腔小而不规则,上皮细胞为立方形或锥形,细胞体较大、分界不清,腔面有刷状缘,胞质呈强嗜酸性,细胞核圆形,位于近基底部;远端小管切面少,管壁薄,管腔大而规则,上皮细胞为立方形,细胞体较小、分界清楚,游离面无刷状缘,胞质呈弱嗜酸性,细胞核圆形,位于中央。IR 组病理改变明显,血管球和肾小囊变形,血管球内毛细血管严重淤血,肾小囊腔变窄或消失;近端小管改变明显,上皮变厚,管腔变窄,上皮细胞肿胀,细胞内出现较多空泡变性,腔面刷状缘消失,小管腔内出现坏死细胞碎片,间质水肿,小血管淤血。IPO 组肾组织改变比IR 组明显减轻,肾小管上皮细胞轻度水肿,有少量小的空泡,肾小管管腔内可见少量脱落的上皮细胞,管周可见少量淤血;血管球内毛细血管轻度淤血,肾小囊腔部分狭窄,间质充血。提示IPO 可以有效减轻缺血再灌注损伤后的肾损害。见图1A。
Sham 组、IR 组和IPO 组肾小管损伤评分分别为(0.10±0.32)、(5.20±1.48)和(1.90±0.99)分(n=12)。IR 组肾小管损伤程度明显高于Sham组,IPO 组明显低于IR 组,差异有统计学意义(F=61.439,P<0.01)。
2.3 各组Cleaved Caspase3蛋白表达比较
免疫组织化学染色法检测结果显示,Sham 组肾组织近端小管上皮细胞胞质可见极少阳性着色;IR 组近端小管上皮细胞胞质出现大量棕褐色着色,表明Cleaved Caspase3蛋白在IR 组呈强阳性表达,提示Cleaved Caspase3 蛋白激活,细胞凋亡严重;IPO 组近端小管上皮细胞胞质有少量黄棕色着色,表明Cleaved Caspase3 蛋白在IPO 组阳性表达较低,提示Cleaved Caspase3蛋白部分激活,细胞凋亡减少。见图1B。
Western blotting 检测结果显示,Sham 组、IR组和IPO 组Cleaved Caspase3 蛋白的相对表达量分别为0.12±0.01、1.27±0.11和0.32±0.02(n=12)。IR 组Cleaved Caspase3蛋白表达量明显高于Sham 组,IPO 组明显低于IR 组,差异有统计学意义(F=439.230,P<0.01)。表明IPO 可以通过抑制肾小管上皮细胞凋亡来减轻肾损伤。见图2。
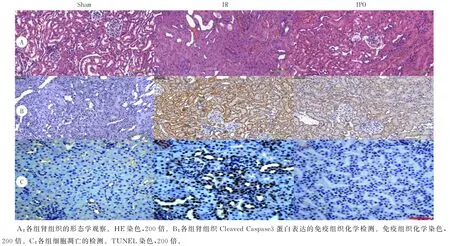
图1 各组肾组织的形态学观察以及Cleaved Caspase3蛋白表达和细胞凋亡的检测

图2 各组大鼠肾组织Cleaved Caspase3 蛋白表达的Western blotting检测
2.4 TUNEL染色检测细胞凋亡
TUNEL染色阳性定位于近端小管上皮细胞胞核内。Sham 组近端小管上皮细胞胞核内有极少棕褐色颗粒,几乎没有阳性表达;IR 组近端小管可见大量的上皮细胞胞核呈深棕色,阳性表达明显多于Sham 组;IPO 组近端小管有少量的上皮细胞胞核染色阳性。见图1C。
Sham 组、IR 组和IPO 组细胞凋亡率分别为0.07±0.01、0.50±0.09和0.15±0.01(n=12)。IR组细胞凋亡率明显高于Sham 组,IPO 组明显低于IR 组,差异有统计学意义(F=92.818,P<0.01)。表明IPO 通过减少肾小管细胞凋亡来保护肾脏免受缺血再灌注损伤。
2.5 免疫荧光检测GRP78、CHOP 和E-Cadherin蛋白表达
Sham 组GRP78和CHOP蛋白荧光信号极弱,E-Cadherin蛋白荧光信号强,尤其是近端小管上皮细胞E-Cadherin 蛋白表达较强。IR 组GRP78 和CHOP蛋白荧光信号强,在近端小管上皮细胞中呈强阳性表达;E-Cadherin 蛋白荧光信号弱,在近端小管上皮细胞的信号强度明显低于Sham 组。IPO组的GRP78和CHOP蛋白荧光信号较IR 组弱,较Sham 组强;E-Cadherin蛋白的荧光信号介于IR 组和Sham 组之间。另外,在IPO 组还观察到少量远端小管上皮细胞E-Cadherin 蛋白荧光信号较强。上述结果表明,IR 组近端小管上皮细胞内质网应激强度大且细胞凋亡数量多,而IPO 可以减轻肾小管细胞凋亡。见图3、4。
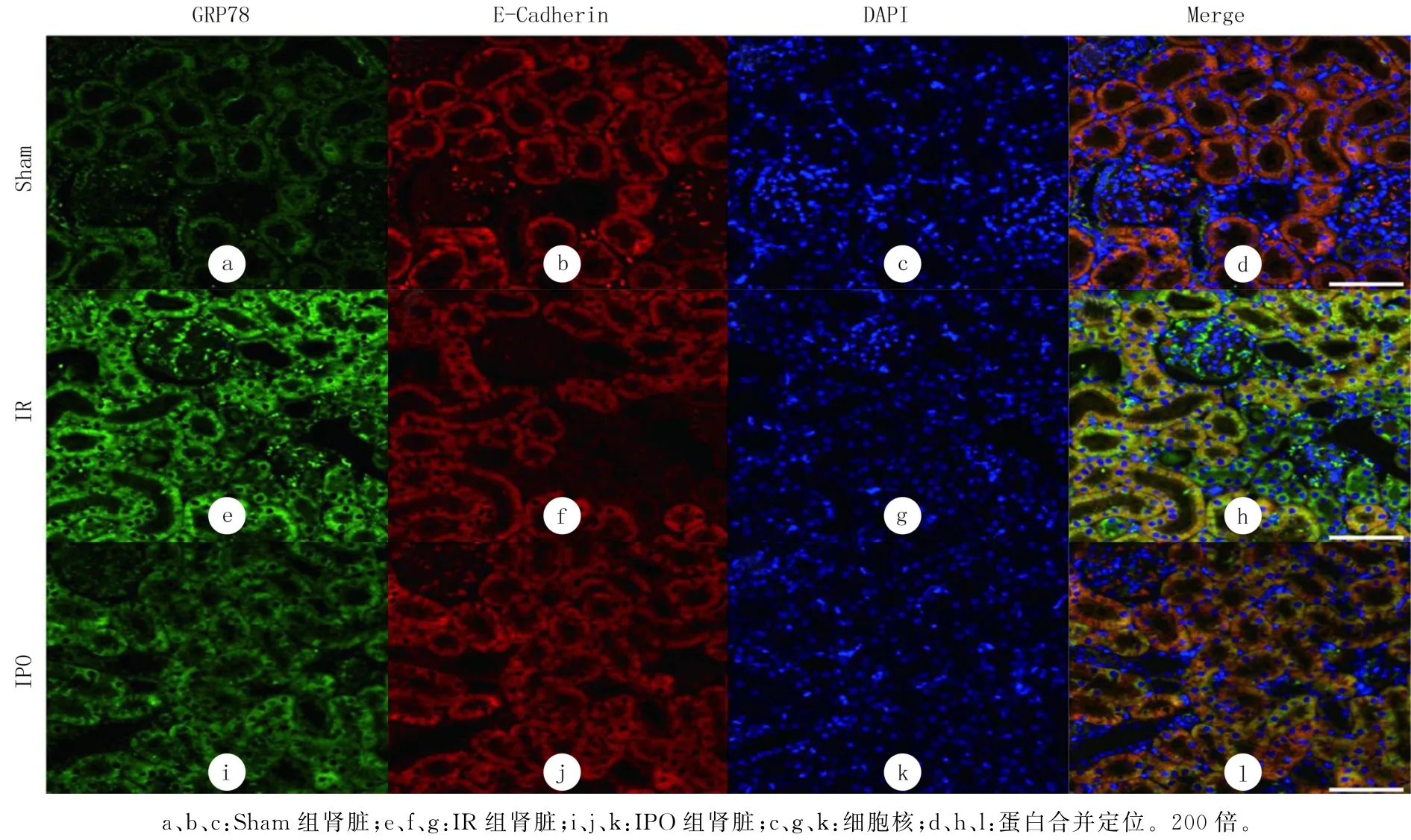
图3 免疫荧光检测各组GRP78和E-Cadherin蛋白表达

图4 免疫荧光检测各组CHOP和E-Cadherin蛋白表达
3 讨 论
本实验通过建立大鼠肾缺血再灌注模型,并给予IPO,探讨IPO 对缺血再灌注损伤的保护作用及机制。为保证动物实验模型的有效性,对各组肾功能指标(血清肌酐和尿素氮)及肾组织形态的变化进行了观察,结果显示,血清肌酐和尿素氮的浓度在各组的表达变化明显,IR 组明显高于Sham 组,IPO组明显低于IR 组,提示大鼠再灌注损伤后肾小球滤过功能严重下降,IPO 可使滤过功能得以改善。光镜下观察和肾小管损伤评分分析显示,相对于正常组织形态的Sham 组,IR 组近端小管上皮细胞肿胀明显,出现大量空泡,并有大量上皮细胞脱落到管腔内,肾小管损伤严重;IPO 组近端小管上皮细胞肿胀轻微,空泡变性较少,肾小管损伤程度比IR 组轻。上述结果表明动物实验建模成功,IPO 可以减少肾小管上皮细胞凋亡,减轻肾组织损伤。
缺血再灌注损伤可致细胞内许多信号转导通路的异常激活,出现级联反应,导致细胞功能障碍和凋亡的发生。Caspase家族是细胞凋亡过程中最重要的蛋白酶。其中Caspase12定位于内质网,当内质网过多蛋白积聚时内质网可激活Caspase12,活化Caspase12 可进一步剪切Caspase3[16]。Caspase3为Caspase家族的核心成员,是调节细胞凋亡的关键蛋白酶,因此也被称为“死亡蛋白酶”,是目前已知细胞凋亡最后执行因子,在肿瘤、缺血再灌注损伤等许多疾病的发生发展中发挥重要作用[17]。Cleaved Caspase3是Caspase3活化过程中经剪切产生的活性片段,其表达水平可以反映Caspase3的活性和细胞凋亡情况[18]。
本实验对Cleaved Caspase3蛋白进行免疫组织化学和Western blotting检测,并采用TUNEL 染色对细胞凋亡的情况进行分析。3种技术检测得到的结果一致。Sham 组近端小管上皮细胞胞质有极少Cleaved Caspase3蛋白阳性表达,黄色颗粒极少,TUNEL染色阳性表达也非常弱,属于正常生理性的细胞凋亡;IR 组大量近端小管上皮细胞胞质中Cleaved Caspase3蛋白高表达,棕褐色颗粒在近端小管上皮细胞胞质分布广泛,TUNEL 染色呈强阳性表达;IPO 组近端小管上皮细胞胞质中有少量Cleaved Caspase3蛋白阳性表达,褐色颗粒稀少,表达量介于Sham 组和IR 组之间,TUNEL 染色有少量阳性表达。表明肾脏缺血再灌注后发生损伤,Caspase3被激活,启动细胞凋亡,使近端小管上皮细胞大量凋亡;但IPO 抑制了Caspase3的激活,减弱了缺血再灌注后肾小管上皮细胞的凋亡,对缺血再灌注损伤具有保护作用。
本实验采用免疫荧光技术检测了内质网应激调节因子GRP78 和CHOP 蛋白以及上皮标志物ECadherin蛋白的表达。GRP78 是一种内质网上的多功能钙结合蛋白,在内质网蛋白质合成、内质网稳态维持、细胞信号控制、细胞生存等多方面起着关键作用[19]。在应激过程中,作为内质网分子伴侣及钙结合蛋白,过表达的GRP78可与错误折叠或未折叠蛋白的疏水性残基端以及钙离子结合,减少内质网上错误折叠或未折叠蛋白的积累并维持钙离子平衡,恢复内质网生理功能;此外,GRP78作为内质网应激标志蛋白,可与内质网应激激活的促凋亡受体结合,抑制其信号转导,从而保护细胞,维持机体内环境稳态[20]。CHOP 作为核转录因子可抑制抗凋亡基因Bcl-2表达,促进Bim、PUMA、TRB3等多种凋亡相关基因表达,诱导细胞凋亡[21]。E-Cadherin是钙黏附蛋白分子家族中跨膜蛋白亚型的一种,主要分布于上皮组织中,对维持上皮细胞的形态和结构完整性起着重要作用。作为上皮细胞间彼此连接的主要蛋白,E-Cadherin在正常细胞组织中保持高表达,从而维持细胞之间的聚集功能;若其低表达,则表明细胞的完整性受损[22]。本实验观察到,Sham 组近端小管上皮细胞中几乎没有GRP78和CHOP蛋白荧光信号,而E-Cadherin蛋白荧光信号较强;IR 组近端小管上皮细胞中GRP78和CHOP蛋白荧光信号增强,而E-Cadherin蛋白荧光信号减弱;IPO 组近端小管上皮细胞中GRP78、CHOP 和E-Cadherin蛋白的荧光信号强度介于Sham 组和IR 组之间。上述结果表明,缺血再灌注损伤后,内质网应激发生并处于持续应激状态,细胞黏着连接受损严重;IPO 后内质网应激反应减弱,上皮细胞间的连接增强。
综上所述,缺血再灌注可以引起内质网应激因子GRP78、CHOP 在肾小管上皮细胞中高表达,激活Cleaved Caspase3,诱导上皮细胞大量凋亡,从而导致急性肾损伤,使肾功能受损;IPO 能够抑制缺血再灌注所致的内质网应激因子的表达,阻止细胞凋亡,减轻肾损伤。IPO 作用的发挥与抑制内质网应激强度有关,IPO 可通过降低内质网应激反应,稳定肾小管上皮细胞结构,减少细胞凋亡,从而减轻因缺血再灌注损伤造成的肾小管上皮细胞功能障碍或丧失,减轻缺血再灌注后肾组织损伤。

