加温CO2气腹对机器人辅助全膀胱切除术患者体温的影响研究
陈国立 黄一乐 陈哲颖
(上海交通大学医学院附属仁济医院,上海 200127)
核心体温是指机体深部重要脏器的温度,正常人核心体温为36.5~37.5°C,围术期低体温是指围手术期由于各种原因导致患者非控制性的体温下降,致使机体核心体温低于36°C的现象[1]。围术期低体温发生率高,影响因素多,手术患者发生围术期低体温可能会导致患者术后复苏时间延长,出现术后疼痛、凝血功能异常、心律失常及切口感染等一些列并发症[2]。根治性全膀胱切除术及尿道改流是治疗膀胱癌最为有效的方式,而机器人辅助全膀胱切除术(Robot-assisted radical cystectomy,RARC)代表了膀胱癌根治术的最高新技术和前沿水平,近十余年来其手术量不断增加[3]。机器人辅助全膀胱切除术手术时间和气腹时间远高于一般腔镜手术,有研究[4]表明长时间使用低于生理温度的21°C的CO2建立气腹,会导致患者围术期低体温发生率增加,因此本研究在常规保暖的基础上,将注入腹腔的CO2气体加温至生理温度37 °C,然后比较2种不同的CO2气腹温度对机器人辅助全膀胱切除术患者术中低体温、术后寒战、热舒适度及其他并发症的影响,现报告如下。
1 资料与方法
1.1一般资料 选取2018年8月-2020年8月于上海交通大学医学院附属仁济医院行机器人辅助全膀胱切除术的患者240例作为研究对象,将其随机分为观察组和对照组各120例。纳入标准:(1)年龄≥50岁。(2)意识清晰。(3)无智力障碍。(4)麻醉ASA分级为1~2级,无全身麻醉禁忌证。(5)无明显心肝肺等系统疾病。(6)无精神、神经疾病。排除标准:既往有甲状腺疾病及甲状腺手术史患者。本研究经医院伦理委员会审查通过。
1.2干预方法 2组均采用相同保温措施接入手术间,手术间温度控制在23~24°C,湿度控制在30%~60%;2组均采用静脉呼吸复合麻醉,运用多功能监护仪监测患者心率、血压、呼吸、氧饱和度等,呼气末P(CO2)维持在30~40 mmHg(1 mmHg≈0.133 kPa);2组均采用同一组达芬奇机器人手术系统,手术由同一组医生进行,术中气腹压力维持在12 mmHg,流量15 L/min,输液加温至37°C;观察组采用带有加温模块的Storz气腹机将加温至37°C的CO2气体注入腹腔,对照组将常温21°C的CO2气体注入腹腔建立气腹。
1.3观察指标及资料收集方法
1.3.1核心体温 测量鼻咽温,测温导管的放置深度为鼻翼到同侧下颌角的距离,测量麻醉诱导后即刻(T1),气腹注入时(T2),气腹注入20 min(T3),40 min(T4),60 min(T5),90 min(T6),120 min(T7),180 min(T8),240 min(T9)气腹结束时(T10),手术结束时(T11)共11个时间点的体温。
1.3.2术后寒战 术后寒战测量方法为巡回护士在麻醉苏醒期进行测量。寒战等级根据 Wrench等[5]提出的划分标准分为 5 级,0 级为没有寒战;1 级为竖毛或(和)外周血管收缩或(和)外周青紫,但无肉眼可见寒战;2 级为仅1组肌群颤抖;3 级为超过一组肌群颤抖;4 级为全身颤抖。当寒战级别为 1 级及 1级以上时,视为患者出现寒战。
1.3.3热舒适度 热舒适度的测量方法为在患者出复苏室前进行测量,采用Wanger等[6]制定的热舒适度评分标准评定,巡回护士使用长约10 cm的标尺,一面标有10个刻度,两端分别为“0”分端和“10”分端,要求患者指出其术后热舒适度,0分为很冷,10分代表非常热,中间位置的5分为热舒适。
1.4统计学方法 利用SPSS 22.0进行数据录入与分析,分析包括描述性统计分析,计数资料采用例描述,计量资料采用均数和标准差进行描述,组间比较采用t检验,卡方检验或者非参数检验。全部检验均为双侧检验,P<0.05 时有统计学意义。
2 结果
2.12组一般资料 对照组共120例,其中男性57例,女性63例,平均年龄64.9岁,平均体质量指数为25.27,平均手术时间347.90 min,平均麻醉时间400.75 min,平均气腹时长207.30 min;观察组共120例,男性51例,女性69例,平均年龄65.1岁,平均体质量指数为23.42,平均手术时长为366 min,平均麻醉时长为405.00 min,平均气腹时长为225.20 min;2组患者一般资料比较差别均无统计学意义(P>0.05)
2.2患者术中体温观察指标比较 患者术中及术后低体温发生情况的比较,见表1;患者术中各阶段体温情况比较,见表2。
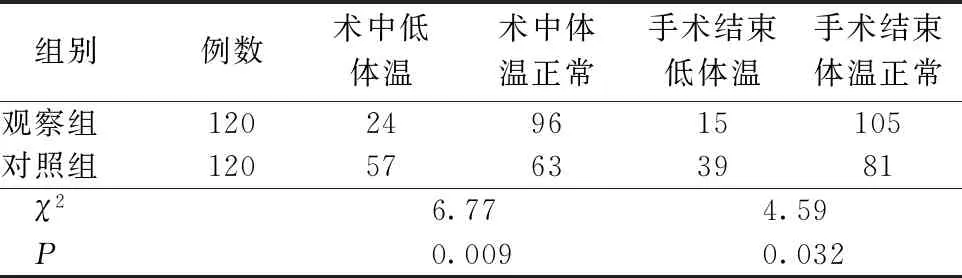
表1 患者术中及术后低体温发生情况的比较 例

表2 2组患者术中各阶段体温情况比较 °C
2.3患者术中及术后观察指标比较 见表3。

表3 患者术中术后观察指标比较
3 讨论
3.1加温CO2气腹有利于维持RARC患者术中体温稳定,减少术中低体温的发生 围术期低体温作为麻醉和外科手术常见的并发症,2017年全国部分地区横断面调查报道的数据为44.5%[7],低体温的发生影响因素众多,包括患者自身因素,手术相关因素,麻醉相关因素,环境相关因素以及是否采取人为干预等等,手术患者低体温的发生往往是多种因素共同作用的结果[1-2]。机器人辅助全膀胱切除术患者具有手术时间长,气腹时间长及手术难度高的特点,致使其围术期并发症的发生率要高于一般腔镜手术,围术期低体温的问题则更加明显[8]。CO2作为一种惰性气体,具有良好的组织和血液可溶性,临床上通常在腹腔镜手术中用来建立气腹,为满足手术需要,机器人辅助全膀胱切除术中需要更多的CO2气体用于维持清晰的术野和操作空间,大量的热量从温度较高的人体传导至温度较低的CO2气腹,致使机体热量流失,从而导致低体温的发生。本研究将CO2气体加温至生理温度37 °C后注入腹腔,患者术中低体温的发生率显著下降,与国外Dean[9]的研究结果一致。同时,本研究结果发现,RARC患者术中体温会经历快速下降期,缓慢下降期,平台期和上升期4个阶段,这在Sessler[10]的研究中也得到了证实,观察组和对照组的术中体温变化趋势类似,但是CO2加温组的患者术中体温整体水平高,能够较早地进入体温保持相对稳定的平台期,且平台期的时长与平均体温均高于常温组。因此,加温CO2气腹有利于维持腹腔镜手术患者术中体温稳定,减少术中低体温的发生率,促进患者的预后。
3.2加温CO2气腹能够维持患者术中体温稳定,减少术后寒战的发生,提升患者热舒适度 本研究结果表明,CO2加温组患者术后热舒适度显著高于常温组,这与陈沅等[4]的研究结果相同。热舒适度是外科手术患者对围术期温度感知评价的一个主观指标,在国内的研究较少,国外Perl[11]的调查结果表明,热舒适度是手术患者继疼痛治疗和体位舒适外最关心的护理问题,患者围术期热舒适度高有利于提高患者围术期护理满意度。手术患者术中体温大幅度波动,术后复苏期间仍处于低体温状态,术后寒战的发生均是影响患者术后热舒适度的不利影响因素。本研究的结果显示,CO2加温组患者术中体温下降幅度小,郎荣蓉[12]通过在新生儿及小婴儿腹腔镜手术中注入加温CO2气体,发现加温CO2气腹有利于维持患儿体温恒定,与本研究的结果一致。同时,本研究还显示,CO2加温组患者手术结束时仍为低体温的发生率显著低于常温组,术后寒战的发生率显著低于常温组。寒战是外科手术患者术后常见的并发症,大多数是由于患者术后体温过低引起,患者寒战的同时会产生不适感,导致机体做工,增加心脏负担,使得机体的耗氧量与CO2的产生量增加,易引发患者发生酸中毒,导致手术部位感染发生的风险增加,甚至造成机体更严重的损伤[13]。加温CO2气腹可以通过维持患者术中体温恒定,减少手术结束时体温不升与术后寒战的发生率,从而提高患者的热舒适度,确保围术期患者安全,提升手术室护理满意度。目前临床上普遍采用的保温措施包括术前预保温,术中控制室温,输血输液加温以及充气式加温毯和循环水毯等主动加温设施,而CO2气腹作为一种经济有效的保温方式并未引起足够的重视。因此手术室护士在术前访视时应识别出危重患者及需要长时间建立气腹等高危患者,术中应采取多模式保温措施联合使用,在做好常规被动保温和主动加温措施的基础上,重视建立气腹的CO2的温度管理,在气腹正式建立前预先将CO2加温至37°C,从而减少气体交换造成患者的热量损失,维持患者术中体温稳定,减少围术期低体温及相关并发症的发生。 本研究旨在观察加温CO2气腹对RARC患者术中体温、术后寒战、热舒适度的影响,样本量较小且手术类型单一,领还需大样本的数据进行验证。本研究结果提示:加温CO2气腹能够减少机器人辅助全膀胱切除术患者术中低体温和术后寒战的发生。提高患者的热舒适度,建议手术室护理人员将加温CO2气腹与其它加温措施联合使用,维持患者体温稳定,保障围术期患者安全。

