银硫二元掺杂聚合氮化碳光催化快速降解四环素
宋继梅,朱婉蓉,汪旭乐,王文媛,杨 捷,裴泽平
(安徽大学 化学化工学院,安徽 合肥 230601)
抗生素被广泛用于治疗各种人畜疾病,生物体吸收代谢后多数以原型排出.环境中抗生素难以生物降解,高效去除环境中的抗生素已经成为环境治理的重要研究课题.四环素(tetracycline)作为典型的抗生素,在人类健康、畜牧和农业等领域已经使用了半个多世纪,生产和使用量仅次于磺胺类抗菌药物.由于四环素具有强毒性、高水溶性、持久性、致癌性以及可诱导病原体产生耐药性,所以进入环境后会严重影响人类健康和生态平衡.因此,迫切需要一种有效的、经济的技术降解四环素.研究发现,光催化技术是降解环境污染物的有效办法.众所周知,光催化剂催化降解反应主要涉及下列过程:(1)催化剂吸收光能产生电子-空穴对;(2)电子-空穴对进行分离和迁移;(3)发生氧化还原反应,降解有机污染物.因此要想提高光催化活性需要从以上几个方面进行改进.
类石墨状氮化碳(g-CN)具有合成方便、带隙较窄和结构稳定等特点,在析氢、析氧、环境修复、二氧化碳减排、污染物降解等方面受到越来越多的关注.然而,g-CN的光催化活性较低,主要表现为可见光利用率低、光生电子-空穴对易复合.因此,提升g-CN的光催化效率,成为研究者关注的焦点.
非金属掺杂能够通过调节带隙结构、增强可见光的利用率、增加载流子的转移率和创造更多活性位点来提升光催化效率.研究发现,硫元素掺杂能够调节催化剂能带位置、扩宽光响应范围、提高光生电子的电导率、迁移率和分离度以及使相邻碳原子兼有电子受体和电子给予体的双重作用.Wang等利用硫元素掺杂g-CN并复合TiO,构建复合型光催化剂,于60 min内实现了刚果红的完全降解.
贵金属掺杂能够改善催化剂的导电性能,有利于电荷载流子的转移和传输.金属Ag的制备简单、化学稳定性好,常常被负载于催化剂表面,能够促进光生电子和空穴的转移.另外,Ag具有等离子体(surface plasmon resonance, 简称SPR)效应,可提高和改善催化剂对可见光的吸收利用.Li等报道,当Ag,Au,Pd等贵金属沉积在介孔g-CN上,温度低于20 ℃时,也可以在120 min内完全降解甲醛.宋亚丽等发现光还原法制备的Ag/g-CN催化剂降解磺胺甲恶唑所需时间比g-CN缩短了3.12倍.
笔者成功制备了Ag沉积的S掺杂的g-CN光催化剂(Ag-S-CN),对其化学成分、物相结构、光-电学性能等进行了详细表征.可见光照射下,Ag-S-CN催化剂对四环素、卡马西平、罗丹明B和甲基橙均可在较短时间内完全降解.根据紫外可见吸收光谱、粉末固体荧光光谱和光电化学性能等测试结果,提出了Ag-S-CN催化剂在可见光下可能的光催化降解污染物的反应机制.
1 实验部分
1.1 催化剂的制备
以三聚氰胺为原料制备g-CN,用硫代乙酰胺和硝酸银作为硫源和银源进行掺杂改性.具体操作如下:分别称取0.100 0 g三聚氰胺和1 mg硫代乙酰胺,550 ℃下煅烧4 h.冷却,水洗、醇洗各3次,离心,干燥,收集灰黑色样品,研磨待用,产物记为S-CN.g-CN的制备方法同上,只是不添加硫代乙酰胺.
采用简单的光还原法在硫掺杂的类石墨氮化碳(S-CN)中沉积银单质(Ag).具体方法如下:分别称取0.1 g S-CN粉末和不同质量的AgNO,溶于100 mL蒸馏水中.磁力搅拌10 min,置于300 W氙灯下照射0.5 h.离心,反复洗涤,沉淀置于60 ℃烘箱中干燥12 h.所得样品记为Ag-S-CN,其中x
表示复合物中加入AgNO的质量(x
= 1,2,3,4(mg)).1.2 催化剂的表征
采用X射线衍射仪(XRD),在Cu-K
α辐照下,2θ
=10°~60°范围内扫描,表征催化剂的物相和结构.利用N吸附/解吸表面积分析仪(美国麦克,ASAP2460),进行比表面积Brunauer-Emmette-Teller(BET)测量.利用FTIR分光光度计(德国布鲁克,Nicolet 380)测定催化剂的傅里叶变换红外光谱,波数范围2 000~400 cm.采用Axis Ultra DLD X射线光电子能谱仪(XPS,美国热电公司),以Al-K
α线单色源(hv
= 1 486.69 eV)为光源,以284.8 eV的C1s峰作为参考,对催化剂的元素组成及价态进行分析.采用铂电极、ITO玻璃(15 mm × 15 mm × 1.1 mm)、Ag/AgCl电极分别作为对电极、工作电极和参比电极,用100 mL 0.5 mol·LNaSO(pH 6.8)溶液作为电解质溶液,在此三电极体系下通过电化学工作站(IM6ex,德国Zahner),测定催化剂的光-电学性质(瞬态光电流,电化学阻抗,LSV).用日立S-4800冷场发射扫描电子显微镜获得光催化剂的能量色散X射线能谱(EDX)和元素映射图(Mapping).将相同质量的样品用固体粉末荧光光谱(HORIBA JOBIN YVON)来测定催化剂的荧光.1.3 光催化降解实验
称取50 mg催化剂,分散在100 mL 污染物的水溶液中.黑暗下搅拌0.5 h,达到吸附和脱附平衡.光照,每隔10 min取5 mL分散液,离心,取上清液,用UV-Vis分光光度计检测溶液中残留污染物的浓度A
(A
=Kbc
,其中K
为摩尔吸光系数,b
为吸收层厚度,c
为吸光物质的浓度).污染物的降解率D
依下式计算:D
=(c
-c
)/c
×100 %,其中:c
为原溶液中污染物的浓度,c
为不同光照时间后污染物的浓度.2 结果与讨论
2.1 催化剂的物相、结构及成分分析
合成催化剂的X射线衍射花样(XRD),(100)和(002)晶面的衍射峰位置与g-CN的标准卡片(JCSD No.50-1512)如图1所示.

图1 合成催化剂的XRD衍射花样(a)和样品的JCSD标准卡片谱图(b)
由图1可知,合成催化剂的X射线衍射花样(XRD),(100)和(002)晶面的衍射峰位置与g-CN的标准卡片(JCSD No.50-1512)一致.样品S-CN的衍射花样,与纯g-CN的比较,(002)晶面的衍射峰从27.35°位移至27.40°,表明g-CN结构的层间距离有所减小,即硫的掺杂降低了类石墨化氮化碳聚合物的结晶度,改变了其有序排列和层与层之间的相互作用.此外,Ag-S-CN 样品的X射线衍射花样中均出现了(111)晶面的强衍射峰,并且随着x
的增大衍射峰强度逐渐增强,可以指认为Ag(JCPDS No.04-0873).合成催化剂的傅里叶红外光谱如图2所示.

图2 g-C3N4,S-CN,Ag3-S-CN的FT-IR光谱
由图2可以看出,样品g-CN碳氮杂环(C—N和C=N)振动的红外吸收位于1 200~1 700 cm区域,g-CN的特征峰出现在806和889 cm处,分别对应于N—C=N和N—H键的伸缩振动.S-CN位于889 cm处的特征峰在875 cm,可能是由于硫元素的引入(S元素的电负性(2.58)比N(3.04)低)使得g-CN化学键极性发生了变化.Ag-S-CN催化剂的红外吸收峰与S-CN的基本一致.
合成催化剂的元素组成及其含量可以通过EDS测试来确定,结果如图3所示.

图3 Ag3-S-CN的EDS谱(a)和元素映射图(b)
图3(a)表明复合催化剂的组成元素为C,N,O(可能来自表面的水分子或O),Ag,S.S元素含量很低,仅占0.03%.图3(b)是Ag-S-CN催化剂元素映射图,可以看出:催化剂中C,N,Ag,S元素分布均匀,但S元素分布密度较低.
XPS全谱图4(a)表明:g-CN和S-CN催化剂主要由C,N,O 3种元素组成,没有明显的S元素峰出现;Ag-S-CN催化剂的全谱则出现了银的峰.如图4(b)所示,结合能位于368.12,374.23 eV的谱峰分别对应于Ag 3d3/2和Ag 3d5/2,可以指认为Ag.将Ag-S-CN的XPS全谱局部放大,发现有较弱的S元素峰出现.从S 2p高分辨能谱(图4(c))可以看到,164.12,164.75 eV处出现了两组峰,对应于C—S键中的S.图4(d)给出了O 1s的高分辨能谱拟合结果,531.34 eV处的O峰来自催化剂表面吸附的氧,而532.40 eV处的O峰认为是催化剂表面吸附水中的氧.有趣的是,3个样品中都出现了O 1s的峰,且Ag-S-CN样品中的O 1s峰强度最大,意味着g-CN改性后,其表面更加容易吸附O和HO,即Ag-S-CN催化剂吸附氧的能力大大增强了,有利于其光催化活性的改善和提升.

图4 XPS谱图:总谱(g-C3N4, S-CN 和 Ag3-S-CN)(a);Ag3-S-CN催化剂的Ag 3d(b), S 2p(c), O 1s(d)
Ag-S-CN的高分辨透射电镜(HR-TEM)照片如图5所示.可以看见,晶格条纹的间距为0.235 nm,与Ag的(111)晶面的晶格间距一致,表明样品中存在Ag,与XRD的结果一致.综上,Ag沉积的S掺杂的g-CN光催化剂Ag-S-CN被成功合成了.

图5 Ag3-S-CN的高分辨透射电镜(HR-TEM)照片
2.2 光催化降解四环素
图6是不同催化剂对四环素(TC)的降解率随时间变化的折线图.

图6 TC光催化降解曲线
由图6可以看到,光照射70 min,g-CN和S-CN对TC的降解率分别为66.70%和89.80%,而负载银的催化剂Ag-S-CN均大大地提高了四环素的降解率,其中Ag-S-CN只需大约28 min,降解率就达到了100%.显然,Ag-S-CN是降解TC的高效光催化剂.
为进一步探索Ag-S-CN的光催化能力,以Ag-S-CN为催化剂,以甲基橙(MO)、罗丹明B(RhB)和卡马西平(CBZ)为模拟污染物进行光催化降解实验,结果如图7所示.
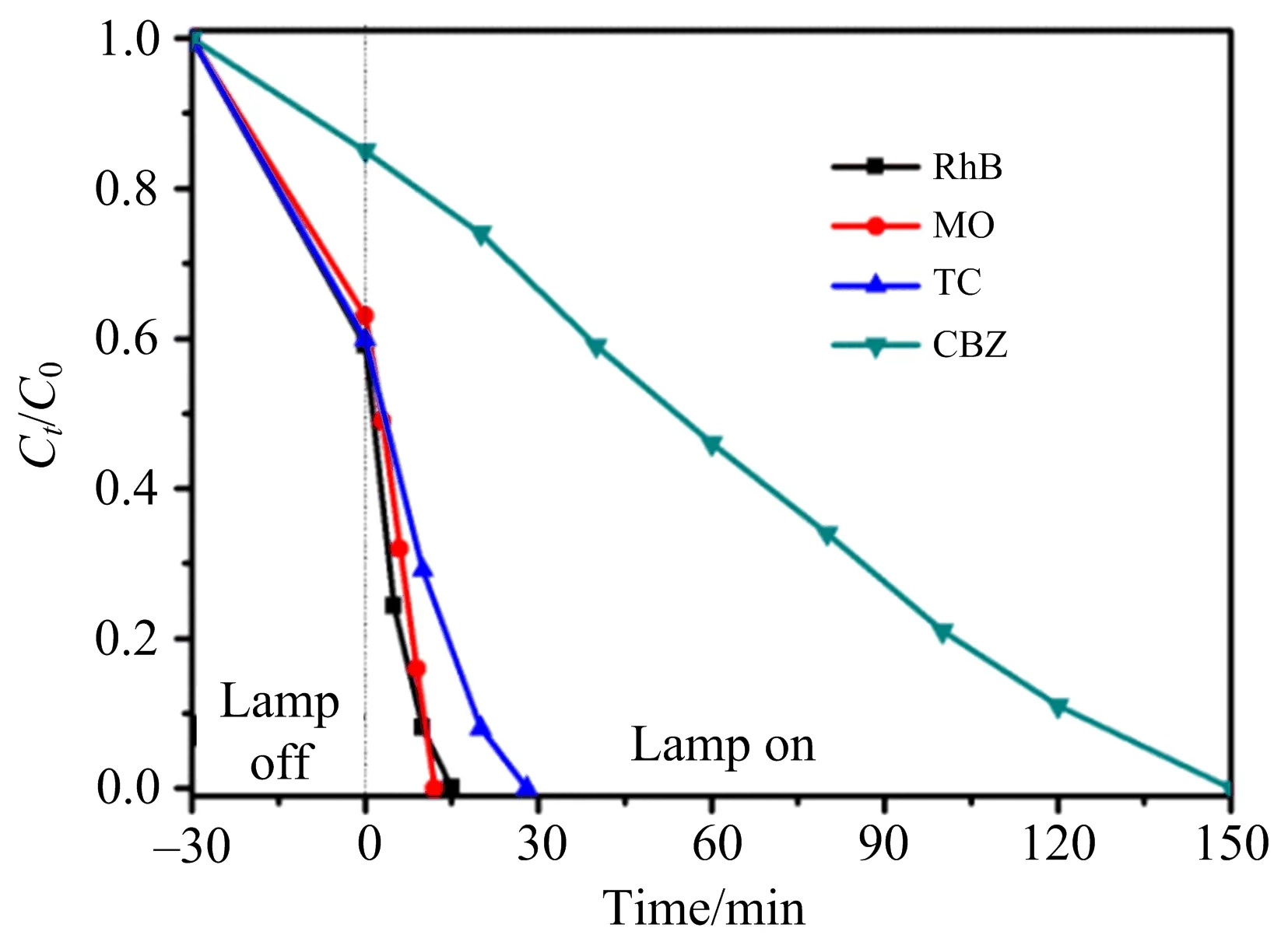
图7 不同污染物的光催化降解曲线
由图7可以看出,Ag-S-CN催化剂对以上3种污染物皆表现出强的降解能力,在很短的时间内,实现了污染物的完全降解((MO 12min)、(RhB 15min)、(CBZ 150min)).综上,Ag-S-CN光催化剂具有优异的光催化活性,可以很好地对难降解污染物进行降解.
2.3 催化剂的光电化学性质
合成催化剂的紫外-可见漫反射光谱、带隙以及XPS谱如图8所示.

图8 g-C3N4、S-CN和Ag3-S-CN的紫外-可见漫反射光谱(a);(αhν)0.5与光能(hν)的关系图(b); g-C3N4和S-CN的XPS价带谱图(c,d)
图8(a)给出了合成催化剂的UV-Vis DRS光谱,S元素的掺杂和Ag的沉积,不仅扩宽了催化剂的可见光区的吸收范围,还提升了可见光的吸收强度(红色和蓝色曲线),就是说复合物Ag-S-CN极大地改善了g-CN催化剂对可见光的吸收和利用.
根据公式(αhv
)=A
(hv
-E
)计算了催化剂的带隙(E
),g-CN、S-CN和Ag-S-CN的E
值分别为1.75,2.25,2.75 eV(图8(b)).催化剂的价带位置可由X射线光电子能谱(XPS)测定.从图8(c)~(d)得知:g-CN的E
为1.60 eV,而S-CN的E
为0.50 eV.根据经验公式E
=E
+E
,确定g-CN的E
位置为-1.15 eV,S-CN的E
位置为-1.75 eV.图9为催化剂的氮气吸附-解吸等温线.

图9 合成催化剂的氮气吸附-解吸等温线
根据图9可知,Ag-S-CN的比表面积约为54.50 m·g,是g-CN(10.15 m·g)的5.37倍,复合光催化剂显著增大了比表面积.大的比表面积意味着有更多的催化反应活性位点,可以使反应物和生成物更好地吸附、反应和扩散,还能够使小分子(如O和HO)更好地渗透.
众所周知,光生电子-空穴对的复合程度越小,意味着催化剂的催化活性越好.图10(a)显示Ag-S-CN具有低的荧光强度,表明Ag-S-CN催化剂的载流子的重组程度低,分离率高.此外,通过光电流响应(PC)、阻抗谱(EIS)、线性扫描伏安曲线(LSV)测试,可以了解催化剂中光生载流子的转移程度.一般而言,PC中光电流密度越高、EIS中弧半径越小以及LSV中电压相同时电流密度越大,催化剂中的电子-空穴对的分离程度越高、重组率越低.从图10(b)~(d)可以发现,Ag-S-CN的光电流强度最高、圆弧半径最小、在电压相同时,Ag-S-CN的电流密度最大.也就是说,Ag-S-CN复合催化剂的构建有利于电子和空穴的分离.

图10 g-C3N4、S-CN和Ag3-S-CN在370 nm激发时的粉末固体荧光谱图(a);模拟阳光照射下0.5 mol·L-1Na2SO4电解质中g-C3N4、S-CN和Ag3-S-CN的瞬态光电流响应(b);EIS Nyquist曲线(c);LSV曲线(d)
2.4 光催化降解污染物反应机制


图11 Ag3-S-CN光催化降解TC反应的活性物种捕获实验结果

综上,笔者提出了Ag-S-CN光催化降解TC反应可能的光催化机制如图12所示.

图12 g-C3N4(a)和S-CN(b)光催化降解TC的反应机制示意图


由于单质银(Ag)具有优良的导电能力、较强的电子存储能力和合适的费米能级,催化剂表面的光生电子可迅速转移至Ag,抑制了电子与空穴的复合,促进了电子-空穴对的分离,Ag-S-CN体系可以产生更多的电子和空穴参与光催化降解污染物的反应.
总之,光生电子(e)激发到催化剂的导带,导带上部分电子可转移并聚集在Ag的表面,价带上则留下空穴(h),实现电子-空穴对的有效分离.由于催化剂的导带的电极电势低,还原性强,光生电子可以直接与氧气反应生成超氧根负离子,进而降解污染物.此外,Ag表面聚集的电子也可与氧气结合,生成超氧根负离子参与污染物的降解.留在价带上的空穴则可以直接氧化目标污染物,从而提升催化剂的催化活性.可能涉及的有关反应如下



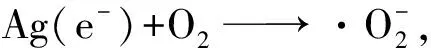

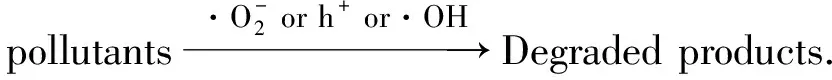
2.5 催化剂的循环稳定性
为评估催化剂的实际应用潜能,对光催化剂的可重复使用率和稳定性进行了测定,结果如图13(a)所示.连续5次循环后,Ag-S-CN光催化降解TC的效率仍高达到98.60%.从图13(b)的XRD衍射花样可以看出,5次反应前后催化剂的衍射峰没有明显变化,表明催化剂结构稳定.因此,复合物Ag-S-CN是高效、循环性好和结构稳定的光催化剂.

图13 Ag3-S-CN光催化降解TC的循环实验结果(a); Ag3-S-CN催化剂降解TC反应前后的XRD衍射花样(b)
3 结束语
(1)Ag沉积在硫掺杂的g-CN上,可实现快速光催化降解有机污染物.
(2)光催化活性增强的原因:Ag-S-CN复合催化剂对可见光吸收范围扩宽、比表面积增大、光生载流子分离能力的增强,S掺杂调节g-CN的能带位置,使得电子与空穴分离率更高,产生的活性物种变多,光催化活性增强.
(3)复合催化剂Ag-S-CN具有良好的循环使用率和较高的结构稳定性,有着很好的应用前景.

