Fe(Ⅱ)活化Na2S2O8-NaClO耦合体系处理垃圾渗滤液生化尾水参数优化及水质特性试验探究
余茂杨 管国安 邱 婷
(乐安县水利局,江西 抚州 344300)
垃圾渗滤液是一种含有高浓度难降解有机物、高浓度氨氮、成分异常复杂的液态有机污染物,处理不当会严重威胁周围水环境安全[1-2]。由于生物法具有高效、低廉、处理流程简单等优点,因此被当做渗滤液最理想的处理手段[3]。随着填埋时间的延长,渗滤液中C、N、P元素的比例失调,可生化性降低。仅采用生化法处理,最终不能达标排放,需进一步深度处理[4]。
在常温条件下,过硫酸盐较稳定,需借助光、过渡金属离子等活化手段,活化过硫酸盐生成SO4-,因具有对污染目标氧化性强、选择性低等优点而受到广泛关注。研究证明SO4-能将大多数污染有机物氧化,最终生成CO2和无机酸。同时Fe(Ⅱ)因高效易得、廉价无毒,在常温条件下就能够活化过硫酸盐而备受瞩目。大量研究证明SO42-自由基对于污染水体中氨氮处理往往达不到预期效果,去除率一般只有30%左右[5]。很多研究者发现NaClO溶于水会生成NaOH和HOCl,其中HOCl能够与水体中NH4+反应生成N2,同时生成的NaOH会升高水体pH值,发生氨吹脱反应。然而NaClO作为氧化剂对于污染有机物进攻方面有欠缺[6-7]。利用2种氧化剂(NaClO、Na2S2O8)处理污染的种类的差异进行耦合,能够巧妙的避开各自缺陷[8-9],耦合后的体系对COD和氨氮都有较高的去除率,从而达到高效、经济的处理污染水体目的,同时2种氧化剂(NaClO、Na2S2O8)在Fe(Ⅱ)的催化下,具有一定的协同作用。利用Fe(Ⅱ)活化Na2S2O8-NaClO体系处理垃圾渗滤液生化尾水,优化相关参数,进行水质分析,有为渗滤液生化出水治理寻找新的思路,同时有为其他污水处理提供参考的学术意义和实用价值。
1 试验材料与方法
1.1 试验水样
试验所用垃圾渗滤液取自江西省南昌市某垃圾填埋场渗滤液的生化尾水,渗滤液颜色呈深褐色,主要是由于渗滤液中大部分有机化合物都含有高浓度的腐殖质,有明显恶臭,其水质指标情况见表1。

表1 渗滤液生化尾水水质
1.2 试验药品与仪器
主要药品:过硫酸钠,分析纯,天津市恒兴化学试剂制造有限公司;纳米零价铁,分析纯,上海试剂化学有限公司;稀盐酸,分析纯,南昌赣江盐酸化工厂;氢氧化钠,分析纯,南昌赣江盐酸化工厂。
主要仪器:微波密闭消解COD速测仪,型号为Galanz-WMX,汕头市环海工程总公司生产;分光光度计,型号为GC126N,上海仪电分析仪器有限公司生产;气相色谱—质谱联用分析仪,型号为Agilent7890A-5975C,美国Perkin Elmer公司生产。
1.3 试验方法
烧杯试验:取6个容积为250 mL的锥形瓶,分别标为1~6号。在每个锥形瓶中加入100 mL垃圾渗滤液生化尾水,采用稀HCl和NaOH调节水样pH。依次添加氧化剂Na2S2O8、NaClO和催化剂Fe(Ⅱ)放在恒温水浴振荡器(控制氧化体系反应温度)中进行反应。反应一定时间后,取水样置于离心机中(转速3000 r/min)进行离心20 min,取离心后上清液进行水质水样分析。
2 试验结果与分析
2.1 pH对氧化效果的影响
在常温状态下,当Fe(Ⅱ)投加量为0.3 g/L,氧化剂Na2S2O8投加量为2.5 g/L,NaClO投加量为40 mL/L(有效氯为>10%),pH值为4、6、8、10、12时氧化体系效果如图1(a)所示。
由图1(a)可以看出,在试验pH范围内,随着水样pH的增大,COD去除率先缓慢增加,然后开始减小,在pH=5左右效果最佳,此时去除率为82%左右。这是因为随着pH值的增大,Fe(Ⅱ)会发生沉淀反应,会使游离态的Fe(Ⅱ)浓度降低,导致下列反应:Fe(Ⅱ)+S2O82-→Fe3++SO4-·+SO42-和Fe(Ⅱ)+HClO→Fe3+HO+Cl-,生成的自由基浓度也减少,表现为COD去除率下降[10],影响催化氧化效果。对于氨氮去除率而言,随着pH值的增大,氨氮去除率缓慢增加最后趋于平缓,在pH=7时达到最高,此时氨氮去除率为91%。继续增大pH值不会出现COD那样大幅度降低,这是因为根据反应式1.5NaClO+NH3→0.5N2+1.5NaCl+1.5H2O可知,水体中pH越大越有利于氨氮的去除,但是过高pH不利于HClO的生成,在试验范围内认为pH=6为最佳pH[11-12]。
2.2 催化剂Fe(Ⅱ)对氧化体系的影响
调节水样初始pH=6,Na2S2O8投加量为2.5 g/L,NaClO投加量为40 mL/L(有效氯为>10%)时,不同Fe(Ⅱ)投加量氧化效果如图1(b)。
由图1(b)可以看出,对于COD而言,在催化剂Fe(Ⅱ)投加量由0.1 g/L增大到0.3 g/L时,COD去除率由43%增加到82%,继续增加投加量,COD去除效果略微下降,这是因为过量的Fe(Ⅱ)投加会与自由基发生竞争反应,进一步恶化氧化体系。对于氨氮而言,和COD的去除趋势存在一定差异,随着Fe(Ⅱ)投加量的增加,去除率先快速增加后增速放缓最终趋于平缓,而不是表现为最终略微下降。这是因为当Fe(Ⅱ)投加量时,氧化水体中Fe(Ⅱ)的浓度急剧升高,会发生下列反应:SO4-·+Fe(Ⅱ)→SO42-+Fe3+和HO·+Fe(Ⅱ)→H2O+Fe3+,,导致SO4-·和HO·的被恶性消耗,表现为COD的去除率下降。对于氨氮而言,上式反应式中生成的Fe(Ⅲ)会与水体中氨氮发生络合反应[13-14]。
2.3 氧化剂Na2S2O8对氧化体系的影响
调节水样初始pH=6,当Fe(Ⅱ)投加量为0.3 g/L,NaClO投加量为40 mL/L(有效氯为>10%)时,不同Na2S2O8投加量氧化效果如图1(c)。
由图1(c)可以看出,随着过硫酸钠的投加量增加,氨氮与COD的去除率均逐渐上升,最后趋于平缓,因为过硫酸钠的投加量直接影响体系中SO4-·浓度,随着过硫酸钠投加量的增加,水体中SO4-·浓度也升高,大大增加自由基(SO4-·,HO·)与目标污染物的接触概率,致使COD和氨氮的去除率升高。上图的趋势图可以看出,过硫酸钠的投加量由1.0 g/L上升到3.0 g/L时,氨氮的去除率增幅为22%,COD的去除率增幅为50%[15]。COD的增幅明显大于氨氮的增幅,这证明了氧化剂过硫酸钠的投加量的增加更加有利于COD的去除。实际应用中考虑到渗滤液生化出水水质波动这一重要因素,当出水水质COD和氨氮为800 mg/L~1200 mg/L和90 mg/L~130 mg/L时,氧化剂Na2S2O8投加量选用2.5 g/L为宜。
2.4 氧化剂NaClO对氧化体系的影响
调节水样初始pH=6,当Fe(Ⅱ)投加量为0.3 g/L,Na2S2O8投加量为2.5 g/L时,不同NaClO投加量氧化效果如图1(d)。
由图1(d)可以看出,随着NaClO投加量的增加,氧化体系中COD和氨氮的去除率在NaClO投加量40ml的时候迅速增加,这是因为在反应初期NaClO的投加直接决定了体系中HO·和[O]的浓度(Fe(Ⅱ)+NaClO→Fe3++NaCl+[O];Fe(Ⅱ)+HClO→Fe3+HO·+Cl-),体系中HO·和[O]的浓度升高有利于增加氨氮和COD的去除效果[16]。继续投加NaClO,氧化效果不再显著上升,这可能是因为体系中催化剂(Fe(Ⅱ))达到了饱和,不再随着氧化剂的投加而大幅度改善氧化效果。上图也可以明显看出,NaClO投加量从10 mL到40 mL时,COD的去除率从62%上升到81%,增幅为19%;氨氮的去除率从31%上升到92%,增幅为61%。氨氮的增幅明显高于COD的去除率,这可能是因为氨氮可以与NaClO发生2NH3+3NaClO→N2+3H2O+3NaCl,致使体系中氨氮得到大量去除[17]。
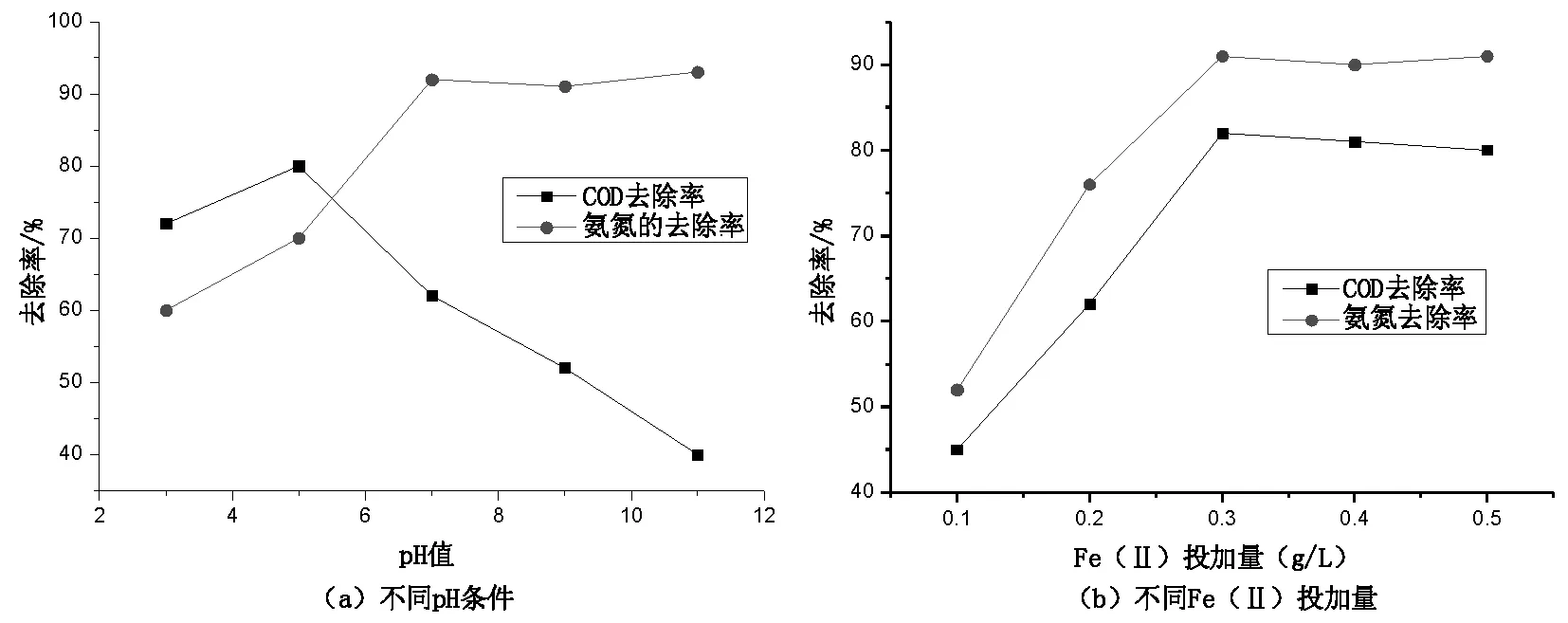
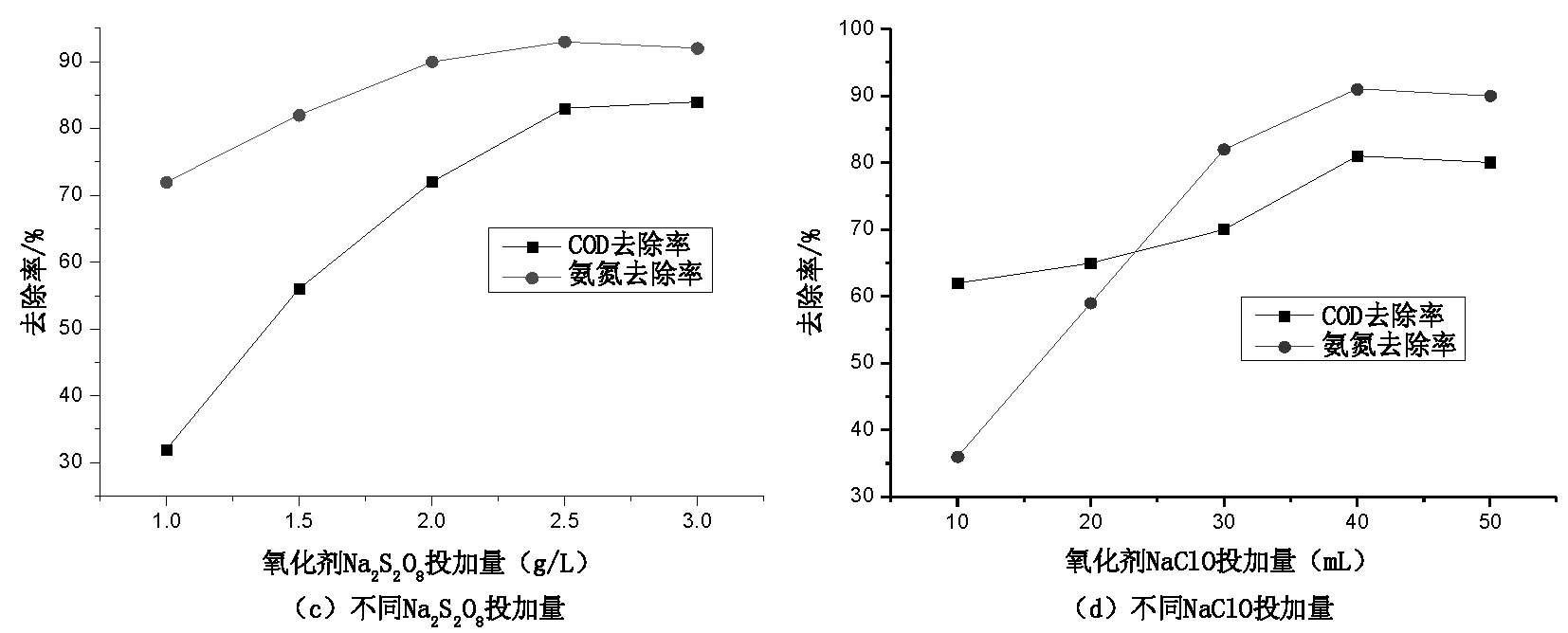
图1 不同条件下氧化效果
2.5 氧化前后GC-MS分析图
为了进一步研究处理前后水质变化,采用GC-MS对处理前后水样中有机物组分进行定性分析。
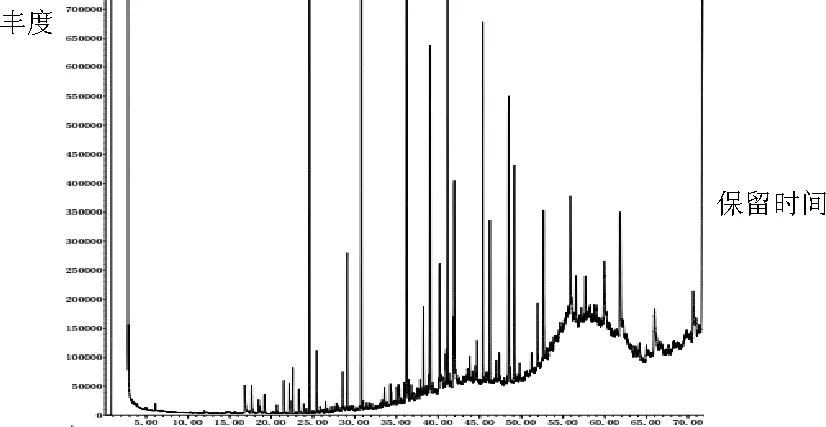
图2-5 处理前水样氧化降解产物分析
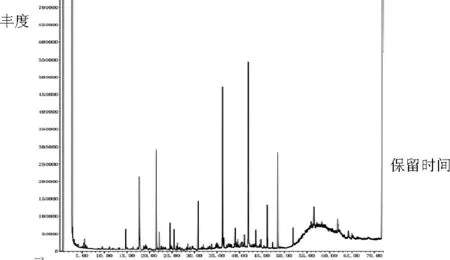
图2-6 处理后水样氧化降解产物分析
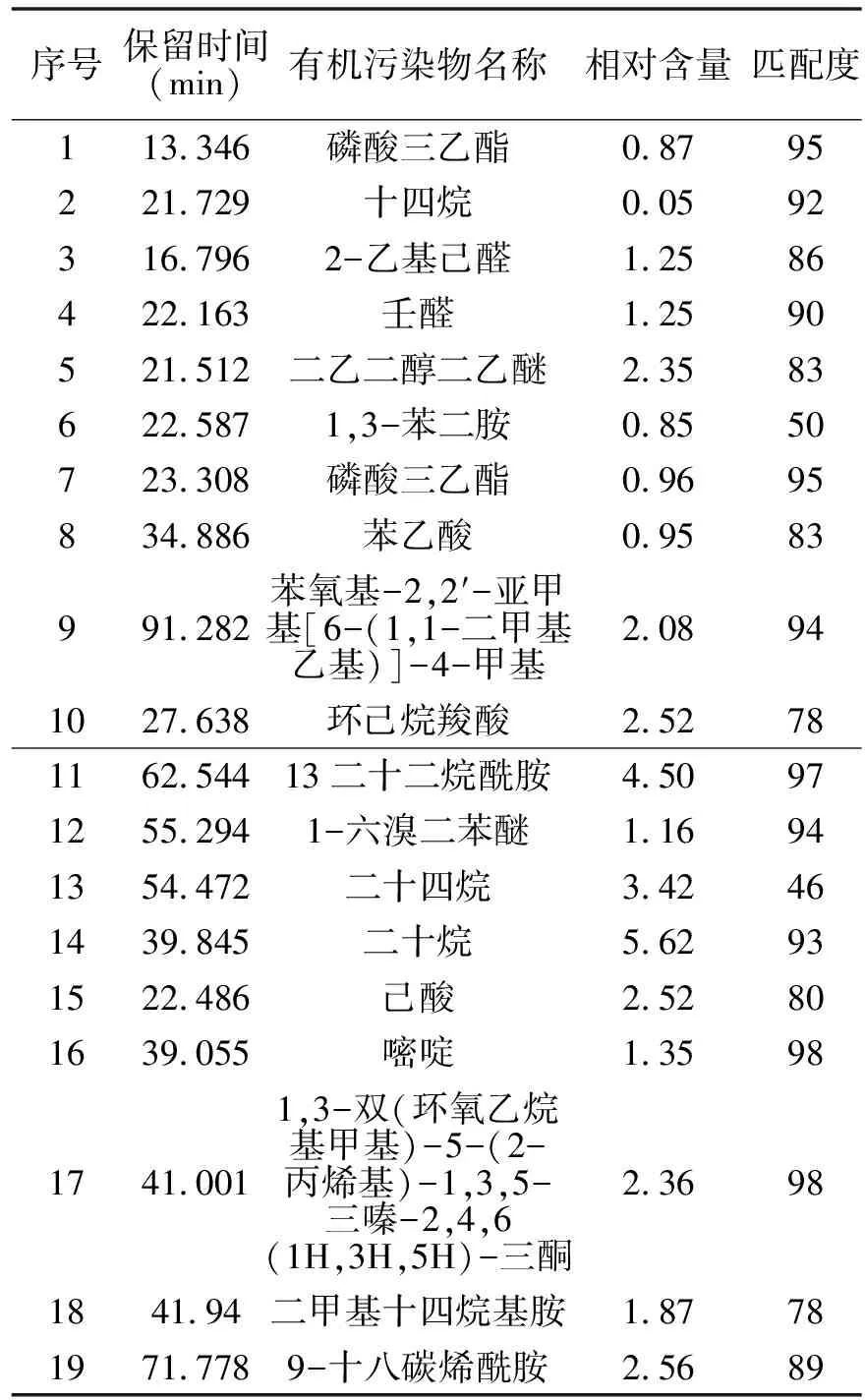
表2 处理前GC-MS主要特征峰分析
图2-5可以看出,垃圾渗滤液生化尾水有机组分复杂,GC-MS显现很多特征峰,同样渗滤液生化尾水中有污染物成分种类繁多而且结构复杂,在出峰时导致特征峰重叠,与NIST05 谱库难以匹配。未处理水样中与谱库相匹配的主要有机物见表2中,可以看出渗滤液生化尾水中主要的有机污染物是分子量大、芳香性高的烷烃类、芳烃类、酯醚。经Fe(Ⅱ)活化Na2S2O8-NaClO体系处理后出水特征峰明显减少,表明有一部分污染有机物被自由基所氧化,与COD和氨氮的去除结论一致[18-19]。
3 结论
本文利用Fe(Ⅱ)活化Na2S2O8-NaClO工艺处理垃圾渗滤液生化尾水进行单因素优化试验和采用GC-MS方法分析系统最优条件下处理前后水样中有机物组分,得到如下结论:
(1)利用Fe(Ⅱ)催化Na2S2O8-NaClO体系深度处理垃圾渗滤液生化尾水有理想的去除效果,通过优化单因素试验得出结论:催化剂Fe(Ⅱ)投加量为0.3 g/L、Na2S2O8投加量为2.5 g/L、NaClO投加量为40 mL/L(有效氯为>10%)、水样pH为6时,COD和氨氮的去除率分别为82%和91%。
(2)采用GC-MS分析技术对Fe(Ⅱ)催化Na2S2O8-NaClO体系处理垃圾渗滤液生化尾水的氧化效果进行了分析。结果表明:经过Fe(Ⅱ)催化Na2S2O8-NaClO体系处理后的废水中有机污染物的种类大幅度降低,结构复杂程度也有所降低。

