针刺联合中药对肥胖型多囊卵巢综合征患者肠道菌群、糖脂代谢及炎症因子水平的影响
李东海,李永攀,王雪
(1.宣城市人民医院中医科,安徽 宣城 242000;2.安徽中医药大学国医堂门诊部中医内科,安徽 合肥 231000;3.宣城市骨科医院康复科,安徽 宣城 242000)
多囊卵巢综合征(polycystic ovary syndrome,PCOS)是育龄期女性最常见的内分泌疾病,临床特征为生殖障碍、内分泌异常、代谢失调,主要表现为月经失调、不孕、多毛、痤疮、肥胖等[1]。青春期及育龄期女性PCOS的发病率高达5%~10%,且一半以上为肥胖者(体重指数≥25 kg/m2),均呈腹部肥胖型(腰围/臀围≥0.80)[2],因此容易引发女性糖尿病、心血管疾病、妊娠高血压综合征以及子宫内膜癌等多种疾病,威胁女性的健康。关于PCOS的治疗,西医主要使用周期性适用孕激素或短效复方口服避孕药等药物治疗以缓解高雄激素症状,或采用腹腔镜卵巢打孔术(LOD)治疗,但副作用较大,难以使患者满意。导致PCOS主要原因是胰岛素抵抗与高胰岛素血症,而肠道菌群可以调整胰岛素敏感性,改善胰岛素抵抗,从而降低血液中的胰岛素。以中医基础理论为依据进行中医辨证、中药序贯周期治疗,同时配合针刺辅助疗法有调节患者肠道菌群,改善肠道功能、纠正代谢障碍等作用[3]。本研究通过在口服炔雌醇环丙孕酮的基础上使用针刺联合中药治疗,借以探讨其对肥胖型PCOS患者肠道菌群数、肠道屏障功能、糖脂代谢及炎症因子水平的影响,为PCOS提供新的治疗策略。
1 资料与方法
1.1 一般资料
选取2018年5月至2021年5月宣城市人民医院100例确诊为肥胖型PCOS的患者为研究对象,按照治疗方式不同分为观察组和对照组,每组各50例。本研究获院伦理委员会批准,患者签署知情同意书,两组患者年龄、体重、BMI等一般资料比较,差异无统计学意义(P>0.05)。见表1。纳入标准:(1)符合2003年鹿特丹国际会议标准[3]:月经稀发、闭经或异常子宫出血;高雄激素血症或表现为雄激素过多;超声检查显示双侧卵巢可见大于12个且直径为2~9 mm小卵泡;满足其中两项即可诊断为PCOS;(2)符合《中药新药临床研究指导原则》的肥胖型PCOS诊断标准:月经后期、闭经、不孕症、肥胖症、癥瘕[4];(3)年龄20~40岁,体重66~78 kg, BMI 27.0~29.9 kg/m2(肥胖型);(4)高血压患者,病程在1~5年内。排除标准:(1)合并其他高雄激素病;(2)卵巢早衰和垂体或下丘脑性闭经等引起排卵障碍的疾病;(3)严重心、肝、肾等重要器官疾病;(4)患有精神性疾病;(5)患有免疫系统疾病;(5)近期服用激素类药物。
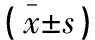
表1 两组患者一般资料比较
1.2 方法
对照组口服炔雌醇环丙孕酮片(拜尔医药保健有限公司广州分公司)治疗,从自然月经或撤退性出血第5天开始服用, 1片/d,服用21 d后停药7 d为1个周期,共3个周期。观察组在对照组基础上使用治肾化痰的中药联合针刺治疗。中药药方:柴胡 10 g,白芍 15 g,当归 15 g,香附 12 g,枳壳 15 g,川芎 10 g,甘草 6 g,苍术 15 g,陈皮 10 g,茯苓 15 g,半夏 12 g,薏苡仁 15 g,黄芩 10 g,补骨脂 10 g,紫石英 10 g;水煎服, 1剂/d,早、晚饭后各1次,100 mL/次, 25 d为1个周期,共3个周期。针刺法操作如下:患者行仰卧位,暴露操作部位皮肤,医师首先双手清洗消毒,选取肝俞、肾俞、关元、脾俞采用补法,阴陵泉、丰隆、三阴交、天枢行平补平泻手法,针刺气候留针30 min/次,1次/d,连续5 d后,停止2 d,1个月为1个周期,共3个周期。
1.3 观察指标
(1)糖脂代谢、炎症因子及肠道屏障功能指标:于治疗前、治疗3个周期后的早晨8∶00,采集患者肘部空腹静脉血3 mL,3 000 rpm离心10 min,取上清液。采用全自动生化分析仪(日本日立公司)检测糖代谢空腹胰岛素(FINS)、空腹血糖(FPG)、胰岛素抵抗指数(HOMA-IR)水平及脂代谢指标总胆固醇(TC)、三酰甘油(TG)、高密度脂蛋白(HDL)水平。酶联免疫吸附法(试剂盒购于上海邦景实业有限公司)检测炎症因子白细胞介素-6(IL-6)、C反应蛋白(CRP)、肿瘤坏死因子-α (TNF-α)及肠道屏障功能指标二胺氧化酶(DAO)、D-乳酸水平,操作严格按试剂盒说明书进行。(2)肠道菌群:于次日8∶00采集所有患者治疗前、治疗3个周期后未进食前的新鲜无污染粪便,稀释,振荡均匀,随后在肠道菌群发酵培养基(蛋白胨10 g, 大豆胨3 g,消化血清粉13.5 g,酵母浸膏5 g,牛肉膏2.2 g,牛肝膏1.2 g,葡萄糖3 g,KH2PO42.5 g,NaCl 3 g,可溶性淀粉5 g,L-半胱胺酸盐0.3 g,硫乙醇酸钠0.3 g,琼脂1.5 g,蒸馏水1 000 mL,pH为7.2~7.4,110 ℃灭菌20 min,冷却至50 ℃左右,倾入无菌平皿)[5]上进行细菌培养,包括肠杆菌、肠球菌、乳杆菌、双歧杆菌。采用革兰染色法进行染色,在显微镜下对细菌进行分类、计数,阳性菌为紫色,阴性菌则为红色。菌种的计数:菌群培养48 h后开始计数无菌平皿上的菌落数,计数时选取菌落数30~300的器皿。记下各器皿的菌落数后,求出同稀释度的各器皿平均菌落数,计算出原始样品每毫升中的菌落数[6]。
1.4 统计学分析
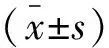
2 结果
2.1 两组患者糖代谢指标比较
治疗前,两组患者糖代谢指标比较,差异无统计学意义(P>0.05);治疗后,两组患者FINS、FPG、HOMA-IR水平均降低(P<0.05),且观察组低于对照组(P<0.05)。见表2。
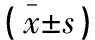
表2 两组患者糖代谢指标比较
2.2 两组患者脂代谢指标比较
治疗前,两组患者脂代谢指标比较,差异无统计学意义(P>0.05);治疗后,两组患者的TC、TG水平均降低(P<0.05),且观察组低于对照组(P<0.05),HDL-C水平均升高(P<0.05),且观察组高于对照组(P<0.05)。见表3。
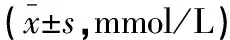
表3 两组患者脂代谢指标比较
2.3 两组患者炎症因子水平比较
治疗前,两组患者炎症因子水平比较,差异无统计学意义(P>0.05);治疗后,两组患者IL-6、CRP、TNF-α水平均降低(P<0.05),且观察组低于对照组(P<0.05)。见表4。
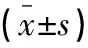
表4 两组患者炎症因子水平比较
2.4 两组患者肠道屏障功能指标比较
治疗前,两组患者肠道屏障功能指标比较,差异无统计学意义(P>0.05);治疗后,两组患者D-乳酸、DAO水平均降低(P<0.05),且观察组低于对照组(P<0.05)。见表5。
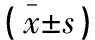
表5 两组患者肠道屏障功能指标比较
2.5 两组患者肠道菌群比较
治疗前,两组患者肠道菌群菌落数比较,差异无统计学意义(P>0.05);治疗后,两组患者肠杆菌与肠球菌菌群数均降低(P<0.05),且观察组低于对照组(P<0.05),乳杆菌和双歧杆菌的菌群数均升高(P<0.05),且观察组高于对照组(P<0.05)。见表6。
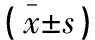
表6 两组患者肠道菌群比较
2.6 肠道菌群与肠道屏障功能、糖脂代谢、炎症因子水平的相关性
相关性分析显示,治疗后肠杆菌、肠球菌与D-乳酸、DAO、IL-6、CRP、TNF-α、FINS、FBG、HOMA-IR、TC、TG呈正相关(P<0.05),与HDL呈负相关(P<0.05);而乳杆菌、双歧杆菌与D-乳酸、DAO、IL-6、CRP、TNF-α、FINS、FBG、HOMA-IR、TC、TG呈负相关(P<0.05),与HDL呈正相关(P<0.05)。见表7。
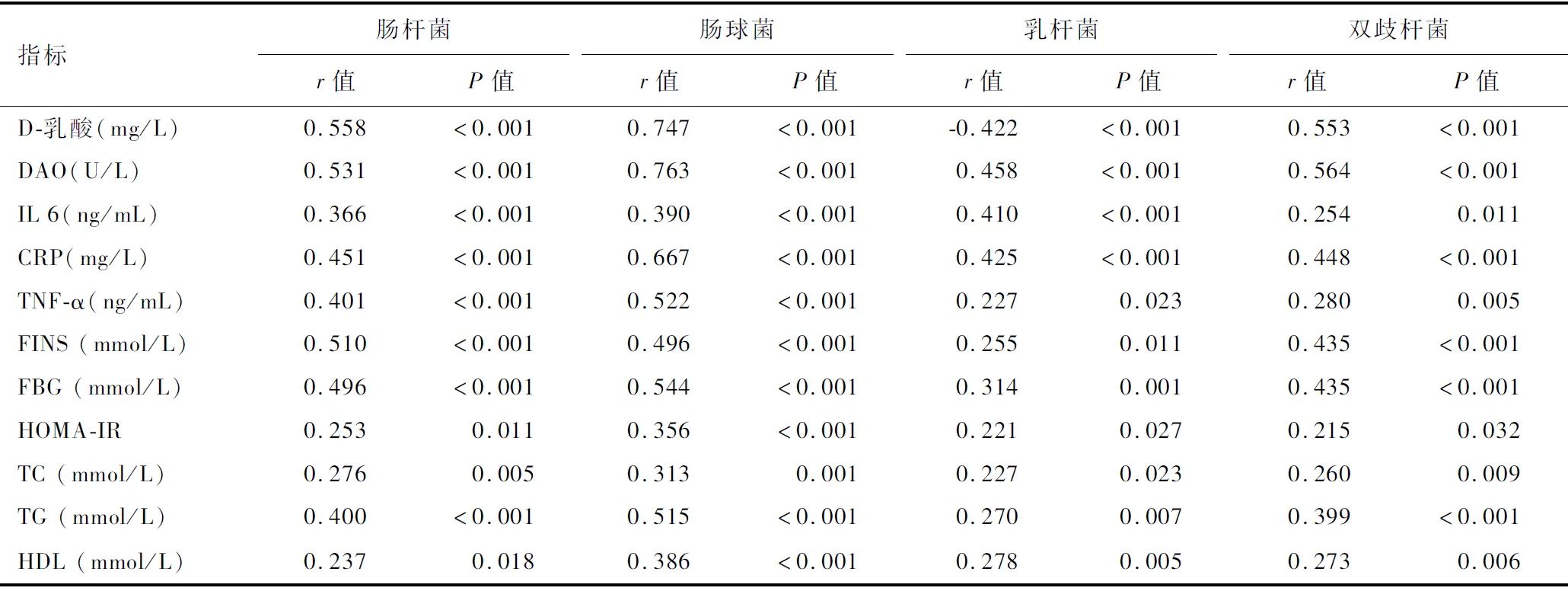
表7 治疗后肠道菌群与肠道屏障功能、糖脂代谢、炎症因子水平的相关性
3 讨论
肥胖型PCOS是一种多系统复杂性内分泌疾病,由于脂肪细胞膜上特异性胰岛素受体相对减少,胰岛素敏感性降低,因此患者常伴有高胰岛素血症和胰岛素抵抗[7]。而高水平胰岛素可使机体分泌过量雄激素,进而促进PCOS的发展。依据PCOS的临床表现,该病属于中医“不孕症”、“月经稀少”、“月经后期”、“闭经”等范畴[8]。《傅青主女科》云:“经水出诸肾”。肾阳亏虚不能暖土,则不能化气行水,水湿内停,聚湿成痰,水液痰湿壅塞胞宫,经水不行则出现闭经。因此,肥胖型PCOS的发病机制主要位于子宫中肾脏缺乏和痰湿的停滞。这种疾病应主要通过滋养肾,强化脾,溶解痰,去除湿度来治疗[9]。不同穴位进行不同强度的刺激,可以进一步调节神经和血管,改善人体的内环境,对于辅助治疗疾病具有很好的作用。根据中医病因进行穴位调理:肝脾肾三经交汇穴三阴交,补脾兼顾肝肾,可调理气血,阴阳双补;关元益气纳肾、培元固本;肾俞壮元阳,补腰肾,祛水湿;阴陵泉清利湿热,健脾理气;天枢和丰隆,可理气和胃化湿、化滞调肠[10]。因此治疗PCOS使用补肾化痰中药配合针刺能发挥更好的疗效。
糖类、脂类代谢异常是PCOS生理病理改变的主要特征之一。糖脂代谢异常易引起糖尿病和心血管疾病,中药联合针刺不仅能够提高胰岛素敏感性,增加胰岛素受体数量或活性改善胰岛素抵抗,降低血糖,还可促进肠蠕动,减少胆固醇和脂肪在肠道吸收并促其排出,以此降低血脂[11]。本研究结果显示,两组患者治疗后FINS、FPG、HOMA-IR、TC、TG水平降低(P<0.05),HDL-C水平升高(P<0.05),且观察组指标变化幅度大于对照组(P<0.05),说明在改善糖脂代谢方面,该疗法与西医的单纯促排卵和激素类药物治疗相比具有更好的疗效,与Qin等[12]的研究结果一致。肠道菌群的改变可使宿主摄取食物能量发生改变,导致肥胖,并且增加雄激素水平,使PCOS程度加重。中药联合针刺可作用于肠道菌群的靶器官,促进菌群正常生长,增加菌群多样性,从而改善菌群紊乱[13]。本研究结果显示,两组患者肠杆菌与肠球菌的菌群数均降低,而乳杆菌和双歧杆菌的菌群数则是升高(P<0.05);肠道屏障功能指标D-乳酸、DAO水平均降低,且观察组低于对照组(P<0.05),说明该疗法能有效改善人体内环境,加强肠道功能。有研究[14]表明,在PCOS患者体内如卵泡液、子宫内膜细胞、卵巢组织等均发现较多的炎症细胞因子。这些炎症介质通过激活Toll样受体4,降低胰岛素敏感性,诱发胰岛素抵抗。中药联合针刺可降低促炎因子水平,增加抑炎因子的表达,以此改善炎症微环境。治疗后两组患者的IL-6、CRP、TNF-α水平均降低,且观察组下降幅度大于照组(P<0.05),表明相比单纯的西药治疗,加用中药联合针刺对抑制机体炎症反应效果更好。还有研究[15]证明,经中药方案预处理后的促排卵药物治疗可优化治疗效果,有效提高妊娠率、疗效和安全性,加以针刺治疗能改善患者心理状态,疗效显着,不良反应少。
肠道菌群是人体不可缺少的“微生物器官”,影响宿主的物质代谢和免疫功能[16]。肠道菌群处于肠道屏障上,是肠道中的保护屏障之一,菌群改变会引起屏障功能强弱变化;糖脂代谢主要位于肠道,菌群改变对肠道吸收糖脂能量呈正相关;炎症因子的产生取决于肠道菌群,当肠道菌群失调,肠道可产生脂多糖进入体循环,并激活免疫系统,引发炎症反应。本研究结果显示,肠杆菌、肠球菌与D-乳酸、DAO、IL-6、CRP、TNF-α、FINS、FBG、HOMA-IR、TC、TG呈正相关,与HDL-C呈负相关(P<0.05);而乳杆菌、双歧杆菌与D-乳酸、DAO、IL-6、CRP、TNF-α、FINS、FBG、HOMA-IR、TC、TG呈负相关,与HDL-C呈正相关(P<0.05),显示PCOS患者接受针刺联合中药治疗后肠道菌群得到改善,可使肠道屏障功能增强,肠道黏膜屏障通透性减低,渗透性减弱,进而循环系统中的细菌及其代谢物大量减少[17]。同时能改善糖脂代谢,使肠道对葡萄糖的吸收减少,促进糖的无氧酵解,提高脂肪转化率,降低患者的体质量。另外还会降低炎症因子水平,促进卵泡发育,排卵、胰岛素的生成[18]。以上因素都可以造成外周血胰岛素敏感性增加、胰岛素抵抗改善,抑制雄性激素,促进雌性激素生成,进而在一定程度上改善PCOS患者的临床表现[19]。
综上所述,针刺联合中药对肥胖型多囊卵巢综合征患者有良好的治疗作用,可有效改善患者肠道菌群、肠道屏障功能、糖脂代谢和炎症因子水平,值得推广使用。

