甲醇-丁酮共沸物萃取精馏的模拟与优化
安永胜 谢小强 胡 南 张鑫海 孙雪飞 冯 凯 刘 亮 李群生*
(1.中国石油天然气管道工程有限公司, 廊坊 065099; 2.北京化工大学 化学工程学院, 北京 100029)
引 言
甲醇(MeOH)是一种重要的工业原料,常用于合成甲酸甲酯、氯甲烷、甲胺、硫酸二甲酯、甲醛等化合物,还可以作为燃料和溶剂使用[1]。而丁酮(MEK)是一种重要的有机合成原料[2-3],常用于制取醋酸纤维素、醇酸树脂、油墨等化工产品。在木醋液生产加工过程中,会形成MeOH和MEK混合物。常压下,MeOH与MEK会形成二元最低共沸物,MeOH的共沸摩尔分数为0.84,因此采用普通精馏工艺无法得到高纯度的MeOH和MEK产品。对共沸物系的分离有变压精馏、萃取精馏及膜分离等工艺技术[4-6],工业上一般采用萃取精馏工艺进行分离回收,因而萃取剂的选择非常重要。针对MeOH-MEK共沸物系萃取剂的选择问题,有很多学者进行过研究。张亲亲等[7]合成了3种离子液体(IONIC)用于分离MeOH-MEK体系,实验结果表明,[EPy][Br]可以提高甲醇和丁酮的相对挥发度,增大溶剂比能够显著提高离子液体的选择性;孙雪婷[8]选用[EMIM]BF4、[BMIM]BF4、[OMIM]PF6及[MMIM]DMP这4种离子液体作为萃取剂,测定了MeOH-MEK-IONIC三元物系的等压气液平衡数据,实验结果表明,[MMIM]DMP 的分离效果最好。李卓[9]选择[HMIM][NTF2]、[BMIM][NTF2]及[EMIM][NTF2]这3种离子液体作为萃取剂测定了MeOH-MEK-IONIC三元体系的等压气液平衡数据,结果表明[HMIM][NTF2]的分离效果最优。姜占坤等[10]选用苯甲醚(MPE)、甲苯(MP)及氯苯(CB)为萃取剂,采用间歇精馏的方式对MeOH-MEK体系进行了实验研究,结果表明3种物质都可以破坏MeOH-MEK共沸体系,分离出高纯度的产品,且操作灵活、设备费用低。尽管离子液体是一种很好的溶剂,具有蒸汽压低、稳定、无毒等优点,还可以降低设备投资,但目前以离子液体作为萃取剂的工艺还没有实现工业化,其操作性、控制性及安全性都未知,需要进一步的实验分析。而阻碍离子液体替代传统有机溶剂最重要的因素是离子液体的价格昂贵,从而导致操作费用增加。
本文针对MeOH-MEK共沸物系,以苯甲醚、甲苯、氯苯这3种化合物为萃取剂,利用Aspen Plus 进行模拟计算。以全年总费用(TAC)为目标函数,对萃取剂用量S、理论板数NT、原料进料位置NF以及萃取剂进料位置NEF等工艺参数进行了优化,得到的MeOH和MEK的纯度可达99.9%以上。此外,还针对普通的精馏工艺进行了热量集成,并从经济角度开展了分析讨论。
1 萃取剂的选择
本文通过比较无限稀释相对挥发度的大小来确定适宜的萃取剂,无限稀释相对挥发度越大则分离越容易。无限稀释相对挥发度的计算公式为
(1)
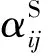
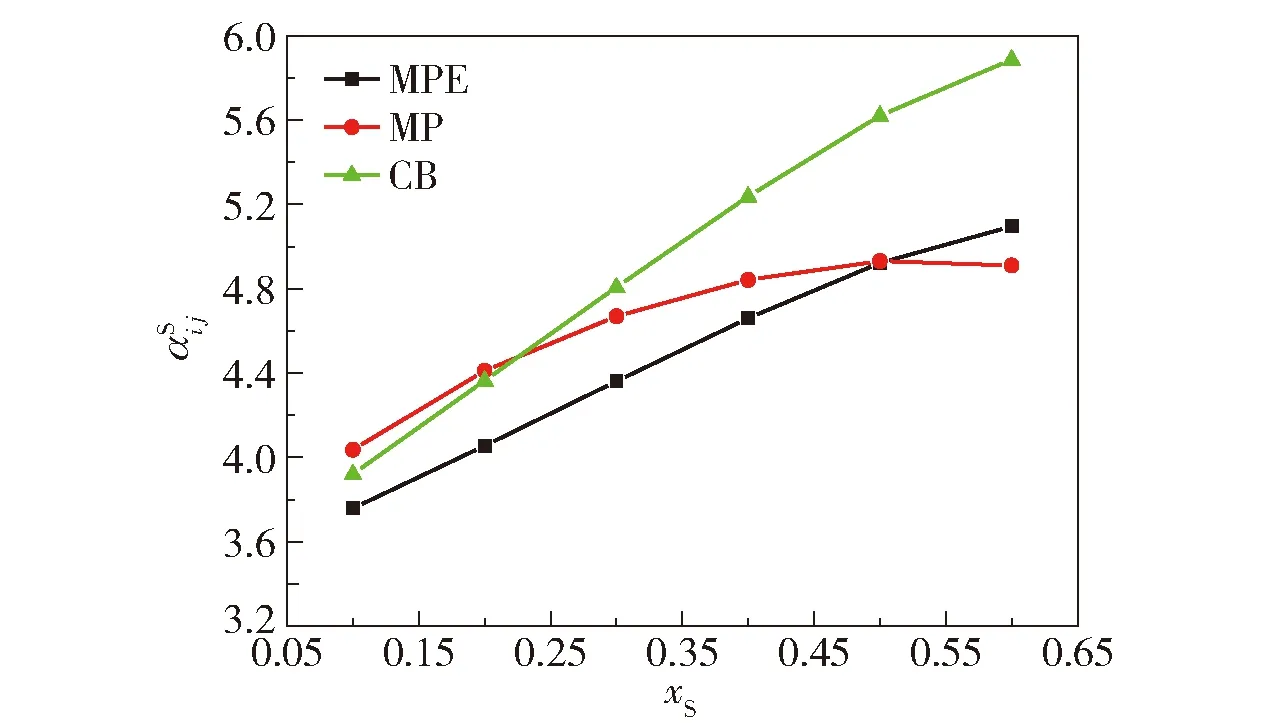
图1 不同萃取剂的摩尔分数对无限稀释相对挥发度的影响Fig.1 The value of for different extractants
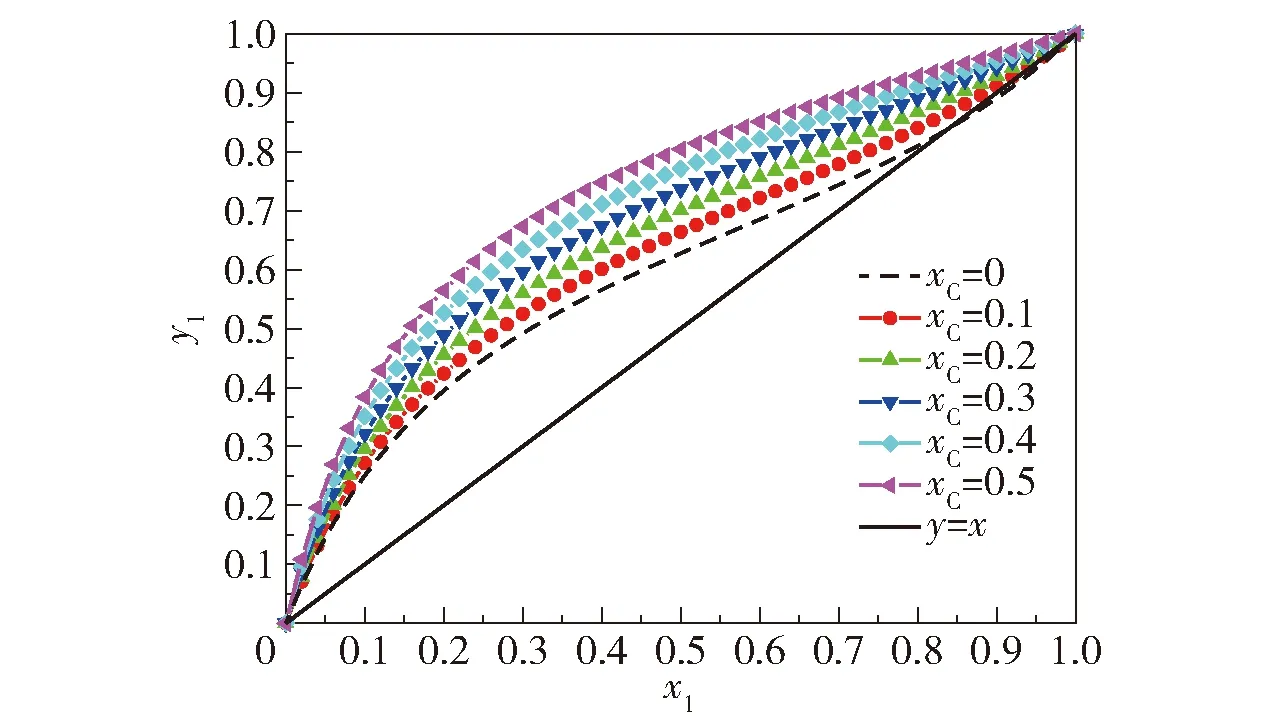
图2 不同浓度组成的氯苯对平衡体系的影响Fig.2 The effect of varying the concentration of CB on the equilibrium system
图3是运用Aspen Plus绘制的MeOH-MEK-CB三元体系的剩余曲线(RCM)图。从图中可以看出,MeOH-MEK的恒沸点为不稳定点,CB为稳定点,MeOH和MEK的恒沸点为鞍点。剩余曲线均按箭线方向指向CB。进料F1与循环溶剂B2在萃取塔中分离为D1和B1,萃取塔塔底混合物B1-F1在回收塔中可以分离为D2和B2。以上分析结果表明,采用CB作为MeOH-MEK体系的萃取剂是可行的。
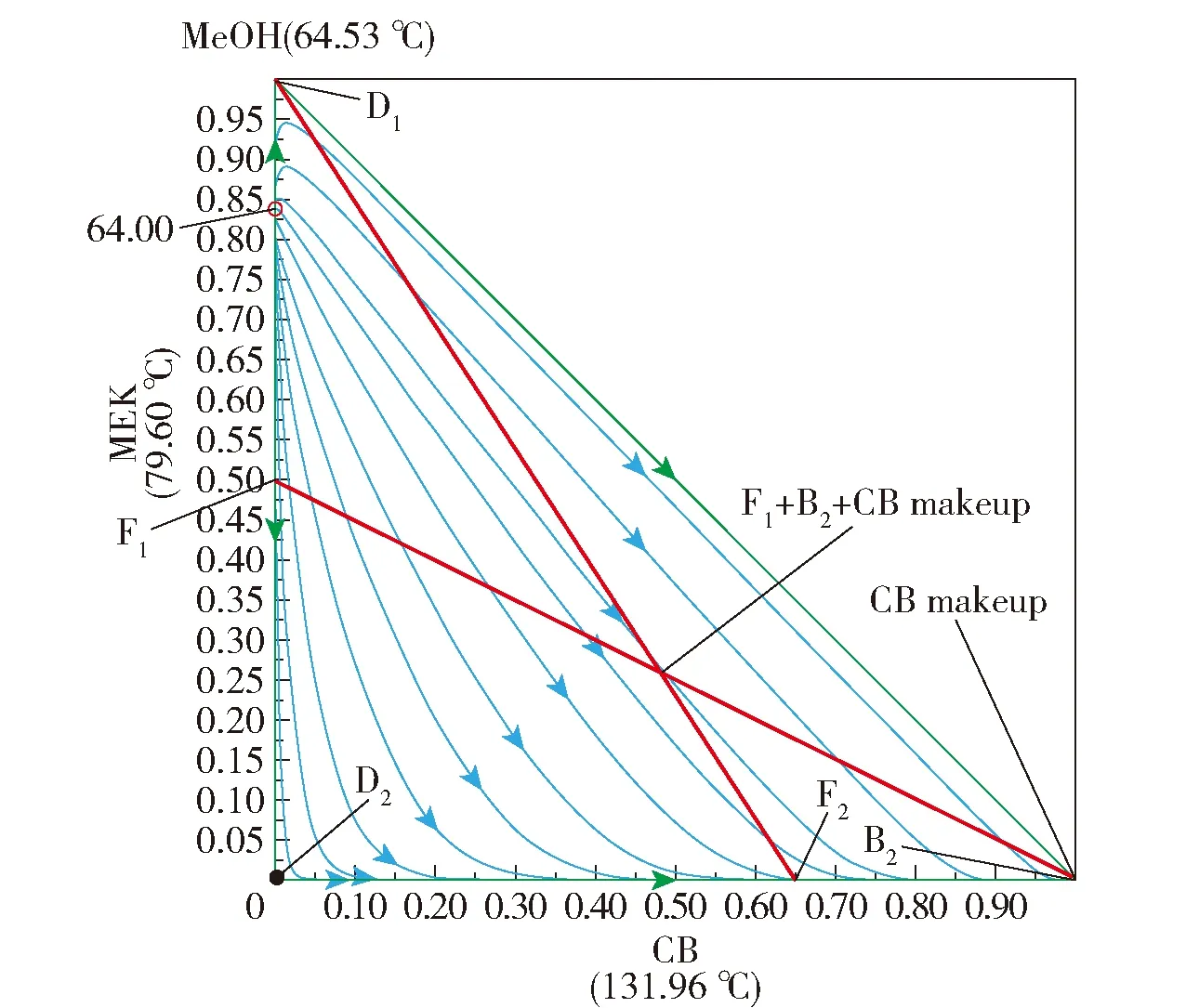
图3 MeOH-MEK-CB体系的剩余曲线图Fig.3 Residual curves of the MeOH-MEK-CB system
2 过程设计及经济优化
2.1 过程设计
如图4所示,待分离物系为F1,萃取剂循环量为S,从萃取精馏塔(T101)顶部获得高纯度的MeOH,MEK与氯苯的混合物从T101塔釜采出,由泵输送至溶剂回收塔(T102)。经过精馏分离,于T102塔顶部获得高纯度的MEK,萃取剂从T102塔釜馏出,经换热冷却后返回T101塔。因两塔顶部采出物流时有少量的溶剂损失,为了维持整个系统的质量守恒,需要在塔顶补充少量的萃取剂。
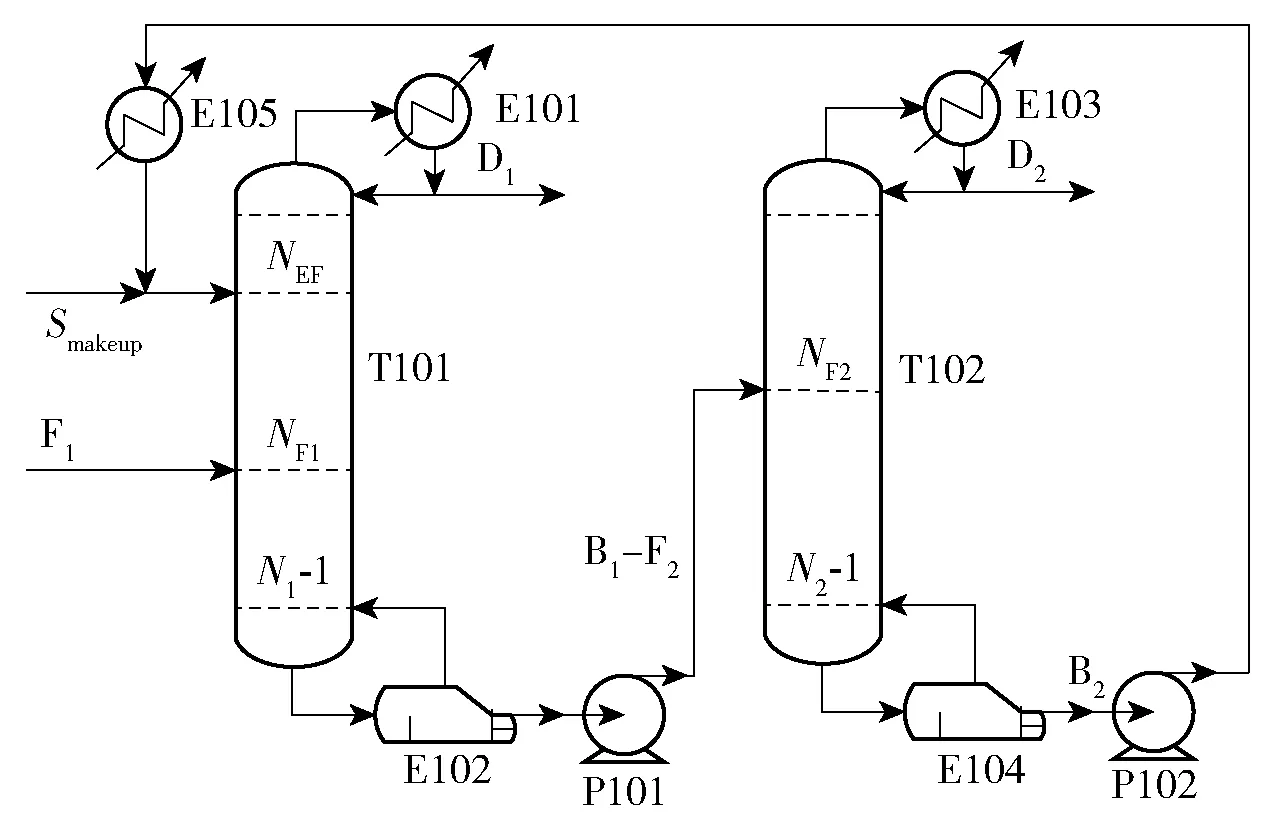
图4 萃取精馏过程工艺流程Fig.4 Process flow chart for extractive distillation
进料流量为100 kmol/h,其中MeOH摩尔分数为50%,MEK摩尔分数为50%,全年操作时间为8 000 h,设备回收期估算为3年。MeOH-MEK-CB三元体系的热力学行为采用非随机(局部)双液体模型方程(NRTL)描述,计算公式见式(2)。模型的二元相互作用参数见表1,其他物性参数全部来自Aspen物性数据库,输入初值后进行稳态模拟和优化。
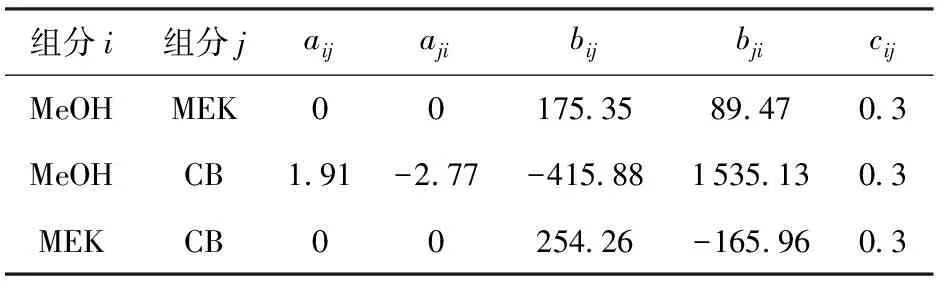
表1 MeOH-MEK-CB体系NRTL模型二元交互作用参数Table 1 Binary interaction parameters of NRTL model forMeOH-MEK-CB system
(2)
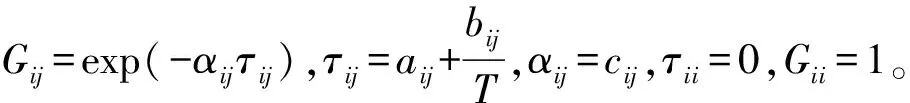
2.2 经济优化
本文以TAC为目标函数对萃取精馏系统进行了经济核算。核算依据参照Luyben[11]提出的计算方法。具体参数的计算如表2所示。流程中需要进行经济优化的参数有T101塔的总理论板数N1、进料位置NF1、萃取剂进料位置NEF、萃取剂的循环量S、T102塔总理论板数N2和T102塔进料位置NF2,经济核算的迭代流程如图5所示。
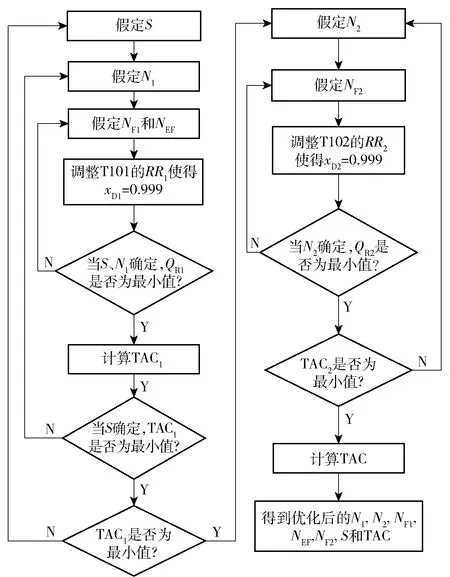
图5 优化的迭代流程Fig.5 Optimization iteration process

表2 经济核算依据Table 2 Basis of economic accounting
T101塔的参数优化结果如图6所示。图6(a)为S=90 kmol/h、N1=45时,T101塔热负荷QR1随NF1和NEF的变化曲线。可以看出,物料的最佳进料位置为NF1=40,萃取剂的最佳进料位置为NEF=30。图6(b)为S=90 kmol/h时,T101塔的全年总费用TAC1随N1的变化曲线。可以看出,当N1=45时,TAC1的值最小,因此,T101塔的最佳理论板数为45。图6(c)为TAC1随S的变化曲线,可以看出,最佳的萃取剂用量为90 kmol/h。
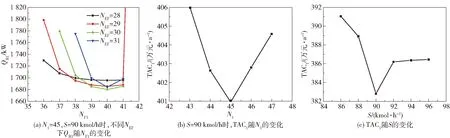
图6 T101塔参数优化结果Fig.6 Optimization results for T101
图7为T102塔的参数优化结果。图7(a)为N2=25时,T102塔热负荷QR2随NF2的变化曲线。可以看出,在进料位置NF2=14处,T102塔热负荷QR2的值最小。图7(b)为TAC2随N2的变化曲线,当N2=26时,TAC2的值最小。因此,T102塔的最佳理论板数为26块。T101塔和T102塔的最终优化结果见表3。
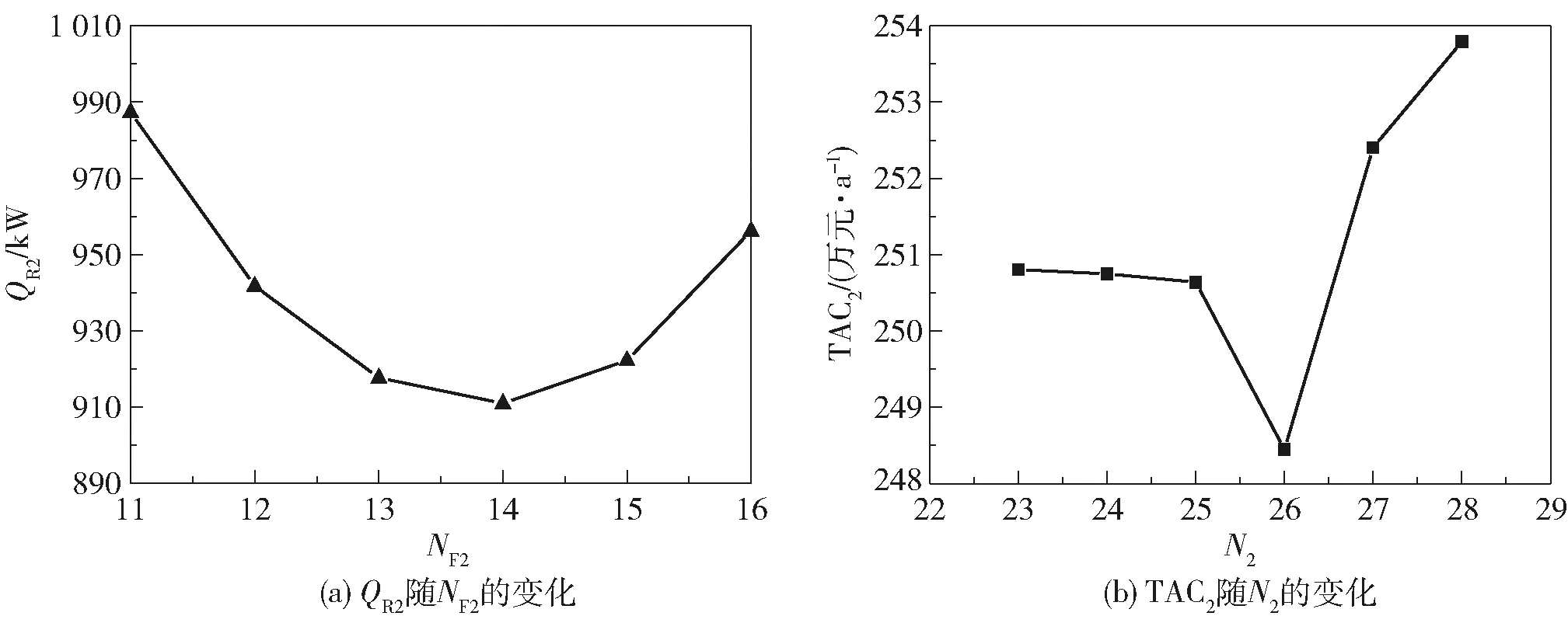
图7 T102塔参数优化结果Fig.7 Optimization results for T102
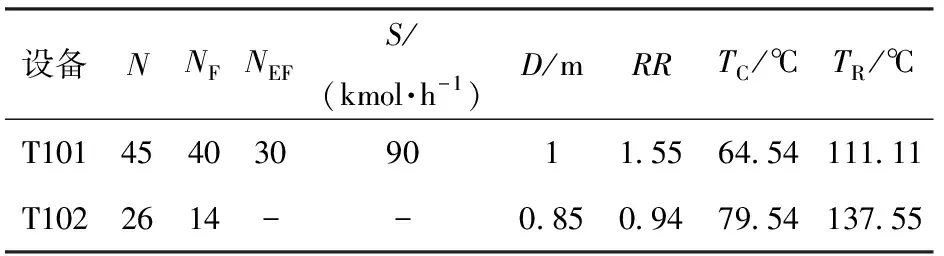
表3 T101和T102塔的参数优化结果Table 3 Optimization results for the process parameters ofT101 and T102 towers
2.3 热量集成
从图4和表3可以看出从T102塔底采出的物流温度为137.55 ℃,即返回T101塔时温度过高,对T101塔的分离效果不利,需要冷却至一定温度,此时需要添加一台额外的冷却器E105进行冷却。由于原料的进料温度较低,在同等进料条件下,要达到一定的分离效果,需要的理论板数多、能耗较大。因此,考虑用T102塔釜的采出物料与原料进行热交换,以降低T101塔的能耗费用。热量集成的工艺流程如图8所示。保持T101塔和T102塔的基本工艺参数不变,对热量集成后的工艺进行能量衡算和经济分析,计算结果见表4、5。
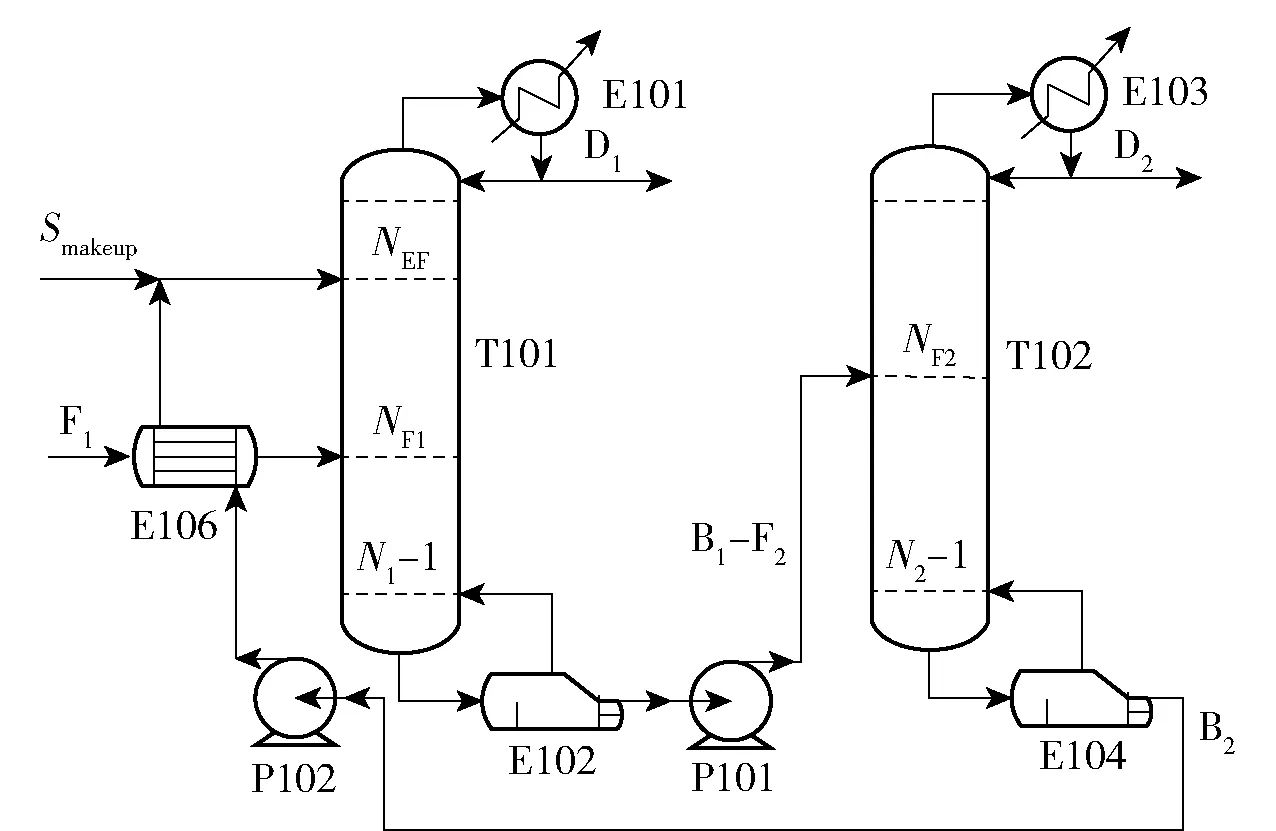
图8 热量集成工艺流程图Fig.8 Process flow chart after energy integration
从表4、5可以看出,经过热量集成后,T101塔的理论板数不变,再沸器(E102)能耗降低288.44 kW,蒸汽费用降低41.94万元。使用热交换器(E106)后,设备费用增加3.28万元,但TAC降低42.77万元。上述结果表明,采用热量集成精馏工艺提高进料温度,能够达到降低能耗费用的目的。
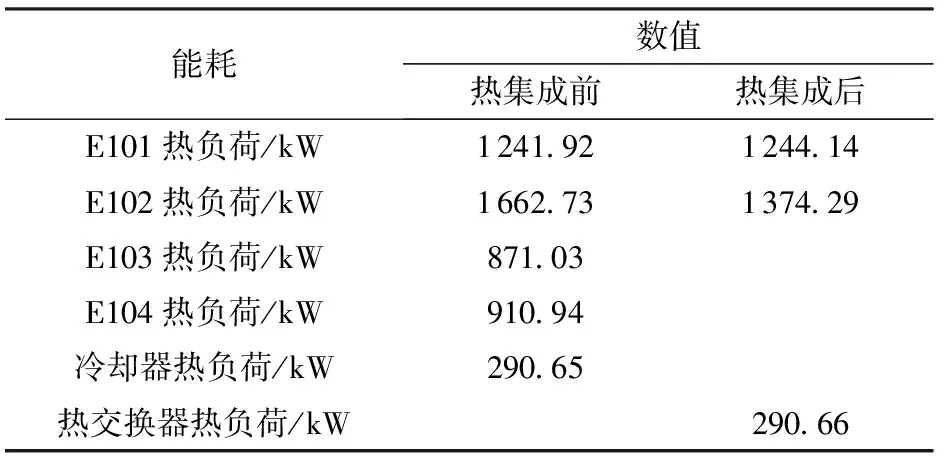
表4 节能前后的能耗对比Table 4 Comparison of energy consumption beforeand after energy saving
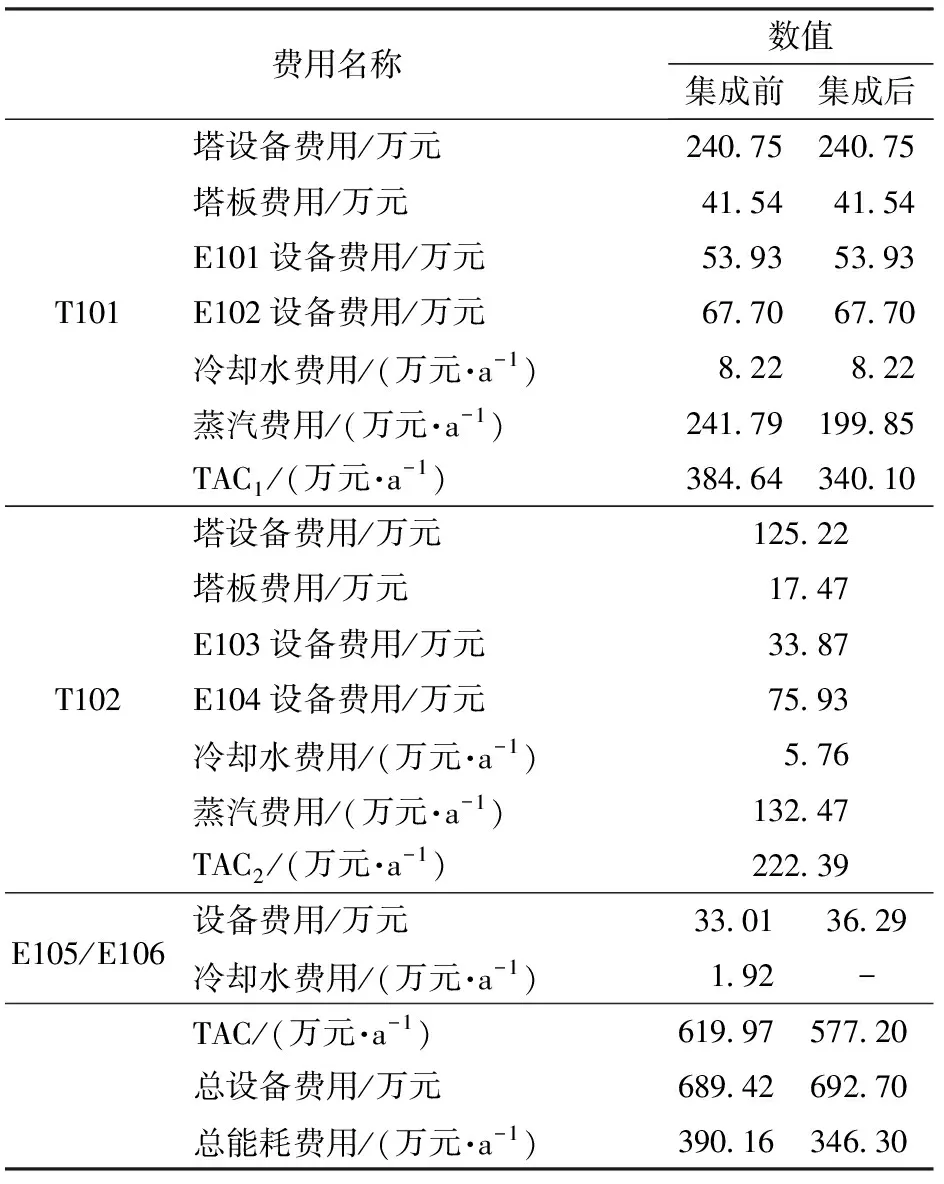
表5 经济分析Table 5 Economic analysis
3 结论
(1)计算了MeOH-MEK体系中苯甲醚、甲苯、氯苯3种组分的无限稀释相对挥发度值,结果表明,氯苯的分离效果最优。
(2)以全年总费用TAC为优化函数对萃取精馏塔和溶剂回收塔进行优化,获得了最佳的工艺操作参数。其中,T101塔的理论板数为45,原料最佳进料位置为40,溶剂的进料位置为30,回流比为1.55;T102塔的理论板数为26,最佳进料板位置为14,回流比为0.94。在最佳的工艺参数操作下,可获得99.9%的MeOH和99.9%的MEK产品。
(3)通过对余热进行热量集成后,设备费用增加3.28万元,能耗费用降低43.86万元,TAC降低42.77万元。

