氨基磺酸钠对碱/脲体系低温溶解棉纤维的影响
刘慧敏,迪丽达·马塔,贾丽霞
(新疆大学纺织与服装学院,新疆乌鲁木齐 830046)
纤维素是以D-吡喃葡萄糖基通过1,4-β 苷键形 成的具有线性结构的天然高分子化合物[1],绿色环保、生物相容、可降解[2-3],但是由于其高密集结构以及分子间、分子内存在大量氢键,纤维素的可及性和溶解性低[4-5],使废弃纤维素的回收以及再利用均受到很大的限制。自从张俐娜团队[6-7]发现NaOH/尿素/水溶液是环境友好、价格低廉的低温纤维素溶解体系后,许多学者在该体系的基础上添加ZnO、己内酰胺等提高纤维素的溶解度[8-9],但是这些低温体系仅能溶解可及性高的纤维素,如棉浆粕、竹浆、木浆以及纸浆等[10-12]。石岩[13]发现包含合适氢键受体与供体的添加剂有助于溶解聚合度较高的纤维素。氨基磺酸钠有2 个氢键供体以及4 个氢键受体,类似于尿素(硫脲)有4 个氢键供体以及3 个氢键受体,有利于破坏纤维素分子的氢键。本实验以聚合度较高的天然原棉纤维为原料,在优化NaOH/尿素/硫脲/水溶液体系(SUT)的基础上,添加少量氨基磺酸钠以促进原棉纤维溶解,可应用于废弃棉织物和涤棉混纺织物中棉纤维的溶解和回收。
1 实验
1.1 材料和仪器
材料:原棉纤维[三师农科所实验地44 团14 连(南疆)],氢氧化钠(NaOH,天津市致远化学试剂有限公司),尿素(天津市水晟精细化工有限公司),硫脲、氨基磺酸钠(上海阿拉丁生化科技股份有限公司),双氧水(国药集团化学试剂有限公司),蒸馏水(自制)。
仪器:Y(B)802K 八篮恒温烘箱(温州市大荣纺织仪器有限公司),DF-101Z 集热式恒温加热磁力搅拌器(巩义市英峪仪器厂),GP153 电子天平[奥豪斯仪器(常州)有限公司],TG16 湘仪台式高速离心机(常州普天仪器制造有限公司),FYL-YS-128L 低温保存箱(北京福意联电器有限公司),SNB-1 数字式黏度计(上海菁海仪器有限公司),LEO-1430VP 扫描电镜(德国Zeiss 公司),VERTEX 傅里叶红外光谱仪(德国Bruker 公司),D8 Advance X 射线粉末衍射仪(德国布鲁克AXS 有限公司),Q600热重分析仪(美国TA 公司)。
1.2 原棉纤维的预处理
取一定量棉纤维,剪碎后放入配制好的NaOH/双氧水/水溶液中,95 ℃处理30 min,清洗至中性,再在70 ℃恒温烘箱中放置12 h至恒重。
1.3 原棉纤维的溶解
配制NaOH/尿素/硫脲/氨基磺酸钠/水溶液,放入低温保存箱内预冷,达到所需温度后将一定量原棉纤维放入其中快速搅拌一定时间。将得到的黏稠纤维素溶液倒入离心管内,以10 000 r/min 离心10 min,去除下面未溶解的部分,得到透明纤维素溶液。溶解率=(1-m1/m0)×100%,式中,m0为溶解前棉纤维的质量,g;m1为溶解后棉纤维的质量,g。
1.4 再生纤维素的制备
将透明纤维素溶液倒入1 000 mL 烧杯中,不断加入蒸馏水并搅拌,直至出现白色絮状物;静置沉淀1 h,倒去上层清液,余下部分倒入离心管,以6 000 r/min离心10 min,过滤,清洗沉淀至中性,烘干,得到再生纤维素。
1.5 测试
黏度:室温下用数字式黏度计测量。
扫描电镜:从烘干的纤维中取样,粘在样品台上进行喷金,用扫描电镜观察。
傅里叶红外光谱:原棉纤维以及再生纤维素70 ℃烘干12 h,研磨,通过KBr 压片法用傅里叶变换红外光谱仪进行测试,扫描精度为4 cm-1,扫描范围为400~4 000 cm-1。
X 射线衍射:用X 射线粉末衍射仪测试,波长λ=0.154 nm,电压40 kV,电流40 mA,扫描速率10°/min。
热重(TG):用热重分析仪测试,温度35~600 ℃,氮气氛围,升温速率10 ℃/min。
2 结果与讨论
2.1 SUT 体系优化
采用L9(33)正交实验优化SUT 体系,得出氢氧化钠、尿素、硫脲质量分数分别为7%、6%、6%,此时棉纤维溶解率最佳(64.8%)。
2.2 SUT 体系溶解棉纤维的影响因素
2.2.1 氨基磺酸钠用量
氨基磺酸钠在棉纤维溶解过程中起辅助作用,其用量对棉纤维溶解性的影响见图1。

图1 氨基磺酸钠用量对棉纤维溶解性的影响
由图1 可知,随着氨基磺酸钠用量的增加,棉纤维溶解率增大,0.15%时,溶解率和黏度均达最大值(90.21%、86.8 mPa·s),与未添加氨基磺酸钠相比分别增加了39.21%和37.41%。这是因为氨基磺酸钠结构中有2 个氢键供体和4 个氢键受体,可以更好地破坏纤维素分子的氢键结构,促进棉纤维分子中可及度低的高聚合度纤维素分子溶解[14]。
2.2.2 预冷温度
由图2可以看出,添加氨基磺酸钠后,-12 ℃时溶解率以及黏度均最大(91.20%、89.59 mPa·s);温度升高时,溶解率以及黏度不断降低。这是因为棉纤维溶解是一个放热过程,在低温情况下,NaOH 使纤维素溶胀,穿透纤维素并破坏其分子内和分子间氢键;另外,低温时溶剂中的硫脲、尿素以及氨基磺酸钠容易与棉纤维形成氢键,阻止纤维素分子重聚,使其均匀分散在溶液中。低于-12 ℃时,溶解率和黏度也降低。这是因为溶液中开始有大量溶质(硫脲)析出,并且开始结冰。
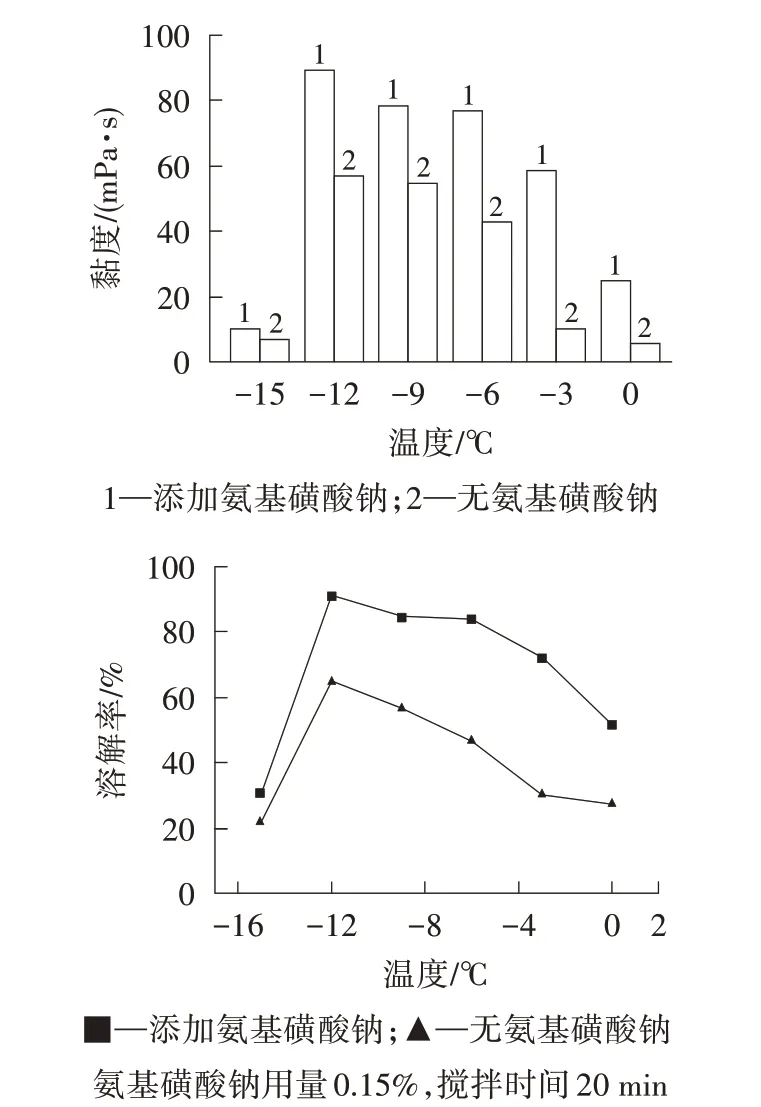
图2 预冷温度对棉纤维溶解性的影响
2.2.3 搅拌时间
由图3 可以看出,添加氨基磺酸钠后,5 min 时溶解率达到61.83%,说明在添加氨基磺酸钠的体系中,大部分棉纤维在5 min 内已经被溶解;随着搅拌时间的延长,溶解率和黏度增大,20 min 时溶解率和黏度达最大值(91.52%、89.51 mPa·s);超过20 min 时,溶解率略下降。这是因为随着搅拌时间延长,溶剂不断渗入棉纤维内部,从非结晶区到结晶区,溶解率增大;但是超过20 min 时,溶液温度不断上升,溶解率降低,溶液也会发生凝胶化。
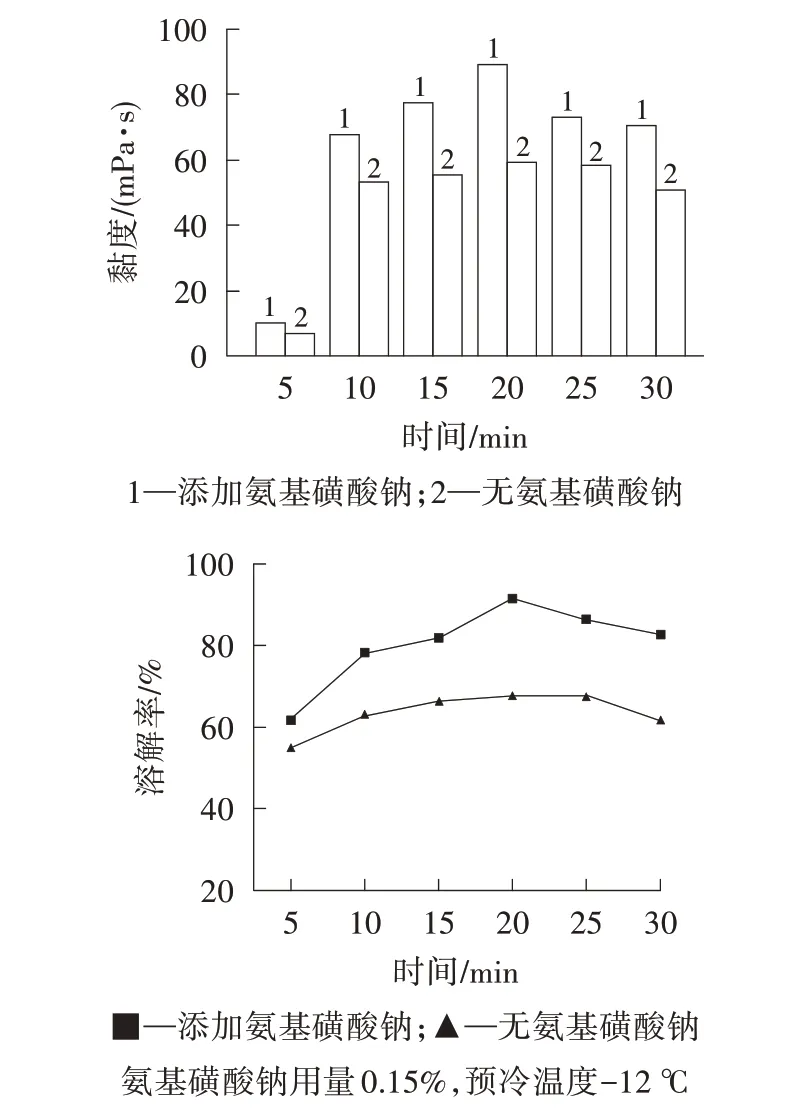
图3 搅拌时间对棉纤维溶解性的影响
由表1 可知,添加氨基磺酸钠后,优化条件下的溶解率达92.00%,与未添加氨基磺酸钠溶解体系相比增加了41.97%。由此可见,加入一定量氨基磺酸钠有助于提高棉纤维的溶解度。
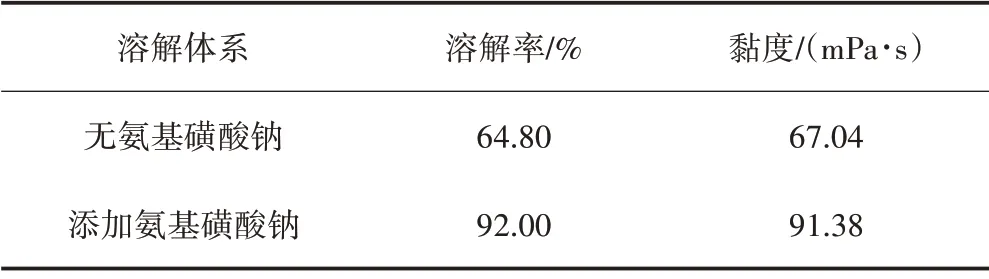
表1 未添加与添加氨基磺酸钠溶解体系棉纤维溶解率对比
2.3 氨基磺酸钠对再生纤维素结构与性能的影响
2.3.1 扫描电镜
由图4a 可知,原棉纤维是扁平的转曲带状结构,表面光滑。经过低温溶解后,棉纤维开始溶胀变得粗大,出现弯折现象,表面变得粗糙,有裂纹(见图4b)。这是因为经过低温溶解体系溶解后,棉纤维与NaOH结合溶胀,分子中的氢键被破坏;同时尿素、氨基磺酸钠和硫脲分子中含有,可与棉纤维的—OH 形成新的氢键[15]溶解纤维素,棉纤维表面形貌发生明显变化。再生纤维素则呈现絮块状(见图4c),说明被溶解的棉纤维再生后容易发生团聚现象。
2.3.2 傅里叶红外光谱
由图5 可知,3 349 cm-1附近是棉纤维的特征吸收峰,由O—H 伸缩振动吸收导致;再生纤维素此处的吸收峰面积明显增大,峰值向高波数方向移动,发生“蓝移”现象[16],说明溶解体系破坏了棉纤维分子间的氢键,使—OH 增多,增大棉纤维的可及性,导致棉纤维溶解。1 645 cm-1附近是纤维素吸附水的吸收峰,由纤维素吸收水分导致;再生纤维素此处的吸收峰面积增大,说明纤维素吸收水分增加,混合溶剂体系破坏纤维素的分子结构,提高纤维素的吸水能力。1 430 cm-1处的吸收峰与纤维素Ⅰ晶型有关[17];再生纤维素中未出现该吸收峰,说明纤维素晶型发生变化。由此可见,棉纤维在添加氨基磺酸钠的SUT 体系中溶解,未产生新的吸收峰,说明该过程是物理变化。

图5 棉纤维(a)和再生纤维素(b)的傅里叶红外光谱图
2.3.3 X 射线衍射
由图6 可知,棉纤维有3 个衍射峰,分别在2θ=14.8°、16.3°和22.6°处,对应(101)、(101)和(002)晶面,是纤维素Ⅰ晶型的特征衍射峰;而再生纤维素的衍射峰在2θ=12.0°、19.9°和21.6°处,分别对应(101)、(101)和(002)晶面,是纤维素Ⅱ晶型的特征衍射峰[18-19]。这表明棉纤维经过添加氨基磺酸钠的SUT 体系低温溶解后,经再生、重新结晶,已经从Ⅰ型转变为Ⅱ型。原因是该溶剂破坏了棉纤维的结构,使分子中的—OH构象发生变化。同时,从衍射峰的强度还可以看出棉纤维的结晶度降低,原因是溶解过程中棉纤维发生溶胀,分子的氢键被破坏,导致结晶区被破坏。

图6 棉纤维(a)和再生纤维素(b)的X 射线衍射图
2.3.4 热重分析
纤维素的裂解主要分为3 个阶段[20-21]:(1)初始裂解阶段(30~270 ℃),主要是纤维素中游离水的不断析出、蒸发;(2)主要裂解阶段(270~380 ℃),主要是纤维素大分子结构中的糖苷键和C—C 键断裂;(3)残渣裂解阶段(380~600 ℃),主要是裂解后残余物的再次分解,脱水、石墨化后最终生成炭和灰分。棉纤维和再生纤维素的TG/DTG 图见图7。
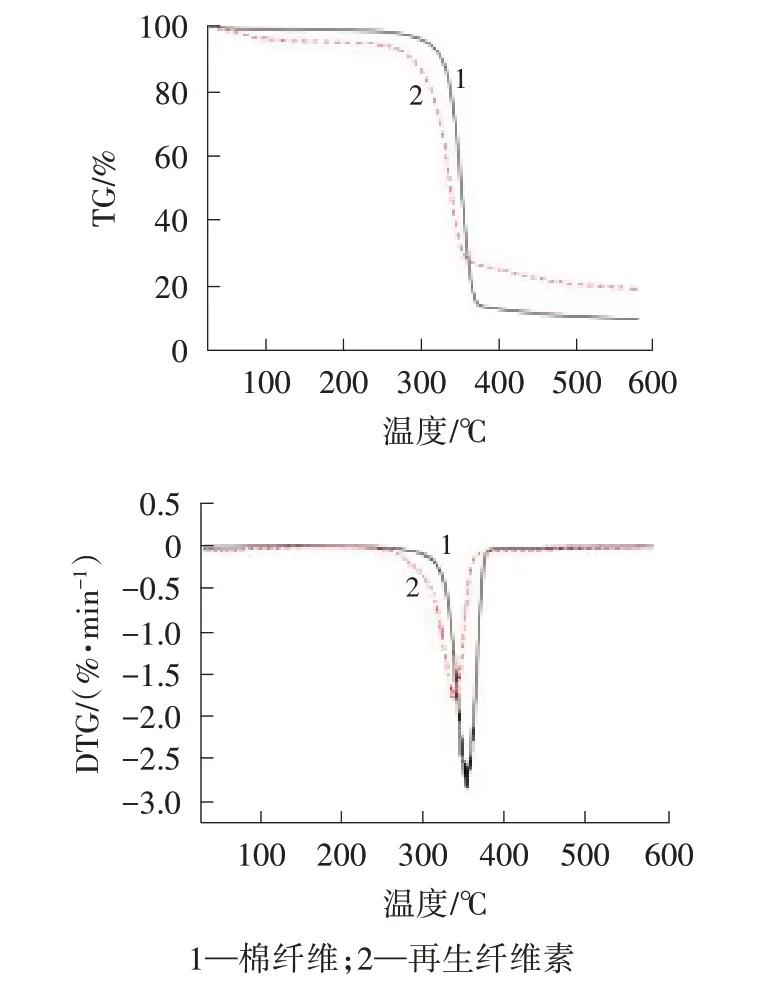
图7 棉纤维和再生纤维素的TG/DTG 图
由图7 可知,初始裂解阶段再生纤维素比原棉纤维的分解温度低,由266.14 ℃降至230.55 ℃;主要裂解阶段再生纤维素最大失重率分解温度比原棉纤维低,由355.75 ℃降至341.49 ℃;残渣裂解阶段再生纤维素残留率比原棉纤维多(19.20%、10.03%)。这表明添加氨基磺酸钠的SUT 体系低温溶解再生的纤维素热稳定性比原棉纤维差。原因是经过低温溶解再生后,棉纤维分子中的氢键断裂减少,纤维素Ⅰ型转变为Ⅱ型,结晶度降低。
3 结论
(1)在SUT 体系中添加氨基磺酸钠,可使棉纤维溶解率提高41.97%,优化溶解条件:NaOH、尿素、硫脲、氨基磺酸钠质量分数分别为7%、6%、6%、0.15%,预冷温度-12 ℃,搅拌时间20 min。
(2)棉纤维经过低温溶解后出现裂缝、弯折,表面变粗糙,再生纤维素则呈现絮块状结构。
(3)添加氨基磺酸钠后,SUT 体系溶解棉纤维仍然是直接溶解;棉纤维晶型由纤维素Ⅰ型转变为Ⅱ型,结晶度降低;与原棉纤维相比,再生纤维素热稳定性降低。

