伊伐布雷定对缺血性心肌病伴心力衰竭患者的治疗效果观察
李谌
冠状动脉粥样硬化所致冠脉狭窄,使心肌细胞长期处于心肌缺血,细胞因长期供血不足,心肌细胞持续处于炎症反应,氧化应激的不良状态,代谢废物堆积,促使心肌细胞提前进入缺血坏死、凋零进程,最终导致心肌细胞数量不断减少,引起心肌组织弥漫性纤维化,最终演变为缺血性心肌病(ischemic cardiomyopathy,ICM)[1]。ICM发生发展过程中显著特点是心室重塑,心室收缩力下降,心功能降低,最终使各种心血管不良事件如恶性心律失常、心肌梗死、心衰等的发生,具有很高的致死致残风险,严重影响ICM患者疾病预后及生活质量,但是传统的药物治疗对ICM患者的临床疗效非常有限,且大部分ICM患者往往起病隐匿,待疾病发现时往往已失去了介入和冠状动脉旁路移植术的手术机会,而且对部分ICM晚期患者即使勉强实行介入或外科治疗等手段的干预,其收益仍不明显。因此如何进一步改善及提高ICM患者的临床治疗效果,改善心脏功能,提高患者活动耐量成为如今心血管内科医师关注的焦点之一。故本研究旨在探讨ICM基础治疗联合伊伐布雷定对ICM患者心率控制、心室重塑、心功能的影响,为将来ICM治疗提供新思路。
1 资料与方法
1.1 一般资料
选取2019年7月-2020年10月笔者所在医院收治的70例缺血性心肌病并心力衰竭患者为研究对象,(1)纳入标准:①有长期心肌缺血症状;②纽约心脏病协会(NYHA)心功能分级Ⅱ~Ⅳ级;③心脏超声提示左室射血分数(LVEF)≤45%,且左室舒张末期内径>55 mm;④窦性心律,静息状态下平均心率>70次/min。并且慢性心衰持续6个月或以上。(2)排除标准:①对伊伐布雷定药物过敏;②急性心力衰竭;③严重的慢性病,肝、肾功能不全等严重疾病或癌症病史;④对酒精或药物成瘾史,以及其他能增加死亡率的因素。按数字随机法分为对照组和伊伐布雷定组,每组35例。对照组患者中,男17例,女18例;年龄57~73岁,平均(65.33±8.55)岁;病程6个月~5年,平均(22.24±16.23)个月。伊伐布雷定组患者中,男16例,女19例;年龄58~76岁,平均(67.26±7.24)岁;病程6个月~5年,平均(23.17±15.48)个月。两组患者临床基本资料方面比较差异无统计学意义(P>0.05),具有可比性。
1.2 方法
两组患者均按照《中国心力衰竭诊断和治疗指南2018》推荐,予以两组患者口服药物治疗[2],具体如下:呋塞米片(天津力生制药股份有限公司,国药准字H12020163)20 mg/次,1次/d;螺内酯片(杭州民生药业有限公司,国药准字H33020070)20 mg/次,1次/d;赖诺普利片(江苏黄河药业股份有限公司,国药准字H20066146)5 mg/次,1次/d;富马酸比索洛尔片(北京华素制药股份有限公司,国药准字H10970082)5 mg/次,1次/d;阿司匹林肠溶片(拜耳医药保健有限公司,国药准字J20171021)100 mg/次,1次/d;阿托伐他汀钙片(乐普制药科技有限公司,国药准字H20163270)20 mg/次,1次/d;地高辛片(上海上药信谊药厂有限公司,国药准字H31020678)0.125 mg/次,1次/d。在此基础上,伊伐布雷定组加用伊伐布雷定(Les Laboratoires Servier Industrie,注册证号H20150217)口服,5 mg/次,2次/d。两组患者均进行6个月的治疗。
1.3 观察指标及评价标准
比较两组患者6个月后的静息心率(RHR)、血清肌钙蛋白I(cTnI)、脑钠肽(BNP)、超敏C反应蛋白(hs-CRP)的水平。比较两组患者治疗前后的左心室射血分数(LVEF)、左心室舒张末期内径(LVEDD)及左心室收缩末期内径(LVESD)大小。
1.4 统计学处理
本研究数据采用SPSS 20.0统计学软件进行分析和处理,符合正态分布且方差齐的计量资料以(±s)表示,两独立样本均数的比较采用t检验,计数资料以率(%)表示,采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组治疗前后RHR、血清cTnI、BNP、hs-CRP水平比较
两组治疗前RHR、血清BNP、cTnI、hs-CRP水平比较,差异无统计学意义(P>0.05);与治疗前比较,伊伐布雷定组各指标均有降低,对照组RHR、BNP相关指标降低,差异有统计学意义(P<0.05),对照组治疗前后cTnI、hs-CRP水平比较差异无统计学意义(P>0.05);治疗后伊伐布雷定组RHR、血清cTnI、BNP、hs-CRP水平低于对照组,差异均有统计学意义(P<0.05),见表 1。
表1 两组治疗前后RHR、cTnI、BNP、hs-CRP水平比较 (±s)
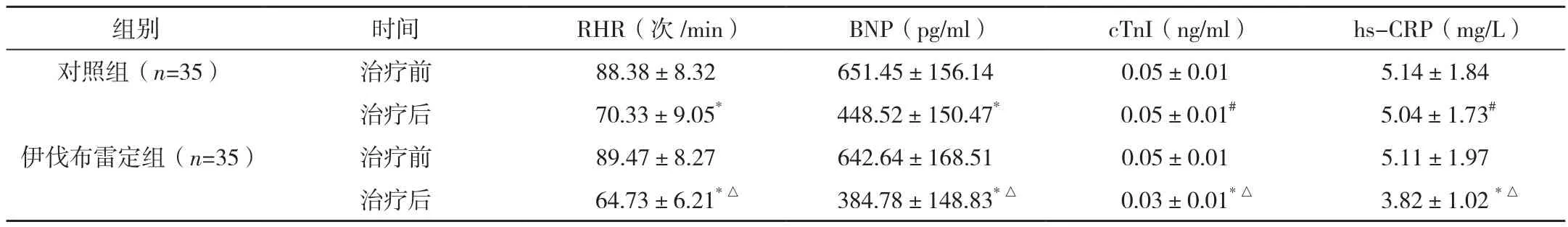
表1 两组治疗前后RHR、cTnI、BNP、hs-CRP水平比较 (±s)
*与本组治疗前比较,P<0.05;#与本组治疗前比较,P>0.05;△与对照组治疗后比较,P<0.05。
组别 时间 RHR(次/min) BNP(pg/ml) cTnI(ng/ml) hs-CRP(mg/L)对照组(n=35) 治疗前 88.38±8.32 651.45±156.14 0.05±0.01 5.14±1.84治疗后 70.33±9.05* 448.52±150.47* 0.05±0.01# 5.04±1.73#伊伐布雷定组(n=35) 治疗前 89.47±8.27 642.64±168.51 0.05±0.01 5.11±1.97治疗后 64.73±6.21*△ 384.78±148.83*△ 0.03±0.01*△ 3.82±1.02 *△
2.2 两组患者治疗前后LVEF、LVEDD及LVESD水平比较
治疗前,两组LVEF、LVEDD及LVESD比较差异无统计学意义(P>0.05);与治疗前比较,两组治疗后LVEF升高,LVEDD及LVESD水平减小,差异有统计学意义(P<0.05);治疗后伊伐布雷定组LVEDD和LVESD均小于对照组,且LVEF高于对照组,差异有统计学意义(P<0.05),见表2。
表2 两组治疗前后LVEF、LVEDD及LVESD水平比较 (±s)

表2 两组治疗前后LVEF、LVEDD及LVESD水平比较 (±s)
*与本组治疗前比较,P<0.05;#与对照组治疗后比较,P<0.05。
组别 时间 LVEF(%) LVEDD(mm) LVESD(mm)对照组(n=35) 治疗前 31.24±5.03 64.34±3.29 49.29±3.54治疗后 35.12±4.42* 61.89±3.85* 47.37±2.41*伊伐布雷定组(n=35) 治疗前 32.42±5.93 64.12±5.26 50.28±3.16治疗后 39.51±5.82*# 57.35±3.25*# 45.96±2.69*#
2.3 两组不良反应发生率比较
两组患者在治疗期间未发生严重不良反应,对照组有心动过缓1例,低血压2例,不良反应发生率为8.57%(3/35);伊伐布雷定治疗组有心动过缓慢1例,低血压1例,视力模糊1例,不良反应的发生率为8.57%(3/35)。两组不良反应发生率比较,差异无统计学意义(P>0.05)。
3 讨论
有研究结果表明,心率增快与冠心病发病率与致死率密切相关[3]。ICM心衰患者往往伴有交感神经兴奋性升高,心率偏快的特点,β受体阻滞剂做完临床上经典调控心药物,其用于改善ICM心衰预后的重要原理即为减慢心率、抑制交感神经兴奋,遗憾的是这类药物在降低心率的同时还将会抑制心肌收缩,导致低血压,不仅如此,β受体阻滞剂还具有不少临床禁忌证,如:严重的支气管哮喘、高度房室传导阻滞、急性心力衰等,以上情形均限制了β受体阻滞剂在临床使用以及剂量的调整[4]。伊伐布雷定作为一种新型的If电流抑制剂,通过阻断钙离子通道,调节窦房结细胞的自律活动,达到降低心率的作用,从而减少心肌的氧耗,进而可改善心力衰竭患者的心功能[5]。本次研究的结果证实,β受体阻滞剂与伊伐布雷定联用,可在不升高不良反应发生率的同时降低患者心率,进一步减少心脏氧耗,同时增加心脏舒张期冠脉灌注,进而达到改善ICM患者心功能,提高其活动耐量的作用。
国内外近年均有研究表明,伊伐布雷定具有抑制心肌细胞内炎症因子的表达[6-8],下调单核巨噬细胞的特异性趋化的过程,从而减缓动脉粥样硬化进程,具有重要的内皮保护作用[9-11]。有研究表明,hs-CRP在体内通过介导的补体可促进炎性反应发生,导致细胞微环境紊乱,损伤血管内皮,导致脂质在血管内沉积,促进动脉粥样斑块的形成,与冠脉粥样硬化有着密切的联系[12-14]。并且本研究结果提示两组患者在治疗前后心室重塑情况均有改善,但伊伐布雷定组比起对照组具有更优秀的调控局部炎症反应、减少细胞损伤的能力,但对照组中该方面作用不明显。故本研究表明伊伐布雷定不仅仅只是一种单纯控制患者心率的药物,它还具有一定的对抗炎症反应、减轻细胞损伤的作用,在缺血性心肌病伴心力衰竭的患者治疗之中有优秀的应用前景,但本研究样本较少,伊伐布雷定的其他功效仍需要进一步临床试验研究。

