超高效液相色谱-串联质谱法测定医用口罩中有机磷酸酯
侯敏敏,史亚利,蔡亚岐
(1. 中国科学院生态环境研究中心,环境化学与生态毒理学国家重点实验室,北京 100083;2. 国科大杭州高等研究院 环境学院,浙江 杭州 310024;3. 中国科学院大学,北京 100049)
有机磷酸酯(OPEs)作为阻燃剂和增塑剂广泛应用于建筑材料、电子产品、纺织品、泡沫家具以及涂料等消费品中[1-2]。随着卤系阻燃剂,如多溴联苯醚的限制使用,有机磷酸酯作为替代品,其生产和使用量逐年增加[3]。由于有机磷酸酯主要作为添加型的阻燃剂,因此很容易从消费品中释放进入环境,进而通过呼吸、灰尘摄食或饮食暴露于人体[4-6]。部分毒理学研究证实有机磷酸酯与生物体的一些不良健康状况有关,如癌症[1]、内分泌紊乱[7-8]、不良妊娠结局[9-10]、发育以及神经发育疾病[11]等。因此,有机磷酸酯作为一类在环境中广泛存在且危害人体健康的污染物引起了研究者的广泛关注。
2019 年以来,随着新冠病毒(COVID-19)的爆发和全球病例的逐渐增多,戴口罩被认为是一种能够有效对抗病毒传播的物理干预措施[12]。因此,受新冠病毒的影响,口罩的需求大幅增加,我国众多具有生产资质的企业纷纷加入了医用口罩的生产行列。2019年,我国口罩产量超50亿只,可用于防护病毒的医用口罩占比54%。2020年3月到年底,我国共出口医用口罩650亿只[13]。医用口罩一般是由两层纺粘无纺布中间增加一层熔喷无纺布制成,所用原材料属于纺织品。已有研究在各种纺织品类消费品中检测到有机磷酸酯[14-16]。我国关于医用口罩的国家标准要求,医用口罩所用材料不应具有易燃性,续燃时间不超过5 s[17-18]。由于缺乏更为详细的相关标准以及生产监管制度的不完善,我国所生产的医用口罩中是否添加有机磷酸酯为其提供阻燃性能目前尚不清楚。近两年,口罩已成为人们日常生活的必需品,而口罩中存在的化学物质可能会通过呼吸以及皮肤接触进入人体,因此有必要对医用口罩中的有害物质进行监测。
本研究首先建立了医用口罩中磷酸三甲酯等16 种有机磷酸酯的超高效液相色谱-串联质谱(UPLC-MS/MS)检测方法,并采用该方法对我国市售的医用口罩中16 种OPEs 进行测定,旨在判断其中是否添加有机磷酸酯阻燃剂。
1 实验部分
1.1 仪器与试剂
UltiMate 3000 超高效液相色谱仪(美国Thermo Fisher 公司);Triple quadTM三重四极杆串联质谱检测系统(MS/MS,美国AB SCIEX 公司);固相萃取柱(ENVI-18,6 mL/500 mg,Supelco 公司);超纯水制备系统(美国Millipore 公司);KQ-500DB 型数控超声波清洗器(昆山市超声仪器有限公司);氮吹浓缩仪(东莞市谱标实验器材科技有限公司)。
甲醇、乙腈、二氯甲烷、正己烷(色谱纯,美国Fisher 公司);16 种目标分析物(表1)及内标的标准品:包括磷酸三甲酯(TMP)、磷酸三乙酯(TEP)、磷酸三丙酯(TPrP)、磷酸三正丁酯(TnBP)、磷酸三异丁酯(TiBP)、磷酸三丁氧酯(TBOEP)、磷酸三(2-氯乙基)酯(TCEP)、磷酸三(1-氯-2-丙基)酯(TCIPP)、磷酸三(1,3-二氯-2-丙基)酯(TDCPP)、磷酸三苯酯(TPHP)、磷酸三甲苯酯(TMPP)、2-乙基己基苯基磷酸酯(EHDPP)和磷酸甲苯二苯酯(CDPP)购自i国Dr. Ehrenstorfer 公司;间苯二酚双(磷酸二苯酯)(RDP)、双酚A 双(磷酸二苯酯)(BABP)、四(2-氯乙基)二氯异戊基二磷酸酯(V6)、TCIPP-D18和TCEP-D12购自加拿大Toronto Research Chemicals 公司;TMP-D9、TEP-D15和TPrPD21购自加拿大C/D/N Isotopes 公司;TnBP-D27和TPHP-D15购自美国Cambridge Isotope Laboratories公司。
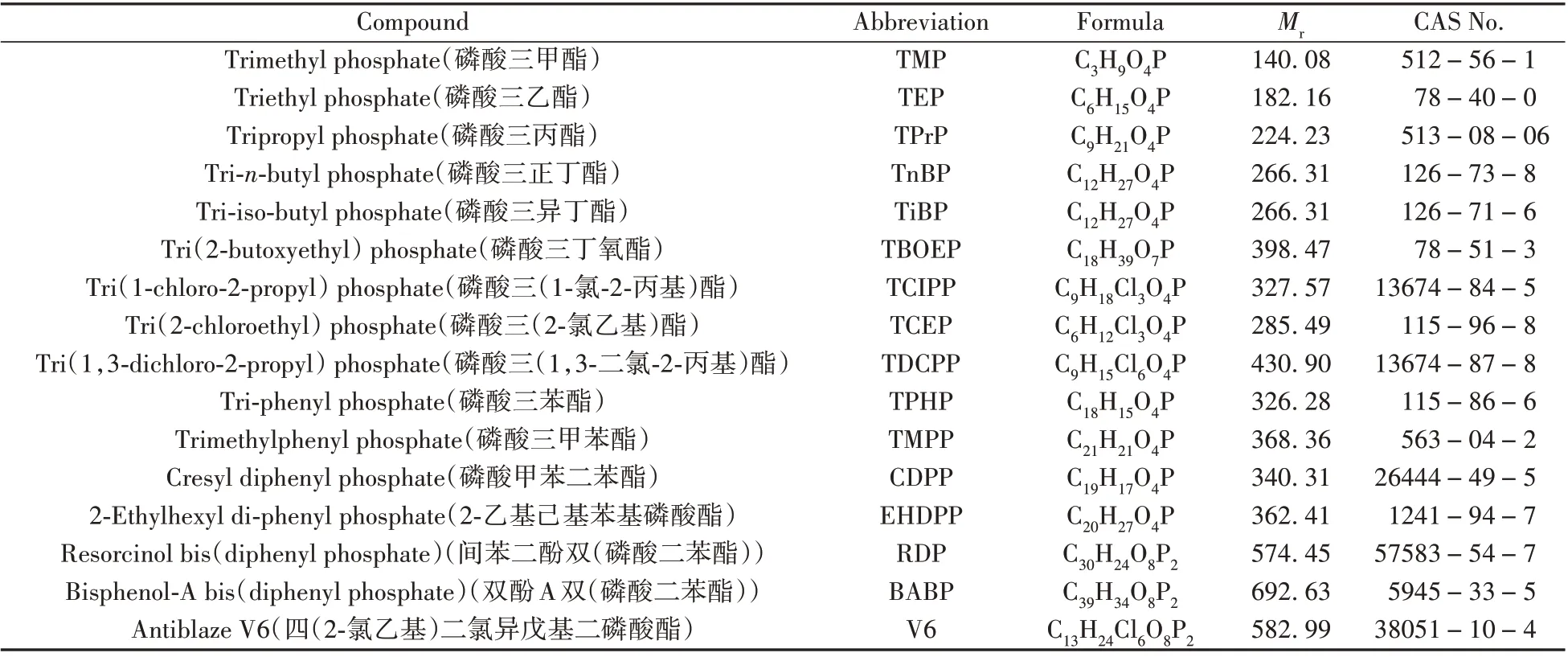
表1 16种OPEs的分子式、相对分子质量及CAS号Table 1 Formulas,relative molecular masses and CAS numbers of 16 OPEs
1.2 标准溶液的配制
将各有机磷酸酯标准品以及内标标准品用乙腈配制成质量浓度为1 000 mg/L 的标准储备溶液。分别量取10 μL标准储备溶液,用乙腈定容至10 mL,配制成质量浓度为1 mg/L的混合标准储备溶液和内标混合溶液,于-4 ℃保存。使用时,用甲醇配制质量浓度为0.1、0.5、2、5、10、20、50 μg/L 的标准工作溶液。
1.3 样品采集与前处理
2020 年9 月购买42 个来自37 种品牌的医用口罩,包括医用外科口罩(n= 21),一次性医用口罩(n=18)以及医用护理口罩(n=3)3种类型。
用剪刀准确剪取口罩四分之一的面积(0.416 dm2),剪成直径约3×3 mm 的碎片于15 mL 玻璃离心管中。加入10 μL质量浓度为1 mg/L的内标混合溶液,再加入10 mL甲醇,超声萃取30 min后,转移上清液至另一干净的玻璃离心管中;再向残余部分加入5 mL 甲醇,重复超声萃取2 次;将3 次萃取所得上清液合并,氮吹浓缩至近干后,加入30 mL超纯水待净化。
样品净化过程参考本课题组的前期研究[19]:依次采用5 mL 乙腈和5 mL 超纯水活化ENVI-18 固相萃取小柱;将30 mL 萃取溶液加载到萃取小柱上,用5 mL 超纯水清洗小柱,负压下抽干约40 min;然后用6 mL含有25%二氯甲烷的乙腈进行洗脱,洗脱液氮吹至近干,以甲醇定容至1 mL,过0.22 μm 的有机滤膜后上机检测。
1.4 仪器条件
色谱条件:色谱柱选用Acquity UPLC BEH C18(2.1 mm × 100 mm,1.7 μm)连接保护柱Acquity UPLC BEH C18(2.1 mm×5 mm,1.7 μm);柱温为25 ℃;流动相:A为5 mmol/L 乙酸铵缓冲溶液,B为甲醇;流速:400 μL/min。梯度洗脱程序为:0~1 min,10%~40% B;1~4 min,40%~90% B;4~4.1 min,90%~100%B;4.1~9 min,100%B;9~9.1 min,100%~10%B;9.1~13 min,10%B。
质谱条件:离子源为电喷雾离子源正离子模式(ESI+);检测方式为多反应监测(MRM)模式;离子源喷雾电压为5 000 V,温度为600 ℃,气帘气压力为0.14 MPa,碰撞气压力为0.02 MPa,雾化气压力为0.34 MPa,辅助雾化气压力为0.28 MPa。目标物质的定性定量离子对及其他质谱检测参数见表2。
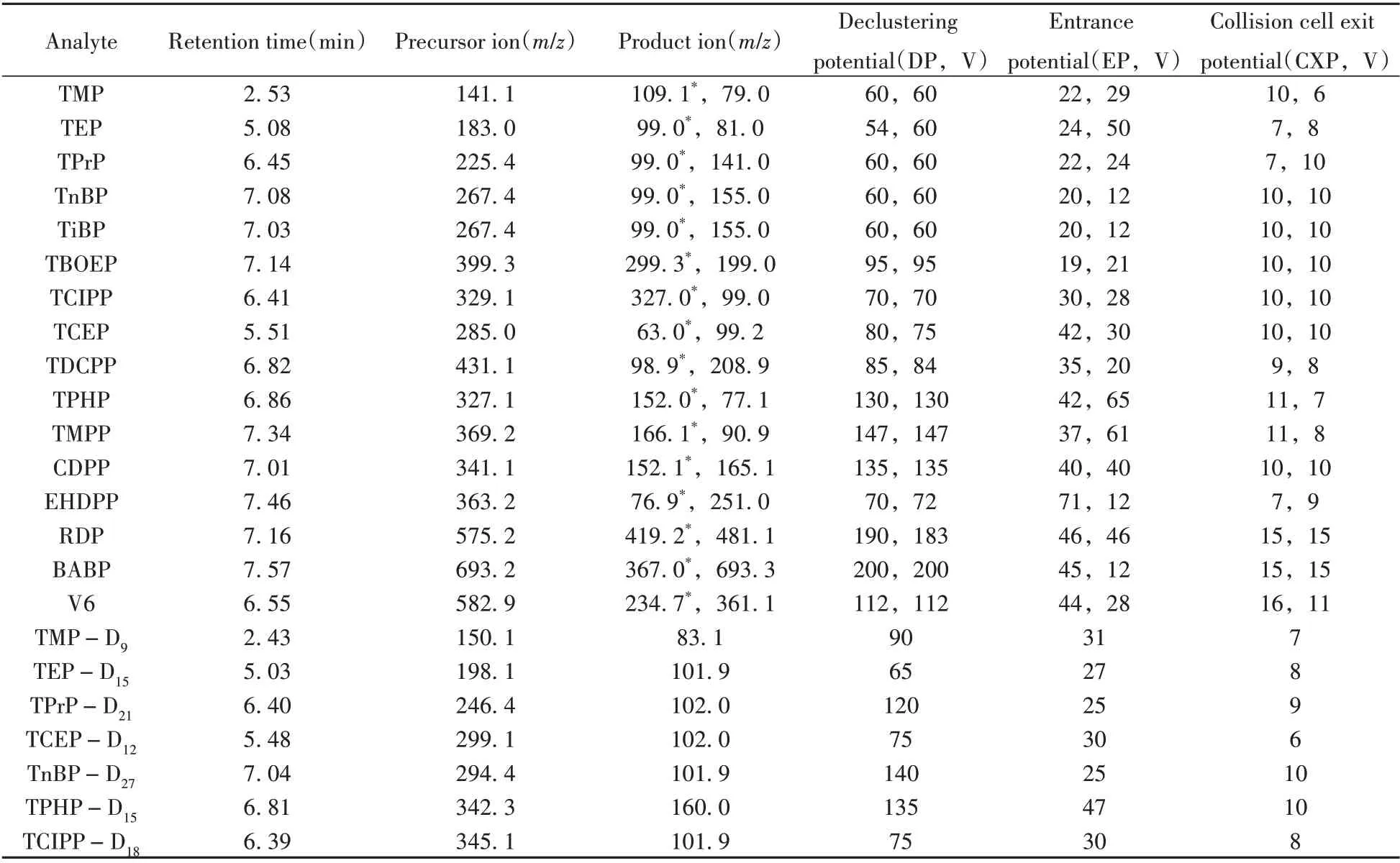
表2 16种OPEs的质谱参数Table 2 MS parameters for 16 OPEs
2 结果与讨论
2.1 萃取溶剂的优化
本研究涉及的16 种OPEs 具有较广泛的物理化学性质,为有效地提取口罩中目标物质,选择合适的萃取溶剂至关重要。实验对比了二氯甲烷-正己烷(1∶1,体积比)、二氯甲烷-乙腈(1∶1,体积比)和甲醇3种萃取溶剂对口罩样品中16种OPEs的提取效果(见图1)。结果显示,二氯甲烷-正己烷(1∶1)对于芳香基的OPEs(如EHDPP、TMPP、RDP和BABP)的提取效果较差,回收率均低于20.0%。使用二氯甲烷-乙腈(1∶1)为萃取溶剂时,TMPP、CDPP、RDP 和BABP 受基质效应影响,回收率均大于120%,且CDPP 和BABP 的回收结果精密度较差,相对标准偏差(RSD)大于15%。而使用甲醇为萃取溶剂时,16 种OPEs 均有较好的回收效果,回收率为75.0%~126%,RSD 为0.80%~18%。因此,实验选择甲醇为萃取溶剂。
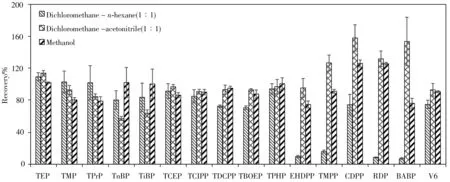
图1 3种萃取溶剂对16种目标化合物的萃取回收率(n=3)Fig.1 Recoveries of 16 OPEs using three different extracting solvents(n=3)
2.2 净化方法的优化
本课题组之前的研究已证实ENVI-18 小柱对于OPEs 具有良好的净化效果[19]。但考虑到净化过程中需要负压抽干柱子40 min,消耗时间,因此参考文献方法[16],本实验对比了以下两种净化方法:①ENVI-18 小柱用乙腈和超纯水依次活化后,将换相成水溶液的萃取液上样,负压抽干柱子后,采用6 mL 含25%二氯甲烷的乙腈溶液进行洗脱并收集;②ENVI-18 小柱用甲醇活化后,直接加载甲醇萃取液并收集,再用6 mL 甲醇进行洗脱并收集,将两次收集的溶液合并。两种净化方法收集的洗脱液氮吹至近干,加入1 mL 甲醇定容,上机分析。结果表明,两种净化方法对16 种OPEs 均有较好的回收效果,回收率分别为75.0%~126%和76.2%~182%,RSD 分别为0.80%~18%和0.10%~13%。第二种净化方法虽然节省了负压抽干净化小柱的时间,但CDPP 的回收率为182% ± 7.6%,存在较大的基质干扰。因此,最终选择第一种净化方法。在最佳实验条件下,16 种OPEs 标准溶液(10 μg/L)的色谱图见图2。
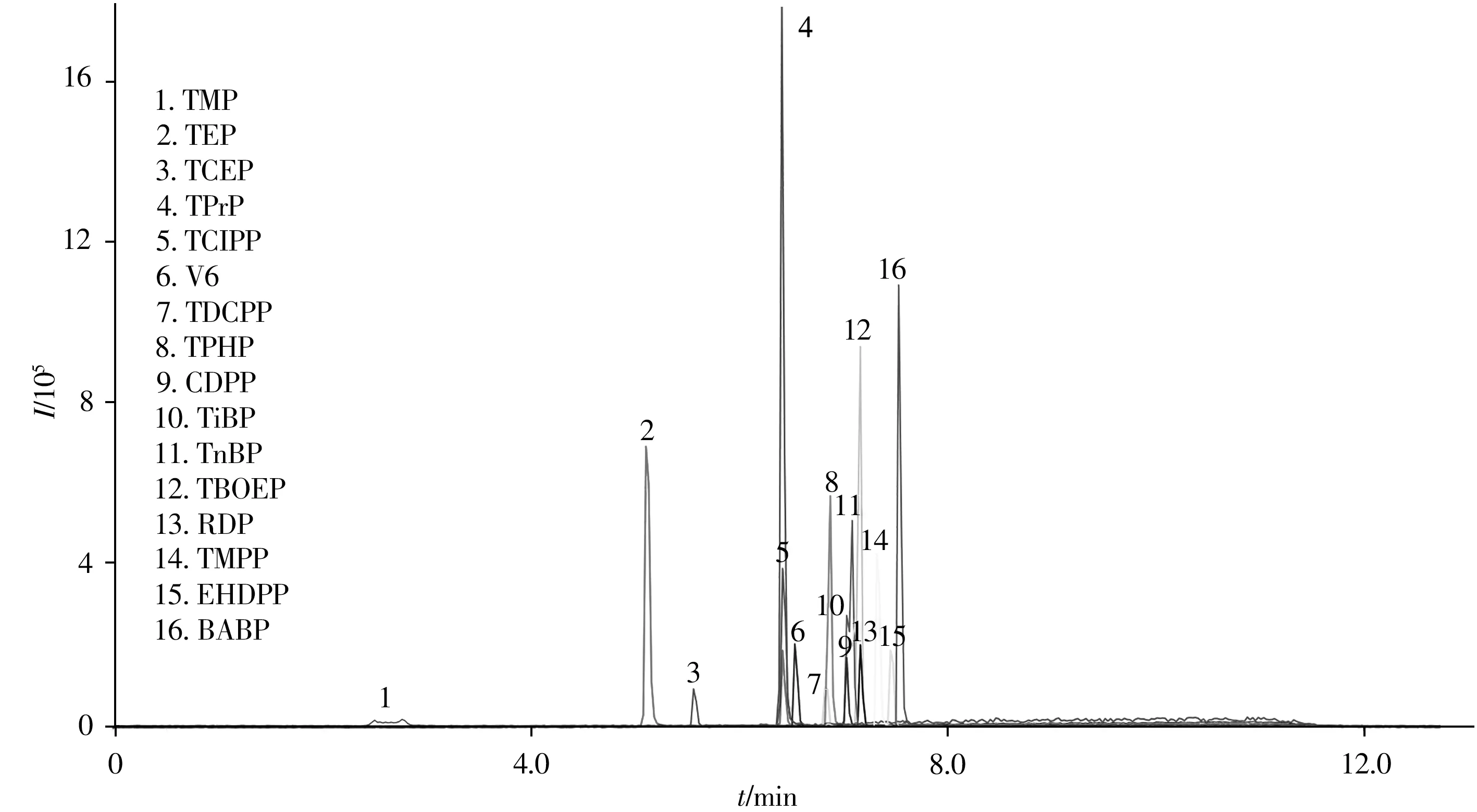
图2 16种OPEs标准溶液的总离子流色谱图Fig.2 Total ion chromatogram of 16 OPEs standard solutions
2.3 线性关系、检出限与定量下限
按照“1.4”仪器条件,分析一系列不同质量浓度的标准溶液(0.1、0.5、2、5、10、20、50 μg/L),以目标物质与内标的质量浓度比为横坐标(x),峰面积比为纵坐标(y)绘制标准曲线。结果表明,16 种OPEs在0.1~50 μg/L 范围内均呈良好的线性关系(r>0.995)。分别以3倍和10倍的信噪比计算方法的检出限(LOD)和定量下限(LOQ),16 种OPEs 的LOD 为0.004 60~1.03 ng/dm2,LOQ 为0.015 2~3.43 ng/dm2(见表3)。
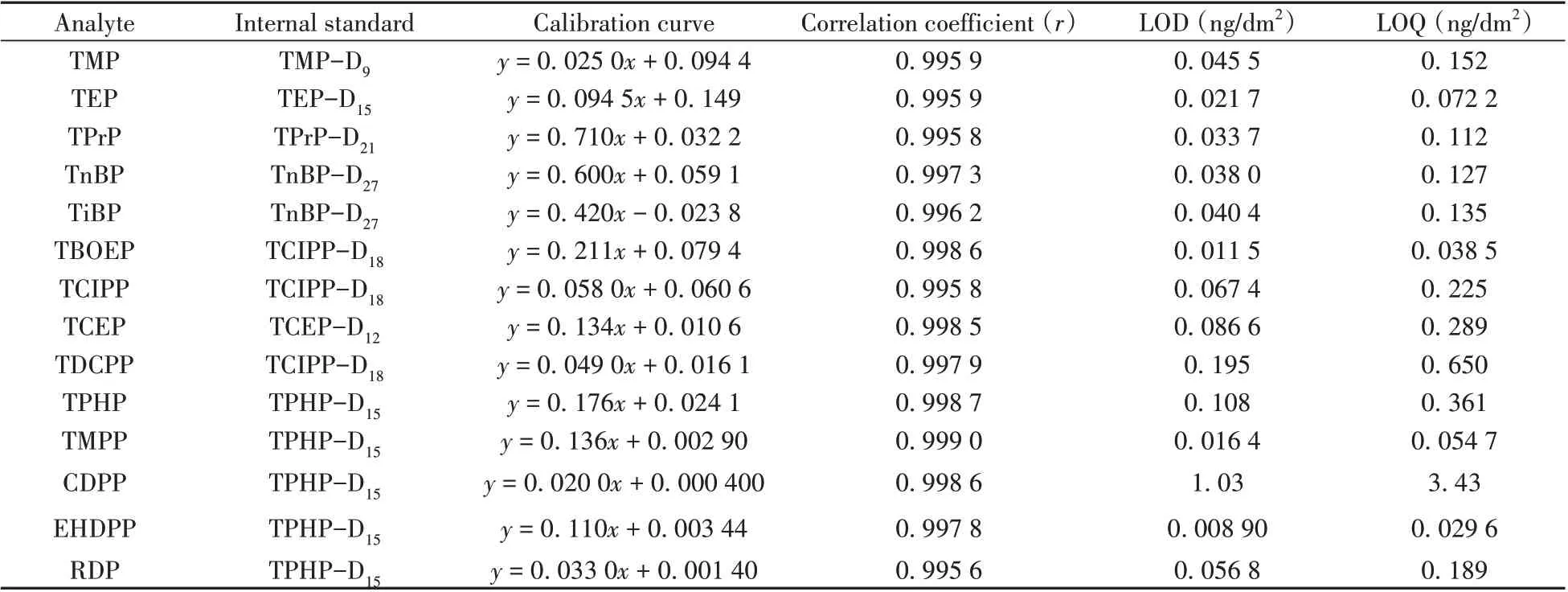
表3 16种OPEs的线性关系、检出限和定量下限Table 3 Linear relations,limits of detection(LOD)and limits of quantitation(LOQ)of 16 OPEs

(续表3)
2.4 加标回收率与相对标准偏差
为进一步确认前处理与仪器方法的有效性和精密度,以含有较低浓度OPEs 的口罩样本为空白基质,分别取0.416 dm2面积,加入5、20、40 ng的混合标准物质,按照本方法进行检测,每个浓度水平进行3 个平行样本,计算加标回收率。16 种OPEs 的加标回收率为68.8%~140%,RSD 为0.70%~18%(见表4)。7种内标的加标回收率为(76.3±0.90)%~(98.1±5.4)%。表明该方法满足检测要求,精密度良好。
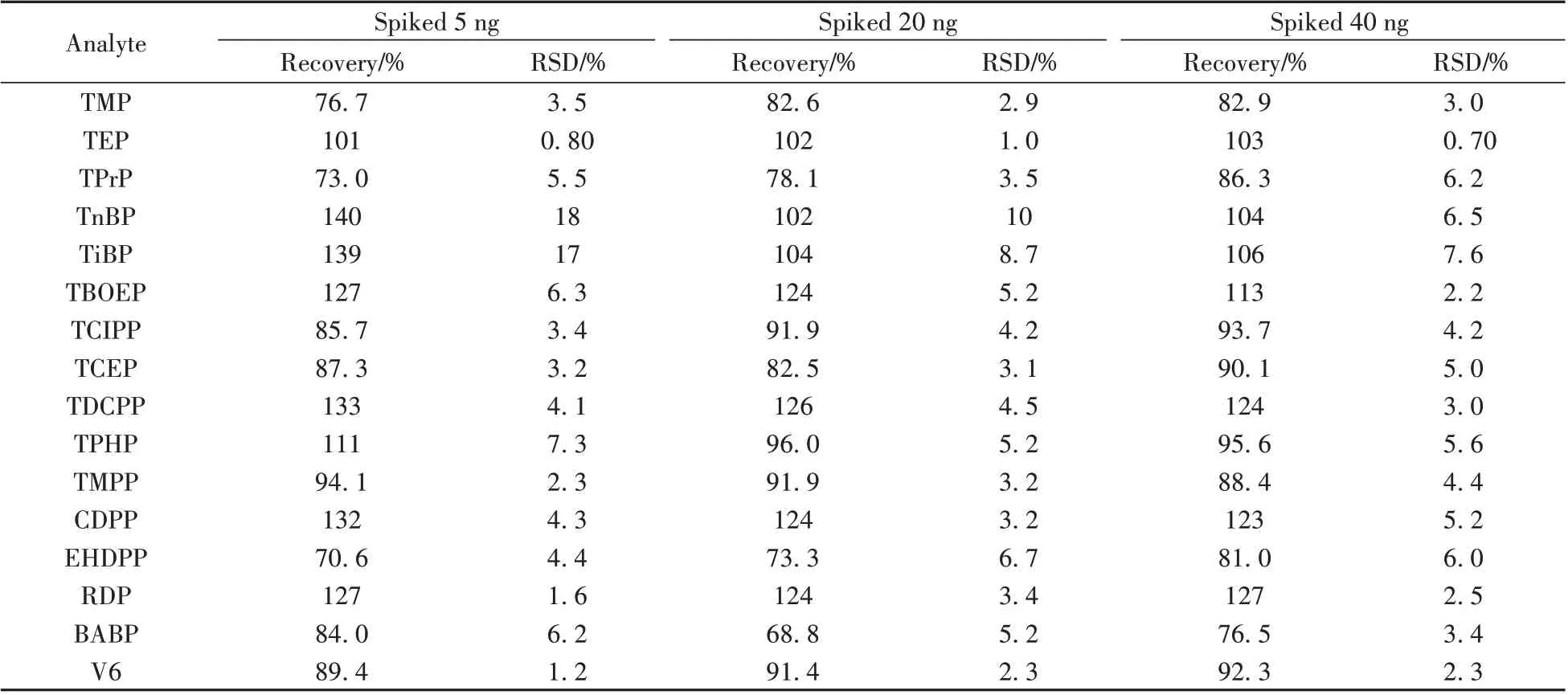
表4 16种OPEs在口罩中的回收率和相对标准偏差(n=3)Table 4 Spiked recoveries and relative standard deviations(RSD)of 16 OPEs in mask samples(n=3)
2.5 样品分析
利用本方法对42 个市售口罩样本进行分析,结果见表5。结果显示,16 种OPEs 的总浓度范围为6.60~2 387 ng/dm2,中位浓度为34.2 ng/dm2。除TMP、TPrP、CDPP 和RDP 外,其余12 种OPEs 的检出率均大于50%,其中TCIPP、TCEP、TPHP 和EHDPP 在全部样本中均检出,表明这些OPEs在口罩中普遍存在。TPHP 是口罩中检出的最主要物质,占16 种OPEs 总浓度的42%,浓度范围为0.131~2 274 ng/dm2,中位浓度为6.88 ng/dm2;其次为TCIPP,占总浓度的23%,浓度范围为0.370~79.8 ng/dm2,中位浓度为3.70 ng/dm2。此外,不同品牌与类型的口罩中各OPEs的浓度无显著差异(p>0.05)。整体来看,口罩中虽有12 种OPEs 普遍检出,但浓度较低,加之OPEs 在室内空气和灰尘中普遍存在,可在一定程度上说明口罩中检出的OPEs并非人为添加,可能是在生产和包装过程中受空气或塑料包装污染所致。
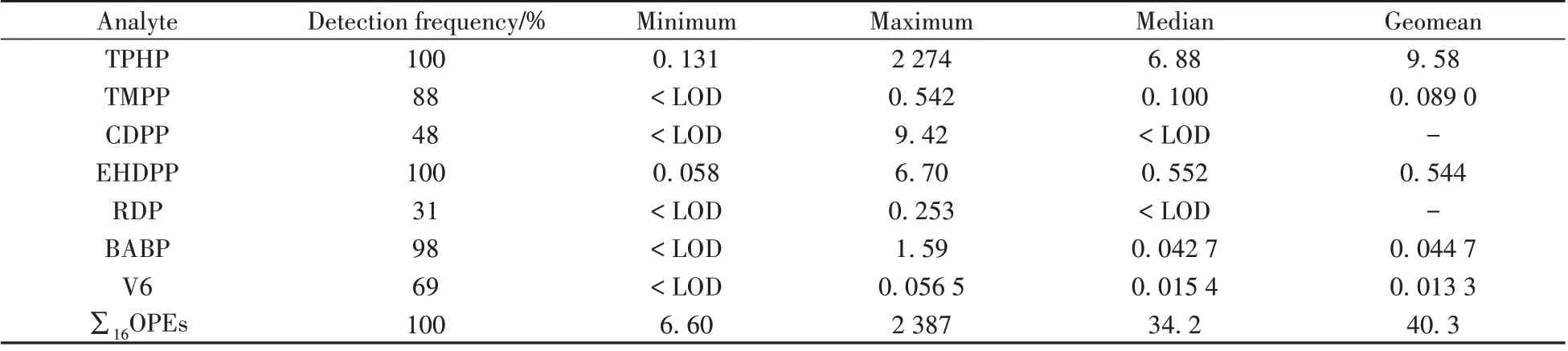
(续表5)
3 结 论
本研究采用超声萃取结合超高效液相色谱-串联质谱,建立了医用口罩样本中16种有机磷酸酯的检测方法。方法学考察表明该方法灵敏度高,对目标物质有较好的萃取效果,重现性好。基于该方法对市售口罩样本分析结果表明,有机磷酸酯普遍检出但浓度较低,可能是由于空气污染或塑料包装污染所致。

