金线莲黄酮调控RKIP抑制喉鳞癌细胞增殖、迁移和侵袭的机制
王慧敏 李静波 王俊杰 陈文明 蔡纪堂
(河南省中医院耳鼻喉科,河南 郑州 450000)
喉癌属于头颈部恶性肿瘤,随着环境污染及生活节奏的加快导致喉癌发病率逐年增加,其主要病理类型为喉鳞状细胞癌,目前临床主要采用手术、放疗及化疗等方式治疗喉癌,虽有一定治疗效果,但仍有大部分患者仍发生复发及转移而降低治疗效果〔1,2〕。由于喉癌患者早期症状较为隐匿,导致早期诊断准确率较低,大部分患者就诊时已处于进展期,导致患者预后差,已有研究表明饮食不健康、吸烟等均可能诱发喉癌〔3〕。中医药抗癌已成为研究热点,研究表明部分中医药可有效治疗喉癌,但关于其具体作用机制尚未完全阐明〔4〕。因而基于喉癌发病机制积极寻找治疗喉癌的新型中药对提高治疗效果及临床合理用药均有重要意义。研究发现金线莲对宫颈癌、结肠癌、喉癌的生长增殖有一定的抑制作用〔5〕。但金线莲黄酮对喉癌增殖等生物行为的影响及其机制目前还未有研究。Raf1激酶抑制蛋白(RKIP)在下咽癌下调表达,RKIP低表达可促进下咽癌发生转移〔6〕。相关研究报道指出RKIP可能通过下调血管内皮生长因子(VEGF)表达进而抑制喉鳞癌发生及转移〔7〕。但有关金线莲黄酮是否通过调控RKIP表达而杀伤喉鳞癌细胞的内在机制尚未见报道。因此,本研究旨在探讨金线莲黄酮对喉鳞癌细胞增殖、迁移及侵袭的影响,初步分析其是否可通过调控RKIP表达而发挥作用。
1 材料与方法
1.1材料与试剂 喉癌Hep-2细胞购自美国ATCC细胞库。金线莲购自福建漳州且经属性鉴定为兰科开唇兰属植物福建金线莲,精密称取1 g金线莲,全株剪碎,磨成汁液,水浴提取,过滤,按照参考文献进行操作〔8〕,测定吸光度,计算金线莲中总黄酮含量。DMEM培养基、胎牛血清与胰蛋白酶均购自美国Gibco公司;LipofectamineTM2000转染试剂盒购自美国Invitrogen公司;siRNA-RKIP及其阴性对照均购自上海吉玛制药技术有限公司;四甲基偶氮唑蓝(MTT)检测试剂盒购自美国Amresco公司;Transwell小室与Matrigel基质胶均购自北京乐博生物科技有限公司;Trizol试剂、反转录试剂盒与实时荧光定量聚合酶链反应(qRT-PCR)试剂盒均购自大连宝生物工程有限公司;蛋白裂解液与BCA蛋白定量试剂盒均购自上海碧云天生物技术有限公司;兔抗人RKIP多克隆抗体、兔抗人p21、CyclinD1抗体与辣根过氧化物酶(HRP)标记的山羊抗兔IgG二抗均购自美国CST公司;兔抗人E-cadherin抗体购自美国BD公司;兔抗人基质金属蛋白酶(MMP)-2抗体购自美国Santa Cruz公司。
1.2方法
1.2.1细胞培养、药物处理及分组 喉癌Hep-2细胞常规复苏后置于含有10%胎牛血清及青霉素-链霉素双抗的DMEM培养基进行培养,收集对数生长期细胞用0.25%胰蛋白酶消化细胞,调整细胞密度为5×104个/ml,放入37℃、5%CO2培养箱内继续培养24 h,随机分为对照组、金线莲黄酮(0.04、0.08、0.16、0.32、0.64 mg/ml)组〔9〕,每组均设置6个复孔。为验证RKIP过表达对喉癌细胞增殖、迁移及侵袭的影响,分别将RKIP过表达载体及空载体分别转染入喉癌Hep-2细胞,分别为pcDNA3.1-RKIP组、pcDNA3.1组。另将siRNA-RKIP及其阴性对照分别转染入喉癌Hep-2细胞12 h,加入浓度为0.16 mg/ml的金线莲黄酮处理48 h,分别为金线莲黄酮0.16 mg/ml+si-RKIP组、金线莲0.16 mg/ml+si-NC组,目的是验证金线莲黄酮是否通过调控RKIP表达进而影响喉癌细胞增殖、迁移及侵袭过程,转染步骤均严格按照LipofectamineTM2000转染试剂盒说明书进行操作。
1.2.2MTT检测细胞增殖 收集对数生长期喉癌Hep-2细胞,胰蛋白酶消化细胞,调整细胞密度为5×104个/ml,收集细胞后以每孔5×104个细胞的密度接种于96孔板,每组均设置3个复孔,分别于转染或处理后的24 h、48 h、72 h时,加入20 μl MTT溶液,放入恒温培养箱继续培养4 h,弃培养基,加入150 μl二甲基亚砜(DMSO),低速振荡混匀20 min,利用酶标仪检测波长为490 nm处各孔吸光度(OD)值。
1.2.3Transwell实验检测细胞迁移 用不含血清的DMEM培养基200 μl稀释各组喉癌Hep-2细胞,细胞密度为1×105/ml,取200 μl细胞稀释液放入Transwell小室上室,取含10%胎牛血清的DMEM培养基600 μl加入Transwell小室下室,置于37℃、5%CO2体积分数、相对湿度95%的培养箱内继续培养24 h,取出Transwell小室,棉签擦拭Transwell小室聚碳酸酯膜表面细胞,多聚甲醛固定10 min,0.1%结晶紫染液染色15 min,置于显微镜下观察并随机选取5个视野计算迁移细胞个数。
1.2.4Transwell实验检测细胞侵袭 取各组对数生长期喉癌Hep-2细胞,用0.25%胰蛋白酶消化细胞,加入无血清的DMEM培养基制备细胞悬液(2×105/ml),预备实验:使用无血清DMEM培养基稀释基质胶,取100 μl稀释液包被Transwell小室底部的上室面,Transwell小室上室内加入200 μl细胞悬浮液,Transwell小室下室内加入600 μl含10%胎牛血清的DMEM培养基,放入恒温培养箱内继续培养24 h,取出Transwell小室,棉签擦拭Transwell小室上室表面细胞,磷酸盐缓冲液(PBS)冲洗3次×5 min,多聚甲醛固定10 min,0.1%结晶紫染液染色15 min,置于显微镜下观察并随机选取5个视野计算侵袭细胞个数。
1.2.5qRT-PCR检测细胞中RKIP mRNA表达水平 收集各组喉癌Hep-2细胞,采用Trizol法提取细胞总RNA,紫外分光光度计检测RNA浓度,选取A260/A280≥1.8的RNA样本进行后续实验,参照反转录试剂盒说明书合成模板链cDNA,采用qRT-PCR法检测RKIP mRNA相对表达量,qRT-PCR条件为95℃ 2 min,95℃ 30 s,60℃ 30 s,72℃ 30 s,循环40次。每个样品均设置3个复孔,采用2-ΔΔCt法计算RKIP mRNA相对表达量。
1.2.6Western印迹检测RKIP、E-cadherin、P21、CyclinD1、MMP-2蛋白表达 收集各组喉癌Hep-2细胞,加入蛋白裂解液冰上裂解30 min,12 000 r/min离心10 min提取细胞总蛋白,BCA法测定蛋白浓度,取30 μg蛋白进行十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE),将分离的蛋白凝胶转移至聚偏氟乙烯(PVDF)膜,室温条件下5%脱脂奶粉封闭1 h,分别加入各蛋白一抗,TBST洗涤,分别加入二抗,室温孵育1 h,TBST洗涤,ECL显影,利用凝胶分析系统及Image J软件分析各条带灰度值。
1.3统计学方法 采用SPSS21.0软件进行t检验、单因素方差分析。
2 结 果
2.1金线莲黄酮对细胞Hep-2增殖的影响 与对照组相比,金线莲黄酮0.04 mg/ml组、金线莲黄酮0.08 mg/ml组、金线莲黄酮0.16 mg/ml组、金线莲黄酮0.32 mg/ml组、金线莲黄酮0.64 mg/ml组喉癌Hep-2细胞增殖活性均显著降低,CyclinD1蛋白水平显著降低,而p21蛋白水平显著升高且呈剂量依赖性(均P<0.05),见表1、图1。表明金线莲黄酮可明显抑制喉癌Hep-2细胞增殖。选用48 h时喉癌Hep-2细胞增殖活性约为50%的金线莲黄酮浓度(0.16 mg/ml)做后续使用。

表1 金线莲黄酮对细胞Hep-2增殖的影响

1~6:对照组;金钱莲黄酮0.04 mg/ml组;金钱莲黄酮0.08 mg/ml组;金钱莲黄酮0.16 mg/ml组;金钱莲黄酮0.32 mg/ml组;金钱莲黄酮0.64 mg/ml组图1 金线莲黄酮对细胞Hep-2增殖蛋白表达的影响
2.2金线莲黄酮对细胞Hep-2迁移、侵袭的影响 与对照组相比,金线莲黄酮0.16 mg/ml组喉癌Hep-2细胞迁移及侵袭细胞数目均显著减少(P<0.001),金线莲黄酮0.16 mg/ml组喉癌Hep-2细胞中E-cadherin表达水平显著高于对照组(P<0.001),而MMP-2表达水平显著低于对照组(P<0.001),见图2、表2、图3。表明金线莲黄酮可明显抑制喉癌Hep-2细胞迁移及侵袭。

图2 金线莲黄酮对细胞Hep-2迁移、侵袭的影响(结晶紫染色,×200)

图3 金线莲黄酮对细胞Hep-2迁移、侵袭蛋白表达的影响
2.3金线莲黄酮对细胞Hep-2中RKIP表达的影响 与对照组相比,金线莲黄酮0.16 mg/ml组喉癌Hep-2细胞中RKIP mRNA及蛋白水平均显著升高(P<0.001),见图4、表2。

表2 金线莲黄酮对细胞Hep-2迁移、侵袭、PKIP表达的影响

图4 金线莲黄酮对细胞Hep-2中RKIP蛋白表达的影响
2.4过表达RKIP对细胞Hep-2增殖、迁移、侵袭的影响 与pcDNA3.1组相比,pcDNA3.1-RKIP组喉癌Hep-2细胞中RKIP蛋白水平显著升高(P<0.001),提示转染效果良好。同pcDNA3.1组相比,pcDNA3.1-RKIP组喉癌Hep-2细胞活性显著降低(P<0.001),迁移及侵袭细胞数目均显著减少(P<0.001),E-cadherin、p21蛋白水平均显著升高(P<0.001),而CyclinD1、MMP-2蛋白水平均显著降低(P<0.001),见表3、图5。

表3 过表达RKIP对细胞Hep-2增殖、迁移、侵袭的影响

图5 过表达RKIP对细胞Hep-2增殖、迁移、侵袭蛋白表达的影响
2.5抑制RKIP表达能逆转金线莲黄酮对细胞Hep-2增殖的作用 与金线莲黄酮0.16 mg/ml+si-NC组相比,金线莲黄酮0.16 mg/ml+si-RKIP组喉癌Hep-2细胞活性显著升高(P<0.001),CyclinD1蛋白水平显著升高(P<0.001),而p21蛋白水平显著降低(P<0.001),见图6、表4。
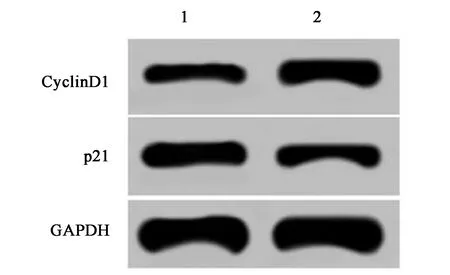
1、2:金线莲黄酮0.16 mg/ml+si-NC组;金线莲黄酮0.16 mg/ml+si-RKIP组;图7同图6 抑制RKIP表达能逆转金线莲黄酮对细胞Hep-2增殖蛋白表达的影响

表4 抑制RKIP表达能逆转金线莲黄酮对细胞Hep-2增殖、迁移及侵袭的抑制作用
2.6抑制RKIP表达能逆转金线莲黄酮对细胞Hep-2迁移、侵袭的作用 与金线莲黄酮0.16 mg/ml+si-NC组相比,金线莲黄酮0.16 mg/ml+si-RKIP组喉癌Hep-2细胞迁移及侵袭细胞数目均显著增加(P<0.001),MMP-2蛋白水平显著升高(P<0.001),而E-cadherin、PKIP蛋白水平显著降低(P<0.001),见表4、图7。

图7 抑制RKIP表达能逆转金线莲黄酮对细胞Hep-2迁移、侵袭蛋白的影响
3 讨 论
头颈部恶性肿瘤中喉癌的发病率相对较高,目前临床治疗手段常可损伤正常组织干细胞增殖活性而引发胃肠道不良反应,严重降低患者生活质量甚至影响治疗效果〔10~12〕。现代医学对中医药治疗癌症的研究进展取得较大突破,因此探究中医药治疗喉癌的作用机制对抗肿瘤新药研发及应用提供理论依据。
金线莲有滋阴降火、消炎止痛及清凉解毒等功效,对高血压、肾炎、类风湿关节炎等均有较好治疗效果〔13〕。研究报道指出金线莲中多种活性成分可用于治疗多种恶性肿瘤,但关于其具体作用机制尚未完全阐明〔14〕。金线莲的多糖成分可通过干扰肺癌、结肠癌等多种恶性肿瘤细胞周期而抑制肿瘤细胞增殖进而发挥抗肿瘤作用〔15〕。金线莲的挥发油成分可通过引发线粒体凋亡途径进而促进肺癌细胞凋亡〔16〕。已有研究报道指出细胞周期改变、细胞凋亡减少及迁移能力增强均可促进肿瘤恶性进展,CyclinD1可正向调控细胞周期进程进而促进细胞增殖,而p21可通过抑制CyclinD1与相关蛋白结合进而抑制细胞增殖,上皮-间质转化(EMT)是促进肿瘤细胞迁移及侵袭的主要因素之一,E-cadherin表达上调预示EMT过程发生逆转,可抑制细胞转移,细胞侵袭相关蛋白MMP-2可明显促进肿瘤细胞侵袭〔17,18〕。说明金线莲黄酮可通过抑制喉鳞癌细胞增殖、迁移及侵袭进而影响肿瘤恶性进展。提示金线莲黄酮可能通过诱导EMT进程进而抑制喉鳞癌细胞迁移及侵袭。
RKIP属于磷脂酰乙醇胺结合蛋白家族成员,其可通过调控转录因子-核因子(NF)-κB及丝裂原活化蛋白激酶(MAPK)等信号通路进而影响细胞增殖及分化过程,研究表明RKIP属于抑癌基因且在肿瘤组织及细胞系中均呈低表达,RKIP低表达可影响肿瘤细胞稳定性进而增加细胞迁移及侵袭〔19〕。研究表明RKIP表达水平降低与鼻咽癌细胞迁移及侵袭密切相关,其可能通过激活NF-κB信号通路进而促进鼻咽癌细胞迁移及侵袭〔20〕。RKIP过表达可明显抑制前列腺癌等多种恶性肿瘤细胞转移〔21〕。本研究结果提示金线莲黄酮可能通过上调RKIP表达而减弱喉癌细胞增殖、迁移及侵袭能力;金线莲黄酮可通过上调RKIP表达进而降低喉癌细胞增殖、迁移及侵袭能力。
综上,金线莲黄酮有抑制喉鳞癌细胞增殖、迁移及侵袭的作用,其作用机制可能是通过上调RKIP表达而影响相关基因及蛋白表达而实现的,可为临床应用金线莲黄酮治疗喉鳞癌提供理论依据及实验基础。但关于金线莲黄酮对RKIP基因上游调控基因及其相关信号通路的调控作用仍需深入研究。

