水滑石衍生镍基纳米催化剂对邻苯二甲酸二辛酯加氢反应的调控
白国义,聂世琳,李文炅
(河北大学 化学与环境科学学院,河北 保定 071002)
增塑剂是高分子材料加工过程中添加的一种重要助剂,广泛应用于医疗用品、食品包装材料和儿童玩具等产品中.其中,邻苯二甲酸酯(PAEs)是目前应用最广泛、产量最大的一类增塑剂,但由于其分子结构中含有苯环,具有致癌性、致畸性,对人类健康存在潜在危害,很多国家都已禁止其在与人体密切接触的聚氯乙烯制品中使用[1].而环己烷-1, 2-二甲酸酯类增塑剂性能优异,无毒环保,被认为是最有可能替代PAEs的环保型增塑剂[2-4].
环己烷-1, 2-二甲酸酯的合成可分为酯化法和加氢法,其中PAEs催化加氢法是其最有效的合成方法.国内外学者[5-9]已经开展了PAEs加氢反应的研究,并取得了阶段性成果.例如,Tan等[5]报道了铝改性能显著提高铑基催化剂在邻苯二甲酸二辛酯(DOP)加氢反应中的活性.总体来说,由于芳环化学稳定性高,目前报道的PAEs加氢催化剂多为以钯、铑、钌等为主催化活性组分的贵金属催化剂,而贵金属储量低、价格昂贵,限制了其在工业生产中的应用.非贵金属催化下PAEs加氢反应的研究报道很少.Zhao等[6]将质量分数60% Ni-Al2O3-B等催化剂应用于DOP加氢反应中,发现活性镍表面积和催化剂孔径是影响催化剂活性的2个关键因素,但未报道催化剂的稳定性.因此,制备高性能非贵金属催化剂实现PAEs高效加氢是非常具有挑战性的.
在本团队长期开展新型镍基纳米催化剂制备及其加氢性能研究的基础上[10-14],考虑到水滑石材料所具有的限域效应、层间阴离子可调性等结构特性,笔者以镍铝水滑石作为前驱体,制备了一种Ni-AlO纳米催化剂,并研究了其在DOP加氢合成环己烷-1,2-二甲酸二辛酯(DEHHP)反应中的性能(图1).该催化剂表现出优异的催化性能,并通过一系列表征阐明了催化剂结构和性能之间的构效关系.

图1 DOP加氢合成DEHHP的反应方程式Fig.1 Synthetic equation of DEHHP by the hydrogenation of DOP
1 实验部分
1.1 催化剂的制备
Ni-AlO催化剂:将1.05 g Ni(NO3)2·6H2O和0.67 g Al(NO3)3·9H2O搅拌下溶于200 mL去离子水中,先搅拌1.5 h,再调节溶液pH值至9~10,继续搅拌0.5 h,再将其转移到水热釜中,升温至150 ℃水热48 h.然后,将混合物抽滤、洗涤、干燥后得到蓝色粉末.然后分别升至350、450、550 ℃,焙烧2 h,最后将焙烧后的粉末在450 ℃用H2还原2 h,得到Ni-AlO-T(T为焙烧温度) 催化剂(图2)[15].
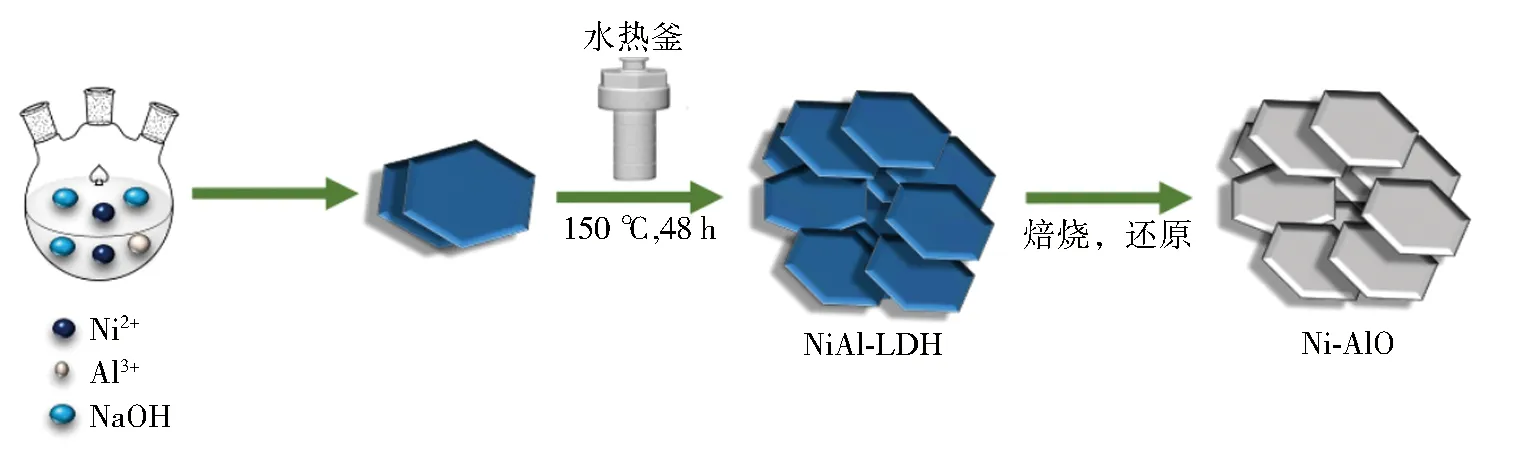
图2 Ni-AlO制备流程Fig.2 Preparation process of Ni-AlO
Ni-Al2O3催化剂:先将6.84 g Ni(NO3)2·6H2O溶于去离子水,在搅拌下加入1.0 g Al2O3载体.先在80 ℃下烘干,再升温至450 ℃焙烧2 h,最后在450 ℃用H2还原2 h,得到Ni-Al2O3催化剂.
1.2 催化剂的表征
采用美国安捷伦公司的7700原子发射光谱(ICP)测定催化剂中镍含量.催化剂的比表面积(BET)和孔体积通过美国麦克公司的TristarⅡ 3020比表面和孔结构分析仪测定.催化剂的物相结构通过德国布鲁克公司的D8 Advance X线粉末衍射仪(XRD)测定.催化剂的氢化学吸附和程序升温还原(H2-TPR)采用美国麦克公司的 AutoChem Ⅱ 2920 化学吸附仪测定.催化剂的形貌通过日本电子的Jsm-7500型扫描电子显微镜(SEM)和日本电子的Jem-2100F型透射电子显微镜(TEM)观察获得.
1.3 催化剂加氢性能测试
DOP催化加氢反应在配备有加热和搅拌装置的高压釜中进行.首先,将3.0 g DOP、0.025 g催化剂、60 mL正己烷依次加入到100 mL的高压釜中,密封并检查气密性后用氢气置换釜内空气3次.然后,用氢气加压到5.0 MPa,在150 ℃下反应1.0 h.反应结束后降温至室温,将反应液与催化剂离心分离,使用Agilent 7820A气相色谱仪进行定量分析,采用面积归一化法计算转化率和选择性[15],使用Thermo Trace1300 气质联用仪对产物进行结构鉴定.
2 结果与讨论
2.1 催化剂的表征
分析了2种镍基纳米催化剂的结构特征(表1),发现Ni-AlO催化剂的比表面积、镍含量、金属分散度等均优于Ni-Al2O3催化剂.这说明以水滑石为前驱体制备纳米催化剂能有效促进活性组分镍在载体上的分散,使所制备的镍基纳米催化剂不但具有更大的比表面积和孔体积,而且具有更大的金属分散度和氢吸附量,从而促进了催化剂中的镍与反应物的接触,提高了其加氢活性.

表1 2种镍基纳米催化剂的结构特征
图3为Ni-AlO和Ni-Al2O3催化剂的N2吸附脱附等温曲线.2种催化剂中均存在Ⅳ型等温曲线,说明其均为介孔材料[16-17],而在p/p0=0.40~1.0的相对压力区,Ni-Al2O3催化剂的回滞环更明显.此外,Ni-AlO催化剂显示出以36 nm为中心的宽中孔尺寸分布,而Ni-Al2O3催化剂主要为以8 nm为中心的孔(图3内嵌图).
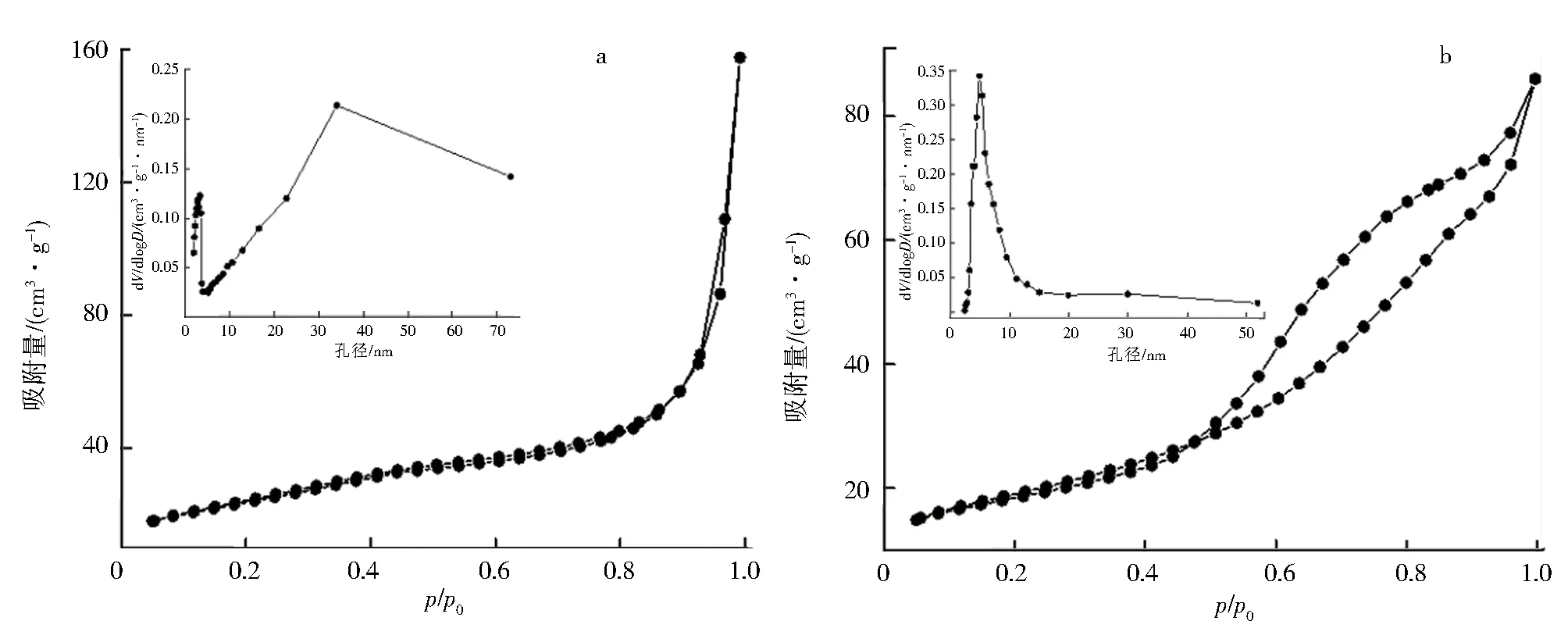
图3 Ni-AlO(a)和Ni-Al2O3(b)催化剂的N2吸附脱附等温线和孔径分布Fig.3 N2 adsorption-desorption isotherm and pore size distribution (inset) of Ni-AlO(a) and Ni-Al2O3(b) catalysts
对NiAl-LDH前驱体和Ni-AlO、Ni-Al2O3催化剂进行了XRD测试,结果如图4所示.NiAl-LDH前驱体在2θ为11.5°、22.1°、34.9°、60.9°、61.9°处出现衍射峰,可归属为水滑石的特征衍射峰[18].这些特征衍射峰在NiAl-LDH经过焙烧后几乎全部消失,同时在2θ为37.4°、43.7°、63.3°处出现了NiO的特征衍射峰[19],说明在焙烧的过程中水滑石转变为复合金属氧化合物.从图4中可以看出,水滑石衍生催化剂中NiO的衍射峰形较宽且不明显,说明该催化剂中NiO的粒径较小;与之对应,负载型催化剂在焙烧后得到的NiO特征衍射峰的峰形尖锐,说明在该催化剂中NiO的粒径明显较大(图4a).在还原后的Ni-AlO和Ni-Al2O3催化剂中(图4b),2θ为44.5°、51.8°、76.4°的峰为单质Ni的特征峰,说明2种氧化物中的NiO均被还原为单质Ni.因此,单质Ni是催化剂的活性中心.此外,还原后的Ni-AlO催化剂中Ni的特征衍射峰峰形弥散,表明Ni-AlO催化剂中Ni保持高分散状态,且粒径较小.
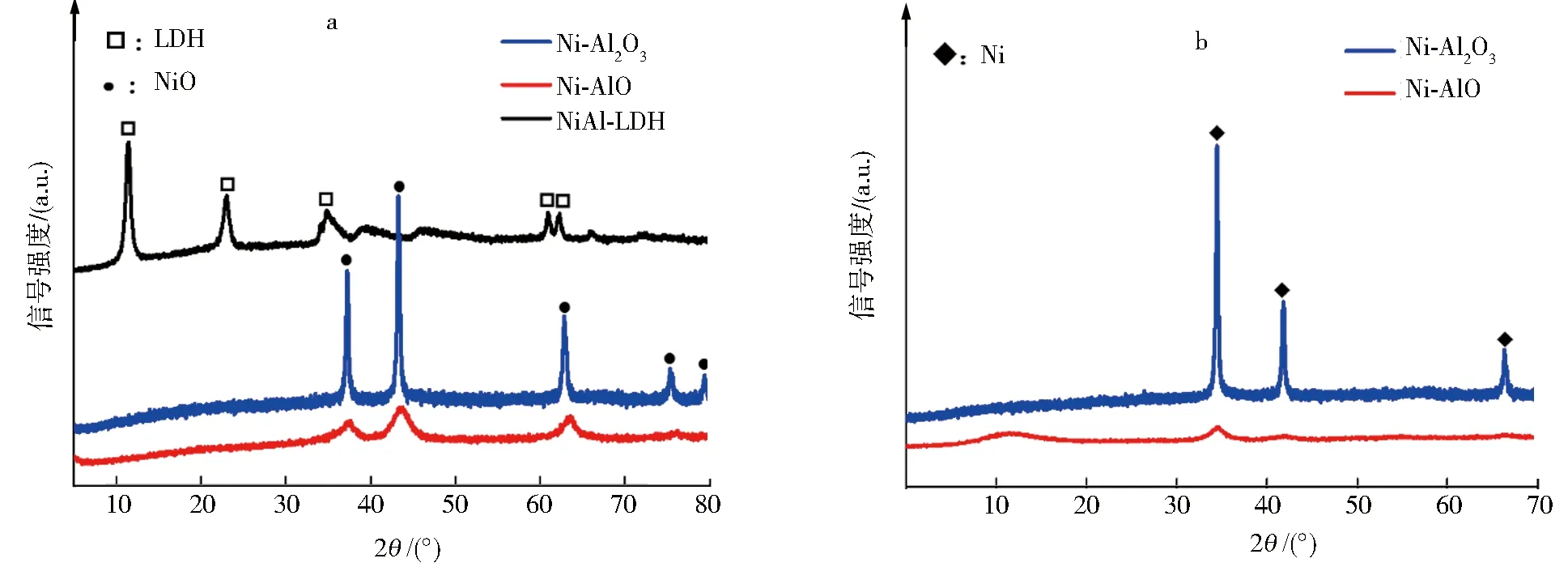
图4 还原前(a)和还原后(b)催化剂的XRDFig.4 XRD patterns of the catalysts before(a)and after(b) reduction
使用SEM和TEM观察了Ni-AlO和Ni-Al2O3催化剂的形貌(图5).SEM结果显示,Ni-AlO催化剂由六边形纳米片无规则分散堆积而成;而Ni-Al2O3催化剂为大量无规则块状颗粒无序堆积,且颗粒团聚严重(图5a和图5c).从TEM图中可以看出(图5b和图5d),镍纳米粒子在Ni-AlO催化剂中均匀分散,其粒径在3~12 nm内,平均粒径为6.7 nm(图5b内嵌图);与之对应,镍纳米粒子在Ni-Al2O3催化剂中团聚严重,平均粒径为23.7 nm(图5d内嵌图).以上结果说明,通过水滑石前驱体原位焙烧还原制备的镍基纳米催化剂中镍纳米粒子均匀分散在金属氧化物层板上,且粒径较小,明显优于通过常规浸渍法制备的催化剂[20].

图5 Ni-AlO(a, b)和Ni-Al2O3(c, d)催化剂的SEM和TEMFig.5 SEM and TEM images of the Ni-AlO(a, b) and Ni-Al2O3(c, d)catalysts
对焙烧后的Ni-AlO和Ni-Al2O3催化剂进行了H2-TPR表征.从图6a中可以看出,Ni-AlO催化剂在371、569 ℃处出现2个峰,其中371 ℃处的峰很弱,说明该催化剂中仅有少量与载体相互作用力较弱、游离的NiO;其在569 ℃处的峰比较强,说明该催化剂中大部分镍是由与载体有较强相互作用力的NiO还原得到的.与之相反,Ni-Al2O3催化剂在355、451 ℃处出现2个峰,其在355 ℃处的峰较强,说明Ni-Al2O3催化剂中的镍主要由大块NiO或与载体相互作用较弱的NiO还原得到.上述结果说明,Ni-AlO催化剂中镍粒子与LDO载体之间存在较强的相互作用力,水滑石层板的限域效应可以抑制镍纳米粒子的团聚与流失,提高其稳定性.

图6 Ni-AlO和Ni-Al2O3催化剂的H2-TPR(a)和XPS(b)结果Fig.6 H2-TPR(a) and XPS(b) results of the Ni-AlO and Ni-Al2O3 catalysts
为了进一步说明2种催化剂表面物质的价态与相互作用,又对其进行了XPS表征(图6b).发现Ni-AlO和Ni-Al2O3催化剂中均存在2种价态的Ni,结合能在852.60和852.44 eV的峰归属于还原态的镍;结合能在855.16和854.67 eV的峰,与861.23和859.94 eV处的卫星峰,归属于氧化态的镍[21].Ni-AlO催化剂中镍的结合能比Ni-Al2O3中镍的结合能略大,表明Ni-AlO催化剂中镍与载体之间存在较强的相互作用.
2.2 催化剂性能评价
首先,考查了不同焙烧温度下制备的Ni-AlO催化剂在DOP加氢反应中的性能,如表2.发现DOP的转化率随焙烧温度的升高先上升后下降:当反应时间为0.5 h时,在350 ℃焙烧的Ni-AlO催化剂作用下,DOP的转化率仅为38%;当Ni-AlO催化剂的焙烧温度提高到450 ℃时,DOP的转化率提高到61%;当Ni-AlO催化剂的焙烧温度进一步提高到550 ℃时,DOP的转化率却下降到55%.同时,目标产物DEHHP的选择性均保持在99%.因而,450 ℃被选为Ni-AlO催化剂的最佳焙烧温度.同时,反应时间对该反应也存在明显影响:当延长反应时间至1 h时,DOP的转化率提高到99%;与之对应,在浸渍法制备的Ni-Al2O3催化剂作用下,在相同反应条件下DOP的转化率仅为20%.上述结果表明,水滑石衍生的Ni-AlO催化剂在DOP加氢反应中具有优异的催化性能.

表2 镍基纳米催化剂在DOP加氢反应中的性能
稳定性是催化剂的一个重要性质.因此,进一步考察了Ni-AlO和Ni-Al2O3催化剂的稳定性(图7).Ni-AlO纳米催化剂表现出良好的稳定性,该催化剂在第7次使用时仍能使DOP的转化率保持在88%左右(图7a).然而,Ni-Al2O3催化剂不但初始活性低(DOP的转化率仅为20%),其稳定性也很差,使用3次后DOP的转化率就下降到10%左右(图7b).因此,Ni-AlO纳米催化剂的稳定性也明显优于Ni-Al2O3催化剂.根据H2-TPR和XPS表征结果,Ni-AlO催化剂中镍与载体之间有较强的相互作用,可有效抑制镍的团聚与流失,从而提高了该催化剂的稳定性[10].

图7 Ni-AlO(a)和Ni-Al2O3(b)催化剂的稳定性结果Fig.7 Stabilities of the Ni-AlO(a) and Ni-Al2O3(b)catalysts
3 结论
综上所述,本文以镍铝水滑石为前驱体,制备了一种镍基纳米催化剂Ni-AlO.其在邻苯二甲酸二辛酯加氢合成环己烷-1,2-二甲酸二辛酯的反应中显示出了优异的活性和良好的稳定性.透射电子显微镜、程序升温还原和X光电子能谱等表征表明,与Ni-Al2O3催化剂相比,Ni-AlO催化剂中镍分散均匀、粒径小、氢吸附量大;而且通过原位还原生成的镍与载体之间的相互作用较强,能抑制镍的团聚与流失,显著提高了催化剂的应用稳定性.

