多指标综合评分结合响应面法优选脂康颗粒提取工艺
许晓莉,李彩霞,吴瑞枫
(中国人民解放军联勤保障部队第九〇〇医院,福建 福州 350000)
脂康颗粒由决明子、山楂、桑椹、枸杞子、红花5味中药材经粉碎、过筛、制粒、干燥、整粒而制得,具有滋阴清肝、活血通络功效,主要用于肝肾阴虚挟瘀之高脂血症,症见头晕或胀或痛、耳鸣眼花、腰膝酸软、手足心热、胸闷、口干、大便干结[1]。现代药理学研究表明,决明子、山楂和桑椹合用有明显的调血脂作用[2]。药食同源的决明子中橙黄决明素、大黄酚及大黄素能显著增强LDLR基因转录水平,为决明子中有效调脂成分[3-4]。山楂调脂、降血压、抗心律不齐、增加冠脉血流量的有效成分主要为黄酮类化合物,其主要成分为芦丁及槲皮素[5-6]。桑椹来源于桑科植物桑Morus albaL.的干燥果穗,黄酮类、有机酸和生物碱为其主要化学成分,而黄酮类成分绿原酸及芦丁具有调节脂质代谢、抗氧化作用[7-8]。现行质量标准中脂康颗粒仅以大黄酚作为定量指标,含量测定的相关报道较少,尚未见同时测定该药品橙黄决明素、绿原酸、芦丁、槲皮素、大黄酚、大黄素6种成分含量的相关报道。Box-Behnken Design(BBD)响应面法是采用多元二次回归方程拟合各因素与响应值间的函数关系,寻求试验优化的方法,在中药成分提取领域应用广泛,与正交试验相比,不仅可考察各因素间的关联,还可通过图形显示其内在函数关系[9-11]。本研究中建立了同时测定脂康颗粒中橙黄决明素、绿原酸、芦丁、槲皮素、大黄酚、大黄素6种成分含量的高效液相色谱法,并以上述成分的综合评分为考察指标,采用BBD响应面法优选脂康颗粒中6种有效成分的提取工艺。现报道如下。
1 仪器与试药
1.1 仪器
e2695 Waters型高效液相色谱仪(美国Waters公司),配有2695Alliance四元梯度泵、2695 Alliance自动进样器、Empower3色谱工作站、2998二极管阵列检测器;ABS-135S型电子天平(瑞士梅特勒-托利多公司,精度为0.01 mg);KQ-250DBG型数控超声波清洗器(昆山超声波仪器有限公司,功率为500 W,频率为40 kHz);明澈-D24UV型纯水/超纯水一体化系统(德国默克密理博公司)。
1.2 试药
橙黄决明素对照品(批号为111900-201605,含量以98.3%计),绿原酸对照品(批号为110753-202018,含量以96.1%计),芦丁对照品(批号为100080-201811,含量以91.7%计),槲皮素对照品(批号为100081-201610,含量以99.1%计),大黄酚对照品(批号为110796-201922,含量以99.4%计),大黄素对照品(批号为110756-201913,含量以96.0%计),均购自中国食品药品检定研究院;甲醇、乙腈均为色谱纯,购自美国默克公司,其他试剂均为分析纯,水为纯化水;脂康颗粒(天大药业<珠海>有限公司,批号分别为190918,191112,020409,规格为每袋8 g)。
2 方法与结果
2.1 含量测定
2.1.1 色谱条件[12-14]与系统适用性试验
色 谱 柱:Waters XTERRA MS C18柱(250 mm×4.6 mm,5μm);流动相:乙腈(A)-0.1%磷酸溶液(B),梯度洗脱(0~16 min时25%A,16~40 min时25%A→45%A,40~50 min时45%A→65%A,50~55 min时65%A→25%A,55~60 min时25%A);流速:1.0 mL/min;检测波长:0~16 min时327 nm(检测绿原酸),16~24 min时370 nm(检测芦丁),24~32 min时280 nm(检测槲皮素),32~60 min时286 nm(检测橙黄决明素、大黄酚、大黄素);柱温:30℃;进样量:10μL。分别精密吸取供试品溶液、混合对照品溶液、阴性对照品溶液各适量,按此色谱条件进样测定,结果各成分理论板数均大于4 000,与相邻色谱峰的分离度均大于1.5,拖尾因子为0.96~1.14。色谱图见图1。

1.绿原酸 2.芦丁 3.槲皮素 4.橙黄决明素 5.大黄素 6.大黄酚A.混合对照品溶液 B.供试品溶液 C.阴性对照品溶液图1 高效液相色谱图1.chlorogenic acid 2.rutin 3.quercetin 4.aurantio-obtusin 5.emodin 6.chrysophanolA.Mixed reference solution B.Test solution C.Negative reference solutionFig.1 HPLC chromatograms
2.1.2 溶液制备
取橙黄决明素、绿原酸、芦丁、槲皮素、大黄酚、大黄素对照品各适量,精密称定,加甲醇制成每1 mL分别含上述成分3.017 0,0.608 7,1.554 0,1.328 0,0.228 1,0.239 6 mg的溶液,摇匀,滤过(0.45μm),取续滤液,室温避光保存,即得混合对照品溶液。取样品(批号为191112)装量差异项下的内容物,研细,混匀,取粉末1.0 g,精密称定,置具塞锥形瓶中,精密加入80%甲醇50 mL,室温超声处理(功率为500 W,频率为40 kHz)45 min,放冷至室温,再用80%甲醇稀释至刻度,摇匀,滤过,取续滤液,经0.45μm微孔滤膜过滤,即得供试品溶液。按脂康颗粒标准工艺方法,分别制备不含决明子、桑椹、山楂的阴性样品,按供试品溶液制备方法制备阴性对照品溶液。
2.1.3 方法学考察
线性关系考察:分别精密吸取2.1.2项下混合对照品溶液0.5,1.0,2.0,3.0,4.0,6.0 mL,置25 mL容量瓶中,加甲醇稀释至刻度,制成系列质量浓度的对照品溶液,按2.1.1项下色谱条件进样测定,记录色谱图。以对照品溶液质量浓度(X,μg/mL)为横坐标、峰面积(Y)为纵坐标进行线性回归,回归方程和相关系数(r)见表1。

表1 6种有效成分的线性关系考察、定量限与检测限测定结果Tab.1 Results of linear relation test,LOD and LOQ of six effective components
定量限与检测限确定:精密量取2.1.2项下混合对照品溶液,用甲醇倍比稀释,按2.1.1项下色谱条件进样分析。取峰面积信噪比(S/N)为10∶1时的混合对照品溶液质量浓度为定量限,取峰面积S/N为3∶1时的混合对照品溶液质量浓度为检测限。结果见表1。
精密度试验:取2.1.2项下混合对照品溶液适量,按2.1.1项下色谱条件分别于0,24,48,72 h时连续进样6次,记录色谱图。结果橙黄决明素、绿原酸、芦丁、槲皮素、大黄酚、大黄素峰面积的RSD分别为0.29%,0.43%,0.51%,0.38%,0.47%,0.62%(n=6),表明仪器精密度良好。
稳定性试验:取2.1.2项下供试品溶液,按2.1.1项下色谱条件分别于0,3,6,9,15,20,24 h时进样测定,记录色谱图。结果橙黄决明素、绿原酸、芦丁、槲皮素、大黄酚、大黄素峰面积的RSD分别为0.69%,1.03%,0.57%,0.78%,0.92%,0.84%(n=7),表明供试品溶液在24 h内稳定。
重复性试验:取样品(批号为191112)适量,依法平行制备供试品溶液6份,按2.1.1项下色谱条件进样测定,记录色谱图,计算6种成分的含量及其RSD值。结果橙黄决明素、绿原酸、芦丁、槲皮素、大黄酚、大黄素的平均含量分别为12.570 0,3.452 0,8.214 0,5.673 0,0.265 1,0.300 7 mg/g,RSD分 别0.86%,0.95%,1.03%,0.92%,1.05%,0.88%(n=6),表明方法重复性良好。
加样回收试验:取已知含量的样品(批号为191112)6份,混匀,研细,每份0.5 g,精密称定,按已知含量的100%加入橙黄决明素、绿原酸、芦丁、槲皮素、大黄酚、大黄素混合对照品溶液(质量浓度分别为1.207 0,0.357 4,0.821 6,0.579 6,0.028 5,0.031 3μg/mL)5.00 mL,依法制备供试品溶液,按2.1.1项下色谱条件进样测定,计算各成分加样回收率。结果见表2。

表2 脂康颗粒中6种成分的加样回收试验结果(n=6)Tab.2 Results of the recovery test of six components in Zhikang Granules(n=6)
2.1.4 样品含量测定及综合评分计算
取混合对照品溶液及供试品溶液,按2.1.1项下色谱条件进样测定,记录色谱图,按外标法计算含量。设满分为100分,按脂康颗粒君臣佐使组方原则,分别赋予各药材指标成分权重系数,橙黄决明素为30,芦丁和槲皮素权重系数均为20,绿原酸、大黄酚和大黄素权重系数均为10。参考文献[15]方法,对6种成分含量(%)进行标准化处理,求综合评分。综合评分(%)=橙黄决明素×30+绿原酸×10+芦丁×20+槲皮素×20+大黄酚×10+大黄素×10。
2.2 单因素试验
甲醇体积分数考察:取样品内容物适量,混匀,取粉末2.0 g,平行6份,置具塞锥形瓶中,分别精密加入50%,60%,70%,80%,90%,100%甲醇溶液各50 mL,室温超声处理(功率为500 W,频率为40 kHz)45 min,考察提取液综合评分,结果见图2 A。可知,甲醇体积分数不超过80%时,综合评分呈上升趋势,随后呈下降趋势。故选取80%甲醇为提取溶剂。
液料比考察:取样品内容物适量,混匀,取粉末2.0 g,平行5份,置具塞锥形瓶中,分别加入20,30,40,50,60 mL 80%甲醇,室温超声处理(功率为500 W,频率为40 kHz)45 min,考察提取液综合评分,结果见图2 B。可知,当液料比从20∶1(V/m)增至60∶1(V/m)时综合评分呈快速上升趋势,50∶1(V/m)时达最高值,超过50∶1(V/m)后变化不明显。故选择液料比为50∶1(V/m)。

A.甲醇体积分数 B.液料比 C.提取时间图2 单因素试验考察结果A.Volume fraction of methanol B.Liquid-solid ratio C.Extraction timeFig.2 Results of the single factor test
提取时间考察:取样品内容物适量,混匀,取粉末2.0 g,平行5份,置具塞锥形瓶中,按液料比50∶1(V/m)加入80%甲醇,分别于室温超声处理(功率为500 W,频率为40 kHz)25,35,45,55,65 min时,考察提取液综合评分,结果见图2 C。可知,提取时间为25~45 min时综合评分处于快速上升阶段,时间再延长,综合评分无明显变化。考虑到工作效率和成本,暂设置提取时间为45 min。
2.3 BBD响应面法优化工艺
回归模型建立及方差分析:采用Design-Expert 8.0.5统计软件,结合单因素试验结果,根据BBD响应面试验设计原理,以对评价指标影响较大的提取时间(A)、甲醇体积分数(B)、液料比(C)为考察因素,以橙黄决明素、绿原酸、芦丁、槲皮素、大黄酚、大黄素含量综合评价指标为响应值,设计三因素三水平17个试验点的响应面分析模型,并对二次多项方程进行显著性分析。因素水平设计见表3,试验结果见表4。由软件得到综合评分(Y)为因变量对自变量提取时间(因素A)、甲醇体积分数(因素B)、液料比(因素C)的二次多项回归方程,Y=85.41+5.92A+5.23B+6.31C-2.07AB-2.19AC-2.58BC-0.03A2-5.77B2-10.01C2。方 差分析数据见表5。可知,F=6.75,P=0.020 1<0.05,表明回归模型显著;失拟项P=0.061 9>0.05,失拟度不显著,表明模型选择合适,可用于工艺的分析和预测。模型的一次项A和B呈显著影响,因素C呈极显著影响,影响顺序为C>A>B;交互项影响不显著,二次项A2影响不显著,二次项B2对模型有显著影响,二次项C2项对模型影响极显著。

表3 因素水平表Tab.3 Factors and levels

表4 响应面试验设计方案及结果Tab.4 Design scheme and results of the response surface test
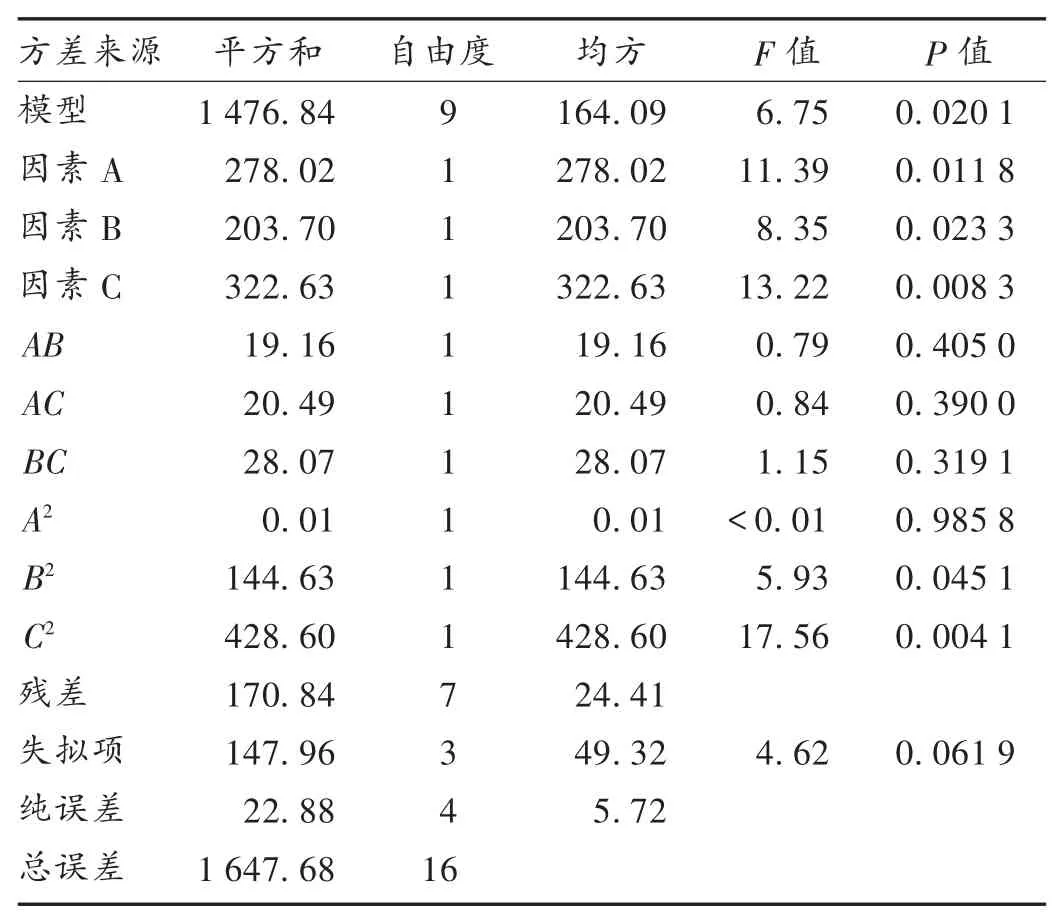
表5 二元多项回归拟合BBD响应面试验设计方差分析结果Tab.5 Results of ANOVA of BBD response surface test design fitted by binary multiple regression
响应面图分析:采用Design-Expert 8.0.5统计软件,得到二次回归方程的3D响应面图(见图3)。可见,提取时间、甲醇体积分数及液料比对综合评分均有不同程度影响,其中因素C(提取时间)的影响最大。
最佳提取工艺确定及验证试验:利用Design-Expert 8.0.5统计软件,以6种成分的综合评分Y值的最大值为指标,通过对回归模型极值的求解分析,得到最佳提取工艺为甲醇体积分数85%,液料比52∶1(V/m),提取时间45 min,此时综合评分为92.31%。取3批样品,按拟订优化提取条件试验,得平均综合评分为90.58%,测得值与预测值相对误差为0.94%(n=3),表明回归模型预测性良好,工艺可行、合理。

A.甲醇体积分数-提取时间 B.甲醇体积分数-液料比 C.提取时间-液料比图3 三因素交互作用对综合评分的响应面图A.Volume fraction of methanol-extraction time B.Volume fraction of methanol-solid ratio C.Extraction time-liquid-solid ratioFig.3 Response surface diagram of three factor interaction on comprehensive score
3 讨论
BBD响应面法广泛应用于中药提取工艺优选,具有直观、方便、科学等优点,能解决正交试验难以解决的非线性数学问题,是集统计学和数学于一体的科学模型。本研究中考察了乙醇体积分数、液料比和提取时间三因素相互作用对综合评分的影响,利用中心效应面法设计试验方案,采用Design-Expert 8.0.5统计学软件对结果进行拟合,求得二次多项方程,并进行了方差分析,推导出脂康颗粒中最佳提取工艺参数。同时,建立了同时测定脂康颗粒中槲皮素、橙黄决明素、绿原酸、芦丁、大黄酚和大黄素含量的高效液相色谱法,并通过验证试验考察方法准确性,模型预测性良好,方法简单实用,具有较好的参考价值。

