负压封闭引流联合人表皮生长因子治疗糖尿病足溃疡的疗效
刘汉胤 孙 劲 宋爱波
(三峡大学 第三临床医学院[国药葛洲坝中心医院] 骨外科, 湖北 宜昌 443002)
糖尿病足溃疡(diabetic foot ulcer,DFU)是糖尿病的一种严重并发症,其致死率、致残率、复发率高,给患者及家属带来沉重负担[1]。由于创面难以愈合,DFU治疗往往耗时长、费用高,且皮瓣移植效果差[2]。负压封闭引流(vacuum sealing drainage,VSD)技术最早由德国Fleischmann教授等于1992年发明,目前已被广泛用于临床DFU等各种难愈创面治疗,疗效显著[3]。重组人表皮生长因子(recombinant human epidermal growth factor,rhEGF)是一种基因重组技术合成产物,主要参与皮肤的修复与代谢等过程,常用于辅助治疗烧伤创面、难愈创面、DFU等各种慢性创面和皮瓣移植区域的新创面[4]。目前对于VSD和rhEGF联合治疗DFU临床有效性评估的研究报道甚少。本研究旨在探讨VSD结合rhEGF治疗DFU的临床效果,为DFU临床治疗策略的制定提供参考。
1 资料与方法
1.1 一般资料
将2017年1月~2019年6月我院骨科收治的56例DFU患者,采用随机数字表法随机分为观察组和对照组,每组各28例。纳入标准:①所有入组对象符合糖尿病诊断[5];②按糖尿病足感染的IWGDF/IDSA分级[6]属轻、中度感染的单足初发DFU患者,溃疡分布于足底(足跟、足趾末节和跖趾关节等处);③溃疡满足Wagner评分[7]3级的患者;④所有患者及家属对本研究充分知情并能签署知情同意书,同意后续随访;⑤足背动脉搏动良好。排除标准:①严重心血管、消化道、肾脏疾病(包括正在透析患者);②难以控制的高血糖(糖化血红蛋白>12%);③各种疾病导致的凝血功能障碍及各种原因引起的贫血(血红蛋白<90 g/L);④正在接受放疗或化疗患者;⑤其他疾病引起的足部溃疡;⑥合并下肢大动脉明显狭窄;⑦合并恶性肿瘤;⑧合并下肢瘫痪;⑨合并严重营养障碍;⑩创面有活动性出血。本研究通过我院伦理审查委员会审查。
1.2 治疗材料及方法
1.2.1 材料
VSD泡沫敷料(武汉维斯第医用科技股份有限公司生产,国械注准:20143642322);人表皮生长因子(深圳市华生元基因工程发展有限公司生产,国药准字:S20010037)。
1.2.2 方法
两组患者VSD均由同一组医师执行。两组患者术后VSD负压均维持于0.02~0.04 kPa,保持有效负压引流,每48 h更换负压引流瓶,5~6 d更换VSD材料,每次更换VSD材料时均观察并记录创面颜色、创面面积、创面肉芽组织生长情况、大小深度及愈合情况。两组患者在术后每日上午均采用生理盐水500 mL冲洗负压引流管,完成上述操作后,观察组将20 000 IU人表皮生长因子通过VSD冲洗管注入并夹闭冲洗、引流管密闭2 h后,松开负压管继续VSD负压吸引。对照组不注入任何物质,也夹闭VSD管道2 h。注意观察引流管是否漏气、阻塞,覆盖创面内是否血肿或者持续出血,出现后立即进行相应处理,必要时重新手术并更换VSD敷料。
1.3 观察指标及判定标准
①观察并记录两组患者治疗1、2、4周后的创面愈合率;②观察两组创面的肉芽组织出现时间、溃疡愈合时间;③观察并记录两组患者治疗4周后的创面愈合治疗总有效率。
创面愈合测量方法:将透明薄膜敷于创面上,描绘其边缘,再将透明薄膜附于硬纸板上,剪裁成对应面积的硬纸板,并进行称重。通过该方法可将难以精准测量的不规则创面面积转化为易测量的物质重量,测量结果更为精准。
不同时间的愈合率:创面愈合率=(初始对照创面面积对应的硬纸板重量-不同时间点创面面积对应的硬纸板重量) /初始对照创面面积对应的硬纸板重量×100%。
创面愈合治疗总有效率评价采用张延祠[8]的评估方法:痊愈:溃疡创面全部或大部分愈合,残余创面面积小于初始创面的25%,并可见新鲜肉芽组织形成,溃疡创面周围未见明显炎症反应;显效:残余创面约为初始创面的25%~50%,可见新鲜肉芽组织形成;延迟:溃疡残余创面较大、较深,为初始创面的50%~75%,创面局部未见新鲜肉芽组织生成,可见瘢痕组织;无效:残余面积大于初始的75%,创面局部及周围未见新鲜肉芽组织形成,且创面周围可见红、肿、热及痛等症状,局部仍可见坏死及渗出。临床总有效率=(痊愈例数+显效例数)/总例数×100%。
1.4 统计学方法
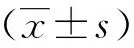
2 结果
2.1 两组患者一般资料
观察组男14例、女14例,年龄(59.10±11.61)岁,糖尿病病程(8.76±1.21)年、DFU发病时间(30.90±5.41)d,初始溃疡面积(34.23±21.74)cm2。对照组男11例、女17例,年龄(59.43±12.81)岁,糖尿病病程(8.81±1.52)年、DFU发病时间(32.83±5.90)d,初始溃疡面积(32.40±21.42)cm2。观察组和对照组性别、年龄、糖尿病病程、DFU发病时间、初始溃疡面积等一般资料比较,差异均无统计学意义(均P>0.05),见表1。
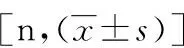
表1 两组患者一般资料比较
2.2 两组患者治疗1、2、4周的创面愈合率
为了对比两种方案治疗DFU的临床疗效,通过透明薄膜结合硬纸板将面积转换成质量方法测量两组治疗方案治疗前后创面面积的差值百分数,从而计算两组治疗后创面愈合率,并进行比较。结果显示,两组患者治疗1、2、4周后创面愈合面积逐渐增大,观察组患者的创面愈合率分别为0.163±0.024、0.477±0.026和0.781±0.026,而对照组分别为0.155±0.017、0.426±0.023和0.732±0.028。与对照组相比,观察组患者经VSD和rhEGF联合治疗1、2、4周后,创面愈合面积明显增大,两组比较差异均有统计学意义(均P<0.05),见表2。

表2 两组患者治疗1、2、4周后的创面愈合率比较
2.3 肉芽组织出现时间、溃疡愈合时间
进一步比较两组患者治疗后溃疡愈合情况。结果显示,观察组肉芽组织出现时间为(3.27±1.80) d,明显早于对照组(5.56±2.51)d,差异具有统计学意义(P<0.05)。并且,与对照组相比,观察组的溃疡愈合时间也显著缩短(P<0.05),见表3。

表3 两组患者治疗后创面肉芽组织出现时间和溃疡愈合时间比较
2.4 治疗4周的临床总有效率
观察组痊愈14例、显效13例、延迟愈合1例,治疗总有效率为96.43%。对照组痊愈10例、显效10例、延迟愈合8例,治疗总有效率为71.43%。观察组临床治疗总有效率优于对照组,差异有统计学意义(P<0.05),见表4。

表4 两组患者治疗4周临床总有效率比较
2.5 治疗期间并发症、不良反应和出院后随访情况
两组研究对比期间均未发现引流管阻塞、负压装置漏气、继发感染和不良反应病例。 VSD联合rhEGF治疗DFU过程见图1。4周研究结束后拆除VSD装置,观察组创面平整无渗液,肉芽组织新鲜红润、生长良好。根据创面情况判断无需使用VSD后,继续每日涂抹rhEGF及常规更换敷料2~3周,创面全部完成上皮化愈合。对照组的整体创面愈合时间较观察组长,平均每例要多更换2~4次VSD装置,但最终也能完成上皮化愈合。出院后随访8月,观察组和对照组各有1例在随访第7月复发,差异无明显统计学意义(P>0.05)。这两例的原发病灶均为足根底部着力点溃疡,予门诊换药及常规治疗后创面愈合。此外,观察组有1例在随访第5月因外出而失访。其余研究对象随访期间均无复发、截肢及死亡。

注:患者为58岁男性,有8年糖尿病病史,由内分泌科转入我科。足溃疡病史26 d,溃疡创面位于右足底第一、二趾骨间。A:第一次彻底清创后,完全清除坏死组织,充分打开足肌间隙,肌腱,使骨质外露;B:治疗4周拆除VSD,创面可见大量新鲜肉芽组织生长,未见坏死组织,无需继续使用VSD;C:治疗第40 d后,创面明显缩小,继续换药5 d治愈出院(左图为治疗前,右图为治疗45 d后);D:行第二次清创时发现患者第二趾骨出现坏死,予以清除坏死骨质及周围肌腱组织;E:治疗4周拆除VSD后,我们发现该患者溃疡创面暴露较大,且由于第二趾的缺失导致创面不连续,予以缝合创面图1 VSD联合rhEGF治疗DFU过程
3 讨论
DFU创面常伴有慢性感染,久之对多种抗生素产生耐药,炎症不易控制而反复发作。VSD可有效缩短创面愈合时间,减少换药次数,同时也能减少创面敷料更换给患者带来的疼痛,有效避免交叉感染。此外,VSD的封闭环境可以保护伤口不受外界污染,持续的负压又能及时清除创面炎性渗出和坏死组织,使体液从创面流向引流管,增加创面血流量,刺激多种生长因子释放,有效促进肉芽组织快速生长,从而促使创面愈合,减轻感染[9]。而且,负压大小可以根据患者身体及创面差异进行调整,在避免对血液循环造成不利影响的同时,能够有效防止残余脓肿及死腔形成[10]。
EGF是创面愈合过程中的重要生长因子,对表皮细胞的分裂和毛细血管的生成有着强烈的促进作用。其中rhEGF是EGF外用溶液中的活性成分,它能促进皮肤创面组织修复,诱导分化成熟的表皮细胞逆转化为表皮干细胞,并加速创面肉芽组织生成和上皮细胞增殖,从而缩短创面愈合时间,提高创面修复质量[11]。同时rhEGF能减轻DFU患者氧化应激反应,恢复人体氧化还原平衡,从而使创面愈合美观[12]。
本研究结果显示,VSD联合rhEGF方案治疗糖尿病足溃疡的效果明显优于VSD治疗方案,其原因可能是在创面修复愈合的三期过程中, rhEGF可趋化巨噬细胞、成纤维细胞向创面聚集,促进DFU患者创面异常或坏死组织的清理[13]。异常或坏死组织在VSD负压的吸引下可及时排出创面,从而降低创面的感染风险。增殖期,rhEGF可刺激内皮细胞、真皮成纤维细胞、上皮细胞分裂增殖,促进创面血管生成及胶原蛋白、糖胺聚糖的合成,同时刺激纤维蛋白酶的活性,调节细胞外基质,有利于纤维组织增生和创面胶原的沉积;在中晚期通过促进上皮细胞向表层移行,先形成单细胞层,然后促进有丝分裂形成复层上皮细胞而加速创面的上皮化,同时通过介导肌成纤维细胞的活性并诱导增殖,进而促进创面收缩和闭合[13]。VSD的负压封闭环境能显著改善创面的微循环和局部血流,加快受损组织皮肤的再生,降低外周组织发生水肿的概率,EGF和VSD可相互促进起到协同作用[14]。此外,rhEGF外用溶液中还含有10%的甘油和1%的甘露醇作为保护剂,这两种成分有利于减少溃疡创面的局部水肿并能促进炎症消退,降低感染风险。
另外,因其粘稠特性可缓慢释放药物成分,有利于保持溃疡创面高浓度rhEGF,延长作用时间。而且,局部水肿的消退也利于VSD引流。本次研究随访期间两例复发病例的原发病灶均为足根底部着力点溃疡,这可能与DFU患者在行走过程中足底区域失去敏感性会不自主地改变步态模式,使得足底着力点区域压力逐渐增大,久之导致足底皮肤破损。因此,原发灶是着力点的溃疡更容易复发。同时在随访过程中还发现,有一部分研究对象(包括这两例复发患者)在出院后对疾病的重视程度下降。莫泽纬等[15]研究认为,患者不注意足部护理、穿不合适的鞋或各种原因导致的足底反复损伤等是DFU的常见复发诱因,而足底溃疡则是DFU复发的独立高危因素。
尽管目前VSD临床应用已非常成熟,但在实际操作中还是会出现漏气、阻塞等一些不良情况。本研究通过每日冲洗VSD装置及检测其密闭性来减少上述事件的发生。现阶段对于局部外用rhEGF治疗DFU的临床数据较少,其药代动力学也尚未研究充分。此外,国内外对于VSD和rhEGF两者联合治疗DFU的临床报道较少,以至于局部rhEGF的给药时间和给药方式没有统一标准。Tan等[16]认为在清创后先用rhEGF涂抹创面,随后行VSD负压吸引,中间不预留rhEGF作用时间可有效促进创面愈合。但该方法可能使rhEGF在VSD负压吸引的作用下流失,导致作用浓度不够和作用时间短,从而无法使rhEGF发挥最佳效果。而许传秀等[17]则认为先行VSD治疗,等拆除VSD再用rhEGF涂抹创面,可有效促进创面愈合。但该方案的VSD治疗周期较长(常规拆换约5~6 d),期间没有rhEGF的作用,因此难以评估VSD与rhEGF两者的联合治疗效果。本研究选择将rhEGF由冲洗管注入密闭VSD内,并夹闭冲洗、引流管作用2 h后再继续VSD负压吸引治疗。这样既能保证创面rhEGF作用浓度及有效作用时间,又能最大程度维持VSD密闭状态,不影响VSD负压效果。同时有利于评估VSD、rhEGF两者联合治疗DFU的效果。且每日冲洗VSD能起到防止管道阻塞的作用。然而本研究仍有局限性,由于样本量有限,且入组时未细分1型和2型DFU;此外,随访时间较短,对于二者联合治疗DFU的远期效果尚需进一步观察。
综上所述,VSD联合rhEGF方案治疗DFU的效果明显优于单用VSD治疗方案。在VSD持续负压下,rhEGF对创面表皮细胞生长的促进作用增强。同时,rhEGF能促进DFU创面消肿,有利于VSD引流。因此,VSD与rhEGF联合治疗可加快创面肉芽组织形成,提高DFU创面愈合速度,且无不良反应及并发症,值得临床推广应用。

