丙烯醛体内外诱导神经元铁死亡的初步研究
彭伟嘉,朱泽宇,杨 扬,侯加卫,皮荣标
(1.中山大学药学院药理与毒理教研室,广东广州510006;2.中山大学医学院药理教研室,广东深圳518107)
阿尔兹海默病(Alzheimer's disease,AD)的临床表现包括持续的智能减退、认知功能障碍、精神和行为异常等[1]。丙烯醛(acrolein)是结构最为简单的α,β-不饱和醛,是人体中重要的脂质过氧化产物,其可与DNA或蛋白质加合从而破坏其功能。丙烯醛可诱导细胞凋亡、脂质过氧化,内质网应激,增加炎症因子的表达等。大量研究已证实丙烯醛与多种神经退行性疾病有关[2]。研究表明,在AD与轻度认知障碍患者的脑组织、血浆及脑脊液中,均检测出明显高于正常受试者水平的丙烯醛[3]。在本实验室前期研究中发现,丙烯醛可较好模拟散发性AD早期的病理改变:包括学习记忆能力下降、出现β-淀粉样蛋白(amyloidβ-protein)/Tau以及神经炎症病理[4-5],因此丙烯醛与AD存在着密不可分的关系。铁死亡(ferroptosis)是一种新发现的程序性细胞死亡形式,伴有线粒体嵴减少或消失,线粒体外膜破裂形态学特征和胞内亚铁、脂质过氧化水平升高的特征,而多种神经退行性疾病包括AD都与铁死亡密切相关[6-7]。铁稳态失衡是诱发铁死亡的重要因素,铁对于维持正常的神经元功能至关重要,但是过量的不稳定铁会导致脂质过氧化和细胞死亡。在AD患者或动物的脑中也观察到了铁死亡的发生[8]。磁共振成像显示AD患者脑的多个区域都有明显的铁蓄积[9-10]。近期研究发现丙烯醛可在植物细胞和大鼠平滑肌上皮细胞中诱导铁死亡样的病理改变[11-12]。考虑到丙烯醛与AD和脂质过氧化密切相关,并且脂质过氧化是铁死亡最重要的生化特征,对丙烯醛是否能够在体内外诱发铁死亡还未见报道。因此本文将从形态学以及生化特征,结合铁死亡特异性抑制剂,对丙烯醛是否能够在体内外诱发铁死亡进行初步探究。
1 材料与方法
1.1 材料
1.1.1 细胞 永生系可传代小鼠海马神经元HT22细胞由中山大学附属第二医院神经科刘军教授惠赠。
1.1.2 动物 8周龄雌性SPF级C57BL/6J小鼠(18~20 g)20只,购于江苏集萃药康生物科技股份有限公司。生产许可证:SCXK(苏)2018-0008;使用许可证:SYXK(粤)2016-0112。动物饲养于安静无噪音、人工昼夜节律环境中,相对湿度为40%~70%,温度为20~26°C。动物分笼饲养,自由饮水、进食,每笼5只,并用耳标标识。所有笼具、饲料、饮水、垫料均严格消毒。动物的使用协议和动物处理程序获得了中山大学实验动物管理与使用委员会的批准。
1.1.3 试剂 丙烯醛(化夏化学,中国,色谱纯);Fer-1(MCE,美国);DFO(Targetmol,中国);MTT(Sigma,美国);DMEM培养(Gibco,美国);胎牛血清(Hyclone,美国);双抗(弗得生物,中国);DMSO(Sigma-Aldrich,美国);BCA蛋白定量试剂盒(Thermo,美国);mouse anti-actin(Thermo,美国);rabbit anti-GPX4(Abcam,美国);rabbit anti-FTH1(Abcam,美国);rabbit anti-COX-2(CST,美国);ROS荧光探针-二氢乙啶DHE(碧云天,中国);亚铁离子探针FerroOrange(同仁化学,日本)。
1.2 方 法
1.2.1 丙烯醛小鼠模型造模 按文献所示方法进行造模[4-5]。首先使用增重法配置丙烯醛工作液,在1.5 mL蒸馏水中加入10µL丙烯醛,得到含x mg丙烯醛的母液,最终稀释成0.12µg/mL工作液用于小鼠每日灌胃。其中对照组用等量生理盐水进行灌胃,丙烯醛组使用3 mg/kg的剂量分别灌胃1,2,4周,后处死分离海马组织。
1.2.2 细胞培养 永生系可传代小鼠海马神经元HT22细胞使用含10%胎牛血清的DMEM完全培养基,在37℃,体积分数5%CO2细胞培养箱中常规培养,待细胞融合度在70%~80%时以2.5 g/L胰蛋白酶消化传代。随后将5 000个/孔细胞接种到96孔板中开展后续实验。
1.2.3 MTT检测丙烯醛对细胞增殖与活力的影响 取对数生长期细胞,用2.5 g/L胰蛋白酶消化后,镜下观察到大多数细胞变圆后弃去消化液,用全培养基终止消化,离心后重悬,以细胞计数板计数并调整细胞浓度为5 000个/孔,以100µL/孔接种96孔板,培养过夜,使细胞贴壁。吸出培养基,加入以完全培养基稀释成一定浓度的丙烯醛溶液,继续培养。培养24 h后,每孔加入MTT储备液10µL,继续培养3 h。吸去上清,每孔加入100µL DMSO,37℃孵育15 min使甲瓒充分溶解,测定570 nm波长处的吸光度值。各样品对细胞的增殖抑制活性以下列公式计算:存活率(%)=(A样品-A空白)/(A对照-A空白)×100%,选出最佳丙烯醛造模浓度(15µmol/L)用于后续试验。
1.2.4 透射电镜观察线粒体形态 透射电镜观察细胞线粒体超微结构。简言之,HT22细胞在用4度预冷的2.5%戊二醛和1%四氧化锇分别处理24 h和1 h。而后细胞在一系列丙酮浓度(50%、70%、80%、90%和100%)下脱水15 min,并包埋在树脂中。将样品切片并用乙酸铀酰和柠檬酸铅双重染色,并使用JEM-1400电子显微镜(JEOL,日本)获得代表性图像。
1.2.5 Dihydroethidium(DHE)二氢乙啶检测ROS含量 取对数生长期细胞接种于48孔板中。细胞经过处理后,吸走培养基并用预温的PBS轻轻洗细胞3次。吸走PBS并向每孔中加入10µmol/L含DHE的无血清DMEM培养基,37℃避光染色30 min,吸走培养基并用预温的PBS轻轻洗细胞3次,使用高内涵荧光分析器进行拍照与分析(Thermo,美国),激发波长为549 nm。
1.2.6 FerroOrange亚铁离子探针法检测胞内亚铁离子含量 取对数生长期细胞接种于共聚焦皿中,细胞经过处理后,吸走培养基并用预温的PBS轻轻洗细胞3次。吸走PBS并向每孔中加入10µmol/L含FerroOrange的无血清DMEM培养基,37℃避光染色30 min,吸走培养基并用预温的PBS轻轻洗细胞3次,使用共聚焦显微镜进行拍摄(Olympus,日本),并用Image J进行分析统计。
1.2.7 蛋白免疫印迹法 对于细胞,弃去培养液,用预冷PBS轻洗细胞2次,吸干PBS;加入适量含裂解液(含蛋白酶抑制剂及磷酸酶抑制剂),将细胞刮下后,冰上裂解30 min,4℃,12 000×g离心15 min,取上清至另一新的EP管中;对于小鼠的海马组织,每组选择3只,1%戊巴比妥钠(40 mg/kg)麻醉后颈椎脱臼处理,用剪刀将小鼠脑组织与头骨剥离,于冰袋上迅速分离大脑的皮层和海马等组织。按照重量:体积=1:10加裂解液(10 mg:100µL)再加入等比例的蛋白酶和磷酸酶的抑制剂,于冰上进行组织匀浆,冰上裂解30 min后,4℃,12 000×g离心15 min后吸取上清液至另一EP管内。根据试剂盒说明书,BCA法检测蛋白含量。各组样品上样量为15µg,进行常规电泳与电转,电转完成后5%脱脂牛奶室温封闭1.5 h。一抗4℃孵育过夜。后孵育二抗,用超敏ECL(Millipore,德国)化学发光液显色。Tanon-5200化学发光成像系统(Tanon,中国)曝光显影条带,ImageJ对图像进行光密度分析。
1.2.8 统计分析 亚铁离子探针荧光和免疫印迹(WB)结果采用image J软件测量荧光灰度值。所有数据为正态分布的计量结果,以均值±标准误(Mean±SEM)表示。采用Graphpad prism 8软件进行多组数据比较。当数据符合正态分布且方差齐时使用One-way ANOVA进行分析,事后用Dun⁃nett-tests法进行两两比较。α=0.05,P<0.05表明差异有统计学意义。
2 结果
2.1 铁死亡抑制剂可减少丙烯醛诱导的HT22细胞毒性
为了初步探究丙烯醛是否能够诱发铁死亡,我们使用铁死亡抑制剂铁抑素(ferrostatin-1,Fer-1)与去铁胺(deferoxamine,DFO)对丙烯醛模型细胞进行预处理和保护。我们在HT22细胞上寻找合适的造模浓度(图1B),结果显示15µmol/L的丙烯醛会诱导半数以上的细胞丧失细胞活力[细胞生存率为(39.78±4.40)%],因此选择15µmol/L进行下一步实验。我们在该浓度下检测了Fer-1(12µmol/L)与DFO(100µmol/L)的保护作用,结果表明Fer-1与DFO都表现出了保护作用(F=42.08,P<0.001)。其中DFO具有更好的保护作用(图1A、C),几乎完全逆转了丙烯醛诱导的死亡[细胞生存率为(89.07±10.48)%,P<0.001]。

图1 铁死亡抑制剂Fer-1与DFO可减少丙烯醛诱导的细胞毒性Fig.1 Fer-1 and deferoxamine reduced acrolein-induced cytotoxicity in HT22 cells
2.2 丙烯醛诱导HT22细胞线粒体铁死亡样病变
在铁死亡的形态学特征中,细胞膜断裂和出泡,线粒体变小、膜密度增高、线粒体嵴减少或消失是最显著的[6]。因此我们使用透射电镜放大2 000与6 000倍对丙烯醛模型细胞中线粒体的形态进行观察。结果显示在丙烯醛诱导后,线粒体出现体积变小,嵴数目减少的情况,提示我们出现了铁死亡样的病理表现(图2)。

图2 丙烯醛诱导线粒体皱缩与嵴减少Fig.2 Acrolein induced mitochondrial shrinkage and cristae reduction
2.3 丙烯醛诱导HT22细胞中自由基与亚铁离子产生
脂质过氧化是铁死亡的一大生化特征,最终可导致细胞死亡。ROS荧光探针-二氢乙啶(dihydro⁃ethidium,DHE)检测结果显示丙烯醛(15µmol/L)作用12 h可以显著诱导ROS的产生[(129.24±1.06)%,P<0.001],而Fer-1[(116.90±2.91)%,P<0.01]与DFO[(106.10±0.66)%,P<0.001]都可降低胞内ROS的含量并且差异具有统计学意义(F=53.64,P<0.001;图3A)。胞内亚铁含量上升是铁死亡的另一大生化特征[13]。FerroOrange染色结果显示丙烯醛(15µmol/L)作用12 h可以显著诱导胞内亚铁离子升高[(123.75±3.68)%,P<0.001]并且差异具有统计学意义(F=14.20,P<0.001;图3B)。

图3 丙烯醛诱导胞内过量自由基与亚铁离子产生Fig.3 Acrolein induced the production of excessive free radicals and ferrous ions in vitro
2.4 丙烯醛诱导HT22细胞中铁死亡相关蛋白表达变化
为了进一步探究丙烯醛是否能诱发铁死亡分子水平上的改变,我们对铁死亡相关蛋白进行检测。与对照组相比,丙烯醛组环氧化酶2(cyclooxy⁃genase-2,COX-2)(F=16.10,P=0.001)和铁蛋白重链1(ferritin heavy chain 1,FTH1)(F=6.52,P<0.05)的蛋白水平明显增加,而谷胱甘肽过氧化物酶(glutathione peroxidase 4 GPX4)的蛋白表达水平明显下降(F=7.94,P<0.01),差异都具有统计学意义。其中10µmol/L丙烯醛组中COX-2,FTH1,GPX4的表达量分别相当于对照组的(1.80±0.17)倍,P<0.05、(1.64±0.20)倍,P<0.05、(0.77±0.09)倍,P<0.05。而15µmol/L丙烯醛组中COX-2,FTH1,GPX4的表达量分别相当于对照组的(2.33±0.15)倍,P<0.001、(1.86±0.19)倍,P<0.01、(0.64±0.05)倍,P<0.01(图4)。
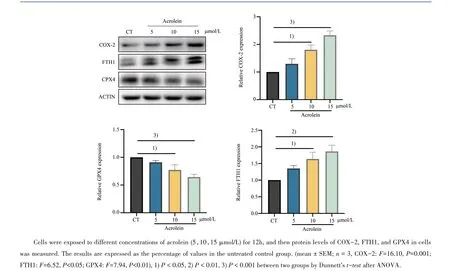
图4 丙烯醛影响HT22细胞中铁死亡相关蛋白的表达Fig.4 Acrolein affected the level of ferroptosis-related proteins in HT22 cells
2.5 丙烯醛在小鼠海马中诱导铁死亡相关蛋白发生改变
小鼠灌胃给予丙烯醛(3.0 mg/kg)1~4周后,对小鼠海马中铁死亡相关蛋白进行检测。与对照组相比,丙烯醛组海马中COX-2的蛋白水平明显增加(F=8.31,P<0.01),而GPX4(F=2.240,P=0.161)和FTH1(F=4.05,P=0.05)的蛋白表达水平有下降的趋势。其中COX-2表达量在造模1周后便显著上升,并有统计学差异(P<0.05)。FTH1表达量在造模1周后有下降趋势(P=0.08),而在造模2,4周后维持低水平的表达,其中在第2周时差异具有统计学意义(P<0.05)。GPX4表达量在造模1周后显著下降,而在造模2周后表达量达到最低,但差异无统计学意义(P=0.09;图5)。
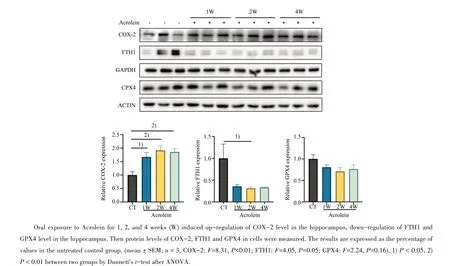
图5 丙烯醛在小鼠海马中诱导铁死亡相关蛋白发生改变Fig.5 Effects of Acrolein on theferroptosis-associated pathologies in mice
3 讨论
在本研究中,通过建立HT22海马神经元与小鼠的丙烯醛损伤模型发现,丙烯醛在体外可以诱导细胞损伤、脂质过氧化和亚铁离子水平升高,该现象可被铁死亡抑制剂所缓解。此外,丙烯醛还可引发线粒体发生铁死亡样改变,并在体内外降低铁死亡相关蛋白GPX4的表达水平。因此我们初步判断丙烯醛可诱导体内外铁死亡的发生。
本文研究结果证实,HT22细胞预先孵育铁死亡抑制剂Fer-1与DFO可以有效缓解丙烯醛诱导的死亡,提示铁死亡参与丙烯醛诱导的细胞损伤过程(图1)。其中DFO的保护效果优于Fer-1,能够逆转丙烯醛诱导的死亡。形态学方面,丙烯醛处理HT22细胞后出现线粒体损伤,使得线粒体体积变小,嵴的数目减少铁死亡经典线粒体特征[6-7](图2)。因此可知丙烯醛可诱导细胞形态学上发生铁死亡样改变,并且其诱导的细胞损伤可被铁死亡抑制剂逆转初步推断丙烯醛可诱导铁死亡。
铁死亡的关键生化信号是细胞内铁依赖性ROS产生和脂质过氧化,以及胞内亚铁离子水平上升造成的铁稳态失衡。而亚铁离子水平升高可触发芬顿反应——即过量的Fe2+与H2O2反应产生大量羟基自由基,从而进一步加重脂质过氧化的程度[14]。铁死亡抑制剂Fer-1与DFO可以减少脂质过氧化的水平,恢复胞内氧化还原平衡[15]。丙烯醛可以诱导细胞内ROS的产生(图3A)和亚铁离子水平(图3B)的升高,而Fer-1与DFO可以缓解丙烯醛诱导的ROS产生。因此我们认为丙烯醛可以诱发脂质过氧化与铁稳态的失衡。
鉴于丙烯醛可以诱发铁死亡的形态学与关键生化指标的改变,我们进一步对丙烯醛模型中铁死亡分子水平指标进行检测。铁死亡相关蛋白的变化是判断是否发生铁死亡的标准之一。GPX4是已知的唯一一种能有效减少生物膜中过氧化脂质的酶,并且被认为是铁死亡的关键调节因子[16]。COX-2是合成前列腺素的关键酶,也是一种重要的脂质过氧化标志物[17]。研究表明COX-2在铁死亡过程中显著上调[18]。丙烯醛在体内外都能都促进COX-2的蛋白表达,并减少GPX4的蛋白表达(图4-5)。FTH1在维持细胞内铁稳态的Fe3+/Fe2+流出和储存中起重要作用,FTH1可催化Fe2+氧化反应中铁离子储存的第一步,进而能够储存Fe3+。FTH1过表达可改善6-OHDA诱导的铁死亡[19]与AD小鼠模型的记忆损伤[8]。短时间体外细胞水平给予丙烯醛诱导FTH1表达上调(图4),可能是细胞应对铁稳态失衡的应激现象。在对铁死亡诱导剂四氯苯醌的体外研究中发现FTH1表达增加[20],同时在Aβ1–42的原代神经元损伤模型中[8]也出现了FTH1水平上调的情况,可能是通过激活核因子-E2相关因子2(nuclear factor erythroidderived 2-like 2)增加FTH1转录发挥短期抗应激作用。而在长期给予丙烯醛的小鼠模型中,由于部分神经元受损因此缺乏抗应激的机制,最终导致FTH1下降和铁稳态失衡(图5)。
综上,本研究提示丙烯醛可以在体内外诱导铁死亡的病理改变,包括线粒体形态学、脂质过氧化、胞内亚铁离子水平升高以及相关蛋白的变化。并且提示我们铁死亡抑制剂可以用来缓解、治疗与丙烯醛有关的中枢神经系统疾病。由于AD中广泛存在着铁死亡,因此本研究揭示了丙烯醛诱导AD样病理改变的新途径,并扩展了丙烯醛模型作为铁死亡模型进行病理研究和药物筛选的用途。但丙烯醛具体是通过何种途径或通路发挥诱导铁死亡发生的,仍需要进一步探究。

