五味消毒饮标准煎液指纹图谱的建立
郑艳萍,张晓琳,彭雲,赵开军,贵书琪,4,刁和芳*(.江苏弘典中药产业研究院有限公司 南京市工程技术研究中心,南京 004;.苏州思源天然产物研发有限公司,江苏 苏州 56;.南京中山制药有限公司 江苏省中药经典名方工程技术研究中心,南京 0046;4.中国药科大学中药学院,南京 98)
五味消毒饮出自《医宗金鉴》,由金银花、蒲公英、天葵子、野菊花、紫花地丁5 味药组成,具有清热解毒、消散疔疮等功效,常用于疔毒等症。现代研究表明,本方主要含有绿原酸、咖啡酸、木犀草苷、蒙花苷等成分[1-5],具有抗菌、抗炎、抗病毒、抗肿瘤、抗氧化、增强机体免疫功能等作用[6-7],临床上广泛用于五官科、内科、外科、妇科等火毒湿热所致的感染性疾患[8-10]。目前,五味消毒饮临床应用以传统汤剂为主[11],然而,其质量一致性易受煎煮方式及原药材品质的影响。因此,为了确保五味消毒饮后续研发的剂型能保持原方的药效,有必要建立标准煎液的质量控制方法。
中药复方制剂成分复杂,部分指标性成分检测并不能充分体现整体质量与药效。中药指纹图谱能全面、系统地反映复方制剂的整体特征,已成为中药质量控制的有效手段[12-13]。本研究采用HPLC 法建立五味消毒饮标准煎液的指纹图谱,为五味消毒饮标准煎液的质量评价提供方法及依据。
1 材料
1.1 仪器
LC-20AT 高效液相色谱仪(日本岛津公司);EL104 电子天平(瑞士梅特勒-托利多仪器有限公司)。
1.2 试药
金银花Lonicera japonicaThunb.产地来源为山东和河南,野菊花Chrysanthemum indicumL.产地来源为安徽和湖北,蒲公英Taraxacum mongolicumHand.-Mazz.产地来源为河南、山西、内蒙古,紫花地丁Viola yedoensisMakino 产地来源为河南、山东、陕西,天葵子Semiaquilegia adoxoides(DC.)Makino 产地来源为安徽、湖北、湖南,各10 个批次(均购于安徽汇中州中药饮片有限公司和安徽金芙蓉中药饮片有限公司,经南京中山制药有限公司李辉执业中药师鉴定)。经检验,以上药材水分、灰分、含量、浸出物等均符合2015年版《中国药典》一部相关规定。
绿原酸(批号:110753-201716,纯度≥99%)和咖啡酸(批号:110885-201703,纯度≥99%)(对照品,中国食品药品检定研究院),木犀草苷(批号:17030405,纯度≥99%)和蒙花苷(批号:15101207,纯度≥99%)(对照品,北京北纳创联生物技术研究院)。
甲醇、乙腈(色谱纯,安徽天地高纯溶剂有限公司),磷酸(分析纯,南京化学试剂股份有限公司),水为娃哈哈纯净水。
2 方法与结果
2.1 样品的制备
2.1.1 对照品溶液 精密称取绿原酸、咖啡酸、木犀草苷、蒙花苷对照品适量,加80%甲醇配制成质量浓度分别为32、19.68、10.7、17.28 μg·mL-1的对照品溶液。
2.1.2 供试品溶液 取金银花150 g、野菊花60 g、蒲公英60 g、紫花地丁60 g、天葵子60 g,加4.5 L 水,浸泡20 min,加热至沸,沸腾20 min 后过滤,药渣加4 L 水,加热至沸,沸腾20 min 后过滤,合并药液,减压浓缩至含生药1.0 g·mL-1。量取浓缩液1 mL,加入1 mL 水,混匀,用80%甲醇定容至50 mL,摇匀,过0.45 μm 微孔滤膜,取续滤液,即得。按照表1对应的产地及批号的药材制备16 批五味消毒饮标准煎液。
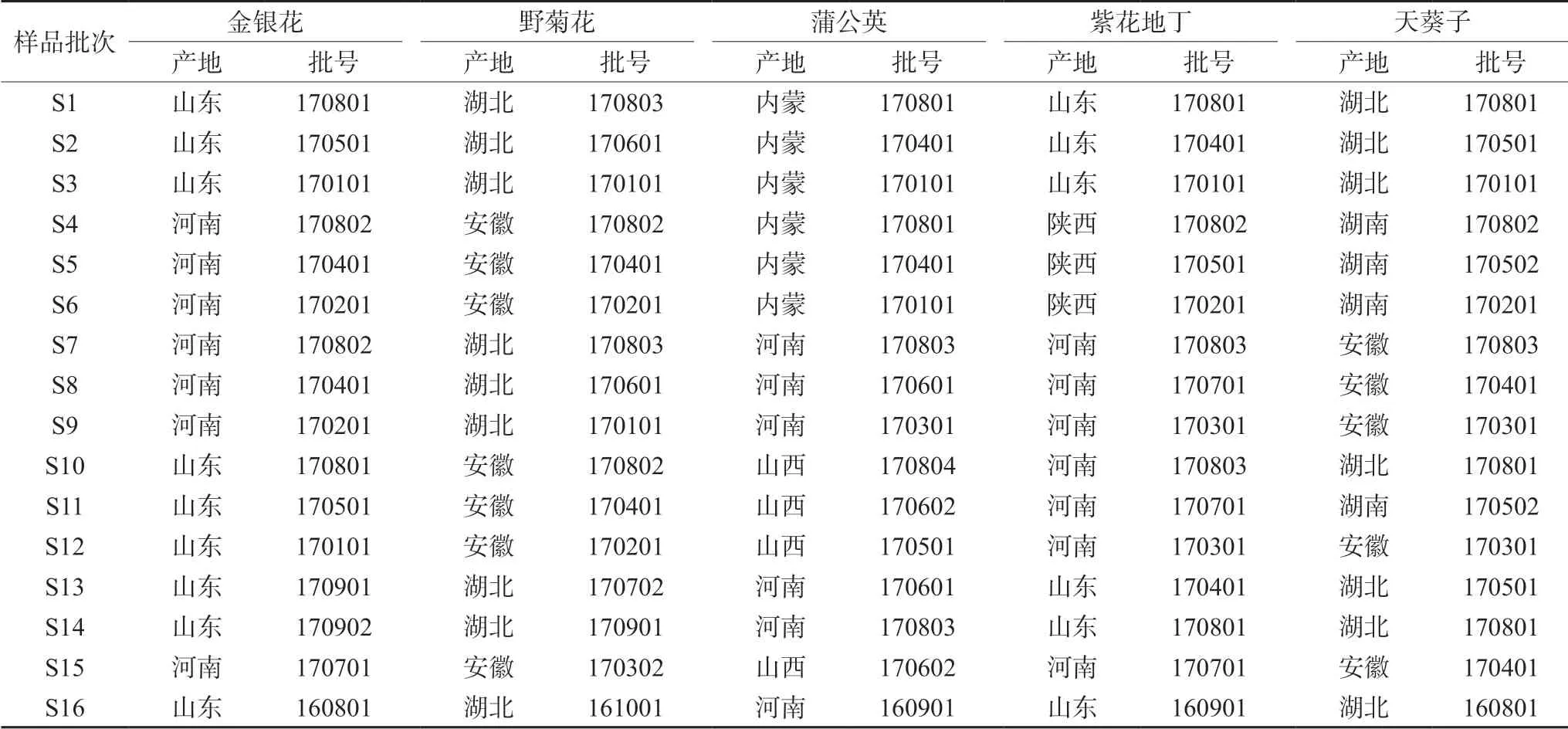
表1 16 批五味消毒饮标准煎液药材样品产地及批号Tab 1 Origin places and batch numbers of herbs in 16 batches of Wuwei Xiaoduyin standard decoction
2.1.3 单味药供试液 分别取金银花150 g,野菊花60 g,蒲公英60 g,紫花地丁60 g,天葵子60 g,按照“2.1.2”项下方法制备,即得各单味药的供试液。
2.2 色谱条件
色谱柱:YMC-Pack ODS-A 柱(250 mm×4.6 mm,5 μm);流动相:乙腈(A)-0.1%磷酸水溶液(B),洗脱梯度(0~20 min,90%~80%B;20~40 min,80%~75%B;40~52 min,75%~70%B;52~52.01 min,70%~90%B;52.01~60 min,90%B);流速:1.0 mL·min-1;柱温:30℃;检测波长:330 nm;进样量:20 μL。
2.3 方法学考察
2.3.1 线性关系考察 分别精密称取绿原酸对照品10.3 mg 和蒙花苷对照品1.1 mg 置25 mL 量瓶中,加甲醇溶解并定容,得到各对照品储备液。绿原酸对照品储备液用甲醇稀释至264、132、66、33、16.5 μg·mL-1,蒙花苷对照品储备液用甲醇稀释至35.2、17.6、8.8、4.4、2.2 μg·mL-1,进样测定,以对照品溶液的质量浓度(μg·mL-1)为横坐标,峰面积为纵坐标,计算回归方程:绿原酸Y=6.11×104X-2.23×104(r=0.9999),线性范围:16.5~264 μg·mL-1;蒙花苷Y=5.03×104X+4.25×103(r=0.9999),线性范围:2.2~35.2 μg·mL-1。
2.3.2 稳定性试验 取同一供试品溶液,分别于0、2、4、6、8 h 进样,按“2.2”项下色谱条件进行测定,结果显示相对保留时间和相对峰面积RSD均小于3%,表明供试品溶液在8 h 内稳定性良好。
2.3.3 精密度试验 取同一供试品溶液,连续进样5 次,按“2.2”项下色谱条件进行测定,结果显示相对保留时间和相对峰面积RSD均小于3%,表明仪器精密度良好。
2.3.4 重复性试验 参照“2.1.2”项下方法平行制备5 份供试品溶液,按“2.2”项下色谱条件进行测定,结果显示相对保留时间和相对峰面积RSD均小于3%,表明该方法重复性良好。
2.3.5 加样回收试验
① 绿原酸加样回收试验:按“2.1.2”项下方法制备9份标准煎液浓缩液,每3份一组,取0.25 mL 置25 mL 量瓶中,加入0.25 mL 水,摇匀,分别加入165 μg·mL-1绿原酸对照品溶液10、13、15 mL,加80%的甲醇定容,摇匀,经0.45 μm 微孔滤膜过滤,取续滤液为供试品溶液,按“2.2”项下色谱条件进行测定,结果低、中、高回收率均在101.0%~102.8%,RSD均小于1.0%。
② 蒙花苷加样回收试验:按“2.1.2”项下方法制备9份标准煎液浓缩液,每3份一组,取0.30 mL 置50 mL 量瓶中,加入0.70 mL 水,摇匀,分别加入44 μg·mL-1蒙花苷对照品溶液4、5、6 mL,加80%的甲醇定容,摇匀,经0.45 μm 微孔滤膜过滤,取续滤液为供试品溶液,按“2.2”项下色谱条件进行测定,结果低、中、高回收率均在97.0%~99.2%,RSD均小于1.0%。
2.4 五味消毒饮标准煎液含量测定
取“2.1.2”项下供试品溶液,按“2.2”项下色谱条件检测,计算绿原酸及蒙花苷含量,结果见表2。
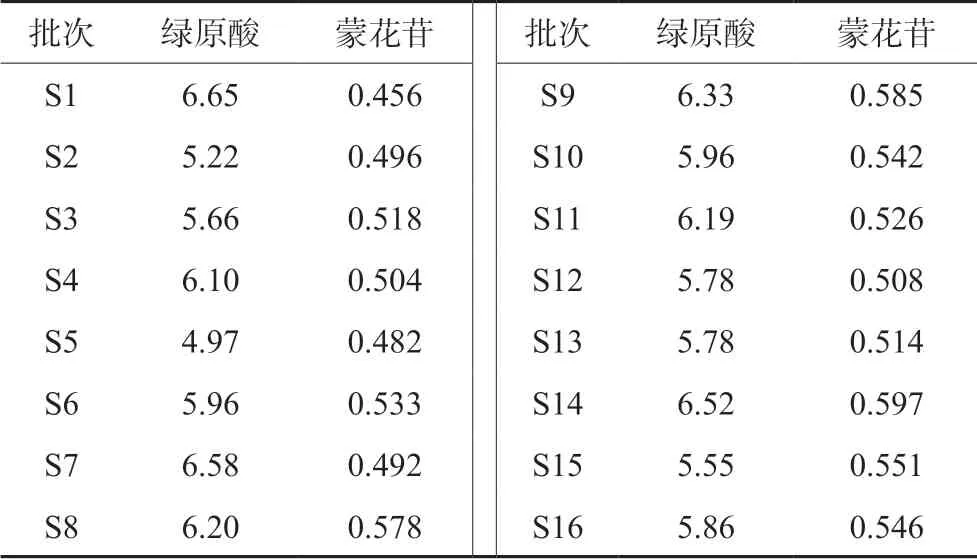
表2 样品含量测定结果(n =3,mg·g-1)Tab 2 Sample content determination (n =3,mg·g-1)
2.5 五味消毒饮标准煎液指纹图谱的建立
将16 批供试品溶液按“2.2”项下色谱条件进行测定,记录1 h 内的色谱图。将其导入“中药指纹图谱相似度评价系统2012 版”,生成五味消毒饮标准煎液特征指纹图谱,见图1,结果确定了13 个共有峰。取混合对照品溶液,按“2.2”项下色谱条件进行测定,见图2,通过比对各峰与混合对照品色谱峰保留时间,确认 3、6、9、13号峰分别为绿原酸、咖啡酸、木犀草苷和蒙花苷。
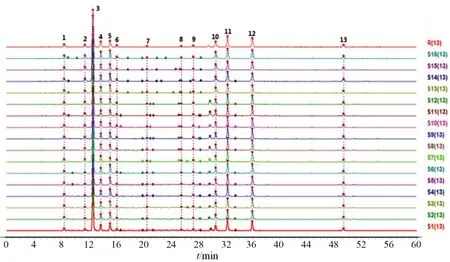
图1 16 批五味消毒饮标准煎液HPLC 指纹图谱Fig 1 HPLC fingerprint of 16 batches of Wuwei Xiaoduyin standard decoction
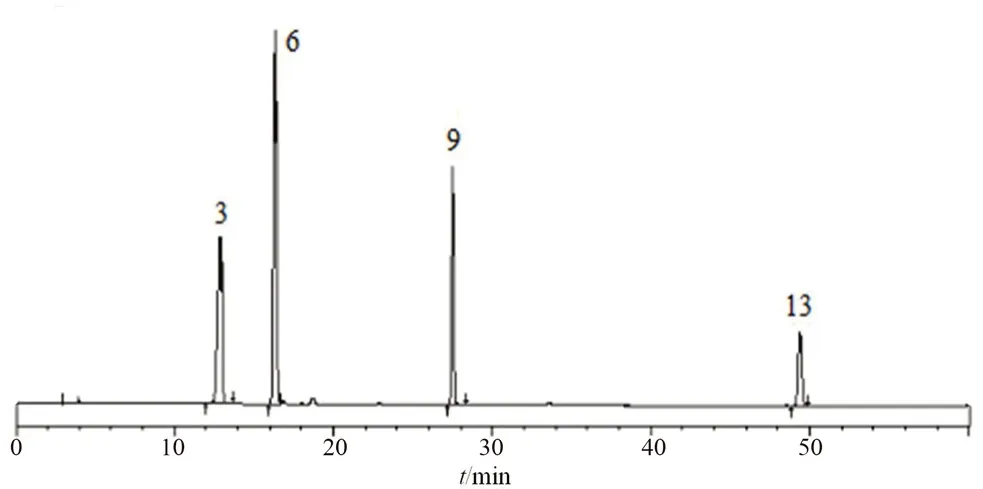
图2 混合对照品HPLC 指纹图谱Fig 2 HPLC fingerprint of mixed reference substances
在16 批五味消毒饮标准煎液指纹图谱中,3号峰(绿原酸)峰面积最大且分离度好,故选用3号峰作为参照峰,计算共有峰的相对保留时间和相对峰面积。
采用“中药指纹图谱相似度评价系统2012版”,对16 批标准煎液的指纹图谱进行相似度分析,结果分别为0.998、0.999、0.999、0.999、0.998、0.998、0.998、0.999、0.999、0.998、0.999、0.999、0.998、0.999、0.996、0.998,均大于0.99,说明样品制备方法及所建立的指纹图谱稳定可靠,能作为五味消毒饮标准煎液质量控制的参考依据。
2.6 指纹图谱特征峰的归属分析
将单味药供试液按“2.2”项下色谱条件进行测定,记录色谱图。通过与标准煎液及其对照指纹图谱进行比较,确定各特征峰归属,结果见图3。指纹图谱特征峰主要由金银花、野菊花、蒲公英、紫花地丁4 味药材所贡献。其中,1 号峰、3号峰、4 号峰、9 号峰、10 号峰、11 号峰、12 号峰主要来源于金银花,次要来源于野菊花;2 号峰单独来源于蒲公英;5 号峰和7 号峰单独来源于紫花地丁;6 号峰来源于蒲公英和金银花;8 号峰来源于紫花地丁和金银花;13 号峰单独来源于野菊花。五味消毒饮标准煎液共有峰归属见表3。
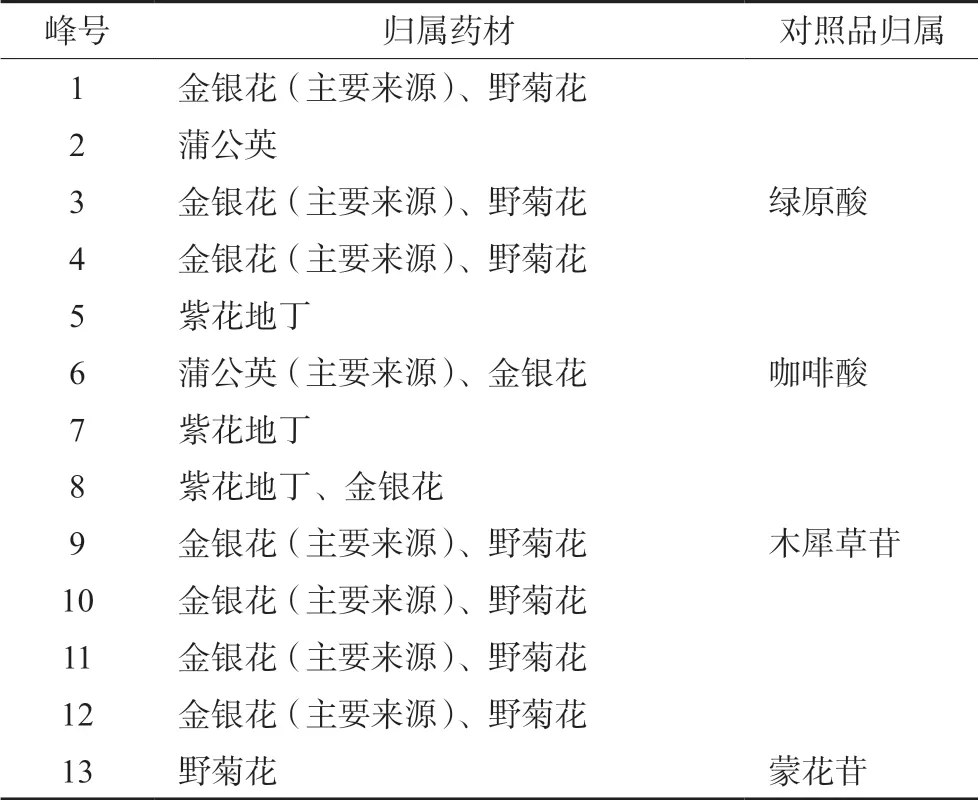
表3 五味消毒饮标准煎液共有峰归属Tab 3 Common peaks attribution in Wuwei Xiaoduyin standard decoction

图3 单味药标准煎液HPLC 指纹图谱及对照指纹图谱Fig 3 HPLC fingerprint of single medicinal material standard decoction and reference substance
3 讨论
在对五味消毒饮标准煎液指纹图谱特征峰进行归属分析时,发现天葵子没有对应特征峰,可能是因为天葵子的主要成分为内酯类和氰苷类化合物[14],其中内酯类化合物微溶于水[5],按照五味消毒饮经典名方的传统工艺,药材加水制备标准煎液后,其溶于标准煎液中的含量很低,难以检测。
为了对五味消毒饮进行质量控制,张宇等[7]采用HPLC 法测定了其口服液中绿原酸和咖啡酸的含量,杨宏静等[6]利用HPLC 法测定了五味消毒饮中绿原酸、咖啡酸、蒙花苷和秦皮乙素的含量。然而,利用己知的少量活性成分的含量来控制中药的质量不充分,指纹图谱能更全面地反映其整体特征[15]。杨晓琴等[11]建立了五味消毒饮口服液的HPLC 指纹图谱,并对其特征峰进行了对照品归属,但并未归属到药材。本研究建立了五味消毒饮标准煎液的HPLC 特征指纹图谱,对共有峰进行了中药材归属和化学成分指认,较全面地反映了五味消毒饮标准煎液的整体化学特征,该方法稳定可靠、重复性好,可为五味消毒饮标准煎液的质量控制提供依据。
此外,本课题组前期对供试品的制备方法进行了优化,发现减压浓缩后,直接用80%甲醇稀释会产生大量浅棕色大片絮状沉淀,沉淀会包裹药液成分,影响测定结果,加水后再稀释,这种情况得到较大改善。对60%甲醇、70%甲醇、80%甲醇稀释溶剂进行比较,发现80%甲醇为稀释溶剂时,各成分的峰面积都较高,故选择浓缩液加水稀释后用80%甲醇稀释定容。比较了色谱柱Comasil ODS AR-Ⅱ、Nucleosil C18、YMC-Pack ODS-A 洗脱效果,结果表明,YMCPack ODS-A 对应图谱的色谱峰分离最佳,峰形最好,因此选用YMC-Pack ODS-A 色谱柱。对流动相甲醇-0.3%磷酸水溶液、乙腈-0.1%磷酸水溶液、乙腈-0.4%磷酸水溶液进行考察,发现以甲醇-0.3%磷酸水溶液洗脱时,色谱峰拖尾;以乙腈-0.4%磷酸水溶液洗脱时,色谱峰分离度较差;以乙腈-0.1%磷酸水溶液洗脱时,色谱峰分离度较好,保留时间适中,故流动相确定为乙腈-0.1%磷酸水溶液。对供试液进行全波长扫描,结果在检测波长为330 nm 时,图谱信息最为丰富,响应值普遍较高,且分离效果较好,因此选择330 nm 为检测波长。

