探讨布地奈德混悬液联合特布他林用于小儿哮喘治疗的可行性
孙倩倩,石涛
滨州医学院附属医院儿童呼吸科,山东滨州 256603
哮喘是一种可逆性、梗阻性的呼吸系统疾病,在4~5 岁儿童中的发病率较高,具体表现为反复发作性的咳嗽、喘鸣、呼吸困难等,患者普遍伴有气道高反应性[1-2]。目前, 临床普遍认为哮喘的发生与精神心理、 空气污染、肥胖、吸烟等有着极为密切的联系[3]。 据不完全统计,世界范围内受哮喘干扰、影响的患者多达3 亿人,且近年来发患者群逐年增多[4]。 布地奈德雾化吸入是临床哮喘的常用药物, 虽然对咳嗽等症状具有一定的缓解作用,但对肺功能、炎症反应治疗效果并不理想,往往需要辅助其他药物治疗。 特布他林属于选择性β2受体激动剂,可有效扩张支气管,缓解气道痉挛,改善缺氧、咳嗽等症状[5]。 基于此,该文对该院 2017 年 9 月—2019 年9 月住院治疗的300 例患儿研究,现报道如下。
1 资料与方法
1.1 一般资料
研究对象为简单随机选取于该院住院治疗的300例哮喘患儿,已得到伦理委员会审批,以“单盲随机抽样法”分组,联药组(150 例),女性 52 例、男性 98 例;年龄在 2~9 岁,平均(5.52±1.68)岁;病程在 4~15 个月,平均(9.31±3.52)个月;体质量在 6.7~39.1 kg,平均(22.57±3.17)kg;哮喘严重程度分级:轻度 45 例、中度 60 例、重度 45 例。 单药组(150 例),女性 58 例、男性 92 例;年龄在 3~9 岁,平均(5.58±1.61)岁;病程在 6~12 个月,平均(9.33±2.67)个月;体质量在 6.9~38.7 kg,平均(22.52±3.09)kg;哮喘严重程度分级:轻度 48 例、中度 59 例、重度43 例。 两组(性别、体质量、年龄、病程、哮喘严重程度分级等)相比,差异无统计学意义(P>0.05),可比较。
纳入标准:①均符合《中西医结合防治儿童哮喘专家共识》[6]中关于“哮喘”诊断标准;②无遗传性、先天性疾病;③家属知情并同意。
排除标准:①免疫、血液、内分泌系统疾病者;②中途从此项研究退出者;③存在药物过敏史者;④合并其他呼吸系统疾病者;⑤近期接受过解痉等对症治疗者;⑥严重营养不良者;⑦严重营养不良、重度贫血者。
支气管哮喘严重程度分级标准: ①轻度: 可以走路,但上楼会咳嗽,休息后会缓解;②中度:活动后出现呼吸困难、气喘等症状,肺部存在哮鸣音,需要吸氧;③重度:连贯说话会累,存在心跳加快、大汗淋漓、端坐呼吸等症状,需及时接受治疗;④危重度:无法说话,存在昏迷、意识不清、缺氧严重、口唇紫绀等症状,不及时抢救就存在生命危险。
1.2 方法
单药组:给予 1 mg 布地奈德混悬液(规格:2 mL∶1 mg×5 支;国药准字 H20203063),溶于 2~3 mL 0.9%氯化钠溶液中,雾化吸入,15 min/次,3 次/d,共计治疗 14 d。
联药组:布地奈德混悬液的用法、用时、用量等均与单药组一致,给予特布他林吸入剂(规格:2 mL∶5 mg×5 支;国药准字 H20140108),>20 kg、≤20 kg 的患者分别给予 5 mg、2.5 mg 吸入,3 次/d,共计治疗 14 d。
1.3 观察指标
两组治疗效果均在治疗14 d 后评价, 观察指标包括:①临床疗效判定标准。 X 线示肺部阴影消失75%以上(包括75%)为显效;X 线示肺部阴影消失50%~74%(包括50%)为有效;未达到以上标准为无效。 总有效率=(显效例数+有效例数)/150 ×100.00%[7]。②肺功能指标。 以肺功能测定仪(型号:PIKO-1;生产企业:上海益联科教设备有限公司)测定FEV1(第1 秒用力呼气容积占预计值的百分比)、PEF(呼气峰流量)。③血清炎性因子指标。 抽取3 mL 空腹静脉血,以3 000 r/min 离心速率、10 cm 离心半径,离心处理10 min 后,分离血清并置于-80℃环境待检,以ELISA 法检测IL-6(白细胞介素-6)、CRP(C 反应蛋白),试剂均由深圳市晋百慧生物有限公司提供,一切操作谨遵相关标准完成,所有的血液样品必须在采集后的2 h 内完成检测。 ④C-ACT评分[8]。 此C-ACT 评价问卷调查表评估患者的哮喘控制情况,满分是27 分,表示哮喘情况控制十分理想。 ⑤不良反应发生率。 统计头晕头痛、恶心呕吐、皮疹乏力发生率。⑥复发率。随访6 个月,统计哮喘复发率,复发率=复发例数/150×100.00%。
1.4 统计方法
采用SPSS 26.0 统计学软件对数据进行分析,计量资料采用()表示,进行t检验;计数资料采用[n(%)]表示,进行 χ2检验。P<0.05 为差异有统计学意义。
2 结果
2.1 两组临床疗效比较
临床总有效率联药组 (98.00%) 高于单药组(87.33%),差异有统计学意义(P<0.05),见表 1。
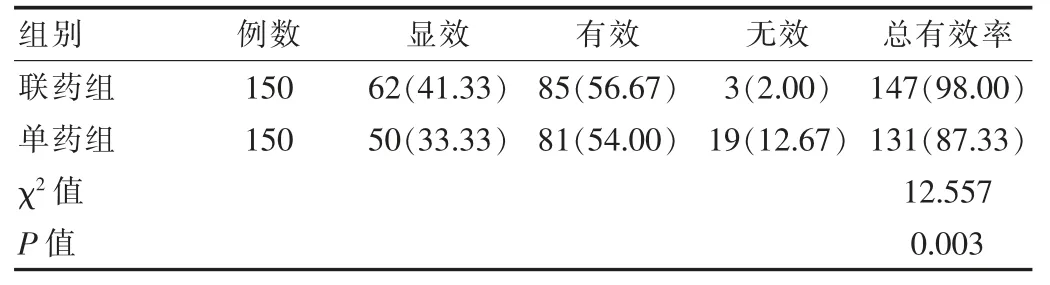
表1 两组患者临床疗效比较[n(%)]
2.2 两组肺功能指标比较
治疗前比较两组FEV1、PEF, 差异无统计学意义(P>0.05);治疗后联药组均高于单药组,差异有统计学意义(P<0.05),见表 2。
表2 两组患者肺功能指标比较()

表2 两组患者肺功能指标比较()
组别FEV1治疗前 治疗后PEF治疗前 治疗后联药组(n=150)单药组(n=150)t 值P 值62.26±3.66 62.36±3.59 0.239 0.811 75.92±8.64 67.26±4.16 11.061<0.001 65.26±4.16 65.33±4.28 0.144 0.886 84.26±9.64 73.26±6.04 11.843<0.001
2.3 两组血清炎性因子指标比较
治疗前比较两组血清IL-6、CRP,差异无统计学意义(P>0.05);治疗后联药组均低于单药组,差异有统计学意义(P<0.05),见表 3。
表3 血清患者炎性因子指标比较()

表3 血清患者炎性因子指标比较()
组别IL-6(ng/L)治疗前 治疗后CRP(mg/L)治疗前 治疗后联药组(n=150)单药组(n=150)t 值P 值305.26±28.62 306.99±27.16 0.537 0.592 62.25±6.34 195.29±11.19 126.690<0.001 5.92±1.64 5.96±1.59 0.214 0.830 2.06±0.16 3.99±0.75 30.823<0.001
2.4 两组C-ACT 评分比较
治疗前比较两组C-ACT 评分,差异无统计学意义(P>0.05);治疗后联药组高于单药组,差异有统计学意义(P<0.05);且两组治疗后均高于治疗前,差异有统计学意义(P<0.05),见表 4。
表4 两组患者 C-ACT 评分比较[(),分]

表4 两组患者 C-ACT 评分比较[(),分]
组别 治疗前 治疗后联药组(n=150)单药组(n=150)t 值P 值9.32±1.26 9.44±1.34 0.799 0.425 18.92±4.62 12.26±2.17 15.980<0.001
2.5 两组不良反应发生率比较
不良反应发生率联药组(3.33%)与单药组(2.00%)比较,差异无统计学意义(P>0.05),见表 5。
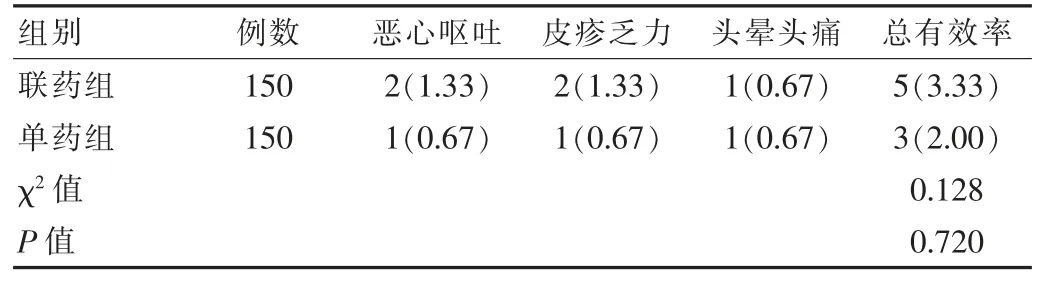
表5 两组患者不良反应发生率比较[n(%)]
2.6 两组患者6 个月内复发率比较
联药组6 个月内复发1 例,占0.67%。 单药组6 个月内复发10 例,占6.67%,联药组6 个月内复发率低于单药组,差异有统计学意义(χ2=7.644,P=0.006)。
3 讨论
当前,临床对于哮喘的发病机制尚不明确,普遍认为该病的发生与精神、遗传、饮食、免疫、环境等联系密切,呼吸道感染、吸入变应原、药物过敏等均会导致哮喘复发[9-10]。据流行病学调查显示,近年来我国哮喘的发生率明显增高[11]。小儿哮喘患者普遍存在胸闷、咳嗽、呼吸困难、喘息、鼻痒、流涕等症状,多在清晨或夜间发作,病程较长、治疗难度大、易反复发作,随着疾病的发展,患者会出现多变的可逆性气流受限,降低了患者生活质量[12-13]。 小儿哮喘如果不及时接受科学、有效的治疗,反复发作的气道炎症,会引发气道高反应性,最终由于气道重塑而降低肺功能,增加发心力衰竭、呼吸衰竭等并发症发生率,威胁患者生命安全[14-15]。
该研究显示临床总有效率联药组(98.00%)高于单药组(87.33%),治疗后联药组 FEV1、PEF、C-ACT 评分均高于单药组,治疗后联药组血清IL-6、CRP 均低于单药组, 联药组6 个月内复发率 (0.67%) 低于单药组(6.67%)(P<0.05)。 表明小儿哮喘患者采纳布地奈德混悬液+特布他林治疗,病情得到良好控制,且无不良反应出现。 分析如下:①布地奈德属于糖皮质激素,可抑制抗体合成及免疫反应,增强内皮细胞、平滑肌细胞、溶酶体膜的稳定性,抑制抗组胺等物质释放,减轻平滑肌收缩反应,达到缓解咳嗽等症状的作用[16]。 ②特布他林可抑制内源性物质释放,增强呼吸道纤毛运动功能,抑制致挛物质释放,有效舒张平滑肌。 特布他林对支气管的扩张效应明显强于布地奈德,且维持时间较长,可较好地抑制哮喘夜间、清晨发作,避免患者夜间由于哮喘而憋醒[17-18]。③特布他林可以增加β2受体表达,长期、有效地扩张支气管,同时不会引发心血管、呼吸道等不良反应, 在布地奈德混悬液治疗的基础上予以特布他林,协同作用,优势互补,可取得理想的治疗效果,弥补了单一布地奈德治疗的不足和缺陷[19]。 在杨立春等[20]研究中, 接受布地奈德混悬液雾化治疗的对照组总有效率是77.14%,接受布地奈德混悬液+特布他林治疗的观察组总有效率是94.29%,观察组高于对照组(P<0.05),与该研究结果接近。该研究存在一定的不足,例如研究时限较短、样本容量较小,对结果的普遍性、一般性有所影响,故仍旧需要临床进一步扩大样本容量、延长研究时限,为评估布地奈德混悬液+特布他林在哮喘患儿治疗中的临床疗效提供更多的参考依据。
综上所述,布地奈德混悬液+特布他林可有效改善哮喘患儿病情及肺功能,减轻炎症反应,降低复发率,且联合用药并未增加不良反应。

