芦可替尼治疗骨髓纤维化患者的疗效及其预测模型
张雪皎 王跃 谭云山 刘澎
经典型骨髓增殖性肿瘤(myeloproliferative neo-plasms,MPNs)是一组起源于造血干细胞的克隆性疾病[1],主要包括真性红细胞增多症(polycythemia vera,PV)、原发性血小板增多症(essential thrombocythemia,ET)和原发性骨髓纤维化(primary myelofibrosis,PMF)。随着疾病的进展,12.7%~21.0%的PV、9.2%~9.9%的ET患者会继发骨髓纤维化(myelofibrosis,MF)[2],分别称为继发于PV的骨髓纤维化(post-polycythemia vera myelofibrosis,PPV-MF)和继发于ET的骨髓纤维化(post-essential thrombocythemia,PET -MF)。MF 是MPNs发展的主要病理学特征,是由促进纤维组织增生的细胞因子分泌过多而引起的骨髓纤维组织增生,发病率为0.1/10万~1/10万[3],通常表现为血细胞减少、髓外造血,常伴有体质性症状、脾大,易向白血病转化[4]。目前认为,MPNs的驱动基因突变如JAK2V617F、JAK2 EXON12、MPL W515I、CALR等都会通过直接或间接的方式激活JAK/STAT信号通路,不仅与MPNs发病密切相关,也与MF进展相关[5]。芦可替尼是一种JAK1/JAK2激酶抑制剂,可以抑制JAK/STAT信号通路活性,目前已被批准用于PMF、PPV-MF、PET-MF的一线治疗,可以缩小脾脏、减轻MF相关体质性症状、改善生活质量,并可以延长患者生存期[6]。2017年,芦可替尼获批在中国上市。本研究回顾分析于本中心采用芦可替尼治疗的MF患者的临床资料,探讨芦可替尼治疗MF的疗效及其预测指标。
1 资料与方法
1.1 一般资料
本研究纳入复旦大学附属中山医院血液科自2017年11月至2020年12月采用芦可替尼治疗的PMF、PPV-MF、PET-MF患者64例,其中PMF 47例,PPV-MF 6例,PET-MF 11例。所有患者诊断均参照世界卫生组织(WHO)2016 标准[7]。纳入标准:年龄≥18岁;接受至少12周芦可替尼为主的方案治疗;有完整的诊疗记录及随访记录。本研究通过复旦大学附属中山医院伦理委员会批准(审查编号:B2017-032R)。
1.2 观察指标及随访
通过门诊/住院病史收集患者的性别、年龄、动态国际预后指数(dynamic international prognostic scoring system,DIPSS)评分[8]、MF分级、芦可替尼起始剂量、血红蛋白、血小板计数、白细胞计数、中性粒细胞计数、外周血有无原幼细胞、红细胞体积分布宽度CV(RDW-CV)、红细胞体积分布宽度SD(RDW-SD)、平均血小板体积、脾脏大小等临床资料。后续通过门诊或电话对患者进行随访,主要随访内容包括芦可替尼剂量有无调整、脾脏大小等。随访截止日期为2021年4月15日,中位随访时间为17个月(范围:4~41个月)。随访期间死亡4例,其中3例因白血病转化死亡,无失访病例。
1.3 统计学方法
采用R 4.0.3和SPSS 21.0软件进行统计学分析。在R语言lars包中完成基于套索(LASSO)回归的变量筛选。统计中用到的主要R包包括psych、lars、gg-plot2、car、gmodels、GGally等。本研究纳入分析的自变量共有23个,其中9个连续变量:年龄、芦可替尼起始剂量、血红蛋白、血小板计数、白细胞计数、中性粒细胞计数、RDW-CV、RDW-SD、平均血小板体积;14个分类变量:性别、诊断(PMF、PET-MF、PPV-MF)、DIPSS评分(低危、中危-1、中危-2、高危)、MF分级(1级、2级、3级)、芦可替尼剂量调整(上调或下调)情况、外周血有无原幼细胞。以芦可替尼治疗12周时超声测量的脾脏长度较基线缩小≥35%为终点事件(因变量)进行分析。LASSO回归筛选出的变量,采用SPSS软件进行二分类Logistic回归分析,采用前进法建立回归模型(纳入标准为P<0.05),并采用受试者工作特征(ROC)曲线下面积(AUC)、灵敏度以及特异度评价该模型的预测能力。参照芦可替尼药物说明书,将标准起始剂量及较低起始剂量的患者进行分组,两组间的疗效比较采用χ2检验,以双侧P<0.05为差异有统计学意义。
2 结果
2.1 一般资料
共64例患者纳入研究,其中男性36例,女性28例。PET-MF患者以女性多见,PMF、PPV-MF均为男性多见。所有患者中位年龄为68岁(范围:34~89岁),其中PET-MF患者中位年龄较小,PPV-MF患者中位年龄较大,分别为59岁和74岁。所有MF患者中,DIPSS评分低危10例、中危-1 22例、中危-2 14例、高危18例。JAK2V617F基因突变45例,MPLW515L/K基因突变3例,CALR基因突变8例,三阴性8例。所有患者的临床资料见表1。

表1 64例骨髓纤维化患者的临床资料Tab.1 Clinical characteristics of 64 patients of myelofibrosis
2.2 芦可替尼药物剂量
多数患者因并发症或经济等原因开始用药时选择较小剂量,芦可替尼起始剂量从5 mg qd至20 mg bid不等,中位起始剂量为10 mg bid,日均起始剂量为20.7 mg。在用药过程中,4例PMF患者、4例PET-MF患者、1例PPV-MF患者上调药物剂量;9例PMF患者、1例PET-MF患者下调药物剂量。剂量调整多发生在初始用药后的第1~5个月。10例下调药物剂量患者中,8例患者起始的日均剂量为30~40 mg;2例患者起始日均剂量为20 mg,其中1例老年高危PMF患者在连续用药17个月后因血小板减少停药,之后未再用药,另1例因发生真菌性肺炎,在治疗肺炎期间减少用量后恢复原剂量。
2.3 LASSO回归分析结果
随访结果显示,23例(35.94%)MF患者的脾脏体积较基线缩小≥35%,其中包括21例(44.68%)PMF患者、2例(33.33%)PPV-MF患者。经LASSO回归分析,共筛选出13个变量与芦可替尼缩脾的疗效相关:药物剂量上调(回归系数为1.598)、MF-3级(回归系数为0.599)、中危-2(回归系数为0.427)、药物起始剂量(回归系数为0.069)、RDW-SD(回归系数为0.062)、中性粒细胞计数(回归系数为0.049)、RDW-CV(回归系数为0.028);PET-MF(回归系数为−4.697)、外周血有原幼细胞(回归系数为−1.821)、中危-1(回归系数为−0.857)、平均血小板体积(回归系数为−0.034)、血红蛋白(回归系数为−0.004)、血小板计数(回归系数为−0.002)。见图1。

图1 LASSO回归筛选芦可替尼治疗MF的疗效预测指标Fig.1 Screening of related indicators of therapeutic effect of Ruxolitinib in MF based on LASSO regression
2.4 Logistic回归预测模型的构建及ROC曲线评价
以芦可替尼治疗后的疗效为因变量(终点事件为脾脏缩小≥35%),LASSO回归筛选出的变量为自变量,采用前进法构建Logistic回归预测模型,见表2。Logistic回归模型公式为 Logit(P)=−3.561+2.398×PLT+0.137×RDW-SD−0.501×MPV−1.230×BLAST。该回归模型预测芦可替尼缩脾疗效的AUC为0.774(95%CI:0.633~0.916,P=0.002),敏感度为81.0%,特异度为69.6%,见图2。
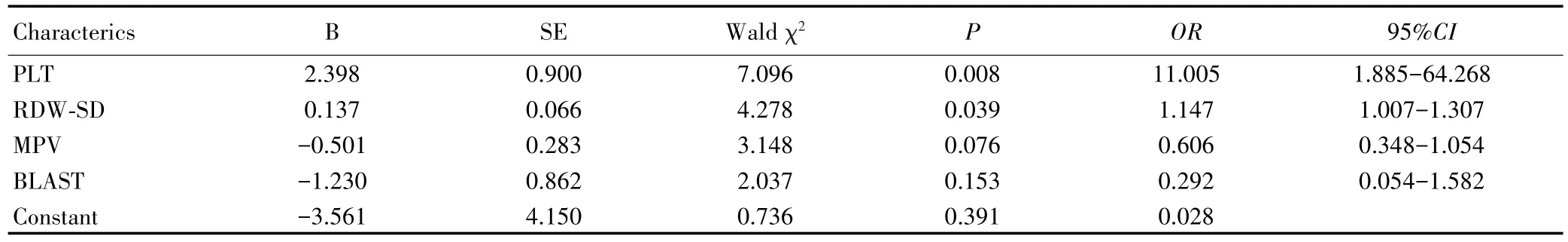
表2 二分类Logistic回归分析结果Tab.2 Results of binary Logistic regression analysis

图2 Logistic回归模型预测芦可替尼治疗MF疗效的ROC曲线Fig.2 ROC curve of Logistic regression model for predicting the efficacy of Ruxolitinib in the treatment of MF
2.5 芦可替尼剂量与预后的关系
15例患者(PMF患者14例、PPV-MF患者1例)按药品使用说明,根据基线血小板计数选择芦可替尼起始剂量(PLT 50×109/L~100×109/L,5 mg bid;PLT 100×109/L~200×109/L,15 mg bid;PLT>200×109/L,20 mg bid),其中7例(46.67%)患者脾脏体积较基线缩小≥35%,与所有MF患者的疗效比较差异有统计学意义(P<0.001)。9例上调剂量患者中,4例患者(44.44%)脾脏体积较基线缩小≥35%,与所有MF患者比较差异无统计学意义(P=0.621)。
3 讨论
COMFORT-I和COMFORT-Ⅱ是2个国际多中心前瞻性研究,分别研究了芦可替尼与安慰剂及最佳治疗对中危-2/高危MF患者的疗效及安全性[6],并证实了芦可替尼治疗MF的有效性。其中COMFORT-Ⅰ是芦可替尼治疗中危-2/高危MF患者的首个国际多中心研究,共纳入了来自澳洲、加拿大及美国的309例MF患者,随机1∶1分配入组,以治疗24周时脾脏体积缩小≥35%为主要终点。最终155例患者接受芦可替尼(15 mg bid或20 mg bid)治疗,154例患者接受安慰剂治疗,41.9%芦可替尼治疗的患者脾脏体积缩小≥35%,而安慰剂组仅为 0.7%(P<0.001)[9]。因真实世界中,每位患者并没有条件参照临床试验要求用MR或CT测量脾脏体积,故临床随访中常以脾脏B超作为复查脾脏大小的首选方式。本研究中64例患者均通过B超随访,35.94%的患者脾脏体积缩小≥35%,对不同亚型进行分析,发现分别有44.68%的PMF患者、33.33%的PPV-MF患者脾脏长度缩小≥35%。但是PET-MF患者均未达到,可能与随访时间不足有关,即最短随访时间仅有4个月,未达24周,因此部分患者尚未达到最大疗效;此外也可能由脾脏不同维度的缩小情况不一致所致。
在真实世界中,受患者自身身体、经济条件、药物可及性等多种因素制约,仅有部分患者在早期足量使用芦可替尼。目前国内也未见芦可替尼药物剂量与MF患者疗效关系的真实世界研究。本研究通过LASSO回归分析筛选出芦可替尼剂量上调及起始剂量与疗效相关。进一步亚组分析发现,与所有MF患者相比,15例(包括PMF患者14例、PPV-MF患者1例)早期足量使用芦可替尼的患者脾脏体积较基线缩小≥35%的比例明显提高,缓解率分别为35.94%和46.67%。这一结果也说明本研究中PET-MF患者均未达到脾脏缓解,其中的一个影响因素可能是未能早期足量应用芦可替尼。有研究已表明,与PMF相比,PPV和PET-MF表现出更高的增生性,在诊断和开始芦可替尼治疗时白细胞和/或血小板计数、血红蛋白水平都较高[10],但实际上不是所有的患者都能按标准剂量用药。由于本研究纳入的病例数较少,这一推论尚需验证。
血常规是患者诊治过程中的常规检查项目,价格低廉、检测快速,普及性很高。本研究发现,血常规检查中的部分指标与芦可替尼治疗MF的疗效有关,例如中性粒细胞计数。也有研究报道,炎症因子会促进MF[11]。还有研究发现MPN患者的血清钙卫蛋白较正常对照组升高,而且血清钙卫蛋白升高与患者的体质性症状呈正相关[12],而血清钙卫蛋白来源于中性粒细胞和巨噬细胞。以此推测,作为JAK抑制剂的芦可替尼可能通过抑制JAK-STAT通路活性,降低机体的炎症状态,从而起到改善脾肿大的作用,未来可进行基础实验证明这一推论。此外,本研究以MPV、BLAST、PLT、RDW-SD为预测因素构建Logistic回归模型,发现该模型对芦可替尼治疗MF的缩脾疗效有较好的预测价值,且所需预测因素均来自血常规检测指标,数据简便易得,值得在大样本中进一步验证其有效性。
既往也有研究显示,在PPV和PET-MF患者中,与高风险患者相比,中危-1风险患者的脾脏反应更高,血液学毒性也更低[10]。本研究亦发现DIPSS中危与患者脾脏缓解有关。但与之相比,本研究包含了PMF的患者,且采用的预后评分系统不同。前者应用的是西班牙学者构建的MYSEC-PM(Myelofibrosis Secondary to PV and ET Prognostic Model)[10],对 PPV 和 PET-MF患者的预后具有更好的区分度,而本研究因病例数过少未采用这一预后模型。
综上所述,早期给予足量芦可替尼治疗的MF患者缩脾疗效最佳,以MPV、BLAST、PLT、RDW-SD为预测因素构建的Logistic回归模型对芦可替尼治疗疗效有较好的预测价值,但本研究为单中心、小样本研究,因此研究结论仍需进一步验证。

