友好戈登氏菌降解内蒙古白音华褐煤的工艺条件探究
石晨,刘向荣,2,胡雪华
(1.西安科技大学 化学与化工学院,陕西 西安 710054;2.自然资源部煤炭资源勘察与综合利用重点实验室,陕西 西安 710021)
我国煤炭储量丰富,特别是风化煤和褐煤[1-2]。但褐煤在燃烧过程中产生NOx,SO2和粉尘等[3-5],容易引起环境污染问题。因此,需要寻找一条绿色转化的新出路,而煤的微生物转化技术是煤炭清洁利用的有效途径之一[6-8]。20世纪初,Fakoussa[9]和Cohen等[10]发现假单胞菌属、担子菌和白腐菌等多种菌种能够降解褐煤。Baylond等[11]研究发现,与真菌相比,细菌具有繁殖能力强、转化率高、操作简便等优点。但是,由于煤与菌种的复杂性和多样性,导致煤的微生物降解实验需要深入的探究。本文选择友好戈登氏菌降解内蒙古白音华褐煤,旨在优化降解工艺条件,探讨降解过程和分析产物组成。
1 实验部分
1.1 材料与仪器
内蒙白音华褐煤;浓硝酸、蛋白胨、酵母粉、MgSO4·H2O和琼脂等均为分析纯;友好戈登氏菌,购买于中国微生物菌种保藏管理中心(CICC),编号为CICC 20664。
CTDG-200875 密封对辊破碎机;XMB-70A型棒磨机;PS-200振筛机;SW-CJ-1FD超净工作台;BL-50A立式压力蒸汽灭器;BC-360生化培养箱;HZQ-F100全温振荡培养箱;Thermo Scientific傅里叶变换红外光谱仪;Mini Flex600 X射线衍射仪;Mettler-Toledo TG-DSC1 HT型热重分析仪;7890A/5975C气相-质谱联用分析仪等。
1.2 煤样的预处理
煤样采自内蒙白音华煤矿,经过粉碎,筛分,选择粒径为0.125~0.250 mm的原煤进行硝酸预处理,用8 mol/L的硝酸浸泡24 h。浸泡结束后,用蒸馏水进行洗涤、过滤,直至pH≈7。将煤样装入烧杯,使用透气膜和报纸封口,灭菌15 min。
1.3 菌种培养
友好戈登氏菌,培养基采用CICC提供的配方,组成为:蛋白胨10 g,酵母粉2 g,MgSO4·H2O 1 g,琼脂 20 g,蒸馏水1 L,pH=7。取斜面活化后的菌种,接于200 mL的液体培养基中,在温度为30 ℃,摇床转速为160 r/min进行培养,时间为3 d,得到扩大培养液。
1.4 微生物降解实验
取0.3 g煤样和50 mL液体培养基分别放入BL-50A灭菌锅中,121 ℃,灭菌15 min。与10 mL扩大培养液混合放入HZQ-F100摇床中,在温度30 ℃, 摇床转速为160 r/min中培养。实验结束后,离心(9 000 r/min,20 min),收集固相产物(剩煤)和液相产物。用蒸馏水对固相产物(剩煤)进行清洗,直至固相产物(剩煤)中无菌体残留,烘干(90 ℃,12 h)备用。
1.5 降解产物分析与表征
1.5.1 固相产物 准确称取1.5 mg干燥后的固相产物(剩煤)与200 mg的KBr混合,制成薄片,在4 000~400 cm-1范围内,分辨率4 cm-1,用Thermo Scientific 傅里叶变换红外光谱仪进行扫描。采用Mini Flex600 X-射线衍射仪,对固相产物(剩煤)进行XRD分析,扫描速度为2(°)/min,扫描范围为10~80°,Cu KaX衍射源,工作电压40 kV,工作电流200 mV。采用Mettler-Toledo TG-DSC1 HT型热重分析仪对固相产物(剩煤)进行热重实验。原煤和氧化煤的分析方法与固相产物(剩煤)相同。
1.5.2 液相产物 将最佳工艺条件下得到的黑色液相产物,使用不同极性的萃取剂进行萃取。萃取剂的极性由小到大的顺序为四氯化碳<苯<丙酮<甲醇。萃取液利用7890A/5975 C型气相色谱-质谱联用仪进行测定。
1.6 降解率的测定和计算
降解过程的测定指标有2种[12]。
1.6.1 降解率 将降解完的煤液,过滤,烘干称重为m和起始加入煤质量m0的差值除以起始煤的质量m0,为降解率η。见公式(1)。
(1)
其中,η为降解率;m0为起始加入煤的质量,g;m为固相产物(剩煤)的质量,g。
1.6.2 吸光度 石开仪等[13]通过测量液相产物中450 nm处的吸光度,用来评估微生物降解效果,并且发现A450值与降解率呈现正相关。
2 结果与讨论
2.1 煤样的预处理
原煤、氧化煤(8 mol/L)和固相产物(剩煤)的工业分析与元素分析见表1。
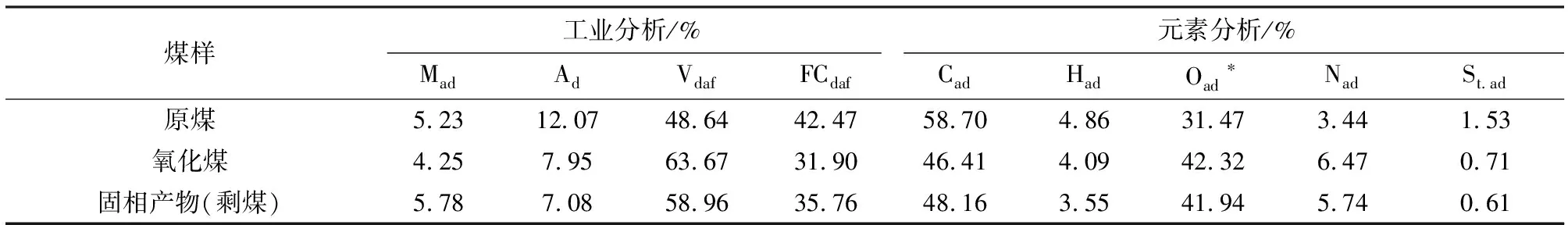
表1 煤样工业分析和元素分析Table 1 Ultimate and proximate analysis of testing coal sample
由表1可知,原煤的挥发分为48.64%,碳含量为58.70%,氧含量为31.47%,属于褐煤。硝酸预处理后,碳含量降低,氧含量升高,发生了氧化反应。石开仪[14]和尹苏东等[15-16]研究发现煤经硝酸氧化后,灰分含量降低,挥发分升高,孔径增大。此外,硝酸与煤中含芳环基团之间发生了化学反应,如芳香环的氧化和芳香环侧链氧化成酯、醛、酮等物质。这些结构的变化有利于生物降解,增加降解率[17-18]。
微生物作用后,氧化煤中的氧和氮含量下降。可能是友好戈登氏菌分泌出来的活性物质与氧化煤中的羧基和氨基发生反应,生成小分子化合物,导致其含量下降[8]。
2.2 煤的微生物降解实验
2.2.1 煤浆浓度对降解效果的影响 由图1可知,随着煤浆浓度的增加,友好戈登氏菌对白音华氧化煤呈现先增加再减少的趋势,当煤浆浓度为0.5 g/50 mL 培养基时,吸光度A450值最大为1.413。原因可能是当煤浆浓度增加时,友好戈登氏菌的生长受到抑制,繁殖空间有限,不能更好利用白音华氧化煤作为碳源,因此最佳煤浆浓度为0.5 g/50 mL 培养基。
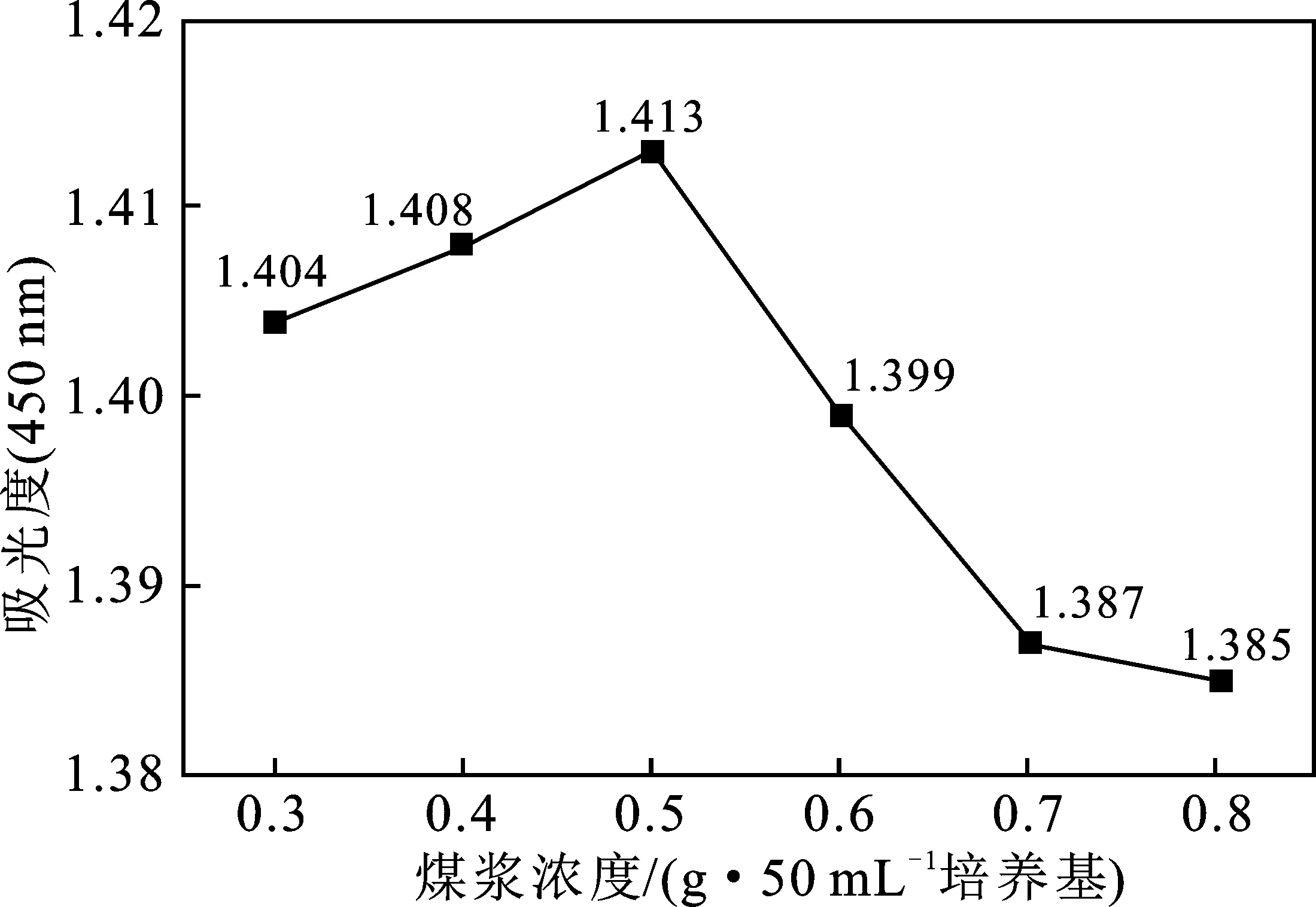
图1 煤浆浓度对降解效果的影响Fig.1 Effect of concentration of coal slurry on coal biodegradation
2.2.2 菌液用量对降解效果的影响 由图2可知,当菌液用量为7 mL/50 mL培养基时,吸光度A450值最大为0.941,此后继续增加菌液用量,降解效果变化不大。由此可见,当菌液用量小于7 mL/50 mL培养基时,友好戈登氏菌对生物降解效果有显著的影响,当菌液用量大于7 mL/50 mL培养基时,菌液用量对生物降解效果的影响不再显著。分析原因,细菌受到生长环境的限制,当细菌个数到达一定数量时,继续增加菌液用量,细菌数量不能再增加,所以生物降解效果也不能继续增强。
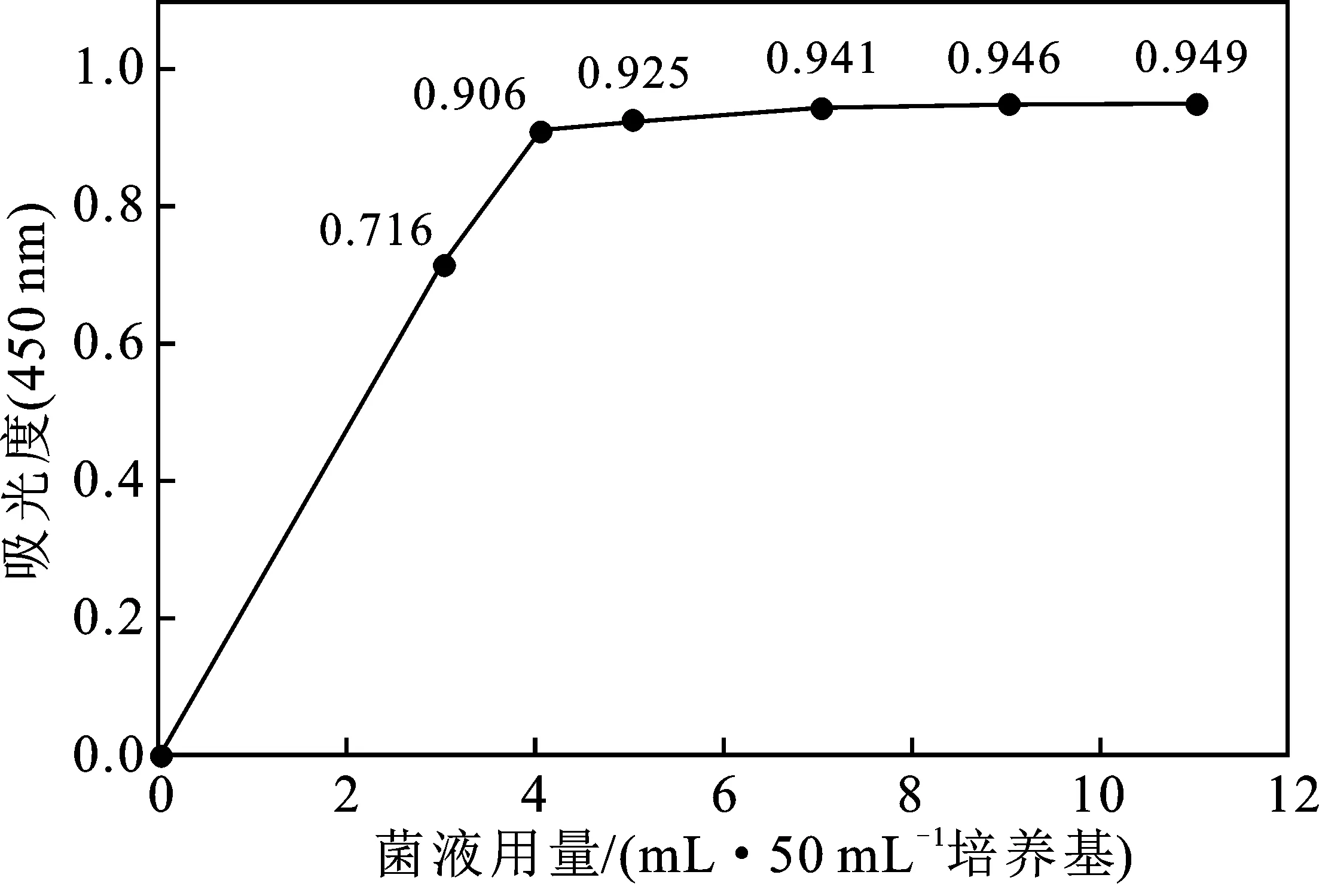
图2 菌液用量对降解效果的影响Fig.2 Effect of inoculum amount on coal biodegradation
2.2.3 降解时间对降解效果的影响 由图3可知,降解时间对降解效果的影响分为2个阶段,分别是快速降解期和平稳期。当降解时间小于21 d时,降解效果受时间的影响比较明显。当降解时间超出21 d时,降解时间对降解效果的影响较小,说明友好戈登氏菌对白音华氧化煤降解达到最大值。分析原因可能是当降解时间增加到21 d以后,培养基中的营养成分已经被微生物消耗殆尽,菌种死亡。最佳降解时间为21 d。
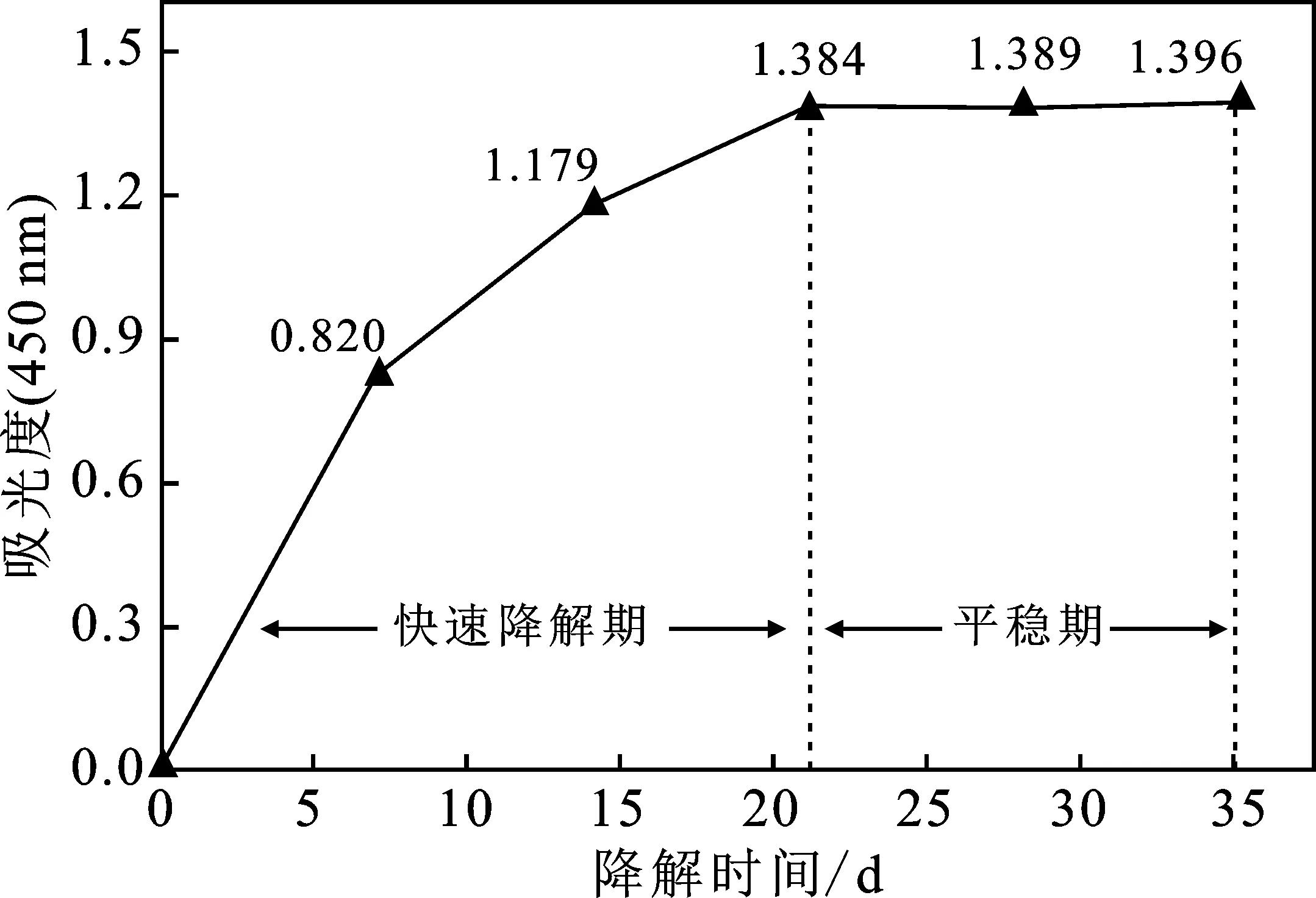
图3 降解时间对降解效果的影响Fig.3 Effect of degradation time on coal biodegradation
2.2.4 培养方式对降解效果的影响 由图4可知,摇床培养的吸光度明显高于水浴培养和静置培养,因此,选择摇床培养为最佳培养方式。分析原因,其一是摇瓶培养能够增加培养基的溶氧率,提高细菌活性,促进煤的微生物降解;其二是摇瓶培养能够使白音华氧化煤与降解活性物质充分接触,从而获得摇瓶培养降解效果高于静置培养。
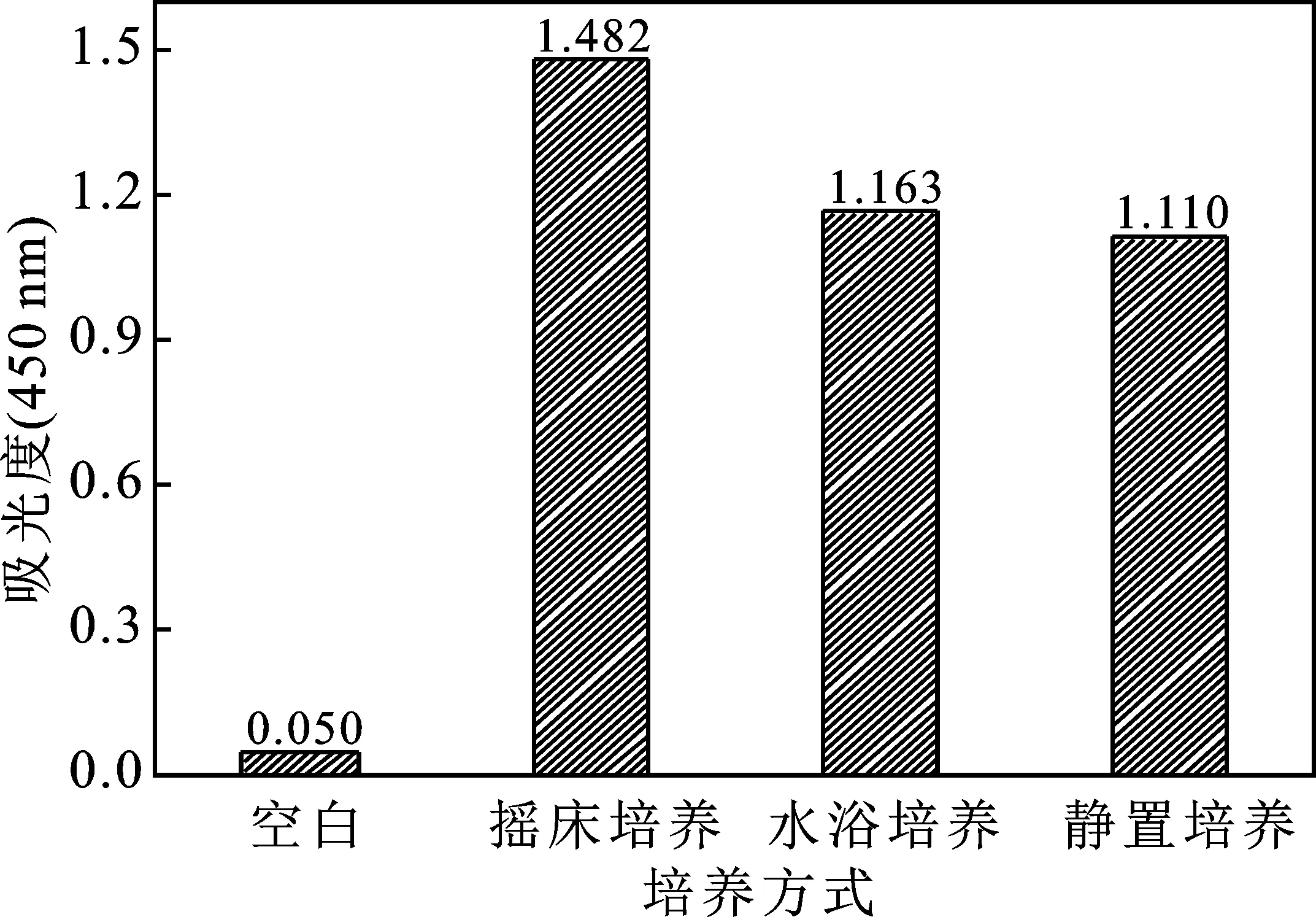
图4 培养方式对降解效果的影响Fig.4 Effect of cultivation ways on coal biodegradation
2.2.5 正交实验 在单因素分析基础上,通过正交实验得出最佳工艺条件。正交实验的因素与水平见表2,选择摇床培养方式,进行煤的微生物降解实验,结果见表3。
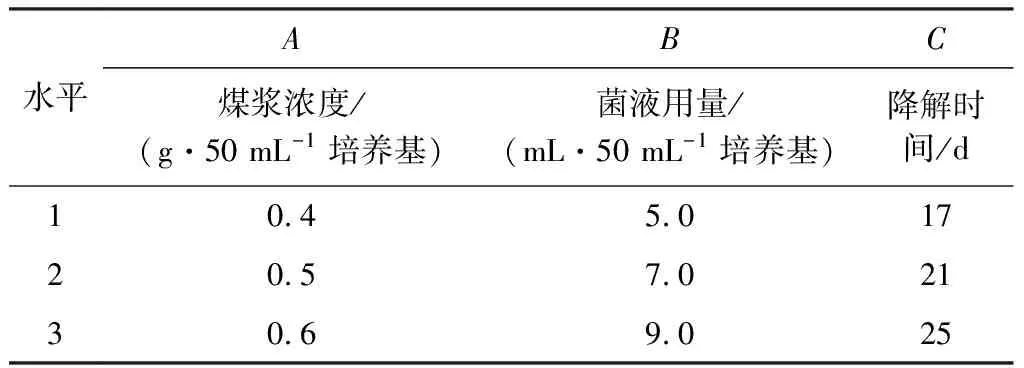
表2 正交实验的因素与水平Table 2 Factors and levels of the orthogonal experiments
由表3可知,3个因素对微生物降解效果影响的权重大小为A>C>B,即煤浆浓度对降解效果影响最大,降解时间次之,菌液用量影响最小。煤浆浓度对微生物降解效果影响最大可能原因是,当其它条件一定时,煤浆浓度越大时,菌种的生长容易受到抑制,微生物分泌的活性物质降低,导致降解效果降低。最佳工艺条件为A3B3C2,即煤浆浓度为0.6 g/50 mL,菌液用量为9 mL/50 mL培养基,降解时间为21 d,此时降解效果最好,A450值为1.555,降解率为57%。
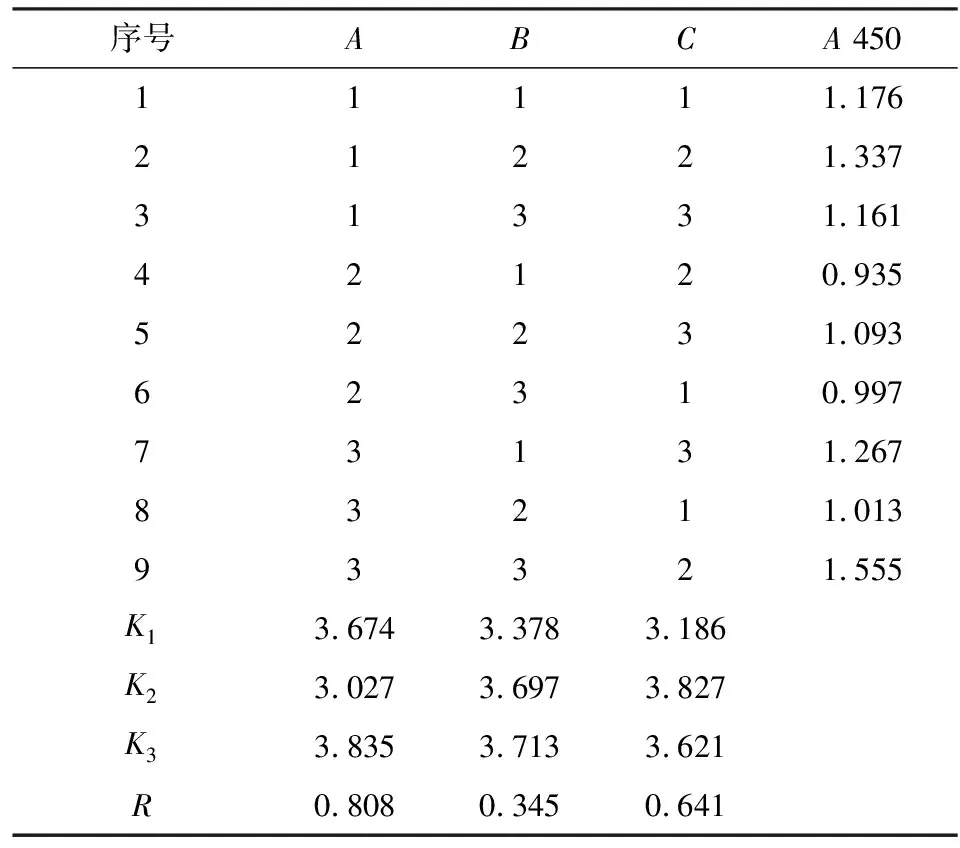
表3 友好戈登氏菌降解白音华 氧化煤的正交实验结果Table 3 Orthogonal experiment results of Baiyinhua oxidized coal degradation by Gordonia amicalis
2.3 产物分析
2.3.1 FTIR分析 图5为原煤、氧化煤与固相产物(剩煤)的红外光谱。
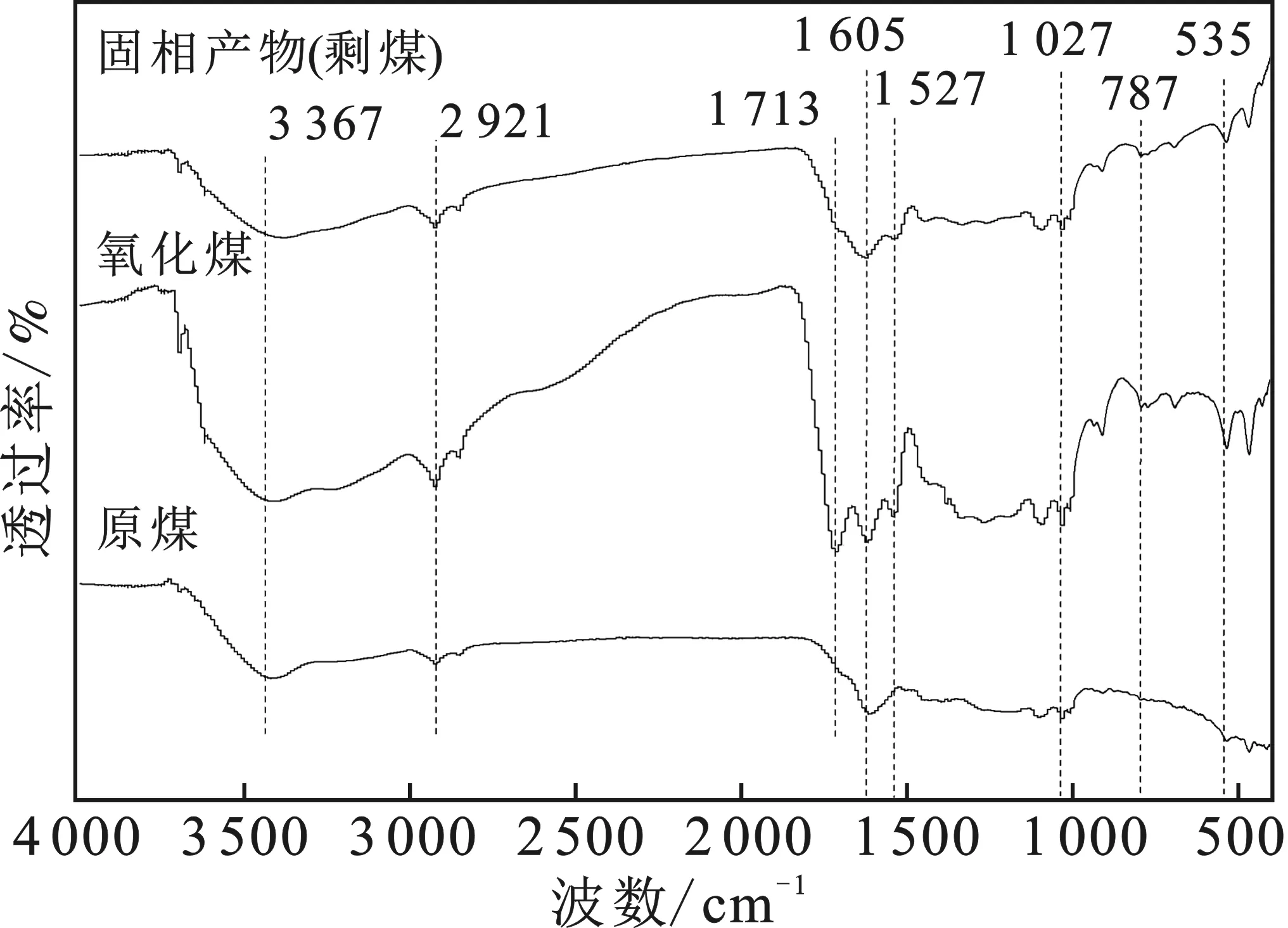
图5 不同煤样的红外光谱图Fig.5 Infrared spectra of different coal samples

2.3.2 TG-DTG分析 图6~图8为原煤、氧化煤和固相产物(剩煤)的热重曲线。
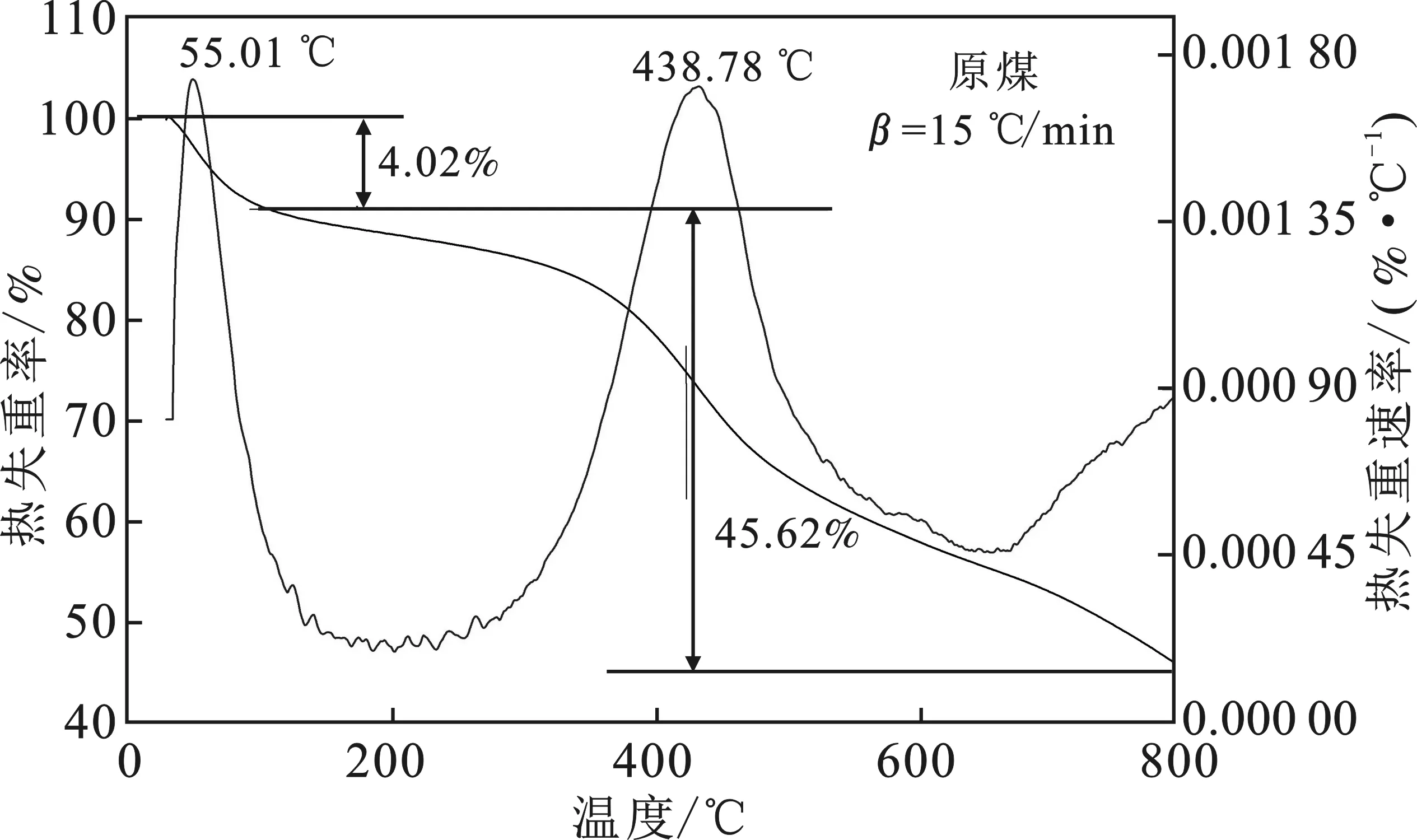
图6 原煤的热重曲线Fig.6 TG-DTG curves of raw coal
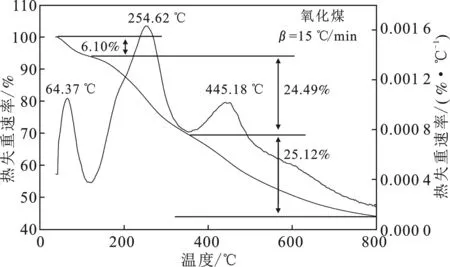
图7 氧化煤的热重曲线图Fig.7 TG-DTG curves of oxidized coal
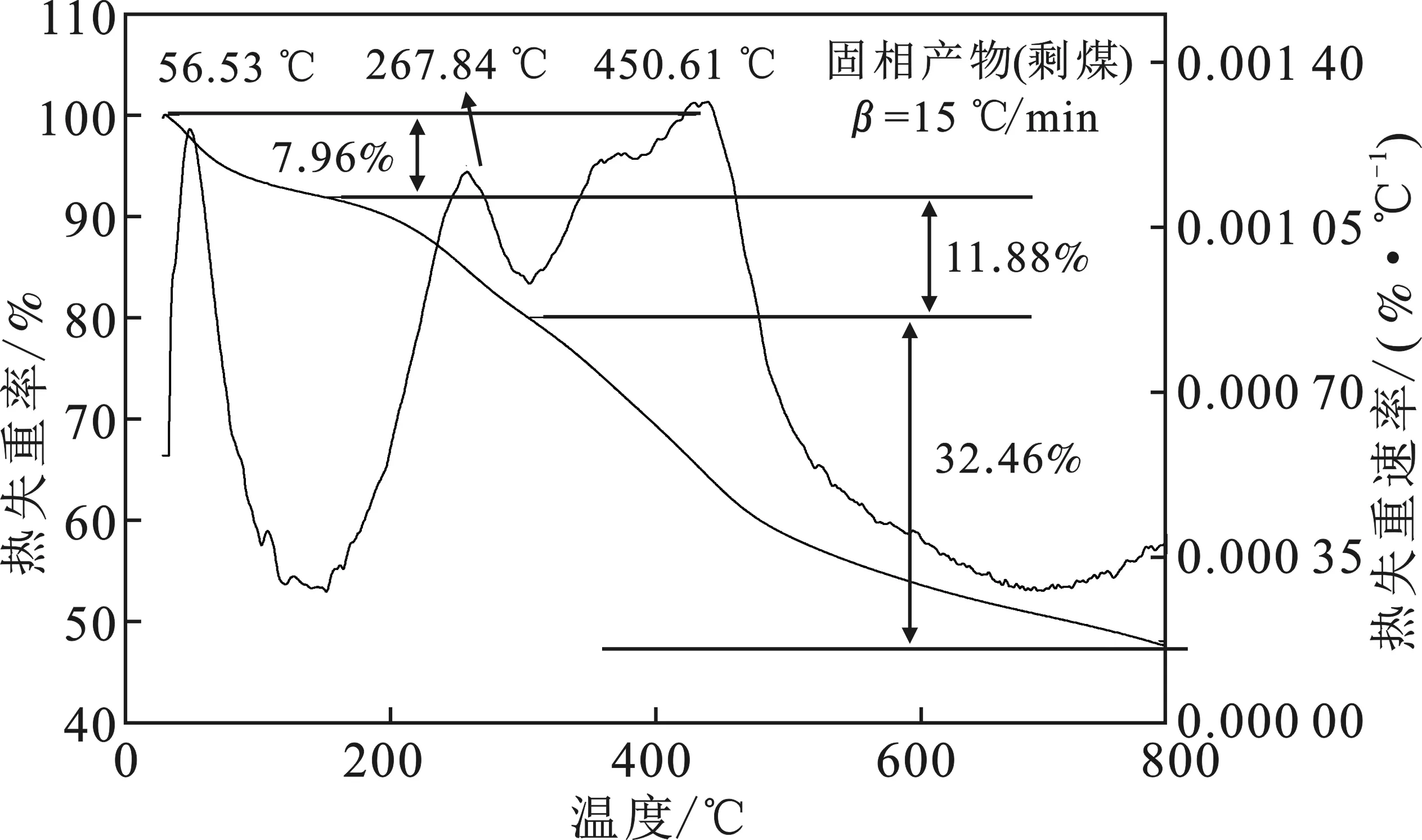
图8 固相产物(剩煤)的热重曲线图Fig.8 TG-DTG curves of residual coal
由图6~图8可知,原煤有两个失重阶段,而氧化煤和固相产物(剩煤)有3个失重阶段。3种煤样的第1个失重阶段相似,温度范围为30~150 ℃,主要是吸附水和吸附气体(CH4、CO2、N2)的脱除,在30~100 ℃之间主要是以物理吸附为主的体相水和毛细水(煤颗粒表面和大孔中的水分)的脱除,在100~150 ℃之间主要是脱除多层水和单层水(吸附或凝聚在煤颗粒内部的中孔或微孔中的水分)。原煤的第2失重阶段的温度范围为151~800 ℃,该阶段主要是煤的软化熔融和热分解阶段,氧化煤和固相产物(剩煤)的第2热分解阶段的温度范围为150~400 ℃,该阶段主要是煤的软化熔融[21]。氧化煤和残煤的第3失重阶段温度范围为401~800 ℃,该阶段是主要的热分解阶段,发生了剧烈的化学反应,煤的物理、化学结构发生破坏,大量挥发分气体析出(气态烃、CO2和CO),并有焦油产生,煤变成半焦[22]。
硝酸氧化后,氧化煤的第2段失重阶段的温度降低,原煤、氧化煤和固相产物(剩煤)的热失重率由大到小的顺序为氧化煤>固相产物(剩煤)>原煤,热稳定性为原煤>固相产物(剩煤)>氧化煤。结果表明,经硝酸氧化后的煤样结构变得松散,热稳定性降低。与氧化煤相比,固相产物(剩煤)的第2阶段(TP2)和第3阶段(TP3)的热失重峰温值均升高,说明细菌降解了氧化煤中结构较松散的部分,煤样的热稳定性提高。
2.3.3 XRD分析 图9为原煤、氧化煤和固相产物(剩煤)的XRD图,表4为3种煤样的XRD晶格参数。
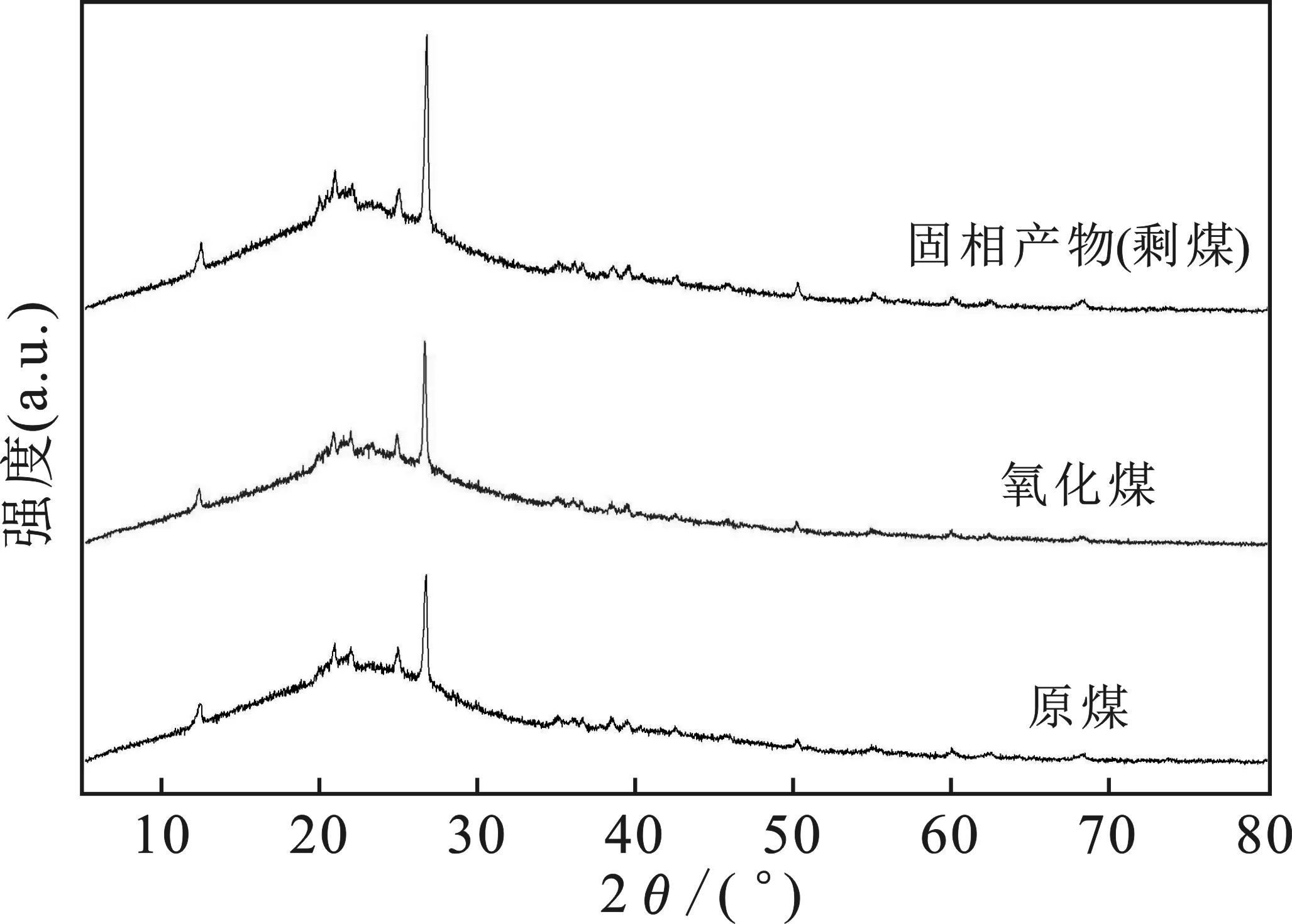
图9 不同煤样的XRD图谱Fig.9 XRD of different coal samples
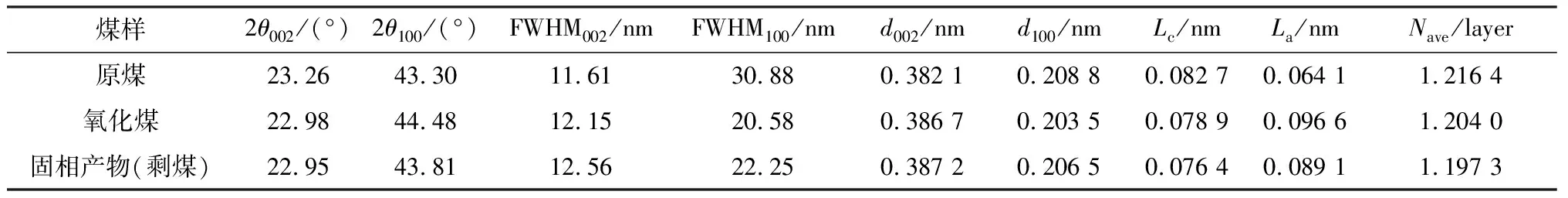
表4 不同煤样的XRD晶格参数Table 4 XRD lattice parameters of different coal samples
由图9可知,原煤、氧化煤和固相产物(剩煤)的XRD谱峰相似,峰型变化呈现一定的规律性。由于褐煤中芳香层片间是以交联键连接,并且在任意方向均可取向。因此,造成了褐煤的多孔立体结构。由表4可知,煤样的芳香层间距d002呈现增加趋势,微晶高度Lc和芳香层数Nave呈现减小的趋势,而微晶直径La在进行硝酸处理后有所上升,微生物降解后又逐渐下降。
硝酸氧化后使得白音华原煤大分子结构遭到破坏,空间的排列逐渐变得不规则,煤中的芳香环打开,在断开处引入羧基、羟基和氨基等基团,并且在空间形成立体结构,这些三维立体结构的间距要比芳香环的键间距大,因此,导致芳香层间距d002增加,微晶高度Lc和芳香层数Nave减小[23]。
微生物降解后,使得氧化煤中的芳香层片数和堆砌高度减少,表明微生物对白音华氧化煤有较好的降解效果,分析原因可能是微生物分泌出来的活性物质降解了氧化煤中的芳香环、脂肪族物质和侧链烷烃,使氧化煤大分子排列更加疏松[24-25],增加了煤大分子重构的可能性,在空间上降低了芳香层堆叠的数量,减少了芳香层之间的垂直距离,从而使芳香层间距d002增加,微晶直径La,微晶高度Lc和芳香层数Nave减小,也进一步说明固相产物(剩煤)稳定性更高这与热重分析结果一致。
2.3.4 GC-MS分析 液相产物分别用四氯化碳、苯、丙酮和甲醇进行萃取,总离子色谱依次见图10~图13,降解液相产物中有机化合物的组成见表5。
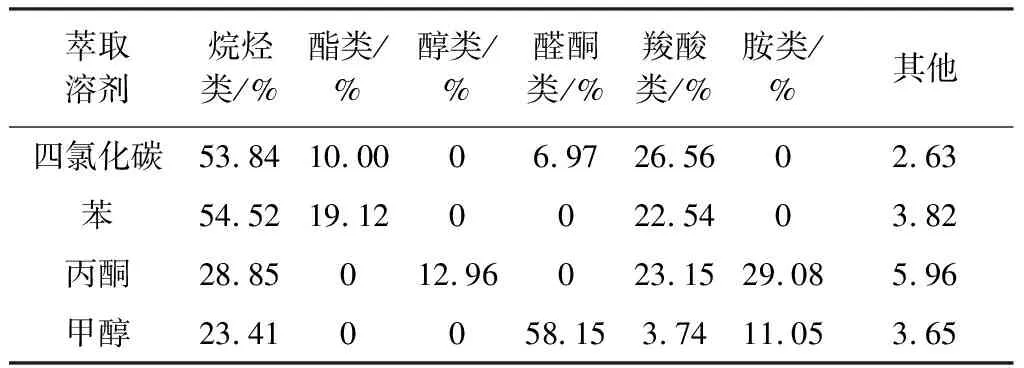
表5 降解液相产物中有机化合物的组成Table 5 Compositions of organic compounds in the biodegradation liquid products
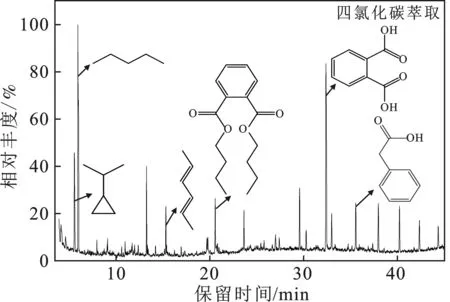
图10 四氯化碳萃取液相产物总离子色谱图Fig.10 Total ion chromatograms of the liquid products extracted by carbon tetrachloride
由图10可知,四氯化碳萃取液相产物总共检测到45种化合物,相对分子量在72~278。其中烷烃类含量为56.47%,羧酸类含量为26.56%,酯类含量为10.00%,醛酮类含量为6.97%。四氯化碳的萃取物中主要含有烷烃类物质。
由图11可知,苯萃取液相产物总共检测出16种化合物,相对分子量在96~266。其中烷烃类含量为54.52%,羧酸类含量为22.54%,酯类含量为19.12%,萃取物中主要含有烷烃类物质。
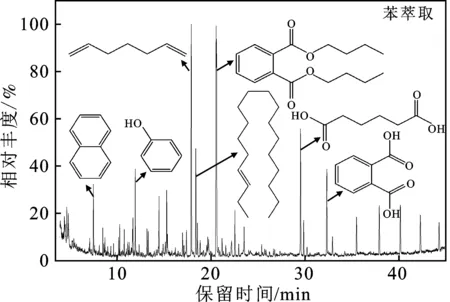
图11 苯萃取液相产物总离子色谱图Fig.11 Total ion chromatograms of the liquid products extracted by benzene
由图12可知,丙酮萃取液相产物总共检测到74种化合物,相对分子量在100~298。其中胺类含量为29.08%,烷烃类含量为28.85%,羧酸类含量为23.15%,醇类为12.96%。
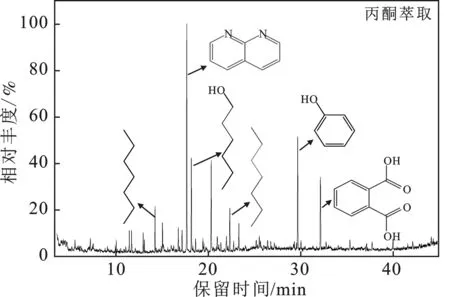
图12 丙酮萃取降解产物总离子色谱图Fig.12 Total ion chromatograms of the liquid products extracted by acetone
由图13可知,甲醇萃取液相产物总共检测出36种化合物,相对分子量在73~367。其中醛酮类含量为61.80%,烷烃类含量为23.41%,胺类含量为11.05%,羧酸类含量为3.74%。综上所述,友好戈登氏菌对白音华氧化煤的降解产物中主要含有烷烃类、羧酸类、醛酮类、胺类、酯类和醇类等小分子物质,其相对分子量在70~370。
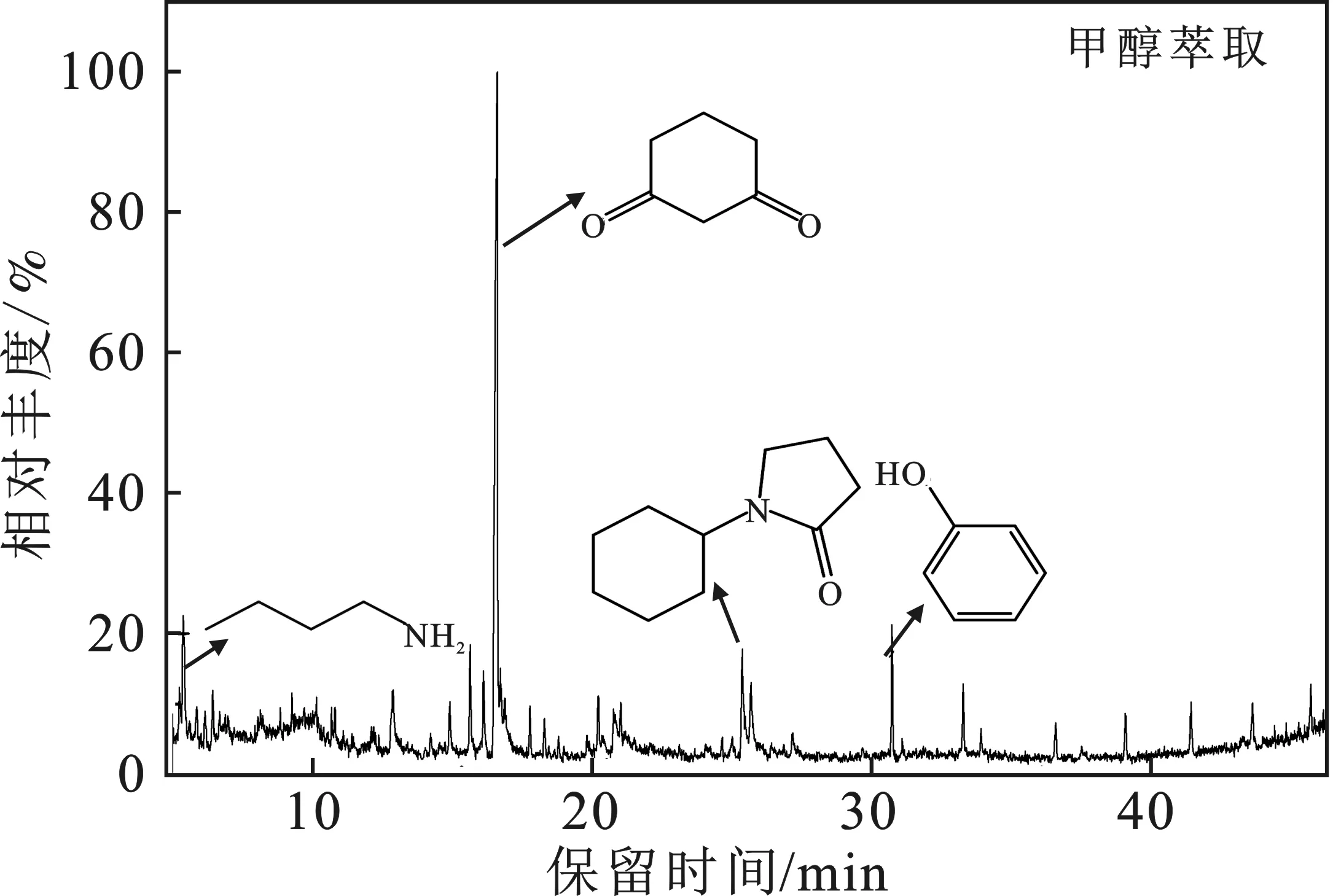
图13 甲醇萃取液相产物总离子色谱图Fig.13 Total ion chromatograms of the liquid products extracted by methanol
3 结论
(1)友好戈登氏菌降解内蒙古白音华褐煤的最佳工艺条件为:煤浆浓度0.6 g/50 mL培养基,菌液用量9 mL/50 mL培养基,降解时间21 d,培养方式为摇床培养,此时降解率最高为57%。影响微生物降解效果的顺序为煤浆浓度>降解时间>菌液用量。
(2) 硝酸处理后,氧化煤中羧基和硝基振动峰增加,芳香环的骨架振动减弱,芳香层间距增加,微晶高度和芳香层数减小,热稳定性降低,热解活性增加,更有利于生物降解。
(3) 微生物降解后,固相产物(剩煤)中芳香环、脂肪烃、羰基、醚键和硝基的吸收峰减弱甚至是消失,芳香层间距增加,微晶直径,微晶高度和芳香层数减小,热稳定性增加,热解活性减弱,说明友好戈登氏菌破坏了白音华氧化煤的大分子结构。
(4) 微生物降解液相产物中含有烷烃类、酯类、醇类、醛酮类、羧酸类和胺类等小分子物质,相对分子量在70~370。

