两例相同混合配体构筑的Pb(Ⅱ)/Ag(I)配位聚合物及其荧光性质
刘 朋,陈洪霞
(1.苏州大学分析测试中心,苏州 215123;2.苏州华源控股股份有限公司,苏州 215000; 3.苏州大学实验室与设备管理处,苏州 215021)
0 引 言
过去的几十年里,金属配位聚合物不仅具有丰富的拓扑结构,而且在光学、吸附、分离、磁性、催化等方面具有潜在的应用价值,所以设计和合成结构新颖的配位聚合物受到了越来越多的关注[1-8]。构建多维的配位聚合物受到很多因素的影响,例如中心金属离子、有机配体、抗衡阴离子、反应体系的pH值、溶剂以及反应的温度等[9-13]。而采用多齿的有机配体,是获得多维框架的配位聚合物的最有效的方法之一。虽然N、O配体是构建配位聚合物常用的配体,但是很少有采用既含有咪唑和羧酸的配体来构建配位聚合物的研究。由于它们是一个柔性和构象多变的配体,很难预测它们的配位方式。一些研究表明,2-咪唑乙酸(Hima)作为柔性的多功能配体,与传统的刚性配体相比,有着鲜明的特点。Hima在不同的条件下,有三种存在形式:第一种是脱质子的ima-,第二种是中性分子Hima,最后一种是两性离子imaH (见图1和图2)。阴离子ima-是构建配位聚合物的很好的桥联配体,因为它可以在金属与金属之间作为一个不对称的桥,而且它还可以作为一个螯合的阴离子参加配位来增强配位聚合物的稳定性。例如:[Ag(ima)]n(2D framework)和[M(ima)2]n(M=Cd,Zn[14], Mn, Ni, Cu[15]),从这些报道的配位聚合物中可见,Hima不仅是一个桥联配体,还是一个多齿的功能配体。Hima可以与金属有很多种不同的配位方式(见图2)[14-17]。
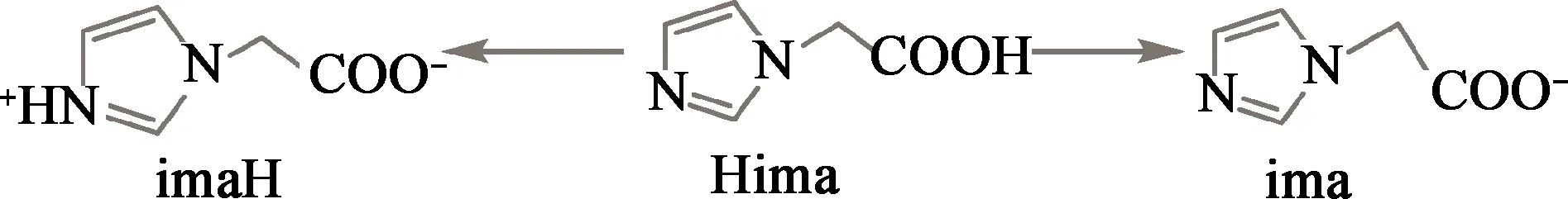
图1 2-咪唑羧酸(Hima)三种存在形式Fig.1 Three forms of Hima

图2 2-咪唑羧酸(Hima)的配位方式Fig.2 Coordination modes of Hima
人们研究发现不仅阴离子在构筑配位聚合物结构的过程中起了很重要的作用,第二配体的作用也不容忽视。第二配体是构筑多维的金属配位聚合物的有效的方法之一。用4, 4’-连吡啶作为第二配体来构筑配位聚合物结构已有很多的报道[17-18]。
为此,在体系中引入盐酸使配体Hima变成2-咪唑乙酸盐酸盐来研究Cl离子对配体Hima与金属配位的影响。并使用中性配体4, 4’-连吡啶作为第二配体来改变配位聚合物的结构。
1 实 验
1.1 试剂和仪器
所有化学药品和试剂均在试剂公司购买,未做进一步处理。红外光谱在Varian 1000 FT-IR光谱仪上用KBr压片测定 (4 000~400 cm-1)。元素分析C、H和N的含量在Carlo-Erba CHNO-S元素分析仪上测得。晶体结构Rigaku Merruy CCD上直接收集数据:石墨单色器,Mo Kα射线,ω-2θ自动变速扫描方式收集衍射数据,采用傅里叶技术、重原子法解析晶体结构。PXRD在PANalytical X’Pert PRO MPD (PW3040/60)X-射线多晶衍射仪测得。TGA是在TA instrument Dynamic TGA 2950上测定,在氮气气流为50 mL·min-1的氛围下以10 ℃·min-1的速度加热。荧光发射光谱是在美国Edinburgh 920 Analytical Instruments上测定,以Xe灯作光源,激发和发射狭缝宽均为5 nm。
1.2 实验方法
1.2.1 配位聚合物[Pb2(4, 4’-bipy)(ima)(NO3)3]n(1)的合成
配位聚合物1是通过水热合成的。将Pb(NO3)2(17 mg, 0.1 mmol)、Hima(6.3 mg, 0.05 mmol)和四滴4, 4’-连吡啶的乙醇溶液加入到容积为10 mL的硬质玻璃管中并封管。玻璃管随后放入烘箱,在140 ℃条件下反应1 d后以5 ℃/h速率缓慢降温。烘箱温度降至室温后得到无色块状晶体1并用EtOH洗涤。收率:50%。
元素分析(%):C15H13N7O11Pb2,理论值:C, 20.42; H, 1.47; N, 11.11;实验值:C, 20.50; H, 1.52; N, 10.99。红外光谱(KBr压片, cm-1):3 441(b), 3 126(w), 1 954(w), 1 589(m), 1 563(s), 1 410(w), 1 384(s), 1 215(w), 1 088(m), 1 071(w), 1 000(w), 921(w), 810(m), 684(m)。
1.2.2 配位聚合物[Ag4(4, 4’-bipy)3(ima)2(NO3)2(H2O)2]n(2)的合成
配位聚合物2也是通过水热合成,方法同1.2.1小节相同。用AgNO3(34.0 mg, 0.2 mmol)、Hima (12.6 mg, 0.1 mmol)和四滴4, 4’-连吡啶的乙醇溶液。水热冷却到室温析出无色晶体。收率:48%。
元素分析(%):C40H38Ag4N12O12,理论值:C, 36.63; H, 2.90; N, 12.82。实验值:C, 20.88; H, 1.80; N, 14.39。红外光谱(KBr压片,cm-1):3 437(b), 3 136(m), 2 373(w), 1 603(s), 1 402(w), 1 382(s), 1 366(s), 1 311(s), 1 210(w), 1 148(m), 1 084(m), 1 022(w), 972(w), 805(m), 749(m), 687(m), 638(m)。
1.2.3 晶体结构的测定


表1 配位聚合物1和2的晶体学参数Table 1 Crystallographic data for compounds 1 and 2

表2 配位聚合物1和2的部分键长和键角Table 2 Selected bond lengths and bond angles of compounds 1 and 2

续表
配位聚合物1的对称操作: #1:x+1/2,y-1/2,z; #2: -x+2,y, -z+3/2; #3:x-1/2,y+1/2,z; #4: -x+3/2, -y+1/2, -z+1; #5: -x+1, -y+1, -z+1;配位聚合物2的对称操作:#1:x,y,z-1; #2: -x+1, -y, -z+1; #3: -x, -y, -z+2; #4:x,y,z+1; #5: -x+1, -y, -z+2。
2 结果与讨论
2.1 光谱分析
配位聚合物1和2对空气和水稳定,均不溶于常规的有机溶剂。通过分析,这两个化合物的元素分析与它们的化学分子式相符。在这两个配位聚合物中,红外光谱中羧酸基的不对称振动分别在:1 589 cm-1(1),1 603 cm-1(2)。红外光谱中羧基的对称振动分别在:1 384 cm-1(1),1 382 cm-1(2)。红外光谱中,羧基分别有2个不同的特征峰,说明这两种羧酸的配位模式不一样,该结果和它们的晶体结构一致。
2.2 晶体结构
2.2.1 配位聚合物[Pb2(4, 4’-bipy)(ima)(NO3)3]n(1)的晶体结构
在配位聚合物1中,Pb1是一个7配位的几何构型,分别与来自两个硝酸根上的两个氧原子、一个来自4, 4’-连吡啶分子中的N原子、一个ima-上的两个氧原子,以及来自另外一个ima-上的一个氧原子,还有来自ima-中的咪唑环上的N原子配位。Pb2是一个8配位的几何构型,分别与来自三个硝酸根上的六个氧原子,第二配体4, 4’-连吡啶分子中的N原子,以及与一个来自ima-上的氧原子配位(见图3(a))。沿着bc平

图3 (a)配位聚合物1中Pb的配位环境(#1: x+1/2, y-1/2, z;#2: -x+2, y, -z+3/2; #3: x-1/2, y+1/2, z; #4: -x+3/2, -y+1/2, -z+1; #5: -x+1, -y+1, -z+1。 氢原子省略);(b)沿着bc面铅原子周围 配位环境(氢原子省略);(c)沿着bc面的三维结构(氢原子省略)Fig.3 (a) Local coordination environments of Pb in compound 1 (#1: x+1/2, y-1/2, z;#2: -x+2, y, -z+3/2; #3: x-1/2, y+1/2, z; #4: -x+3/2, -y+1/2, -z+1; #5: -x+1, -y+1, -z+1. H atoms atoms were omitted for clarity); (b) local coordination environments of Pb in compound 1 along bc plane (H atoms were omitted for clarity); (c) perspective view of the 3D framework along bc plane (H atoms were omitted for clarity)
面看,相邻的两个Pb1之间通过两个氧桥相连,这两个氧桥都是ima-上的羧基中的两个氧原子作为一个螯合桥。第二配体4, 4’-连吡啶与Pb1配位后通过ima-上的氧桥相连接,形成相互平行的一个平面。Pb1和Pb2成蛇形依次间隔形成一条线连接相邻的两个平面,从而使整个分子形成一个3D的几何构型(见图3(b))。

2.2.2 配位聚合物[Ag4(4, 4’-bipy)3(ima)2(NO3)2(H2O)2]n(2)的晶体结构
单晶结构显示:配位聚合物2是一个3D的结构。在配位聚合物2里面,Ag1是三配位,可以描述为一个扭曲的三角形,分别与来自两个不同的4, 4’-连吡啶上的N原子,以及来自ima-中羧基上的一个氧原子配位。Ag2是两配位,只与来自两个不同的4, 4’-连吡啶上的N原子配位。Ag1和Ag2以及长出来的Ag1’在一条直线上,Ag(1)-Ag(2)-Ag(1)#2之间的夹角为180°。Ag1与第二配体4, 4’-连吡啶上配位的N原子之间的平均键长为0.218 7(3) nm,Ag2与4, 4’-连吡啶上配位的N原子之间的平均键长为0.216 3(3) nm。Ag1和Ag2之间的距离为0.332 92(4)nm,表明金属之间存在着相互作用,这种作用是不可忽略的。Ag3是二配位的,与两个ima-中咪唑环上的N原子配位。N(2’)-Ag(3)-N(2)的键角为180°,表明Ag3是直线的几何构型(见图4(a))。
在配位聚合物2里,ima-是一个双阴离子,在里面显-1价,分子之间通过配体ima-沿着ab平面相互连接形成zigzag聚合物链(见图4(b))。链与链之间通过4, 4’-连吡啶分子相互连接沿着c轴形成三维的超分子结构(见图4(b))。
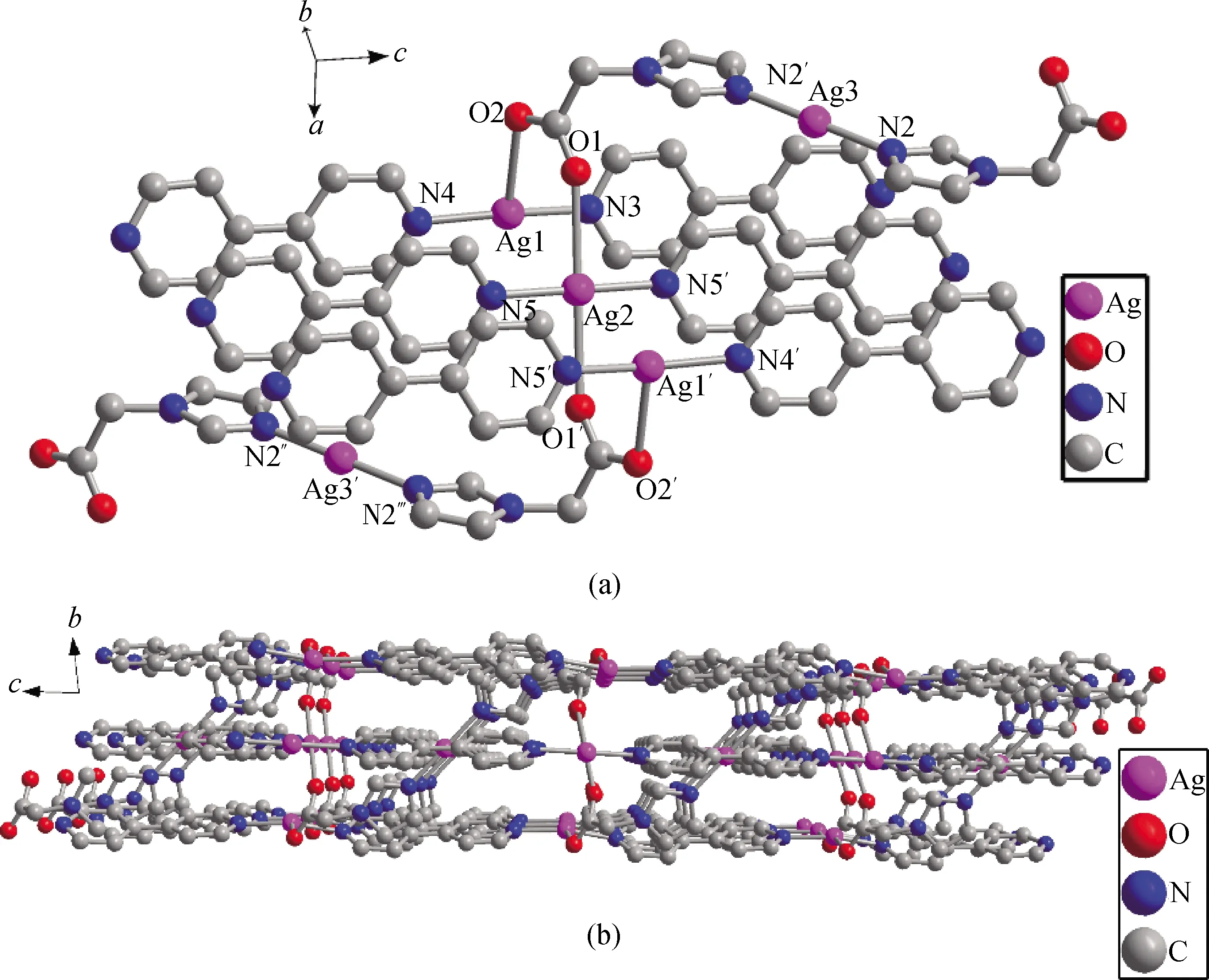
图4 (a)配位聚合物2中金属银原子配位环境(#1: x, y, z-1; #2: -x+1, -y, -z+1; #3: -x, -y, -z+2; #4: x, y, z+1; #5: -x+1, -y, -z+2。 氢原子省略);(b)配位聚合物2中沿着稍微偏离b轴的ac面银离子的配位环境(氢原子省略)Fig.4 (a) Local coordination environments of Ag in compound 2 (#1: x, y, z-1; #2: -x+1, -y, -z+1; #3: -x, -y, -z+2; #4: x, y, z+1; #5: -x+1, -y, -z+2. H atoms were omitted for clarity); (b) local coordination environments of Ag in compound 2 along ac plane showing slightly off the b-axis (H atoms were omitted for clarity)
2.3 配位聚合物的热稳定性
配位聚合物1的热稳定性很高,在410 ℃之前不分解,在898 ℃时失重完全,最终残留物为PbO, 残重为29.27% (理论值25.31%) (见图5)。
配位聚合物2是逐阶段失重,第一阶段从283~340 ℃,失重4.3%,失去配位聚合物表面带有的溶剂分子,在800 ℃时失重完全,最终残留物为Ag2O,残重为18.6%(理论值17.7%) (见图5)。

图5 配位聚合物1和2的热重分析曲线Fig.5 TGA curves of compounds 1 and 2
2.4 配位聚合物的X射线粉末衍射
粉末衍射(PXRD)分析(见图6)显示,理论模拟的PXRD和实验测得的PXRD是一致的,也证明了粉末状态和单晶状态配位聚合物的存在形式是一样的。

图6 配位聚合物1和2的XRD图谱Fig.6 XRD patterns for compounds 1 and 2
2.5 配位聚合物的荧光性质
对这两个配位聚合物的固态荧光性质进行了研究。当用346 nm的激发光对配位聚合物1照射时,它的最大发射波长约在552 nm处,即发绿光。对配位聚合物2,用369 nm的激发光照射,它的最大发射波长为444 nm (见图7),4, 4’-连吡啶的发射在486 nm。

图7 配位聚合物1和2在室温下的固态荧光发射谱Fig.7 Solid-state emission spectra of compounds 1 and 2 at room temperature
这两个配位聚合物的荧光可能是源自配体到金属离子的电荷跃迁(LMCT),而红移的程度不一样可能是由于每个配位聚合物中心金属的配位环境不一样[20-21]。
3 结 论
本文以无机盐与有机柔性多官能团配体2-咪唑乙酸(Hima)进行自组装,制备了2个配位聚合物。配位聚合物1和2是三维网状结构。由于中心金属配位能力的不同,配体Hima采用了不同的配位模式与金属配位,第二配体4, 4’-连吡啶以及抗衡阴离子Cl-对构筑配位聚合物的结构有很重要的影响。配位聚合物的结构又影响了它们的荧光性质。荧光可能源自配体到金属离子之间的电荷跃迁(LMCT),而荧光红移的程度不一样可能是由于每个配位聚合物中心金属周围的配位环境不一样。可以相信,通过改变抗衡阴离子以及第二配体的方法将会应用到其他体系中用于合成多种配位聚合物。

