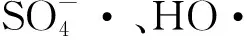Fe(Ⅱ)活化亚硫酸盐降解卡马西平的动力学及机制研究
李阳,关小红,董红钰
(同济大学 环境科学与工程学院,上海 200092)
近年来,随着经济社会的快速发展,人工合成有机化合物的种类每年以惊人的速度增加,在这些有机化合物的生产、运输、使用及废弃过程中,人们的不当行为造成它们进入自然水体,导致大量的水源水受到新型有机污染物(Emerging organic contaminants,EOCs)的污染[1-2]。其中,卡马西平(carbamazepine,CBZ)是一种典型的抗癫痫药物,是水环境中最常见的EOCs之一[3-5]。全世界CBZ的年平均消耗量巨大,高达1 014 t[6],所消耗的CBZ大部分被排放到天然水体中。这些EOCs在水中的浓度低、种类多、性质复杂,传统的污水处理工艺及常规饮用水处理工艺难以将其去除。因此,为保障水环境安全,高级氧化技术越来越多地被引入到水污染物控制工艺中[7-8]。
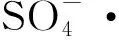
笔者以CBZ为目标污染物,考察不同亚硫酸盐浓度、Fe(Ⅱ)浓度和初始pH值条件下Fe(Ⅱ)/亚硫酸盐体系降解卡马西平的动力学,并采用电子顺磁共振光谱(EPR)检测和醇类(甲醇和叔丁醇)淬灭实验鉴定此体系中活性氧化物种的产生,以更加深入地理解Fe(Ⅱ)/亚硫酸盐体系的作用机制,为此体系在EOCs处理方面提供理论支撑。
1 材料与方法
1.1 材料和仪器
1.1.1 主要材料 七水合硫酸亚铁(分析纯)、甲酸(色谱纯)和乙腈(色谱纯)购于阿拉丁生物科技有限公司。亚硫酸钠、CBZ、叔丁醇、甲醇、氢氧化钠(NaOH)、硫酸(H2SO4)、氯化钠、氯化亚铁和硫代硫酸钠均为分析纯,购于国药集团化学试剂有限公司。5,5-二甲基-1-吡咯啉-N-氧化物(DMPO、GC)购于同仁化学研究所。实验过程中,所有药品均未进行进一步纯化,并采用电阻率为18.2 MΩ·cm的Milli-Q超纯水配制储备溶液。
1.1.2 主要仪器 雷磁pH计(PHS-3C,上海精密科学仪器有限公司);超高效液相色谱仪(ACQUITY UPLC H-Class,美国waters公司);电子顺磁共振波谱仪(EMX plus 10/12,德国布鲁克公司);磁力搅拌器(78型,常州国华实验仪器厂);电子分析天平(T-214,Denver instrument factory);超纯水制备系统(Milli-Q Reference A+System,美国Millipore公司)。
1.2 实验方法
实验在室温、容量为250 mL的敞口烧杯中进行。主要步骤为:先将Fe(Ⅱ)与CBZ混合物配制成100 mL的溶液,使用H2SO4或NaOH调节溶液pH值至特定值,加入一定体积的亚硫酸钠(亚硫酸钠母液pH值已被调节至相同的pH值),立即计时,并在既定的时刻取样,将样品直接加入烧杯中,烧杯中已经提前加入100 μL硫代硫酸钠作为淬灭剂,然后将完全淬灭的样品用0.22 μm的醋酸纤维滤膜进行过滤,使用超高效液相色谱法测定CBZ的浓度。
为确保实验数据的可信性,所有实验均进行了平行实验。
1.3 分析方法
采用配有紫外-可见光检测器的超高效液相色谱仪(UPLC)测定CBZ的浓度。该UPLC使用BEH C18柱(2.1 mm×100 mm,1.7 μm),柱温(35±1)℃。在检测CBZ过程中,所使用的流动相种类及比例为水(含有1‰的甲酸)∶乙腈=50∶50,检测波长为286 nm,流速为0.22 mL/min。
采用电子顺磁共振(EPR)波谱仪分析Fe(Ⅱ)/亚硫酸盐体系中自由基种类。首先,在特定pH值条件下将亚硫酸钠溶液与Fe(Ⅱ)溶液混合反应,在相应时刻取样后,将样品立即加入到含有一定量DMPO的1 mL离心管中迅速混合。用毛细石英管吸取液体后,将毛细管放入EPR的谐振腔中进行检测。EPR仪器的运行参数为:中心场强3 350 Gs;扫频宽度100 Gs;波功率1.0 mW;调谐幅度0.30 Gs;扫描时间41.96 s。
2 结果与讨论
2.1 亚硫酸钠浓度和Fe(Ⅱ)浓度对Fe(Ⅱ)/亚硫酸盐体系降解CBZ动力学的影响
图1为初始pH值为3.0时不同亚硫酸钠浓度和Fe(Ⅱ)浓度条件下Fe(Ⅱ)/亚硫酸盐体系降解CBZ的动力学。如图1(a)所示,固定Fe(Ⅱ)浓度为0.10 mmol/L,当亚硫酸钠浓度由0.20 mmol/L增至1.0 mmol/L时,反应时间20 min时,Fe(Ⅱ)/亚硫酸盐体系对CBZ的去除率由65.0%增至76.0%,而当亚硫酸钠的浓度进一步增至1.5 mmol/L时,反应时间20 min时CBZ的去除率降至73.0%。这是因为过量的亚硫酸钠可与CBZ竞争Fe(Ⅱ)/亚硫酸盐体系中所产生的活性氧化物种。由图1(b)可以看出,固定亚硫酸钠浓度为0.50 mmol/L,当Fe(Ⅱ)浓度分别为0.010、0.050、0.10 mmol/L时,反应时间为20 min时,Fe(Ⅱ)/亚硫酸盐体系对CBZ的去除率分别为63.7%、76.4%和74.2%。由此说明,Fe(Ⅱ)/亚硫酸盐体系对CBZ的去除情况与Fe(Ⅱ)浓度有关。需要注意的是,在相同条件下,单独Fe(Ⅱ)、Fe(Ⅲ)或亚硫酸盐对CBZ无降解作用[20]。综上,Fe(Ⅱ)/亚硫酸盐体系对CBZ的降解源于Fe(Ⅱ)与亚硫酸盐反应所产生的活性氧化物种。

图1 亚硫酸钠浓度和Fe(Ⅱ)浓度对Fe(Ⅱ)/亚硫酸盐体系降解CBZ动力学的影响Fig.1 Influence of sodium sulfite concentration and Fe(Ⅱ) concentration on the kinetics of CBZ degradation in the
2.2 初始pH值对Fe(Ⅱ)/亚硫酸盐体系降解CBZ动力学的影响
当初始pH(pHini) >7.0时,Fe(Ⅱ)以Fe(OH)3的形式沉淀下来。当pHini<3.0时, 溶液中的亚硫酸盐主要以亚硫酸的形式存在,其反应活性低于亚硫酸氢根和亚硫酸根。因此,探究pHini为3.0~7.0条件下Fe(Ⅱ)/亚硫酸盐体系降解CBZ的效能。不同初始pH(pHini)条件下Fe(Ⅱ)/亚硫酸盐体系降解CBZ的动力学以及反应过程中溶液pH值的变化情况如图2所示。由图2可以看出,pHini为3.0~7.0条件下,Fe(Ⅱ)/亚硫酸盐体系对CBZ的去除随着反应时间的增加不断增加,到一定的反应时间不再继续增加,达到平衡。相应地,溶液的pH值随着反应时间的增加而不断减小,达到一定的时间逐渐稳定,即Fe(Ⅱ)/亚硫酸盐体系中生成的氢离子浓度逐渐增加,达到一定时间时,氢离子的浓度逐渐稳定。因此,Fe(Ⅱ)/亚硫酸盐体系对CBZ的降解伴随着氢离子浓度的增加,即卡马西平的降解与溶液pH值的降低随时间的变化规律相一致。pHini值对Fe(Ⅱ)/亚硫酸盐体系降解CBZ具有重要影响。当pHini为3.0、4.0及5.0时,Fe(Ⅱ)/亚硫酸盐体系对CBZ的降解均在反应20 min内达到平衡,反应时间为20 min时,Fe(Ⅱ)/亚硫酸盐体系对CBZ的去除率分别74.2%、82.9%和87.3%。pHini为4.0时,CBZ的降解速率高于pHini为3.0和5.0时CBZ的降解速率。然而,当pHini为6.0和7.0时,Fe(Ⅱ)/亚硫酸盐体系对CBZ的降解速率和去除率显著低于初始pH值3.0~5.0时。pHini为6.0时,Fe(Ⅱ)/亚硫酸盐体系对CBZ的降解在反应时间1 h内达到平衡,此时CBZ的去除率为83.9%。pHini为7.0时,Fe(Ⅱ)/亚硫酸盐体系对CBZ的降解在反应时间4.5 h内达到平衡,此时CBZ的去除率仅为19.0%。由此可以看出,酸性条件下Fe(Ⅱ)/亚硫酸盐体系对CBZ具有较好的降解效果。

图2 不同初始pH值时Fe(Ⅱ)/亚硫酸盐体系降解CBZ动力学及反应过程中pH值的变化Fig.2 Kinetics of CBZ degradation and changes in pH during CBZ removal in Fe(Ⅱ)/sulfite system at different
2.3 铁盐中和Cl-对Fe(Ⅱ)/亚硫酸盐体系降解CBZ的影响

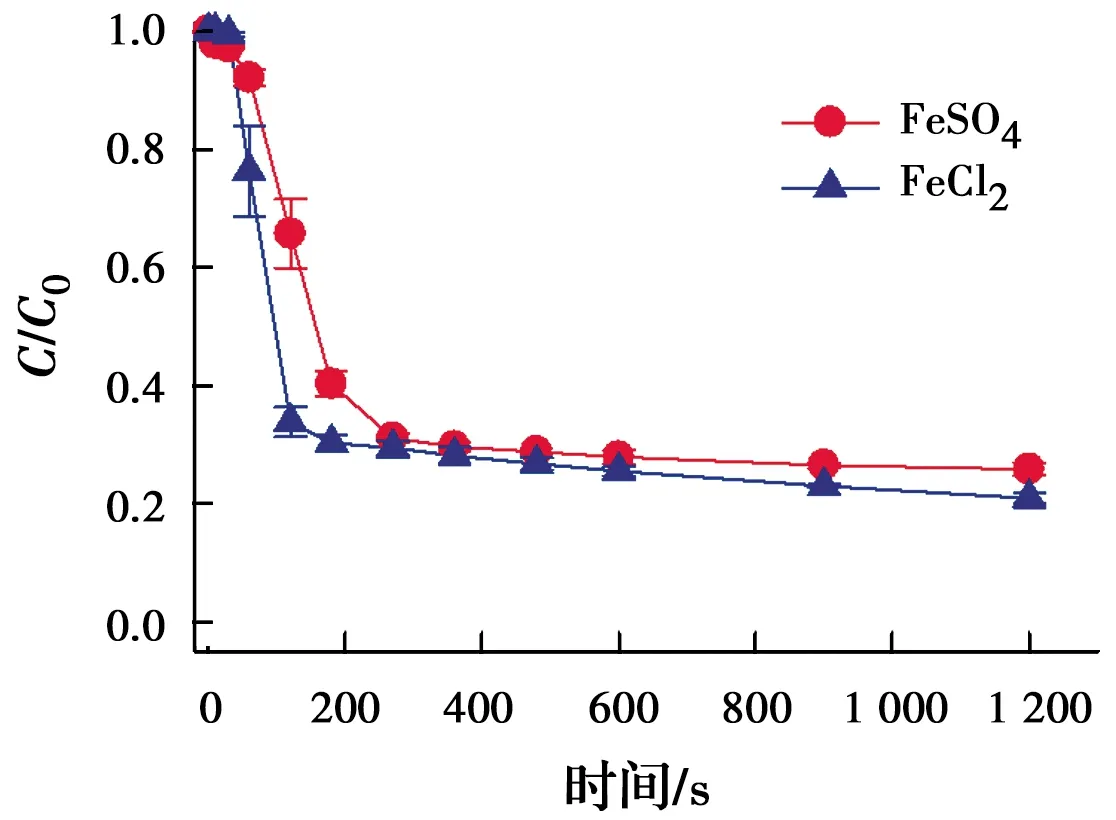
图3 铁盐阴离子对Fe(Ⅱ)/亚硫酸盐体系降解CBZ的影响Fig.3 Effect of anion on the kinetics of CBZ degradation
2.4 Fe(Ⅱ)/亚硫酸盐体系中活性氧化物种的生成情况
为了直接检测Fe(Ⅱ)/亚硫酸盐体系中所产生的自由基,当Fe(Ⅱ)与亚硫酸钠反应270 s时,向反应溶液中加入DMPO后进行检测,EPR谱图如图4所示。Fe(Ⅱ)/亚硫酸盐体系中出现了含有4个特征峰的EPR谱图,其超精细耦合常数为αN=αβ-H=14.8 G,与文献[21]中报道的DMPO-HO·加合物
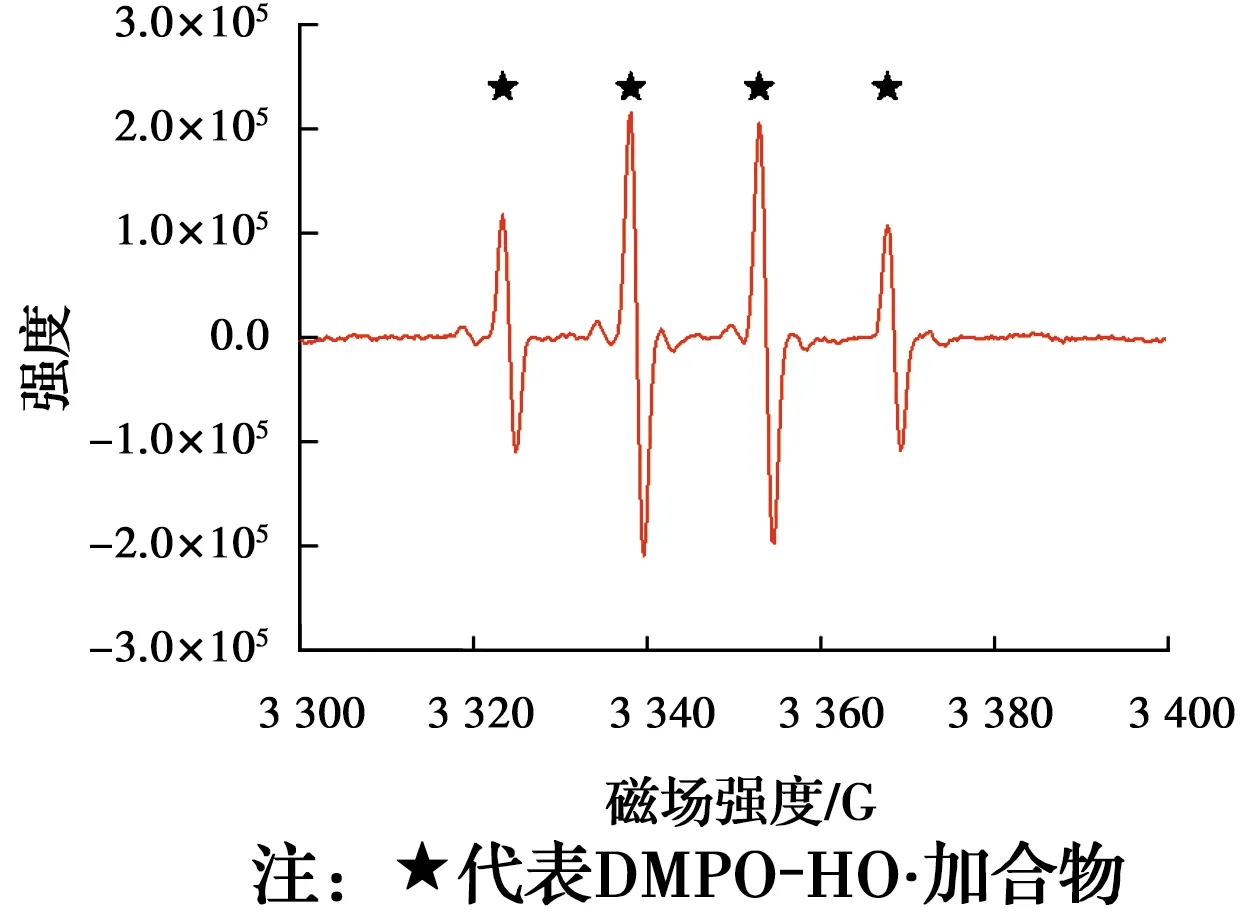
图4 Fe(Ⅱ)/亚硫酸盐体系的EPR谱图Fig.4 EPR spectrum obtained in the Fe(Ⅱ)/sulfite
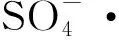
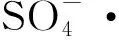
3 结论
根据Fe(Ⅱ)/亚硫酸钠体系中亚硫酸钠浓度和Fe(Ⅱ)浓度、初始pH及铁盐阴离子对CBZ降解动力学的影响及利用EPR检测和淬灭剂实验对Fe(Ⅱ)/亚硫酸钠体系降解CBZ过程中产生的活性氧化物种的分析结果,可得到以下结论:
1)Fe(Ⅱ)/亚硫酸钠体系对CBZ的降解动力学与亚硫酸钠和Fe(Ⅱ)的浓度有关,适量的亚硫酸钠和Fe(Ⅱ)有利于CBZ的去除,而过量的亚硫酸钠会与CBZ竞争Fe(Ⅱ)/亚硫酸盐体系中所产生的活性氧化物种,导致CBZ去除率降低。
2)酸性条件下Fe(Ⅱ)/亚硫酸盐体系对CBZ具有较好的降解效果。pHini为5.0时,反应平衡时Fe(Ⅱ)/亚硫酸盐体系对CBZ的去除率最高。