钒渣加Mg(OH)2焙烧提铬的研究
李 娜,沈少波,张 政,顾金朗,陈元圆
北京科技大学 冶金与生态工程学院,北京100083
钢厂钒渣中通常含有12%~15%的V2O5和 2%~5%的Cr2O3[1-2].传统方法是将Na2CO3-NaCl-Na2SO4混合物粉末添加到钒渣粉中[3],在约800 ℃下将粉样焙烧,然后用热水浸取焙烧产物,使固体中的钒转移到水溶液中,以提取钒渣中的钒[3,5-6],这称之为钠化焙烧法.该方法的铬提取率不高于5%,使得大量有毒致癌的铬元素留在水浸渣中,这些无法处理的含铬水浸渣堆放在环境中对环境带来了极大的潜在危害[4].从环保角度考虑,目前国家对传统钒渣提钒工艺提出改进建议,要求新工艺对钒渣中钒和铬均要充分提取,使得浸出渣中的铬含量尽可能低.此外,传统钒渣提钒工艺的水浸渣中含有高含量的Na元素,这限制了铁含量高的水浸渣入高炉用作铁原料,使得大量水浸渣无法再用.此外,由于钠化焙烧对炉衬腐蚀严重,人们还研究了钒渣加CaO高温焙烧,焙烧样再用硫酸浸取,以提取钒,称为钙化焙烧法[7].钙化焙烧法的酸浸渣中含有大量硫酸根(CaSO4沉淀),这也使得铁含量高的酸浸渣也无法入高炉再用.采用钒渣加MgO高温焙烧,焙烧样再用硫酸浸取,以提取钒,这称为镁化焙烧法[8].由于MgSO4(溶解度为540 g/L)在水中溶解度比CaSO4(溶解度为2 g/L)大得多,镁化焙烧法酸浸渣中硫元素含量极低,这使得此法酸浸渣入高炉再用成为可能.通过热力学计算发现,用Mg(OH)2代替MgO进行钒渣焙烧,铬的提取率有可能更高.因此,研究了用钒渣加Mg(OH)2进行镁化焙烧铬的提取.
1 实验部分
1.1 实验材料
实验所用钒渣由国内某一钢厂提供.钒渣经破碎、干燥、过筛后分粒度包装并储存于干燥器中,供后续实验使用.实验中钒渣样品的粒度为49~74 μm,Mg(OH)2固体粉末(分析纯AR)为国药集团化学试剂,硫酸液体为分析纯.
1.2 铬的提取
将钒渣固定为2.4 g,添加不同质量的Mg(OH)2,碱Mg(OH)2与钒渣质量之比为碱渣比,其比分别为0.2,0.4,0.6,0.8和1.0.
首先将碱与钒渣充分混匀后置于氧化铝坩埚中,然后放入已预热到一定温度的马弗炉中进行焙烧,到了预定时间后将坩埚取出,再室温下冷却.待焙烧后的样品冷却后取出称重,如遇结块将其研磨.经焙烧后的样品破碎至粒度小于49 μm,随后将其放入200 mL的玻璃烧杯中,加入90 ℃的去离子水,液固比为30∶1,再放入电磁转子,用薄膜包裹好烧杯,并将其放在带有加热功能的电磁搅拌器上,控制温度90 ℃及转速300 r/min,搅拌10 min后向溶液中加入不同量的硫酸,调节溶液pH值至预定值,再搅拌120 min.等到浸出液冷却到室温后,用孔径为0.4 μm的Whatman GF-A滤膜过滤,滤液定容到250 mL容量瓶中.将固体残渣和膜在干燥箱中干燥4 h,干燥完成后收集浸出残余物并称重保存.测量滤液中铬的浓度用ICP-AES(Spectro Arcos Eop,SPECTRO Analytical Instruments GmbH).
铬的提取率公式:Cr提取率=([Cr]×V)/WCr,其中WCr为样品中铬的质量,[Cr]为滤液中铬的浓度,V为滤液体积.
1.3 分析和表征
用经典熔矿化学分析法分析钒渣和酸浸渣的化学成分,辅之以X射线荧光光谱仪(XRF)分析(ZSXPrimusII,日本理学公司).钒渣和酸浸渣用X射线衍射(XRD)(D/MAX-RB,日本理学公司)仪分析其物相.
2 结果及分析
2.1 热力学分析
传统的钠化焙烧工艺的铬提取率很低,不到5%.图1和图2分别为提铬反应标准Gibbs自由能随温度的变化图.从图1和图2可见:钒渣中添加Mg(OH)2进行焙烧时,铬的提取率比钒低,因此从钒渣中提铬更加困难;Mg(OH)2代替MgO进行钒渣焙烧,铬的提取率有可能更高,尤其是温度大于700 ℃时MgO的G0值变为正值,而Mg(OH)2的自由能值在1000 ℃时仍为负值.

图1 提铬反应标准Gibbs自由能随温度的变化
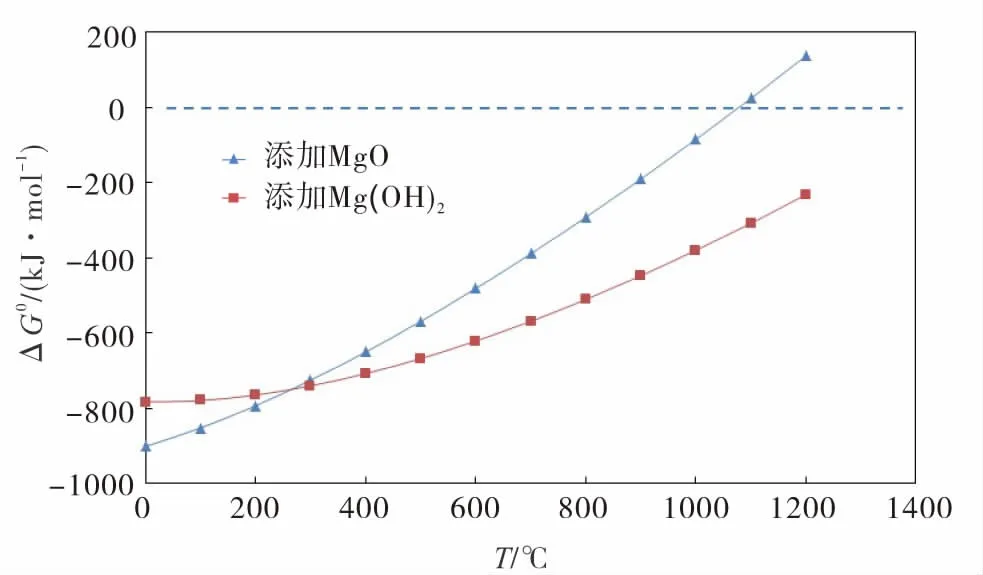
图2 提钒反应标准Gibbs自由能随温度的变化
2.2 钒渣化学组成及物相
实验所用的钒渣是用的国内某一钢厂,经过化学分析,该厂的钒渣化学组成列于表1.由表1可知:钒渣中Cr以Cr2O3计算占总比例为3.18%,V以V2O5计算含量为14.96%;除此之外,钒渣中还有大量的Fe,Mn和Si,其中Fe2O3含量高达49.38%.因此,酸浸渣洗涤除杂质后有可能作为入高炉的原料.
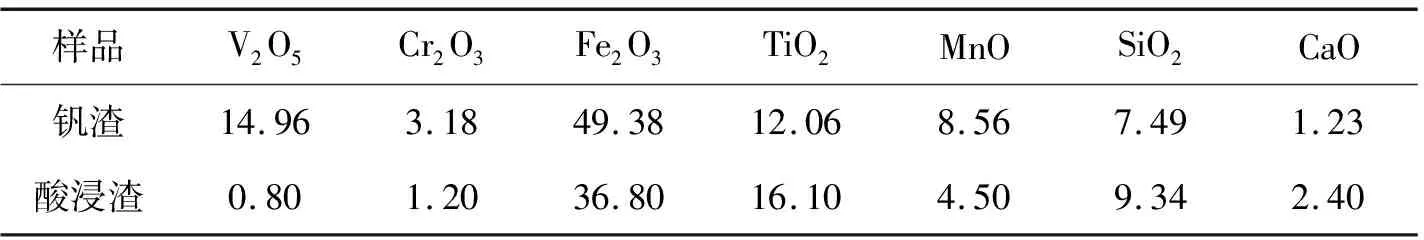
表1 钒渣及酸浸渣主要化学成分
图3为攀钢钒渣的X射线衍射(XRD)图.从图3可见,钒渣由Ca(Mg)Si3O4,Fe(Mg)Si3O4,(Fe,Mn)2SiO4和尖晶石相(Mn,Fe)(Cr,V)2O4组成,钒和铬元素在尖晶石相中很稳定.由于硅酸盐相是包裹在含钒尖晶石相的周围[9],这说明要想将尖晶石相中的铬提取出,必须先破坏外层的硅酸盐相,而破坏酸性物相的最佳物质就是碱性物质,因此选用Mg(OH)2.
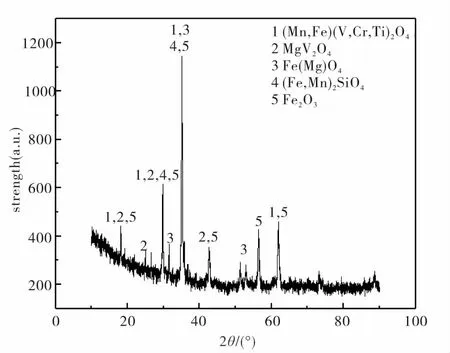
图3 钒渣X射线衍射图谱
图4为Mg(OH)2与钒渣混匀焙烧后酸浸前的XRD图,其中碱渣比为1.0、焙烧温度为1000 ℃、焙烧时间为2 h.从图4可以看出,焙烧渣中铬可能以FeCr2O4形式存在.通过热力学计算,三价铬可被氧化成高价的MgCrO4(图3),但是高价的MgCrO4有可能以非晶型形式存在,XRD检测不到.
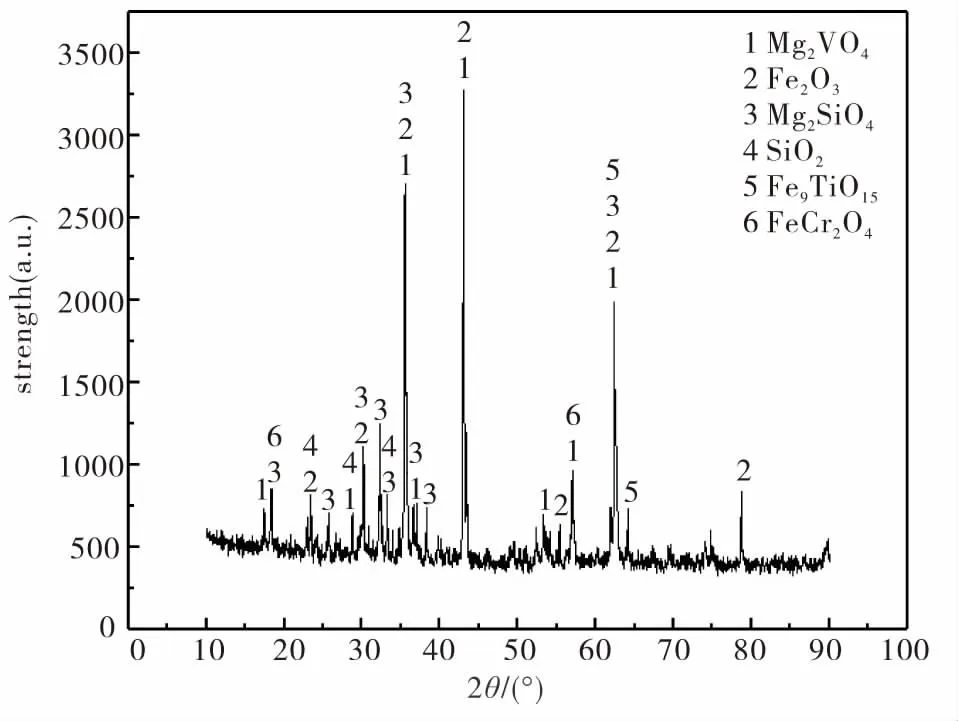
图4 酸浸渣焙烧前X射线衍射图
2.3 氢氧化镁含量对铬提取率的影响
不同碱渣比的焙烧样品如图5所示,其中焙烧时间2 h,温度1000 ℃.从图5可见:当碱渣比为0~0.6时,焙烧后的样品均是黑色的,稍微结块,比较坚硬;当碱渣比为0.8~1.0时,焙烧后的样品不再结块,变成粉末且表面颜色变为棕褐色.碱渣比为0~0.6的样品会发生结块,这不利于空气中的氧气进入,使得钒渣中低价铬难以被高温氧化.碱渣比为0.8~1.0的粉样,有利于低价铬高温氧化.

图5 不同碱渣比试样
图6为铬提取率随碱渣比的变化,其中焙烧时间2 h,温度1000 ℃.从图6可见,随着碱渣比的提升,铬的提取率从0.6%上升到了63%.因此,优化的碱渣比为1.0.
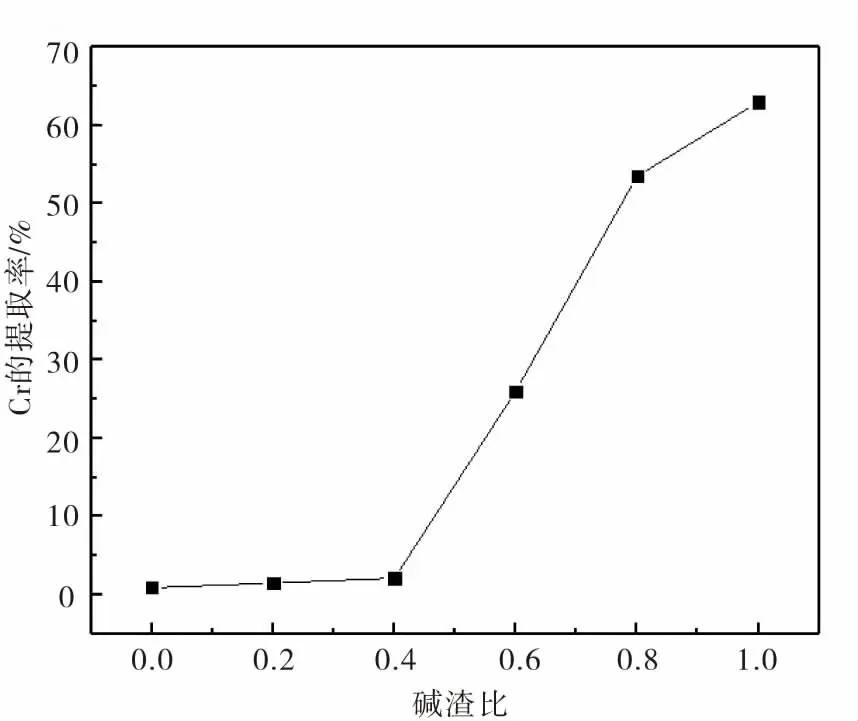
图6 铬提取率随碱渣比的变化
2.4 焙烧温度对铬的提取率的影响
焙烧温度对铬提取率的影响如图7所示,其中焙烧时间2 h,碱渣比1.0.从图7可见,随着焙烧温度的提升,铬的提取率从1%上升到了63%,在焙烧温度为1000 ℃时达到了最大值.从热力学方面来说,反应温度超过1000 ℃,反应标准Gibbs自由能为正,不利于反应进行.因此,优化的焙烧温度为1000 ℃.

图7 铬的提取率随焙烧时间的变化
2.5 焙烧时间对铬的提取率的影响
焙烧时间对铬提取率的影响如图8所示,其中焙烧温度1000 ℃,碱渣比为1.0.从图8可见:随着焙烧时间的延长,铬的提取率从1%上升到了63%,在焙烧时间2 h时达到了最大值;当焙烧时间再延长至2.5 h时,铬的提取率基本不变.因此,从经济角度考虑,优化的焙烧时间为2 h.
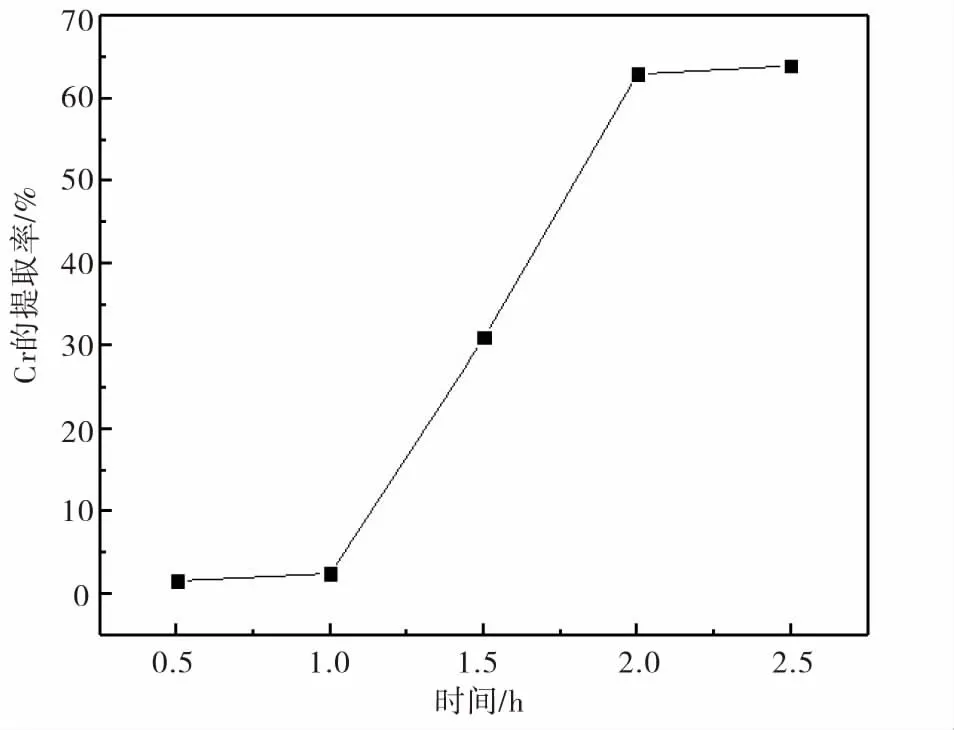
图8 铬的提取率随焙烧时间的变化
2.6 酸浸pH值对铬提取率的影响
图9为酸浸pH值对铬提取率影响,其中焙烧时间2 h、焙烧温度1000 ℃、碱渣比1.0.从图9可见,当酸浸pH值分别为0.1,0.3,0.6,0.8和1.0时,铬的提取率分别为63%,30%,25%,5%和1%.由此可以看出,随着浸取液pH的降低,铬的提取率增加.因此,优化的酸浸pH值为0.1.
为了确定使焙烧后的钒渣酸浸液达到预定的pH值所需加入的硫酸量,故做了钒渣焙烧样的硫酸滴定实验.图10为硫酸滴定曲线.
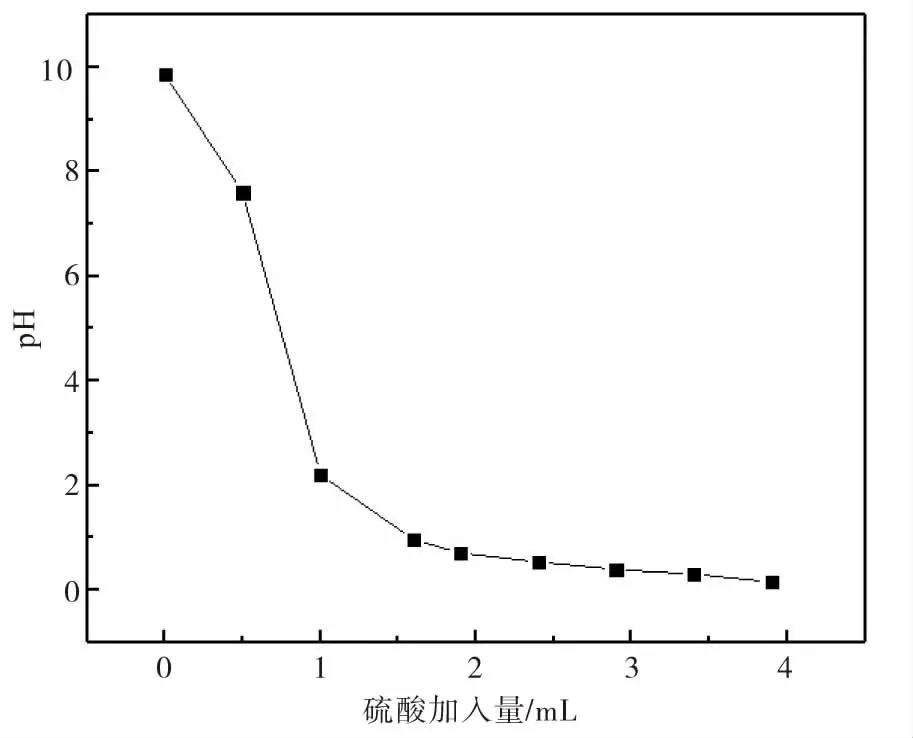
图10 硫酸滴定曲线
3 结 论
(1)从热力学的角度分析和通过热力学计算发现,相同的实验条件下钒比铬更容易提取,而且添加Mg(OH)2的提铬效果要比MgO的好.
(2)铬的提取率随着碱渣比的增加而增加,优化的碱渣比为1.0.
(3)铬的提取率随着焙烧温度的增加而增加,优化的焙烧温度为1000 ℃.
(4)铬的提取率随着焙烧时间的增加而增加,优化的焙烧时间为2 h.
(5)铬的提取率随酸浸pH值的降低而增大,优化的酸浸pH值为0.1.
(6)在优化的条件下,铬的提取率可达63%.

