纤维/芬顿污泥基磁性活性炭对亚甲基蓝吸附性能的研究
王 慧,刘俊杰,夏 洁,朱荣耀,张文晖
(1.中国轻工业造纸与生物质精炼重点实验室,天津市制浆造纸重点实验室,天津科技大学轻工科学与工程学院,天津300457;2.中国制浆造纸研究院有限公司,北京100102)
亚甲基蓝(MB)是一种常见的阳离子偶氮染料,被广泛应用于纺织染色、印刷、皮革和油漆等[1-2]。如不妥善处置,这种碱性染料将会造成严重的环境污染。活性炭具有丰富的孔隙结构和化学官能团,以及较高的比表面积,能高效去除水中MB等有机染料污染物[3]。然而,活性炭存在固液分离困难的问题,限制了其广泛应用。开发磁性活性炭(MAC),使其在外加磁场条件下具备高效固液分离性能,可以有效地解决分离回收问题,降低活性炭应用成本。
芬顿高级氧化处理是造纸废水处理过程中一种常用的三级处理方法[4]。它能有效降解废水中有机污染物和降低色度,但同时会产生大量的芬顿污泥。芬顿污泥中含有大量铁元素,如何对其高效利用是目前研究的一个热点[5]。
本文从造纸行业固体废弃物高值化利用的角度出发,以纤维和芬顿污泥为原料、KOH为活化剂,采用一步热解法制备MAC,并分析了其孔隙结构、比表面积和磁性特征等性质参数,最后通过吸附动力学实验与等温吸附实验考察了MAC对MB的吸附性能。
1 实验
1.1 实验原料与试剂
采用杨木化学浆纤维模拟低灰分造纸初级污泥;模拟芬顿污泥为实验室自制。
H2O2(30%)、FeSO4·7H2O,分析纯,aladdin公司;亚甲基蓝(≥82.0%),国药集团化学试剂有限公司);无水乙醇,分析纯,天津市江天化工技术有限公司;H2SO4、NaOH,分析纯,天津市风船化学试剂科技有限公司;KOH,分析纯,天津大茂化学试剂厂。
1.2 实验仪器
OTF-1200X型管式炉,合肥科晶材料技术有限公司;E120型pH计,梅特勒-托利多(常州)精密仪器有限公司;T6新世纪紫外可见光分光光度计,北京普析通用仪器有限责任公司;DH161108-2T型恒温摇床,上海岛韩实业有限公司;D8 advance型X射线衍射仪,德国Bruker AXS公司;ASIQM0000000-6型比表面积及孔径分析仪,美国康塔公司。
1.3 实验方法
1.3.1 模拟芬顿污泥的制备
在pH=3、FeSO4·7H2O浓度和H2O2浓度分别为0.66 mol/L和1.32 mol/L的条件下反应1 h后,采用NaOH调节pH值至中性,沉淀后得到芬顿污泥。
1.3.2MAC的制备
以纤维和芬顿污泥为原料的MAC制备条件及步骤如下:首先,将纤维和芬顿污泥(质量比2∶1)混合1 h;然后,加入KOH(浸渍比为1∶1)搅拌2 h;浸渍后的样品在105℃下完全干燥。将干燥后的样品研磨至40目,置于管式炉中,在750℃下热解60 min,升温速率10℃/min,氮气流速0.5 L/min。热解后的样品采用去离子水洗至溶液pH值接近中性,然后依次经过60℃真空干燥、研磨和筛分(150~250目),得到MAC样品,用于性能表征及吸附实验。
1.3.3 MAC的表征
采用比表面积及孔径分析仪在77 K条件下对MAC进行N2吸附-解吸实验,测定MAC的比表面积及孔隙结构。BET比表面积在相对压力0.05~0.20区间通过Brunauer-Emmett-Teller(BET)公式计算得出,总孔体积基于相对压力在0.99时的N2吸附量确定,微孔体积和微孔面积采用t-plot方法计算,介孔体积由总孔体积和微孔体积的差值求得,平均孔径由总孔体积和表面积计算(平均孔径=4×总孔体积/BET比表面积),孔径分布采用密度泛函理论(DFT)分析。采用X射线衍射仪分析MAC的物相性质;采用自制的饱和磁化强度测量装置[6]测量MAC的饱和磁化强度。
1.3.4 吸附动力学实验
取50 mL质量浓度为200 mg/L的MB溶液于锥形瓶中,加入0.1 g MAC(质量浓度0.5 g/L),将锥形瓶置于恒温摇床中,在30℃和150 r/min的条件下,分别在吸附时间为0、5、10、15、20、25、30、60、120 min时吸取少量的悬浮液,磁分离后分析MB浓度,根据式(1)计算得出MAC对MB溶液的吸附量。

式中:qt为t时刻吸附量,mg/g;c0和ct分别为溶液的初始质量浓度和t时刻吸附浓度,mg/L;V为溶液体积,L;m为MAC用量,g。
1.3.5 等温吸附实验
分别取50 mL一定质量浓度(25、50、100、200、300、400 mg/L)的MB溶液于锥形瓶中,加入0.025 g MAC(质量浓度为0.5 g/L),将其置于30℃、转速150 r/min的恒温摇床中震荡至吸附平衡(2 h),吸取上清液进行磁分离,分离后分析MB的浓度,根据式(2)计算MAC对MB的平衡吸附量。

式中:qe为平衡吸附量,mg/g;c0和ce分别为溶液的初始质量浓度和平衡吸附浓度,mg/L;V为溶液体积,L;m为MAC用量,g。
1.3.6 MB浓度分析
使用紫外可见光分光光度计在665 nm波长下测量MB溶液的吸光度,根据吸光度(ABS)-浓度(CMB)标准曲线CMB=4.22·ABS-0.196 5可以得到MB的浓度。
2 结果与讨论
2.1 MAC的性质表征
2.1.1 BET比表面积和孔隙结构
MAC样品的BET比表面积和孔隙结构参数见表1。
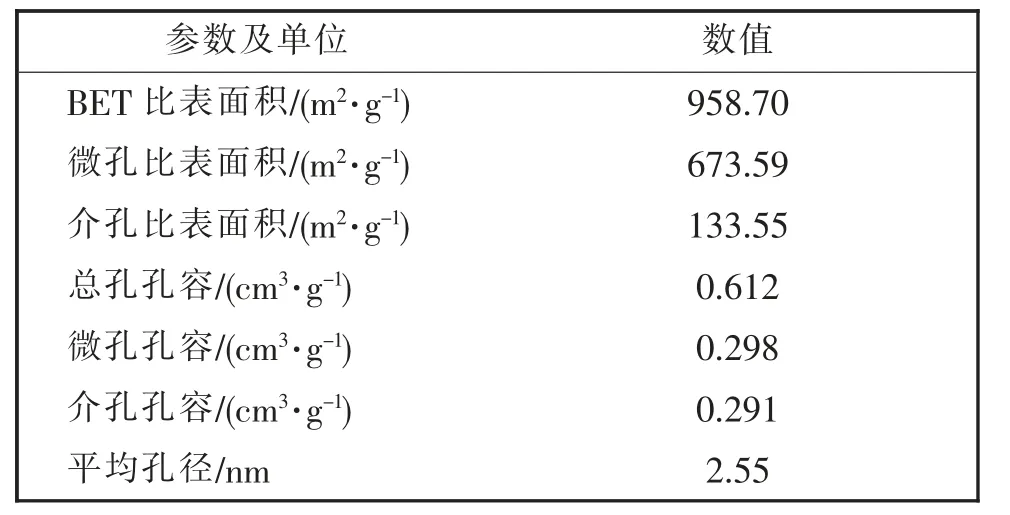
表1 MAC比表面积和孔隙结构参数
2.1.2 XRD分析
MAC样品的XRD图谱如图1所示。从图1可以看出,γ-Fe2O3/Fe3O4的特征衍射峰出现在30.1°、35.5°、43.1°、56.9°和62.6°处[7];α-Fe的特征衍射峰出现在44.7°、65.0°处[8]。对比图中XRD峰面积或峰高度,可知α-Fe是MAC最主要铁基组分或磁性来源。

图1 MAC的XRD图谱
2.1.3 饱和磁化强度
MAC样品的饱和磁化强度为51.88 emu/g,高于文献中废弃生物质基MAC(6.22 emu/g)[8]、花生壳基MAC(8.06 emu/g)[9]、木基MAC(29.68 emu/g)[10]和桉木基MAC(48.65 emu/g)[11]的饱和磁化强度,可见本文制备的MAC样品具有很好的磁性分离性能。
2.2 MAC对MB的吸附性能
2.2.1 MB的吸附动力学
图2为不同初始质量浓度下MAC对MB的吸附动力学曲线。由图2可知,MAC对MB的吸附过程初期(前30 min)为快速吸附阶段,且MB初始质量浓度无论为50 mg/L还是200 mg/L,MB的吸附量都达到83.7%以上;经过60 min后,MAC对MB的吸附过程趋近于平衡,平衡吸附量分别达到98.7mg/g和133.4 mg/g。从吸附位点角度来看,吸附初期吸附位点充足,随着吸附时间的延长,吸附位点被MB占据,剩余活性位点逐渐减少,故吸附过程变缓[12];从传质角度来看,随着吸附时间的延长,液相主体中MB浓度逐渐降低,传质推动力减弱,从而降低了吸附速率[13]。

图2 不同MB初始浓度下,MAC的吸附动力学曲线
本文采用准一级动力学模型(式(3))、准二级动力学模型(式(4))和颗粒内扩散模型(IPD)(式(5))对MAC吸附MB的动力学行为进行拟合分析;采用相关系数R2来评价吸附模型和实验数据的拟合程度(式(6))。


式中:qe和qt分别为平衡吸附量和t时刻吸附量,mg/g;k1为准一级吸附速率常数,min-1;k2为准二级吸附速率常数,g/(mg·min);kp为颗粒内扩散速率常数;C为边界层厚度常数,mg/g;qt,c为模拟数据吸附容量,mg/g;qm为实验吸附容量的平均值,mg/g。
表2给出了准一级动力学模型和准二级动力学模型的拟合参数。由表2可知,尽管当MB初始质量浓度为50 mg/L时,准一级动力学模型的R2达到了0.983 2,但在两种浓度下准二级动力学模型的R2都比准一级动力学模型的高,因此,准二级动力学模型更适合描述MAC对MB的吸附过程,也说明此过程可能为化学吸附过程[14]。

表2 MB吸附动力学模型参数
采用颗粒内扩散模型(IPD)研究了MAC吸附MB的传质过程。从图3可以看出,IPD模型有3个不同的线性阶段,而非单一线性阶段,说明颗粒内扩散不是影响MAC吸附MB过程的唯一机理,其他传质行为(如表面液膜传质)也会影响其吸附动力学[15-17]。此外,对于3个线性阶段,第1阶段表征MAC颗粒表面液膜的扩散行为;第2阶段表征MB在MAC颗粒孔道内的扩散行为;第3阶段表征MB在MAC内部孔隙表面吸附行为,MB通过液体填充孔隙的孔隙扩散过程或固体表面扩散机制,被吸附到吸附部位,这一阶段为最终吸附平衡阶段[18]。
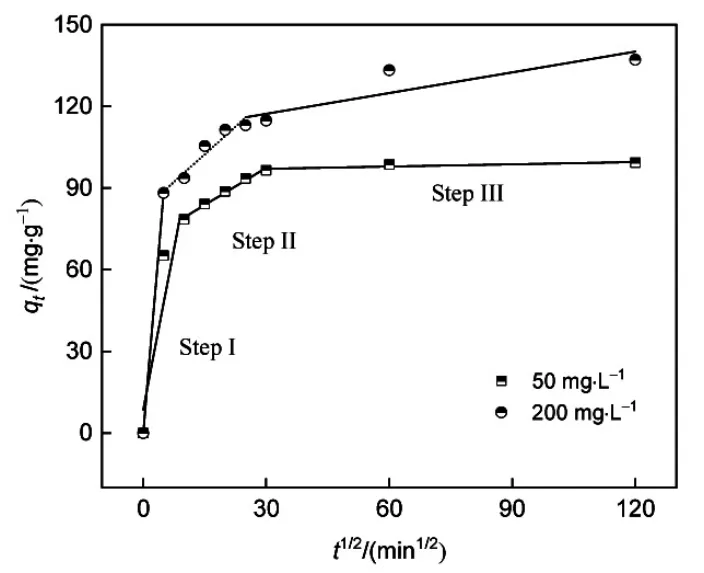
图3 不同MB初始浓度下,MAC的IPD模型拟合
表3表示了IPD模型的拟合参数。由表3可知,颗粒内扩散吸附速率常数kIPD,1>kIPD,2>kIPD,3。在吸附过程中,3个阶段共同控制了分子的吸附速率,第1阶段的MAC外表面液膜扩散(外部传质)最快,其次是第2阶段的颗粒内孔扩散,到达第3阶段时,由于溶液中MB浓度降低,颗粒内扩散减小,逐渐达到吸附平衡[16],因此,MB在MAC上的吸附速率主要由第1阶段和第2阶段决定[19]。扩散阻力由吸附边界层厚度C1、C2、C3来表示,MAC对MB的吸附过程中C3>C2>C1。C值越大,边界层效应就越大。在吸附初期,边界层厚度很小,MAC颗粒外部液膜传质阻力较小,外部扩散阻力低,可以保持良好的分子流动性,许多MB分子被吸附在MAC表面。当吸附位点被填充时,尚未被吸附的MB在体系内的流动受到阻碍,因此在吸附后期扩散阻力增加,MB在MAC颗粒上的吸附变得更加困难。结果表明,MB在MAC内的扩散不仅受颗粒内扩散控制,还受边界层薄膜扩散的影响[20-21]。

表3 IPD模型参数
2.2.2 MB的吸附等温实验
采用Langmuir(式(7))、Freundlich(式(8))和Dubinin-Radushkevich(D-R,式(9))三种吸附等温模型对吸附过程进行非线性拟合。图4为MAC对MB的吸附等温曲线。

图4 MAC的吸附等温曲线

式中:Ce为吸附平衡浓度,mg/L;qe为平衡吸附容量,mg/g;qm为最大吸附量,mg/g;KL为Langmuir常数,L/mg;n和1/nF为Freundlich吸附常数,无量纲;KF为Freundlich吸附常数,(mg/g)(L/mg)1/nF;KDR为D-R吸附常数,mol2/kJ2;ξ为Polanyi吸附势为气体摩尔常数,8.314 J/(mol·K);T为绝对温度,K。
由图4可知,当MAC的质量浓度为0.5 g/L时,最大吸附容量达到168.5 mg/g。参考商品活性炭MB吸附量的国家标准,说明本文所制备的MAC超过活性炭一级品标准(≥135 mg/g)[22]。
表4为三种吸附等温模型相关拟合参数。由表4可知,三种吸附等温模型的R2排序为:Freundlich 表4 MB的吸附等温模型的参数 本文基于Langmuir吸附等温模型,进一步引入分离因子RL(式(10))来表征MAC对MB的吸附过程是否趋向有利吸附平衡。 式中:KL为Langmuir常数,L/mg;C0为MB的初始浓度,mg/L。当RL值>1时,表示吸附过程不利,RL=1为线性,0 本文以纤维和芬顿污泥为原料,KOH为活化剂,采用一步法热解制备磁性活性炭(MAC),其结论如下: (1)所制备MAC的BET比表面积为958.70 m2/g,总孔孔容为0.612 cm3/g,平均孔径为2.55 nm,饱和磁化强度为51.88 emu/g,其磁性来源为α-Fe和γ-Fe2O3/Fe3O4。 (2)吸附动力学实验表明MAC对MB的吸附过程符合准二级动力学模型,通过颗粒内扩散模型分析可知,颗粒内扩散不是MB吸附过程中唯一的传质机理。 (3)对比于Freundlich和Dubinin-Radushkevich两种吸附等温模型,发现Langmuir吸附等温模型可更好地描述MAC对MB的等温吸附过程,且吸附过程是有利的。 (4)当MAC质量浓度为0.5 g/L时,最大吸附容量达到168.5 mg/g,超过商用活性炭一级品的国家标准。

3 结论

