壳聚糖/环糊精复合体系水溶液性质和流变行为
罗国航,上官勇刚,郑 强
(高分子合成与功能构造教育部重点实验室 浙江大学高分子科学与工程学系,浙江 杭州 310027)
1 引 言
表面活性剂、环糊精(Cyclodextrin,CD)等含缔合基团的小分子常被用于与聚电解质(Polyelectrolytes, PEs)、缔合型高分子进行复合[1]。由此得到的复合体系通常结构复杂,除兼具两组分的特性外,还可表现出单一组分所不具备的特殊性能,例如粘度上升、发生sol-gel转变等。近年来,关于以表面活性剂作为第二组分的聚电解质复合体系的研究已有较多报道。表面活性剂均含有疏水基团,可参与溶液中聚合物疏水基团的缔合,形成复合胶束[2-4]。某些带电荷的表面活性剂可通过静电作用与带相反电荷的聚电解质形成复合物[5-7]。以CD作为第二组分的高分子复合体系近年来受到较多关注[8],其中以疏水体系与CD复合的研究最多。
CD为环状结构,环内侧疏水性较强,在疏水聚合物/CD复合体系中可通过特有的包合作用将含疏水基团的高分子包合其中,导致大分子本体间的疏水缔合被破坏[9]。以上特点使得通过改变CD含量来实现复合体系的粘度调节成为可能。同时,CD环外含有大量羟基,可形成分子间氢键。在临界浓度以上,CD分子之间可形成自缔合[10-11]。与内环的包合作用相比,通过环外侧氢键缔合形成的复合体系很少受到重视。在壳聚糖/β-环糊精(CS/β-CD)复合体系的初步实验中发现,β-CD的加入可显著改变CS的流变行为,说明CD可与CS产生复合效应,这种复合效应及其体系的流变行为值得深入探索。因此,本研究成功制备了CS/β-CD的复合溶液,通过对其溶液性质、缔合结构及流变行为的表征,探索其水溶液的流变特性及相关因素的影响规律。
2 实 验
2.1 实验原料
壳聚糖(Chitosan,CS)(Mw=1,000 kDa,DDA=61.5%,分析纯);β-CD(Mw=1,135 Da,分析纯);乙酸(Acetic acid,分析纯);醋酸铵(Ammounium acetate,分析纯),实验前未经进一步提纯,水均为自制高纯去离子水(电导率<5μS/cm)。
2.2 样品制备
称取一定量的CS和CD固体粉末,以1%(w/w)的醋酸溶液为溶剂,在室温下用磁力搅拌器缓慢搅拌(1 r/s左右)进行共溶解。所得样品静置1天后方可进行测试,且同一批次样品测试在1~2天之内完成。
2.3 测试表征
2.3.1流变测试 采用AR-G2旋转流变仪进行流变测试。其中,稳态测试选择φ=40 mm,2°夹具进行,动态测试选用φ=40mm的铝制平板夹具,gap值均设为500 μm。为避免额外剪切或引入气泡,测试样品被直接缓慢倾倒至热台并静置5 min左右,测试温度设定为20 ℃。
2.3.2透射电镜测试 采用冷冻干燥方法抑制CD小分子的结晶。将铜网放置在载玻片上,然后把样品溶液滴加到铜网上,用滤纸吸干溶液形成一层薄薄的液膜,最后将样品进行冷冻干燥处理。所得样品在JEM-1200EX(TEM)透射电子显微镜上进行观测。
3 结果与讨论
3.1 CS溶液的流变行为与溶液性质
图1给出了不同质量浓度的CS溶液的稳态流变曲线。从图可见,随溶液浓度的降低,CS样品的稳态流变行为逐渐从高分子溶液的剪切变稀转变为普通的牛顿流体行为。高分子溶液发生剪切变稀的稳态剪切过程通常包括一个较低剪切速率下的牛顿平台和随后的粘度迅速下降阶段,而普通牛顿流体只呈现牛顿平台[12]。当CS溶液稀释至0.005 wt%浓度以下时,溶液的剪切流变曲线在高剪切速率下甚至会往上翘曲,此时,CS溶液的粘度几乎与纯水的粘度一致。
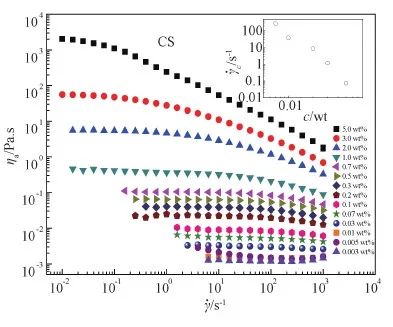
图1 不同浓度下CS的稳态流变曲线
此外,CS溶液发生临界剪切变稀的临界剪切速率(γc)受到浓度影响。根据之前的研究结果[13,29,35],对于纯CS而言,未脱乙酰化的葡萄糖单元组成的疏水缔合链段在溶液中塌缩成疏水的缔合体核,而脱乙酰化的氨基葡萄糖单元则在核的外面形成亲水的壳层结构。溶液浓度越高,CS链间缔合作用点越多,越容易受到剪切的破坏,γc则越小[14-15]。理论上,当实验观察时间尺度小于松弛时间,就可观测到分子链的松弛过程。换言之,当1/γ小于特征松弛时间1/γc,即γ>γc即可观察到剪切变稀。
3.2 CS/CD复合溶液的流变行为
图2给出了在1 wt% CS 溶液中添加不同含量CD的复合溶液稳态流变曲线。如前所述,随剪切速率增大,纯CS溶液首先在低剪切速率下呈现出一个较宽的牛顿平台,然后在高剪切速率下出现显著的剪切变稀。与纯CS溶液不同,CS/CD复合溶液的稳态流变曲线呈现出完全不同的粘度对于剪切速率依赖性,且呈现出明显的CD浓度依赖性。当CD浓度为0.2 wt%时,CS/CD复合溶液样品的初始表观粘度和稳态流变曲线与纯CS样品几乎一致,随CD含量的增加,CS/CD复合溶液的稳态流变曲线在低剪切速率(≤1 s-1)下表现出明显的剪切变稀。当CD浓度达到0.5 wt%时,复合溶液粘度在低剪切速率下出现明显上升,高CD含量样品由于具有更高的初始粘度,其流变曲线在低剪切速率下的剪切变稀更加明显。通常,这种初始表观粘度的明显提高与分子间相互作用形成的新的缔合结构有关[20-22],这种分子间相互作用在较低的剪切速率下即被破坏且回复缓慢,因此在低剪切速率下表现出额外的剪切变稀。当CD浓度为1.5 wt%时(此时CD在溶液中的含量与其在25 ℃水中的溶解度接近),溶液初始粘度不升反降,这可能与CD在水溶液中的溶解度低有关[23]。随着剪切速率增大,在1.0至100 s-1间体系的粘度下降骤然减缓,随着剪切速率继续增大,100 s-1后体系粘度再次迅速下降。此时,所有样品的流变曲线相互接近甚至重合,说明CS/CD形成的缔合结构对剪切很敏感。
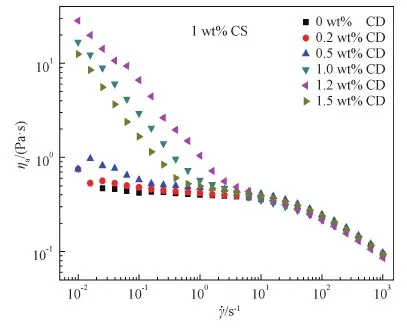
图2 不同CD浓度的CS/CD复合溶液的稳态流变曲线
CD内环疏水性较强,可与尺寸较小的疏水基团产生疏水缔合,形成包合结构。LIU等[24]综述了形成CD包合大分子的三个条件:(1)包合过程产生的热焓为负值,即形成包合物的能量要低于未发生包合前的能量;(2)大分子链的横截面直径要与CD的内环直径吻合,一般而言两者比值在0.9~1.4;(3)客体大分子能够均匀分散在水中(一般为亲水或者两亲性大分子)。而CS主链为环状大分子,分子链横截面直径尺寸在0.85 nm左右[25],β-CD的内环直径在0.6 nm左右[23],两者比值φ>1.4,可见CD无法将CS主链套在其中的。因此复合溶液中CS与CD的相互作用只能是CD外环基团与CS官能团的分子间相互作用。
图3 给出了不同CD浓度的CS/CD复合溶液与纯CS溶液的表观粘度比值ηa’/ηa。在低剪切速率区(≤1 s-1),随着CD浓度的增大,ηa’/ηa逐渐增大,表明CS/CD的复合效果逐渐增强,较高CD浓度下,CS-CD之间的氢键相互作用显著增多。另一方面,随剪切速率增大,CS/CD复合体系的ηa’/ηa快速下降,CD浓度越高,ηa’/ηa的下降速率越快。在高剪切速率区(≥1 s-1),不同CD浓度的ηa’/ηa差异逐渐消失,表明由CS/CD形成的氢键缔合结构对剪切十分敏感,只存在于低剪切速率下,强剪切即能使复合结构完全破坏。
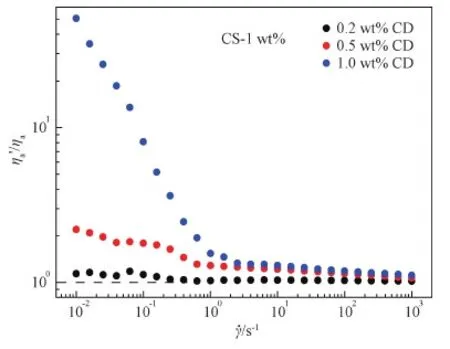
图3 不同CD浓度各剪切速率下CS/CD复合溶液与CS溶液的表观粘度比值
稳态剪切实验结果说明CS与CD之间能发生复合作用。为进一步考察复合溶液中的缔合结构[19,26,27],图4给出了不同CD浓度下的CS/CD复合溶液的动态应变扫描结果。纯CS和0.2 wt% CD的CS/CD复合样品拥有较宽的线性区,随着CD浓度的增加,CS/CD复合溶液的储能模量(G’)增加,且低应变下的线性区明显缩短。0.5和1.0 wt% CD的CS/CD复合样品,在相同频率(6.283 rad/s)下应变大于0.2 wt%时即偏离线性区。偏离线性区通常说明溶液中的结构已发生了显著破坏且无法在短时间内回复或重建[28],该条件下呈现出的极短的线性区可能与溶液中存在显著的由氢键作用导致的CS/CD复合缔合结构有关,这也使得其G’明显升高。适量CD的加入可使溶液中的缔合体形态发生改变,从无缠结的单一松弛转变为分子间氢键相互作用导致的多重松弛。然而这种松弛行为的转变并不会在低CD浓度时发生,所以当CD浓度为0.2 wt%时,样品的应变扫描曲线并没有出现明显的变化。随着CD浓度的增加,CS/CD复合溶液的应变扫描曲线发生了显著变化,G’随应变增加呈现出多阶段的连续减小,表明此时的复合体系存在多重缔合结构。
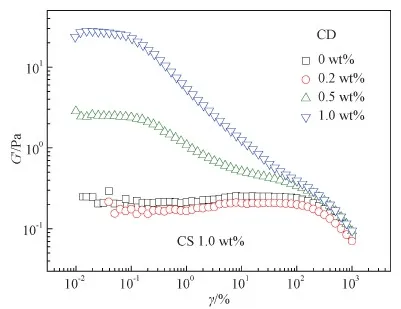
图4 不同CD浓度的CS/CD复合溶液的动态应变扫描曲线
3.3 CS/CD复合溶液的分子间相互作用及其缔合结构
CS在溶液中的缔合形态可通过TEM直接观察,已有较多关于CS缔合形态的研究报道,其中最重要的结论是在相同的溶液环境(温度、离子强度、pH值等一致)下缔合体尺寸与分子量、浓度等条件无关[29]。从图5(a)的TEM结果可知,在测试浓度下缔合体均匀分布与溶液中,缔合体形状以球形为主,呈现出外层疏松内核致密的核壳状,尺寸在80~100 nm左右。需要指出的是,TEM制样过程中存在溶剂挥发,可能使缔合体存在一定程度塌缩,导致观测结果明显偏小。从图5(b)中可见,相对于纯CS样品,含0.5 wt% CD的样品中部分缔合体尺寸和图5(a)保持一致,但还有另一部分缔合体尺寸明显变大,约为200 nm左右,表明该样品至少存在两种不同类型的缔合体,这与之前的流变结果保持一致。由以上TEM结果可知,当CD浓度达到0.5 wt%时,溶液中的CD分子可能同时以如下两种形式存在:一部分CD分子附着在CS缔合体表面;另一部分CD分子则作为一种交联剂将更多的壳聚糖缔合体或者单个壳聚糖分子连接起来,形成CS-CD-CS的复合缔合体。前者无法改变CS缔合体本身的尺寸,后者使得原本致密的缔合体变得松散,缔合体尺寸也随之变大。

图5 (a)1.0 wt% CS溶液和(b)1.0 wt% CS/0.5 wt% CD复合溶液的透射电镜观察结果
在含有氢键缔合的体系中,加入氢键破坏剂是一种常见的评估缔合体中氢键相互作用贡献大小的有效办法[30-33]。由于醋酸铵(AcONH4)只会破坏氢键而不影响疏水缔合,因此选用AcONH4作为该体系测试用氢键破坏剂[32-33]。如图6所示,AcONH4浓度对纯CS溶液几乎没有影响,这是由于对CS溶液粘度贡献最大的相互作用——疏水缔合几乎不受AcONH4的影响。然而,在低剪切速率下,随AcONH4浓度增加,CS/CD复合溶液的粘度逐渐降低,这是因为新的质子供体NH4+离子会取代复合结构中原有的质子供体(-NH2,CS和CD上的-OH),进而破坏原有的CS/CD分子间氢键作用[34]。因此,分子间氢键相互作用是形成CS/CD复合缔合结构的主要驱动力。
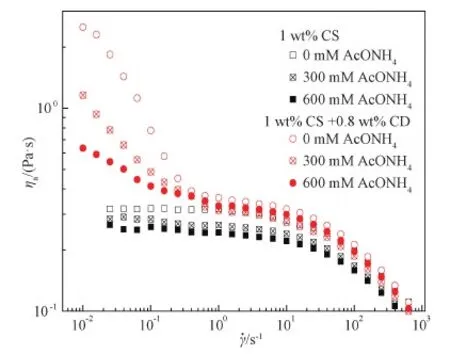
图6 氢键破坏剂AcONH4的加入对于CS/CD复合溶液和CS溶液的稳态流变曲线影响对比
由于氢键会在温度较高时被破坏,因此而发生的分子结构变化会导致一些宏观物化性质的显著改变,如粘度下降,可以用于证明氢键存在[34]。如上所述,足量CD的加入能使得复合体系内部的氢键相互作用明显增加。考虑到温度升高到一定程度能破坏氢键相互作用进而强烈影响CS/CD的复合结构,图7给出了CS/CD和1 wt%纯CS在1%醋酸溶液中的温度扫描结果。从图可见,两种样品的粘度均随着温度升高出现不同程度降低。与纯CS溶液相比,CS/CD复合溶液的粘度下降更快,这说明CS/CD复合溶液中存在比CS溶液更多的氢键相互作用,其结构的破坏对温度的依赖性更加明显。
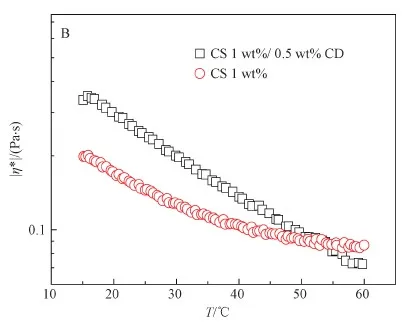
图7 1.0 wt% CS溶液和1.0 wt% CS/0.5 wt% CD复合溶液在0.1%应变下的的动态温度扫描曲线
4 结 论
纯CS溶液发生临界剪切变稀的临界剪切速率γc受浓度影响。浓度越高,越容易受到剪切的破坏,γc则越小。不同含量β-CD的加入使得CS/CD复合溶液呈现出不同的流变特征。相对于纯CS溶液,随着CD含量的增加,CS/CD复合溶液中形成了更大的CS-CD缔合结构,从而导致复合体系表观粘度和模量的上升。氢键破坏剂醋酸铵的加入,能显著降低CS/CD的复合效应,这表明CS-CD分子间氢键相互作用是形成CS/CD复合结构的主要驱动力。与纯CS溶液相比,CS/CD复合溶液的粘度随温度升高下降更快。
- 材料科学与工程学报的其它文章
- Low-temperature Synthesis of TiB2 Nanocrystals Using TiO2, LiBH4 and Mg
- Mg2(Si, Sn)合金大尺寸试样低温固相反应法制备及其热电性能
- 酚醛基碳气凝胶的常压制备及电化学应用
- Preparation of Poly(Silicon-phenyl-arylacetylene)Resin by Polymerizing Dialkynylarylenes and Phenylsilane Catalyzed by Alkali Metal Hydroxide
- 核-壳结构复相生物活性陶瓷微球优化制备及其抗菌性能评价
- 化学气相沉积法制备原位生长三维石墨烯/铜基复合材料

