典型铜铅锌硫化矿的表面氧化机理研究进展
晋艳玲 谢海云 张 培 柳彦昊 孙 瑞 冯艳虎
(昆明理工大学 国土资源工程学院,昆明 650093)
铜、铅、锌是三种常见的有色金属,广泛应用于冶金、化工、机械设备等领域。自然界中的铜、铅、锌矿物多以铜铅锌硫化矿、铅锌硫化矿或铜锌硫化矿等多金属矿床的形式存在。黄铜矿(CuFeS2)、方铅矿(PbS)和闪锌矿(ZnS)是三种最为典型的硫化矿物,他们都具有良好的天然可浮性,通过浮选法可富集得到铜精矿、铅精矿和锌精矿[1]。目前,对铜铅锌多金属硫化矿,优先浮选是最为广泛使用的选矿工艺[2],但由于黄铜矿、方铅矿和闪锌矿表面性质相近且均有良好的可浮性,在生产实践中难以实现三种矿物的彻底浮选分离,往往产出铜铅、铅锌、铜锌或铜铅锌混合精矿,造成精矿质量不达标、销售困难、冶炼工艺复杂化及冶炼成本增加等一系列问题。因此如何高效分离铜、铅、锌多金属硫化矿仍然是选矿工作者面临的重要课题。
在硫化矿的浮选富集和浮选分离过程中,矿物的表面氧化是影响矿物可浮性的重要因素[3-4],采用适当的药剂对矿物表面进行选择性氧化来扩大不同硫化矿之间的可浮性差异,是实现多金属硫化矿浮选分离的主要思路。本文以方铅矿、闪锌矿和黄铜矿为研究对象,分析总结了在常见浮选药剂条件下,三种矿物的表面氧化机理,目的是对铜铅锌多金属硫化矿浮选行为调控及高效浮选分离提供一定的借鉴。
1 方铅矿、闪锌矿和黄铜矿的表面特性
矿物的表面特性与矿物的可浮性密切相关。矿物的晶体结构、化学组成、等电点、静电位和接触角等特性的不同,造成了矿物的复杂多样性以及矿物表面特征及浮选的差异性[5-9]。对方铅矿、闪锌矿、黄铜矿的主要表面特性进行了归纳总结,结果见表1。
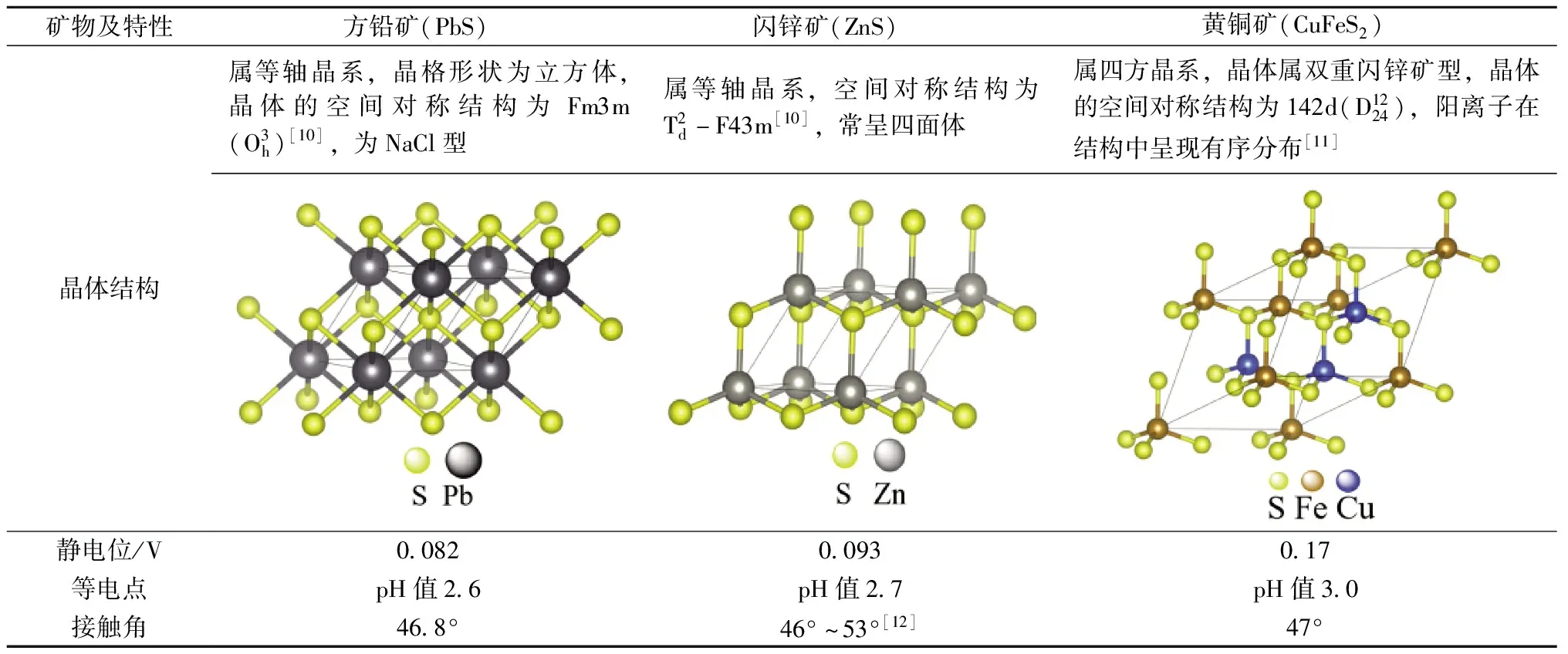
表1 方铅矿、闪锌矿、黄铜矿的主要表面特性
由表1可见,方铅矿、闪锌矿和黄铜矿均属于典型的硫化矿,晶体结构同质多相,且都呈立方最紧密堆积结构,具有天然的疏水性[13]。这三种矿物的静电位介于0.082~0.17 V,等电点对应pH值为2.6~3.0,接触角为46°~53°。三种硫化矿具有相近的等电点和接触角值,从本质上表明它们具有相似的浮选表面特征,都具有良好的天然可浮性,浮选分离时较为困难。
2 铜、铅、锌硫化矿物的表面氧化机理
2.1 方铅矿的表面氧化机理
在铜铅硫化矿选矿中,常常面临方铅矿和黄铜矿的浮选分离问题[14-15]。目前,常用的铜铅分离方法为抑铅浮铜法[16],通过采用适当的氧化剂对方铅矿表面进行选择性氧化以达到降低其可浮性的目的,进而实现铜铅分离。本节分析讨论了重铬酸盐、亚硫酸(盐)和硫酸三种典型氧化剂对方铅矿表面氧化的机理。
2.1.1 重铬酸盐氧化法
重铬酸盐是方铅矿较为有效的抑制剂,曾被广泛应用于铜铅浮选分离。重铬酸盐在弱碱性矿浆中转化为铬酸盐,铬酸根离子再与方铅矿表面发生化学反应生成难溶的亲水性铬酸铅薄膜,增加了方铅矿的亲水性并使其受到抑制,如图1所示。与此同时,重铬酸盐可以破坏方铅矿表面的黄原酸铅,使黄原酸铅不能稳定存在,抑制了方铅矿的浮选[17],反应方程式为式1~3。

图1 重铬酸盐对方铅矿表面氧化的示意图
(1)
(2)
2C2H5OCSS-[18]
(3)
2.1.2 亚硫酸(盐)氧化法

(4)
2PbS+H2O=2Pb2++S2-+HS-+OH-
(5)
(6)
(7)
(8)
PbSO3+H2O=PbSO4+2H++2e
(9)
2.1.3 硫酸氧化法

PbS=Pb2++S2-
(10)
(11)
(12)
(13)
S+O2=SO2
(14)
S2-+2H+=H2S
(15)
SO2+H2O=H2SO3
(16)
(17)
(18)
(19)
2.2 闪锌矿的表面氧化机理
在铜铅锌多金属硫化矿的选矿中,闪锌矿和方铅矿、闪锌矿和黄铜矿的高效浮选分离一直是选矿工作者关注和研究的重点。浮选铜铅锌硫化矿时,铅锌(或铜锌)分离多采用抑锌浮铅(或铜)的工艺,这一工艺主要基于对闪锌矿表面进行选择性氧化来实现。本小节依此分析讨论了氰化物、硫酸锌和亚硫酸钠、高锰酸钾和海藻酸钠、双氧水对闪锌矿的表面氧化机理。
2.2.1 氰化物氧化法
氰化物作为闪锌矿的抑制剂时,随着矿浆 pH值的升高及CN-浓度的增加,闪锌矿受到的抑制作用逐步增强。CN-与 ZnS反应生成Zn(OH)2,而 Zn(OH)2在强碱性矿浆中不稳定,易分解[22],反应式见式20~22。
CN-+H2O=HCN+OH-
(20)
4CN-+3Zn2++2OH-=2Zn(CN)2+
Zn(OH)2↓
(21)
Zn2++2OH-=ZnO-+H2O+e
(22)
具有亲水性的 Zn(OH)2覆盖于闪锌矿表面,使矿物受到抑制。生产实践表明,采用石灰和氰化物组合,既能避免氰化物水解产生氢氰酸,也能在闪锌矿表面生成难溶性的 Zn(CN)2+亲水薄膜,抑制闪锌矿的可浮性[23]。虽然氰化物具有以上的各种优点,但其本身具有剧毒,易对自然环境造成破坏和污染,且存在重大安全隐患,因此大部分选矿厂都朝着无氰工艺发展[24]。
2.2.2 硫酸锌+亚硫酸钠氧化法
随着选矿技术的飞速发展,无氰抑锌工艺被广泛应用[22],尤其以Na2SO3和ZnSO4组合抑制闪锌矿最为常见[25]。这一组合抑制闪锌矿的过程主要有4方面的作用:1)硫酸锌溶液中对闪锌矿起抑制作用的主要为氢氧化锌。氢氧化锌的溶解度小,具有亲水性,容易吸附在闪锌矿表面,导致其亲水而产生抑制效果;2)亚硫酸钠溶于水中会生成亚硫酸根,并与Cu2+生成亚硫酸铜络合物,将Cu2+还原为Cu+,消除Cu2+对闪锌矿的活化[26];3)亚硫酸根可以选择性地阻止捕收剂吸附,还可以解吸捕收剂;4)亚硫酸钠和硫酸锌组合使用时生成亚硫酸锌吸附在闪锌矿表面,增强其亲水性。反应方程式如式23~26。
ZnSO4=Zn2++SO2-4
(23)
Zn2++2H2O=Zn(OH)2↓+2H+
(24)
(25)
Na2SO3+ZnSO4=2NaSO4+ZnSO3
(26)
2.2.3 高锰酸钾+海藻酸钠氧化法
海藻酸钠分子中含有羟基和羧基,可与矿物发生螯合作用并在溶液中形成亲水性胶体从而增强矿物表面亲水的潜力[17]。添加适量高锰酸钾和海藻酸钠对闪锌矿具有选择性协同抑制作用,可抑制闪锌矿的浮选,而对黄铜矿和方铅矿的影响较小,因此可实现铜铅锌硫化矿的分离[27-28]。经分析,海藻酸钠与闪锌矿表面氧化产生的ZnO、Zn(OH)2或ZnSO4等氧化物发生化学吸附,而不与未氧化的闪锌矿表面发生吸附,同时高锰酸钾对闪锌矿的预先氧化作用可增加海藻酸钠在闪锌矿表面的吸附量,实现高锰酸钾和海藻酸钠对闪锌矿的组合抑制作用。
2.2.4 H2O2+海藻酸钠氧化法

ZnS+2O2=ZnSO4
(27)
ZnS=Zn2++S2-
(28)
ZnS+2H2O=Zn(OH)2+S0+2H++2e
(29)
H2O2+SO2=H2SO4
(30)
(31)
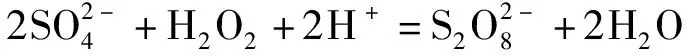
(32)
2.3 黄铜矿的表面氧化机理
我国拥有丰富的铜锌矿产资源,铜锌矿石大多为细粒的浸染状矿石,铜精矿和锌精矿中铜锌矿物往往互含严重[30-32]。在实践中,铜锌分离的主要方法除了抑锌浮铜还有抑铜浮锌法。本小节主要讨论氰化物、石灰和H2O2对黄铜矿的表面氧化机理。
2.3.1 氰化物氧化法
氰化钠(NaCN)、氰化钾(KCN)以及氰的络合物等对铜硫化矿的抑制效果显著[33]。CN-和黄铜矿表面的Cu2+发生反应生成Cu(CN)2沉淀或稳定的络合物,增强矿物的亲水性,从而降低了黄铜矿的可浮性,生成的二价铜氰化物不稳定、易分解。同时氰化物会溶解矿物表面的捕收剂薄膜,进而起到抑制作用。其反应方程式为33~35。
Cu2++2CN-=Cu(CN)2↓
(33)
2Cu(CN)2=Cu2(CN)2↓+(CN)2↑
(34)
C2H5OCSS-
(35)
2.3.2 石灰氧化法
石灰(CaO)是最便宜而且最易得的碱,在硫化矿优先浮选中常用作调整剂和抑制剂,它也可用作黄铜矿的抑制剂[24],抑制机理反应式见式36~38。
CaO+H2O=Ca(OH)2
(36)
Ca(OH)2=CaOH++OH-
(37)
CaOH+=Ca2++OH-
(38)
石灰能有效抑制黄铜矿,原因主要是石灰水解产生的Ca2+和 CaOH+覆盖于黄铜矿表面形成亲水薄膜,抑制黄铜矿上浮。此外,黄铜矿在高碱介质中其表面可生成CuO、Cu(OH)2和FeOOH等氧化产物[11](见图2),导致黄铜矿可浮性降低,达到抑制黄铜矿的目的。

图2 石灰对黄铜矿表面氧化的示意图
2.3.3 H2O2氧化法
浮选过程中添加强氧化性的H2O2可以改变矿物的表面性质,影响其可浮性[34,35]。H2O2可促进黄铜矿颗粒表面的氧化,采用H2O2对黄铜矿进行预处理,可在黄铜矿表面生产亲水性氧化物如CuO、Cu(OH)2、FeOOH和Fe2(SO4)3等,使黄铜矿的可浮性明显降低,从而实现矿物分离。在有氧化剂H2O2存在时,黄铜矿表面的氧化过程如反应式39~42。
CuFeS2=CuS+Fe2++S0+2e
(39)
CuS=Cu2++S0+2e
(40)
CuFeS2+3H2O=CuS+Fe(OH)3+S0+
3H++3e
(41)
CuS+2H2O=Cu(OH)2+S0+2H++2e
(42)
3 结论与展望
1)黄铜矿、方铅矿和闪锌矿表面性质相近且均有良好的可浮性,如何扩大不同硫化矿物之间的表面性质差异并实现铜、铅、锌多金属硫化矿的高效浮选分离,仍然是选矿面临的重要难题。
2)依靠表面氧化技术进行铜铅锌硫化矿物的浮选分离在选矿中应用广泛。目前,采用适当的氧化剂使黄铜矿、方铅矿和闪锌矿表面选择性氧化并生成亲水性氧化膜,以扩大不同硫化矿之间的可浮性差异,是对铜铅锌多金属硫化矿进行浮选行为调控的主要方法。
3)在铜铅锌硫化矿浮选分离研究中,国内外选矿科技工作者在硫化矿氧化剂方面做了大量研究工作,取得了诸多的研究成果,但依然存在诸多问题。首先,对硫化矿的表面氧化机理研究不充分、不彻底;其次,绿色高效的选择性氧化剂缺乏,针对选择性抑制黄铜矿、方铅矿和闪锌矿的氧化剂种类极为有限;第三,新型高效氧化剂的开发不足等。解决这一系列问题需要后续进一步深入开展理论研究和技术攻关。

