CB6F1-Tg(HRAS)Nifdc小鼠与CByB6F1-Tg(HRAS)2Jic小鼠的脏器及血液生理指标测定与比较分析*
刘甦苏 魏 杰 王辰飞 岳秉飞 范昌发
(中国食品药品检定研究院,北京 102629)
潜在致癌性评价是药物临床前安全性评价的重要内容,1997年,人用药品注册技术要求国际协调会(International Conference on Harmonization,ICH)颁发的S1B指南中就提出了基于遗传修饰致癌性动物模型的短期评价方法,目的是减少传统致癌性评价方法存在的周期长、费用高、结果不够准确可靠等局限性。目前这种新的评价方法已经获得美国FDA、欧盟、日本厚生省等机构的认可[1-4]。我国也在2010年提出了建议使用替代方法的致癌性实验指导原则[5],用于指导我国使用啮齿动物进行的药物致癌性评价研究[4]。其中,常用的小鼠模型为日本实验动物中心研究所建立的CByB6F1-Tg(HRAS)2Jic小鼠(简称CB6F1-CIEA)[6-10]。
由于知识产权的限制,如将CB6F1-CIEA癌症模型用于商业用途和法定检验工作需要支付高昂的知识产权费用,从而间接增加药物研发成本。因此,本单位从2004年开始利用传统的转基因方法建立了人类原癌基因c-Ha-ras小鼠模型并开展了相关评估工作[11-13],并于2013年获得国家发明专利(专利号:ZL 2008 1 0101666.0.)[14],以期建立我国具有自主知识产权的动物模型。
鉴于实验动物的脏器质量及血液生理生化参数是药物临床前长期毒性研究中必须观测的项目,受不同基因改造及繁育饲养条件的影响,有必要对将两种模型的相关生物学特征进行测定分析[15-16]。所以,本研究测定了实验用小鼠的脏器及血液学参数,以期验证该模型的合理性并推动我国自建致癌性动物模型的建立及推广。
1 材料和方法
1.1 实验动物及分组
C57BL/6J-Tg(HRAS)转基因小鼠为本单位通过转基因方法自主建立,实验用动物采用近交系繁殖方式,用C57BL/6J-Tg(HRAS)转基因小鼠与BALB/cJ小鼠交配,并对每代出生的仔鼠通过PCR方法筛选阳性,记为CB6F1-Tg(HRAS)Nifdc(简称CB6F1-NIFDC),日本rasH2转基因小鼠的杂交一代,记为CByB6F1-Tg(HRAS)2Jic,来源于日本实验动物中心研究,动物饲养于SPF环境,饲喂SPF级小鼠颗粒饲料,饮用灭菌自来水。日本模型在本设施适应性饲养一周时间。实验动物使用许可证号:SYXK(京)2017-0005。
1.2 主要仪器及设备
日本光电Mek7222血细胞分析仪,仪器精度:WBC 2.0%、RBC 1.5%、HGB 1.5%、MCV 1.0%、PLT 4.0%;Sartorius CPA 423S电子天平;Roche 480Ⅱ荧光定量PCR仪;Thermo Nano Drop超微量分光光度;Eppendorf微量移液器。
1.3 试剂
清洗液DH520、清洗液DH620、稀释液DH640、溶血剂DH910及溶血剂DH680购自上海东湖生物医学有限公司;蛋白磷酸酶抑制剂和BCA法试剂盒购自北京普利莱基因技术有限公司;脱脂奶粉购自France Sparks;38800 Le Pont de Claix及超敏发光液购自Millipore Corporation;RT-PCR 试剂盒、SYBR Premix Ex TaqⅡ荧光定量PCR试剂盒等购自宝生物工程(大连)有限公司;引物由北京诺赛基因组研究中心有限公司合成;TE缓冲液及TAE缓冲液自行配置;其他常见生化试剂(乙醇、异戊醇、苯以及氯仿)购自北京化学工业集团有限公司;蛋白一抗Anti HRAS Antibody cat: 12059-T52 lot: HD08MA1601-B 购自Sino Biological Inc。
1.4 测定项目及方法
1.4.1体质量和脏器指标:分别选取10只,6~8周实验用鼠,雌雄各半。空腹12 h后,活体称质量。眼静脉采抗凝血20 μL测定血液生理指标。安乐处死后解剖取出心、肝、脾、肺、肾、肾上腺、胸腺、卵巢和睾丸,剔除脂肪和包膜,用生理盐水清洗血渍,滤纸吸干表面水分后用电子天平称质量,精确到0.001 g。
1.4.2血液生理指标:红细胞计数(RBC)、血红蛋白浓度(HGB)、红细胞压积(HCT)、平均红细胞体积(MCV)、平均红细胞血红蛋白(MCH)、平均红细胞血红蛋白浓度(MCHC)、红细胞分布宽度(RDW)、白细胞计数(WBC)、淋巴细胞计数(LYM)、单核细胞计数(MON)、中性粒细胞计数(NEUT)、嗜酸性粒细胞计数(EOS)、嗜碱性粒细胞计数(BAS)、淋巴细胞百分比(LYM%)、单核细胞百分比(MON%)、中性粒细胞百分比(NEUT%)、嗜酸性粒细胞百分比(EOS%)、嗜碱性粒细胞百分比(BAS%)、血小板计数(PLT)、平均血小板体积(MPV)、血小板压积(PCT)和血小板分布宽度(PDW),共22项。
1.5 统计学方法
2 结果
2.1 体质量及脏器指标测定结果
表1的脏器绝对值结果表明,同一周龄不同来源的雌性小鼠的心、肝、肺、左肾及右肾5项指标存在一定差异;雄性小鼠的肝、左肾、右肾及胸腺4项指标存在一定差异;其中,肝、左肾及右肾3项指标雌雄均有极显著差异(P<0.01)。表2脏器相对值均值结果表明,同一周龄不同来源的雌性小鼠的肝、肺、左肾及右肾4项指标存在一定差异;雄性小鼠的肝、左肾、右肾及胸腺指标存在一定差异;其中,肝、左肾及右肾3项指标上雌雄均有差异显著性(P<0.01)。

表1 不同性别的两种模型的脏器绝对值指标(g)
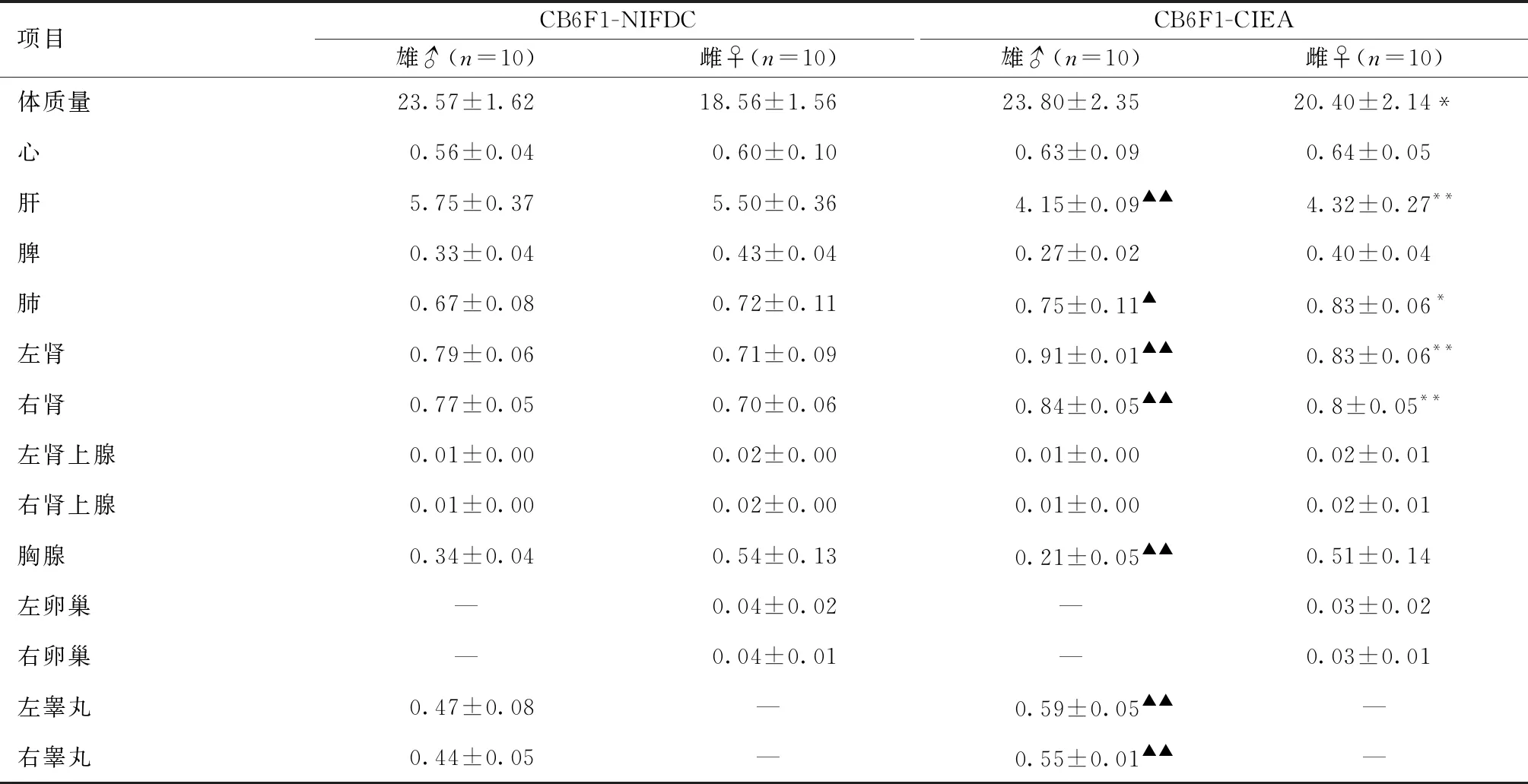
表2 不同性别的两种模型的脏器绝对值指标(g)
2.2 生理指标测定结果
表3的22项血液生理指标方面总体均值结果表明,雌性小鼠在RBC、HGB等7项指标差异极显著(P<0.01),LYM和 NEUT 两项指标存在显著差异(P<0.05),其余指标之间无明显差异;而雄性小鼠在RBC、HCT等5项指标差异极显著(P<0.01),在HCT、PLT及PCT 这三项指标上存在显著差异(P<0.05),其余指标之间无明显差异。

表3 不同性别的两种小鼠模型的血液生理指标
3 讨论
转基因癌症小鼠模型是对临床前药物致癌性评价很有价值的研究模型[2], 也是ICH推荐的快速评价药物潜在致癌性的替代方法,其具有时间短(6个月vs 2年)、费用省、结果可靠、动物使用量少(≤50%/组)等特点,常用的小鼠模型为日本实验动物中心研究所建立的TgrasH2。近几年来,随着新药研发项目增加,国内药物安全评价对该类模型动物的需求不断增加,但多数情况下,通过中介从日本购买,存在价格高、供应周期漫长等弊端。这直接或间接的加重药物研发成本,延缓了国内创新药物走向市场,因而非常有必要建立自主知识产权产权的转基因动物模型,以弥补国内空缺[17]。
为了分析自建模型特点以及与日本来源的小鼠模型异同,本研究分别选取日本和自建的小鼠模型10只,测定并比较基本生物学特性[18]。脏器绝对质量结果表明同一性别的两种模型,雌雄性小鼠在12项指标中存在心、肝等4~5项指标差异。查阅文献分析[15],由于动物本身的个体差异和环境条件不同,都会影响生长发育和脏器系数各项指标,自建模型的肝、肾组织稍大于日本模型可能与制作模型的转基因随机插入方式有关。22 种血液生理指标的初步统计结果显示,雌、雄性小鼠组间部分血液生理参数存在差异,如雌性RBC、HGB 等指标间存在差异,进一步分析原因,由于自建模型出生后一直饲养于本单位饲养设施,而日本模型购入后仅适应性饲养一周时间,本研究所用动物数量相对较少、饲料与饲养环境发生改变可能产生了模型血液生理指标的差异。另外,致癌实验所用的小鼠是杂交一代动物,自建模型杂交采用的是BALB/cA小鼠,但是日本模型采用的是BALB/cByJ,其相较于完整BALB/cJ小鼠的位点,在酰基辅酶α脱氢酶短链(Acad)位点缺失278 bps,这可能也会导致表型有一定的区别。
随着基因编辑技术的发展,本单位进一步分析了日本模型的基因结构,已着手自主建立了c-Ha-ras定点插入及插入拷贝数确定的动物模型,并开展了新建立模型动物研究的相关工作,以期借助现有的技术平台(如临床前药物安全评价平台),建立我国的致癌性小鼠模型,满足未来我国药物安全性评价、药品检定、新药创制中对此类遗传修饰模型的需要[19]。

