原发性高血压患者经典瞬时受体电位通道1基因多态性与左心室肥厚的关系
曹亚萍,张宇,陈玉岚,张向阳,李瑜,徐新娟
1 新疆医科大学第一附属医院高血压科,乌鲁木齐830011;2 新疆医科大学第一附属医院综合内二科
原发性高血压可以导致心脏、肾脏、大脑、血管等多个靶器官受损,心脏靶器官损害中最常见的是左心室肥厚(LVH),临床上有超过30% 的原发性高血压患者可能发生LVH[1-2]。心血管流行病学研究发现,LVH 是独立预测心血管疾病发生发展、预后和死亡的一个关键性指标[3]。LVH 表现为心室壁厚度及心肌重量增加,心肌细胞与组织重构,最终会导致慢性心功能不全等不良心血管事件的发生,而高血压合并LVH 将会加重并促进心血管疾病的发生和进展。原发性高血压引起LVH 的机制相当复杂,是由多种因素参与并导致的。心肌细胞外Ca2+的内向流动和心肌细胞内Ca2+分布紊乱均可以激活CaN/NFAT 信号通路,从而影响心脏中有关调节心肌肥厚基因的表达,并最终导致心肌肥厚[4]。心肌细胞内Ca2+增加是导致心肌细胞肥大的最基本信号,定位在细胞膜上的瞬时受体电位通道C 亚族(TRPC)是Ca2+内流通道之一[5]。TRPC 通道由四聚体形式构成,TRPC1 是TRPC 家族中的核心成员,受控于TRPC1 基因,TRPC1 基因多态性可能在原发性高血压LVH中发挥重要作用[6]。本研究观察了原发性高血压患者TRPC1 基因的多态性改变,并分析其与患者并发LVH 的关系,为高血压合并LVH 患者的个体化治疗和基因治疗提供理论基础。
1 资料与方法
1.1 临床资料 纳入标准:①符合《中国高血压防治指南2010》中的原发性高血压诊断标准[7];②汉族;③年龄18~65 岁。排除标准:①有明确病因的继发性高血压;②合并可能对心脏结构和功能造成严重影响的疾病,如先天性心脏病、心脏瓣膜病、心肌病和恶性心律失常等;③合并1 型糖尿病、2 型糖尿病、甲状腺功能亢进或甲状腺功能减退等内分泌代谢疾病;④合并明显肝肾功能不全、严重感染性疾病、慢性消耗性疾病、风湿免疫系统疾病和恶性肿瘤;⑤使用血管紧张素转化酶抑制剂(ACEI)或者血管紧张素Ⅱ受体拮抗剂(ARB)类药物半年及以上。选取新疆医科大学第一附属医院高血压科2017年4月—2019年1月收治并符合上述标准的原发性高血压患者438 例,参照《2013 欧洲高血压管理指南》[6],根据超声心动图测量的左心室质量指数(LVMI),将患者分为LVH 组73 例(男性≥115 g/m2、女性≥95 g/m2)、对 照 组365 例(男 性<115 g/m2、女 性<95 g/m2)。LVH 组男44 例、女29 例,对照组男263 例、女102 例,两组性别构成比比较P<0.05。LVH 组吸烟25 例、饮酒23 例、有家族史49 例,对照组分别为154、152、251 例,两组比较P均>0.05。两组年龄、高血压病程、BMI、尿素氮、肌酐、空腹血糖、甘油三酯、总胆固醇、低密度脂蛋白(LDL-C)、高密度脂蛋白(HDL-C)比较差异均无统计学意义(P均>0.05)。LVH 组24 小时平均收缩压(24 h SBP)、24 小时平均舒张压(24 h DBP)均高于对照组(P均<0.05)。见表1。本研究通过医院伦理委员会审核,患者及家属均签署知情同意书。
表1 LVH组与对照组一般资料、血生化、血压比较(± s)

表1 LVH组与对照组一般资料、血生化、血压比较(± s)
临床资料年龄(岁)高血压病程(月)BMI(kg/m2)尿素氮(mmol/L)肌酐(μmol/L)空腹血糖(mmol/L)甘油三酯(mmol/L)总胆固醇(mmol/L)HDL-C(mmol/L)LDL-C(mmol/L)24 h SBP 24 h DBP LVH组(n=73)45.22 ± 11.08 68.97 ± 75.97 27.12 ± 3.85 5.49 ± 2.16 76.19 ± 29.42 4.75 ± 0.70 2.04 ± 1.69 4.14 ± 0.79 1.10 ± 0.30 2.71 ± 0.67 143.56 ± 16.14 90.99 ± 13.89对照组(n=365)46.90 ± 9.86 58.81 ± 69.14 26.39 ± 3.42 5.34 ± 1.35 72.03 ± 16.87 4.65 ± 0.63 1.87 ± 1.26 4.25 ± 0.93 1.13 ± 0.30 2.82 ± 0.76 134.42 ± 13.89 85.79 ± 11.56 P 0.195 0.260 0.101 0.592 0.245 0.200 0.302 0.376 0.378 0.288 0.001 0.001
1.2 TRPC1 基因多态性检测方法 采用Sequenom MassARRAY®SNP 技 术。 抽 取 患 者 空 腹 外 周 血5 mL,-70 ℃冰箱保存,参考天根血液基因组DNA提取试剂盒的使用说明书提取TRPC1 基因组DNA,使用紫外分光光度计测量TRPC1 DNA 浓度和纯度。TRPC1 基 因Rs13086677、Rs3821647、Rs7638459、Rs953239、Rs7621642 位点的引物序列见表2,PCR扩增引物及单碱基延伸引物均由Sequenom 公司MassARRAY Assay Design 和Genotyping Tools 软 件设计。PCR 反应体系5 μL。PCR 反应条件:94 ℃4 min;94 ℃20 s,56 ℃30 s,72 ℃1 min,共45 个循环;72 ℃3 min,4 ℃保持。使用基质辅助激光解吸附电离飞行时间质谱进行处理分析点样后的SpectroCHIP 芯片,检测结果由TYPER4.0 软件分型并输出结果。记录两组各位点基因型、等位基因、显性模型、隐性模型、相加模型的频率分布情况。

表2 TRPC1基因5个位点的引物序列
1.3 统计学方法 采用SPSS23.0 统计软件。计量资料以±s s表示,组间比较采用t检验;计数资料以例或率表示,组间比较采用χ2检验。本研究样本的群体代表性由Hardy-Weinberg 平衡来验证,P>0.05则符合Hardy-Weinberg 平衡。原发性高血压患者发生LVH 的危险因素分析采用多因素Logistic 回归模型。P<0.05为差异有统计学意义。
2 结果
2.1 两组TRPC1 基因多态性比较 TRPC1 各位点的基因频率分布均符合Hardy-Weinberg平衡定律(P均>0.05),研究对象具有群体代表性。 两组Rs7638459 位点基因型、隐性模型频率分布比较均有统计学意义(P均<0.05),两组其他位点基因型、等位基因及各模型频率分布比较差异均无统计学意义(P均>0.05)。见表3、4。
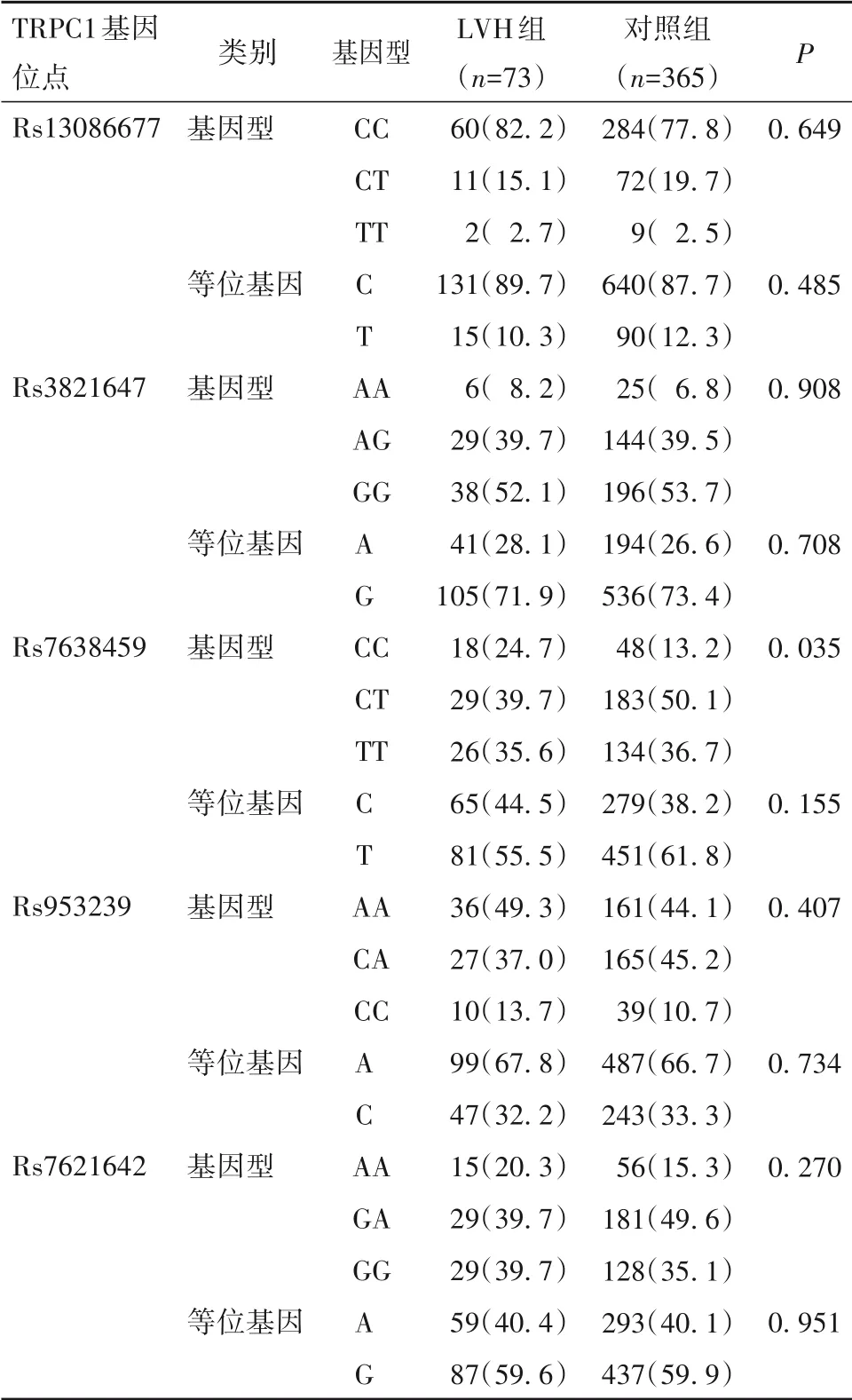
表3 两组TRPC1基因5个位点的基因型、等位基因频率比较[例(%)]
2.2 原发性高血压患者TRPC1 基因多态性与发生LVH的关系 多因素Logistic回归分析结果显示,女性、24 h SBP、Rs7638459 位点CC 基因型频率升高是原发性高血压患者发生LVH 的独立危险因素(OR值分别为0.385、1.822、2.145,P均<0.05),24 h DBP 不是原发性高血压患者发生LVH 的独立危险因素(OR=1.069,P>0.05)。见表5。

表5 原发性高血压患者发生LVH的多因素Logistic回归分析结果
3 讨论
LVH 是机体对血流动力学长期高负荷产生的适应性反应之一[8],然而有临床研究发现,虽然部分高血压患者可以长期有效控制血压,但仍会发生LVH,甚至有些患者LVH 的出现早于原发性高血压的诊断[9]。由此可以看出,压力和容量负荷并不是LVH 发生的惟一危险因素。因此,有必要对LVH 的发病机制进行深入探讨,同时采取积极合理的防治措施。近年来研究发现,引起心肌细胞肥大的最重要的信号转导通路之一是细胞内钙信号[10]。心肌细胞内Ca2+分布失衡和细胞外Ca2+内流,使心肌细胞内的Ca2+长期保持高浓度状态,从而激活CaN;NFAT被进一步活化,去磷酸化后转运到细胞核中,和锌指转录因子相结合,最后调控心脏中参与心肌肥厚有关基因的表达,如心房钠尿肽、BNP、β 肌凝蛋白酶等;加速心肌细胞核酸、蛋白质合成,使心肌细胞体积不断增大,最终发生心肌肥厚[11]。因此,心肌细胞内Ca2+浓度升高是原发性高血压LVH发生发展的中心环节。TRPC1 是钙池操纵的Ca2+通道相关基因,可通过增加细胞质内的Ca2+浓度,进一步激活CaN信号通路;而活化的CaN 可以使NFAT 去磷酸化并转位于细胞核内,参与调控心肌肥厚基因表达,最终导致心肌细胞产生肥大效应[12-13]。动物实验证实,TRPC1 在高血压LVH 的发生发展中发挥关键作用[14]。然而目前有关TRPC1 基因多态性与原发性高血压患者并发LVH 的相关性研究比较少。因此,本研究以原发性高血压患者为研究对象,探讨TRPC1 基因多态性与原发性高血压患者并发LVH之间的关系。

表4 两组TRPC1基因5个位点的基因模型频率比较[例(%)]
本研究结果显示,LVH 组24 h SBP、24 h DBP 明显升高,这与WANG 等[15]的研究结果一致;使用Logistic 回归分析原发性高血压患者LVH 的危险因素,调整了多重混杂因素后,结果显示女性、24 h SBP升高是原发性高血压患者发生LVH的独立危险因素,提示24 h SBP 越高及女性高血压患者更容易出现LVH,这与LEVY 等[16]的研究结果一致。24 h SBP导致原发性高血压LVH发生的相关机制可能包括:①持续升高的血压水平可以显著增加心脏的循环负荷,还可以加重心肌内小血管的硬化程度,加快心肌胶原增生和纤维化,最终导致LVH[17]。②血压持续升高可能伴随心率加快,同时心肌耗氧量增加,使心肌收缩力进一步加强,从而促进心肌细胞发生肥厚。③血压持续升高可以激活肾素—血管紧张素—醛固酮(RAAS)系统,升高血管紧张素Ⅱ水平,引起一系列变化,如促进心肌细胞蛋白合成、加速心肌细胞凋亡、促进心肌成纤维细胞增生等,最终发生心肌重构[18]。
本研究比较了两组的TRPC1 基因频率分布,结果显示两组TRPC1基因的Rs7638459位点基因型分布、隐性模型(CC/TT+CT)分布比较存在统计学差异;多因素Logistic 回归分析显示,Rs7638459 位点的CC 基因型频率升高是原发性高血压患者并发LVH 的独立危险因素。XUE 等[19]认为,除血压及相关因素外,LVH 的个体差异中有60% 是由遗传因素引起的。故我们推测,Rs7638459 位点的变异基因可能是原发性高血压患者发生LVH 的遗传易感基因。TRPC1 基因多态性参与原发性高血压患者并发LVH 可能的作用机制包括:①TRPC1 通道可能参
与RAAS 系统介导细胞增殖肥大、血管平滑肌反应性增强,血管紧张素Ⅱ与对应靶细胞膜上血管紧张素Ⅱ受体相结合,促进TRPC1 通道开放,使心肌细胞内Ca2+内流增加,从而发生LVH[20]。②TRPC1 通道参与构成血管平滑肌细胞的形成,可能通过调节细胞内Ca2+浓度,来参与血管平滑肌细胞的增殖或激动剂诱导高血压的发生发展,进而导致LVH[21]。③TRPC1 通道可以被病理性高压力激活,细胞外Ca2+内流增加,从而使CaN/NFAT 信号通路被激活,诱导心肌肥厚相关基因表达并导致LVH。④TRPC1参与由5-羟色胺受体诱导的LVH。研究表明,在受5-羟色胺刺激的大鼠心肌纤维中TRPC1表达明显增加,TRPC1表达被小RNA 干扰后,NFAT 激活及5-羟色胺受体介导的心肌细胞肥厚效应明显受到抑制[22]。
综上所述,TRPC1 基因Rs7638459 位点基因多态性与原发性高血压患者发生LVH 有关,其中CC基因型患者更易发生LVH。将血压调控在理想范围与逆转心血管重构已成为高血压及心血管疾病防治工作中的重中之重,因此,在临床工作中对高血压合并LVH 患者进行不同危险因素的预防和控制,并且尽可能进行基因检测显得尤为重要。根据患者不同的基因型,给予针对性和精准的药物治疗,使临床治疗趋于个体化,对高血压LVH 的诊治均具有积极作用。本研究证实Rs7638459 位点的CC 基因型与高血压患者并发LVH 具有相关性,为高血压患者心脏靶器官损害的早期干预提供了新思路。

