甲状腺微小乳头状癌全乳晕腔镜手术与开放手术的疗效比较
王俊潇,刘鄂长,伍晓兰
(三明市第二医院普通外科,福建 三明,366000)
甲状腺癌2020年全球发病率排名第9位,新发586 202例,死亡43 646例[1]。甲状腺微小癌指肿瘤直径≤1 cm的甲状腺癌,其中乳头状癌占大部分,随着超声诊断技术的进步,甲状腺微小癌的发病率显著升高[2]。日本学者提出了甲状腺微小癌,如无颈部淋巴结转移,可随访观察[3]。但临床工作中,甲状腺癌的淋巴结转移率并不低,约1/3存在中央区淋巴结转移[4-7],因此发现甲状腺微小癌应积极手术治疗[8]。开放甲状腺微小癌手术是传统的治疗方式。近年,腔镜下甲状腺切除术逐渐成为甲状腺手术的新术式,其美容效果是开放手术所不可及的。随着手术器械的更新及技术水平的成熟,腔镜甲状腺手术的适应证已从良性病变拓展至恶性肿瘤,淋巴结转移的患者同样可行腔镜甲状腺手术[9]。但腔镜甲状腺手术的优势不应局限于美容效果,基于腔镜的放大作用,腔镜手术应追求精细解剖、减少并发症。目前评价腔镜术式能否成为甲状腺微小癌首选术式的文献较少。鉴于此,本研究通过对比腔镜与开放甲状腺微小乳头状癌手术的围手术期相关指标与并发症,以寻找甲状腺微小乳头状癌适合的手术方式。
1 资料与方法
1.1 临床资料 选择2019年1月至2021年1月我科收治的200例甲状腺微小乳头状癌患者作为研究对象,本研究已获得我院伦理委员会的批准。纳入标准:临床资料完整;术前各项检查完善;术前喉镜提示声带位置正常;甲状腺肿物直径≤1 cm;术中冰冻病理提示甲状腺癌且术后石蜡病理提示甲状腺乳头状癌。排除标准:男性;颈侧区淋巴结转移;肿瘤直径>1 cm;双侧甲状腺癌;腔镜手术中转开放。根据手术方法将患者分为两组,100例行开放甲状腺微小乳头状癌的患者纳入开放组,100例行全乳晕入路腔镜甲状腺微小乳头状癌手术的患者纳入腔镜组。
1.2 手术方法 开放组行开放单侧甲状腺腺叶+峡部切除+同侧中央区淋巴结清扫术。采用气管插管全身麻醉,患者取仰卧位,于颈静脉切迹上方两横指处做6 cm弧形切口,逐层切开皮下组织、颈阔肌,游离皮瓣,切开颈白线,暴露甲状腺,切除患侧甲状腺腺叶及峡部,术中冰冻病理报告甲状腺癌后,清扫同侧中央区淋巴结(Ⅵ组)及Ⅶ组淋巴结,彻底止血后,不放置引流管,缝合切口。术中如果种植甲状旁腺,则种植于右前臂皮下肌肉内。腔镜组行腔镜下单侧甲状腺腺叶+峡部切除+同侧中央区淋巴结清扫术。采用气管插管全身麻醉,患者取“人”字仰卧位,双上肢于体侧固定,肩下垫枕,头后仰,头圈固定,充分显露颈前区,使颏、甲状软骨、颈静脉切迹位于同一直线。两侧头发收纳于帽子内,胶布固定。常规碘伏消毒,上至下唇,下至脐平面,两侧至上臂上1/2。双乳晕上缘、右乳晕左缘用10 mL针筒黑色针头注入膨胀液(生理盐水100 mL+0.894%罗哌卡因20 mL+0.1%肾上腺素0.3 mL),然后在镜头主隧道处及胸骨柄处皮下注入膨胀液。双乳晕区10~12点方向分别建立0.5 cm操作孔,右乳晕2~4点方向建立1 cm观察孔,用分离棒分离至胸骨柄处,穿刺Trocar,腔镜下两侧乳晕切口穿刺5 mm Trocar,建立CO2气腹,压力维持在6 mmHg。用电刀分离胸前壁,走行于胸壁深筋膜与胸大肌筋膜之间;颈部,走行于颈浅筋膜与颈深筋膜浅层之间;上达甲状软骨水平,两侧至胸锁乳突肌外缘,见图1。超声刀切开颈白线,分离甲状腺外科间隙,充分显露甲状腺。找到气管后,由峡部切断,沿甲状腺外科间隙分离,见图2。腔镜直视下用红色针头由颈外侧刺入,置入甲状腺拉钩,将颈前肌拉开。分离外侧至颈总动脉鞘内侧,注意是否存在喉不返神经,见图3。超声刀紧贴下极分离出下静脉、下动脉,钳夹切断,显露喉返神经,见图4。注意下甲状旁腺的辨认,见图5。分离出甲状腺中静脉,钳夹切断。分离切断甲状腺悬韧带,暴露甲状腺上极,紧贴上极分离切断上动静脉。沿气管紧贴甲状腺分离背面组织,显露上甲状旁腺,移除甲状腺腺叶及峡部,见图6。用标本袋经10 mm切口取出标本,送术中冰冻检查。术中冰冻病理结果:甲状腺乳头状癌。继续行中央区淋巴结清扫术,清扫舌骨下方、喉前、气管前、气管旁、颈静脉切迹上方、颈总动脉内侧的淋巴脂肪组织,见图7。清扫出6A、6B、6C、7组淋巴结送术后病理。观察上、下甲状旁腺,若缺血,则切除后制成2 mL混悬液种植于右前臂肌肉内。膨胀液与注射用水混合冲洗创面,由拉钩戳孔置入8号引流管于气管前,见图8。可吸收线缝合颈白线及乳晕区切口,见图9。

图1 创建颈部空间 图2 离断甲状腺峡部 图3 显露颈总动脉
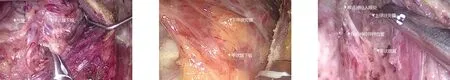
图4 显露喉返神经 图5 下甲状旁腺(A1型),位于甲状腺包膜内,无法原位保留 图6 显露喉返神经入喉处及上甲状旁腺

图7 中央区淋巴结清扫后 图8 放置引流管 图9 手术后切口及引流管情况
1.3 观察指标 观察对比两组患者年龄、肿瘤位置、肿瘤直径、清扫中央区淋巴结总数,术后6 h、24 h切口疼痛的视觉模拟评分及手术前后血清钙水平,分别采集患者入院第2天清晨空腹、术后6 h肘静脉血5 mL,检测血清钙水平(正常2.11~2.52 mmol/L),观察两组术中出血量、术后6 h心率、术后住院时间及术后饮水呛咳、暂时性声音嘶哑、手足抽搐麻木、出血、积液、感染等并发症发生率。
2 结 果
2.1 两组患者临床资料的比较 两组患者年龄、肿瘤位置、肿瘤直径、清扫中央区淋巴结总数差异均无统计学意义(P>0.05)。见表1。
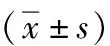
表1 两组患者一般资料的比较
2.2 两组手术前后血钙及疼痛指标的比较 两组术后6 h血钙水平均低于术前,且开放组低于腔镜组,差异有统计学意义(P<0.05)。腔镜组术后6 h、24 h 疼痛评分均低于开放组,差异有统计学意义(P<0.05)。见表2。
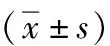
表2 两组患者手术前后血钙、疼痛评分的比较
2.3 两组患者围手术期相关指标的比较 腔镜组术中出血量、术后6 h心率、术后住院时间均低于开放组,差异有统计学意义(P<0.05)。见表3。
表3 两组患者手术相关指标的比较
2.4 两组患者术后并发症的比较 腔镜组暂时性声音嘶哑、手足抽搐麻木及并发症总数少于开放组,差异有统计学意义(P<0.05);两组术后出血、积液、感染发生率差异无统计学意义(P>0.05)。见表4。两组暂时性声音嘶哑患者均予以保守治疗,口服甲钴胺片,避免过度用嗓,半年内均恢复,复查喉镜可见声带闭合良好;手足抽搐、麻木患者均口服葡萄糖酸钙、阿法骨化醇治疗,术后3周内症状均消失。腔镜组术后出血2例,均再次行腔镜下止血,出血部位均为颈浅筋膜处小血管,术后顺利出院。开放组中1例甲状腺出现感染,再次入院行经皮下穿刺置管引流,使用Ⅰ代头孢,治愈出院。腔镜组5例皮下积液,均为镜头隧道及胸前部皮下积液,经穿刺抽液数次后痊愈。

表4 两组患者术后并发症的比较[n(%)]
3 讨 论
腔镜甲状腺手术中,经胸前入路是公认的首选入路[10]。其中腔镜下全乳晕入路手术方式创伤小,美容效果好,操作简单[11]。因此入组患者均行此术式,且为女性,男性无乳腺腺体,若经全乳晕入路施术,左手操作钳与腔镜会相互干扰,影响手术操作。
甲状腺微小癌行腔镜手术不仅是因为美容需求,而且腔镜下组织、血管、神经得以放大,容易辨认小血管、喉返神经、甲状旁腺,损伤几率大大降低,将甲状腺手术上升至真正微创、精细解剖的程度。本研究结果显示,两组清扫中央区淋巴结数量差异无统计学意义,表明腔镜手术的根治效果与开放手术一致。本研究清扫中央区淋巴结的数量与国内众多甲状腺中心的数据一致[12-16]。
对于甲状腺微小癌,笔者团队常规经全乳晕入路行腔镜甲状腺手术,禁忌证为:(1)Ⅵ区以外的淋巴结转移;(2)有甲状腺手术史、消融史、颈部放疗史;(3)术前评估肿物侵犯甲状软骨、气管、食管、颈总动脉、颈内静脉或远处转移;(4)甲状腺癌合并桥本甲状腺炎或其他自身免疫性甲状腺炎;(5)甲状腺未分化癌、甲状腺髓样癌;(6)全身重大疾病或颈胸部畸形不适合腔镜手术。
腔镜甲状腺手术使用含有肾上腺素的膨胀液辅助创建空间,可避免术中出血[10]。腔镜手术全程在筋膜间隙内操作,创建隧道、腔镜下层次的定位与分离非常重要,腔镜甲状腺手术被部分人诟病的原因是胸前区创伤大、间隙创建时间长,我们的经验为:胸前区3枚Trocar均在皮下走行,避免损伤乳腺组织,会师于胸骨柄处,寻找胸深筋膜,在其下方找到疏松间隙(图10A),进入胸深筋膜与胸大肌筋膜之间的天然间隙(图10B)。在颈部,找到双侧胸锁乳突肌后,走行于颈浅筋膜与颈深筋膜浅层之间(图10C)。解剖上极时,需从外侧的颈总动脉与内侧的环甲间隙上行,在胸骨甲状肌下方解剖上极血管,可避免损伤喉上神经外支(图10D)。切除甲状腺时容易辨认小血管,避免不必要的出血。依笔者经验,腔镜甲状腺手术可顺利结束的前提是出血量小(约10 mL),否则一旦出血较多,视野即变成红色,无法辨认小血管及神经,尤其甲状旁腺。失去了腔镜甲状腺手术精细解剖的优势,中转的可能性极大。我中心腔镜甲状腺手术后仅发生2例出血,发生率2%,符合Meta分析数据的0.43%~4.39%[17-18]。术后予以颈部制动,嘱轻声咳嗽,外敷包裹毛巾的冰袋,可降低出血风险[19]。清扫右侧喉返神经后方淋巴结时,需提起喉返神经,这一操作在开放手术时容易由于力度控制不稳导致过度牵拉,引起术后暂时性声音嘶哑。腔镜通过放大效应,可做到局部精细解剖,避免无意中牵拉神经。本研究中,腔镜组暂时性声音嘶哑发生率低于开放组。处理喉返神经周围小血管时,超声刀刀头与神经至少保持3 mm安全距离[20],腔镜下甲状旁腺与甲状腺腺体的颜色对比明显,较开放手术肉眼观察容易辨认,如术中判断无法原位保留,可立即切除后种植于肌肉内,可避免术后永久性甲状旁腺功能减退。甲状腺微小癌行中央区淋巴结清扫可能影响甲状旁腺血供,引起术后甲状旁腺功能减退。如果甲状旁腺稍变色,仅会引起暂时性甲状旁腺功能减退。如果甲状旁腺缺血或血液供应不足,则需果断种植,否则引起永久性甲状旁腺功能减退,会严重影响生活质量[21]。本研究结果显示,两组术后血钙水平均较术前下降,且开放组低于腔镜组,手足抽搐麻木并发症发生率高于腔镜组,这得益于腔镜下甲状旁腺的高辨识度及血管的精细处理。开放组手术切口长,术中切开皮下组织及颈阔肌,均会造成术后疼痛。腔镜组切口小,切皮前予以罗哌卡因配置的膨胀液创建手术空间,全程在解剖间隙内操作,创伤小。研究表明,腔镜甲状腺手术后应激反应较开放手术轻[22-23]。本研究结果显示,腔镜组术后6 h、24 h 疼痛评分均低于开放组;开放组术后心率较腔镜组高,亦考虑切口疼痛所致。文献报道,甲状腺手术后可使用非甾体类抗炎药,少使用阿片类止痛药,可依据患者情况使用多模式镇痛[24]。但据我中心观察,患者术后疼痛程度中等,可耐受,两组术后24 h 疼痛评分明显下降,可避免滥用止痛药物。
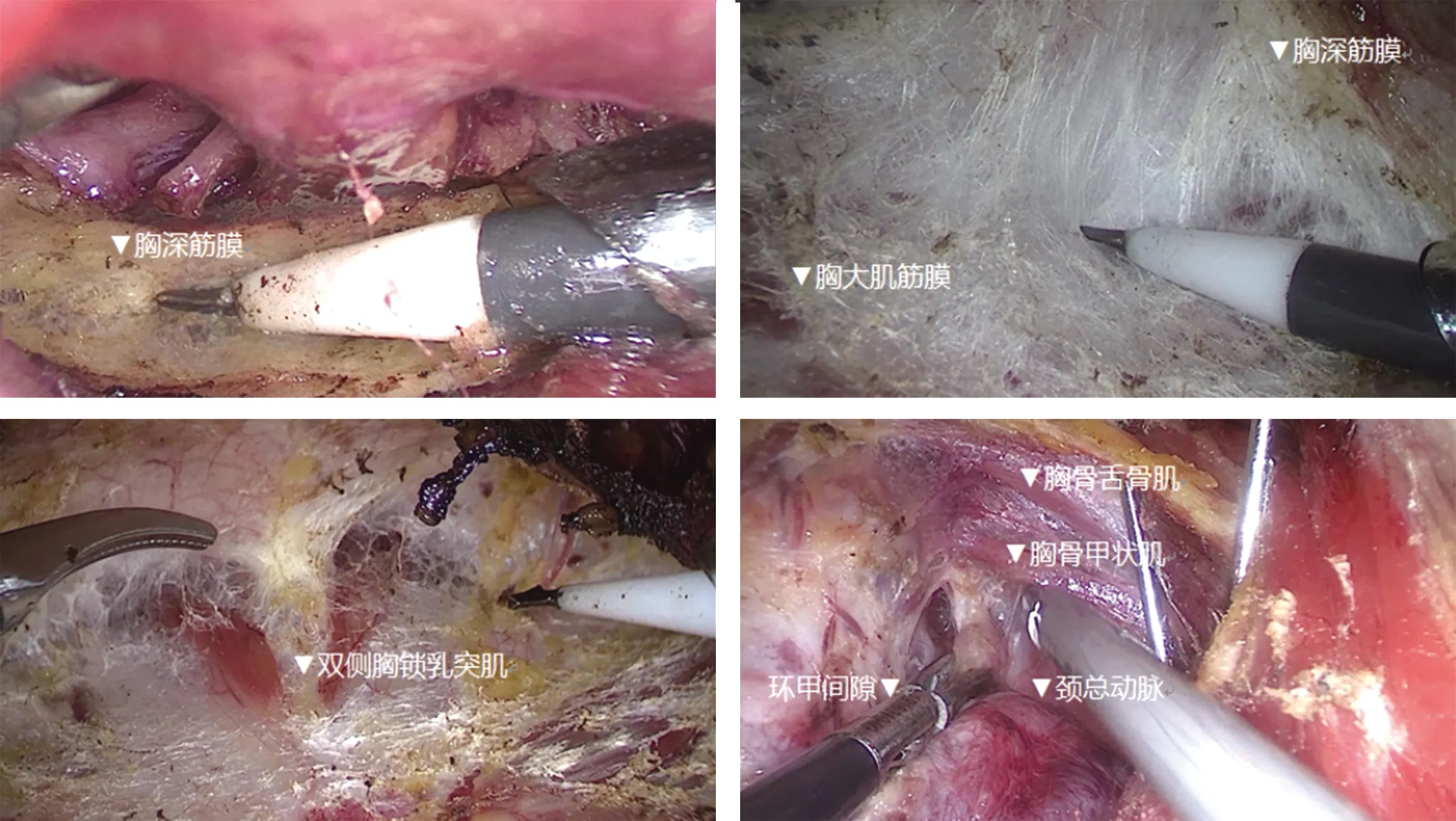
图10 建立腔隙过程中的参照点(A:于胸深筋膜下方寻找疏松间隙;B:于胸前壁走行于胸深筋膜与胸大肌筋膜之间;C:于颈部寻找双侧胸锁乳突肌后,走行于颈浅筋膜与颈深筋膜浅层之间;D:由外侧颈总动脉与内侧环甲间隙上行,汇合处即为上极血管)
本研究中,腔镜组发生5例皮下积液,我们改进引流管后皮下积液明显减少。原来引流管由左侧乳晕切口引出,存在2个缺点:(1)术后当天患者即可下床活动,因重力原因,引流管容易移位,引流效果不佳;(2)引流管走行过长,导致Trocar隧道及颈前皮下存在死腔,无法完全贴紧闭合,术后容易积液,因重力原因均积聚于隧道内。我团队改进了引流管,将8号引流管由颈外拉钩处置于气管前,引流管4~5 cm处再修建一个小缺口,引流颈前空间的引流液,用大块薄膜敷贴将引流管固定于皮肤上,未缝线。缝合乳晕旁切口前用吸引器保持颈前空间的负压,3个切口均用可吸收线连续皮内缝合,如此操作后,颈前空间可贴紧,术后渗液少。从患者体验而言,颈部引流管切口小,未缝线,美观效果好。3个乳晕切口均用可吸收线缝合,术后不用拆线。腔镜组术中出血量少于开放组,因腔镜手术的精细解剖,避免了很多小血管的出血。腔镜组暂时性声音嘶哑、手足抽搐麻木、疼痛评分均低于开放组,最终使得腔镜组术后住院时间缩短。
综上所述,对于甲状腺微小癌,腔镜手术的优势大于开放手术,其围手术期指标、并发症均优于开放组,可作为优选术式。

