气液比对表面活性剂复配促进甲烷水合物生成影响
王平,马贵阳,黄仙智
(辽宁石油化工大学 石油天然气工程学院,辽宁 抚顺 113001)
天然气水合物是在合适的pH值下[1]由水和天然气在高压、低温下[2]形成的笼形化合物[3]。天然气水合物中的碳储量是化石燃料的2倍多[4]。将来会大力发展天然气水合物储运天然气[5]。促进天然气水合物的有效方法包括加入表面活性剂、搅拌、鼓泡及喷雾等[6]。水合物受气液比影响也较大。气液比是指一定温压下,釜内气体与液体体积之比[7]。刘有智等[ 8]研究发现气液比70~200间水合物含气量随气液比增大出现先增大后减小的趋势。魏国栋等[9]研究表明CO2水合物气液比较高时石英砂中最大储气量为3.078 mol。
因此,本文研究不同气液比下SDS、APG1214以及复配溶液对甲烷水合物的影响。
1 实验部分
1.1 实验材料
甲烷(CH4,纯度为99.9%);十二烷基硫酸钠(SDS,纯度≥86%),化学纯;烷基多糖苷(APG1214,纯度≥75%),工业品;实验室自制的去离子水。
1.2 实验装置
实验所采用仪器为 KDSD-Ⅱ型水合物动力学实验装置。设备主要有五大模块,包括甲烷气瓶、反应釜装置、水浴装置、压力控制系统以及数据采集系统,简图见图1。
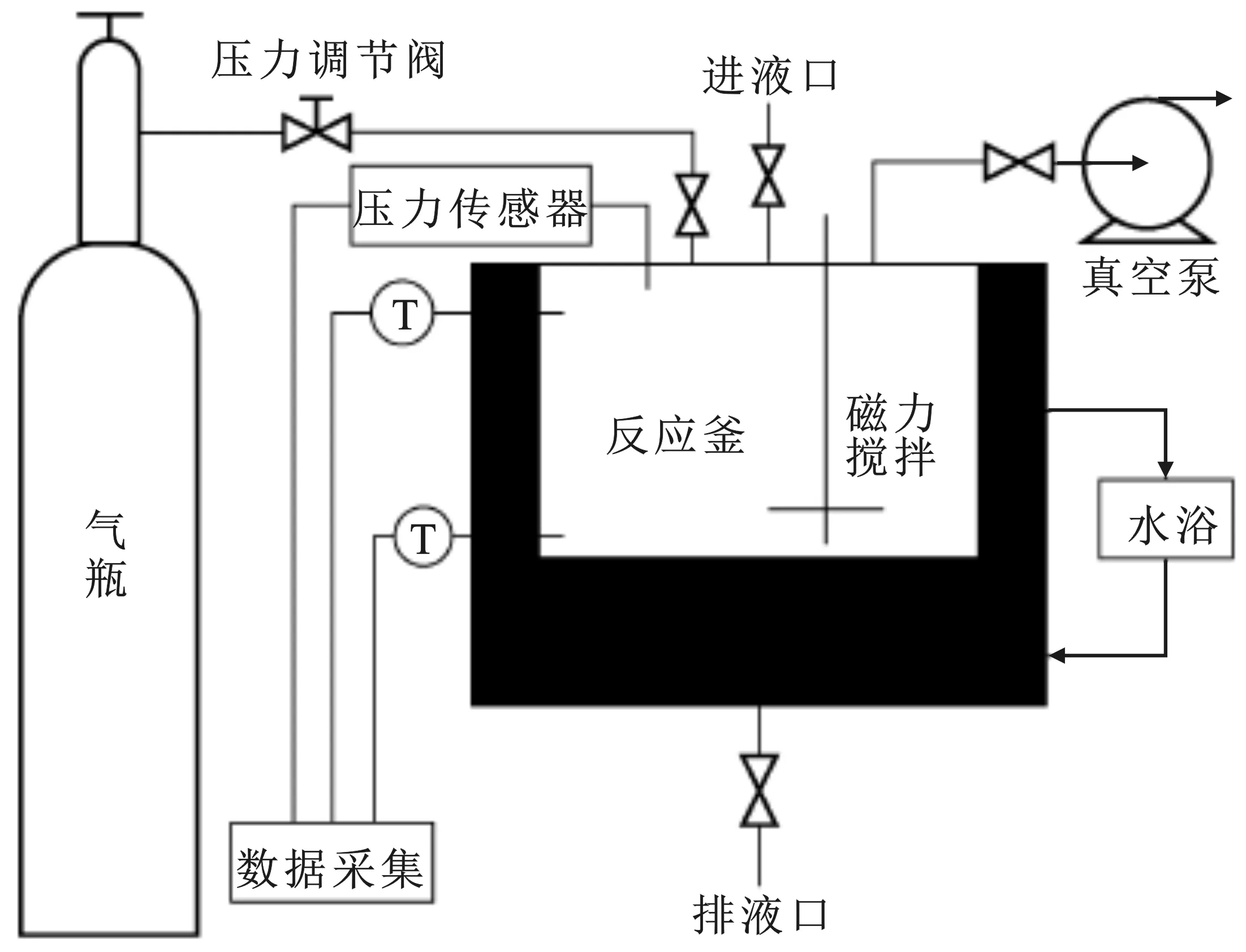
图1 KDSD-Ⅱ型水合物动力学实验装置Fig.1 KDSD-Ⅱ hydrate kinetic experimental apparatus
其中水合物在图中所示的高压反应釜中生成。反应釜材质为不锈钢,有效容积350 mL,最高工作压力25 MPa,工作温度为-10~90 ℃。反应釜内温度由恒温水浴控制,其精度为±0.1 ℃。采用两个Pt100/φ3 mm铂电阻传感器测量水浴温度,其精度为±0.2 ℃;实验压力由平衡釜控制,压力传感器测量压力值,其精度为±0.01 MPa。
1.3 实验方法
①采用去离子水反复清洗反应釜内壁并进行干燥,通氮气吹扫反应釜近2 min,之后将反应釜抽成真空,来避免残留气体和杂质干扰实验结果。②检查反应釜气密性并打开进液阀,将已调配好的SDS、APG1214溶液注入到反应釜中。③当水浴温度降至2 ℃时,将反应釜置于恒温水浴内,然后打开进气阀通入甲烷气体,当反应釜压力达6 MPa时停止。利用数据采集系统记录反应釜内温度、压力的变化,当反应釜压力在120 min内保持不变时,停止实验和记录数据。
1.4 数据处理
本实验所提到的气液比是指在一定温度和大气压强下,反应釜内气体体积与液体体积之比。公式如下:
气液比计算公式[10]:
μ=(Vr-Vb)/Vb
(1)
其中,μ为初始气液比,常数;Vb为理想液体量,mL;Vr为反应釜有效容积,mL。
通常以一定条件下的储气密度或含气率(Vg/V)来表示天然气水合物的储气能力,其公式如下:
气体消耗量计算公式[11]:
(2)
其中,P0和Pt分别为初始时刻压强和在t时刻压强,Pa;V0为实验初始气体体积,m3;T=275.15 K为实验温度,全程保持不变;z0和zt分别为实验初始和在t时刻的气体压缩因子,通过Soave-Redlich-Kwong方程迭代求得天然气的压缩因子;R为气体常数,8.314;M为水合数,6.1;ΔV表示水合物与水的摩尔体积差,m3/mol。
储气密度计算公式[11]:
(3)
其中,Vmg,Vmw分别表示为气体和水的摩尔体积,m3/mol;Vw为水的体积,m3;ΔV表示水合物与水的摩尔体积差,m3/mol。
2 结果与讨论
2.1 不同气液比实验体系对SDS促进效果的影响
孙志高等[12]在研究SDS溶液对甲烷水合物储气特性时,发现SDS溶液临界胶束浓度为300 mg/L,因此本实验在T=275.15 K,P=6 MPa条件下,研究了300 mg/L SDS溶液在不同气液比条件下,对促进水合物生成效果的影响。图2是300 mg/L SDS溶液在不同气液比条件下釜内压强变化曲线,图3是300 mg/L SDS溶液在不同气液比条件下水合物储气密度变化曲线,对比这两个图中能分析出甲烷水合物在不同气液比下的生成状况。
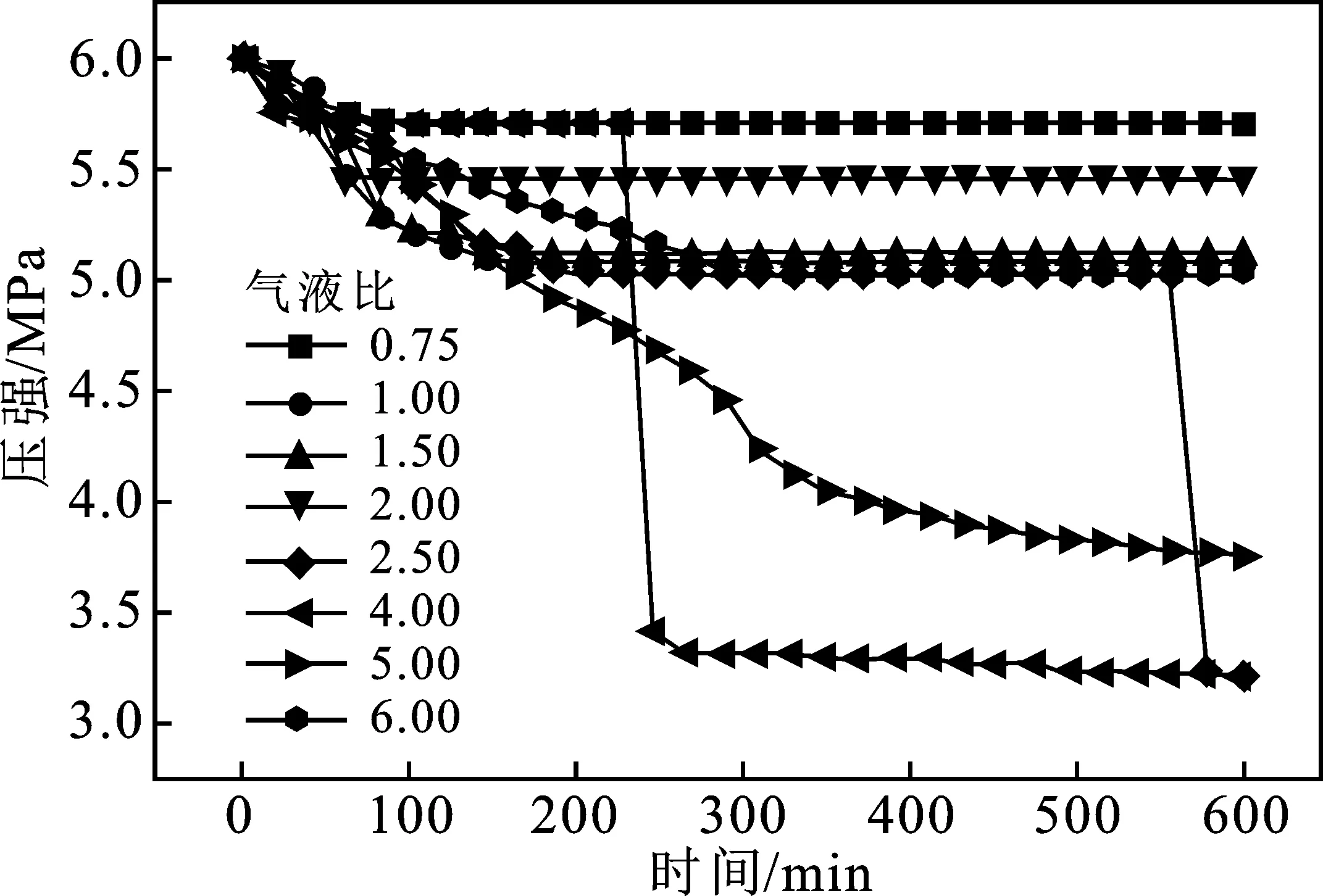
图2 300 mg/L SDS水溶液在不同气液比条件下釜内压强变化Fig.2 300 mg/L SDS aqueous solution under different gas-liquid ratio conditions pressure variation in kettle
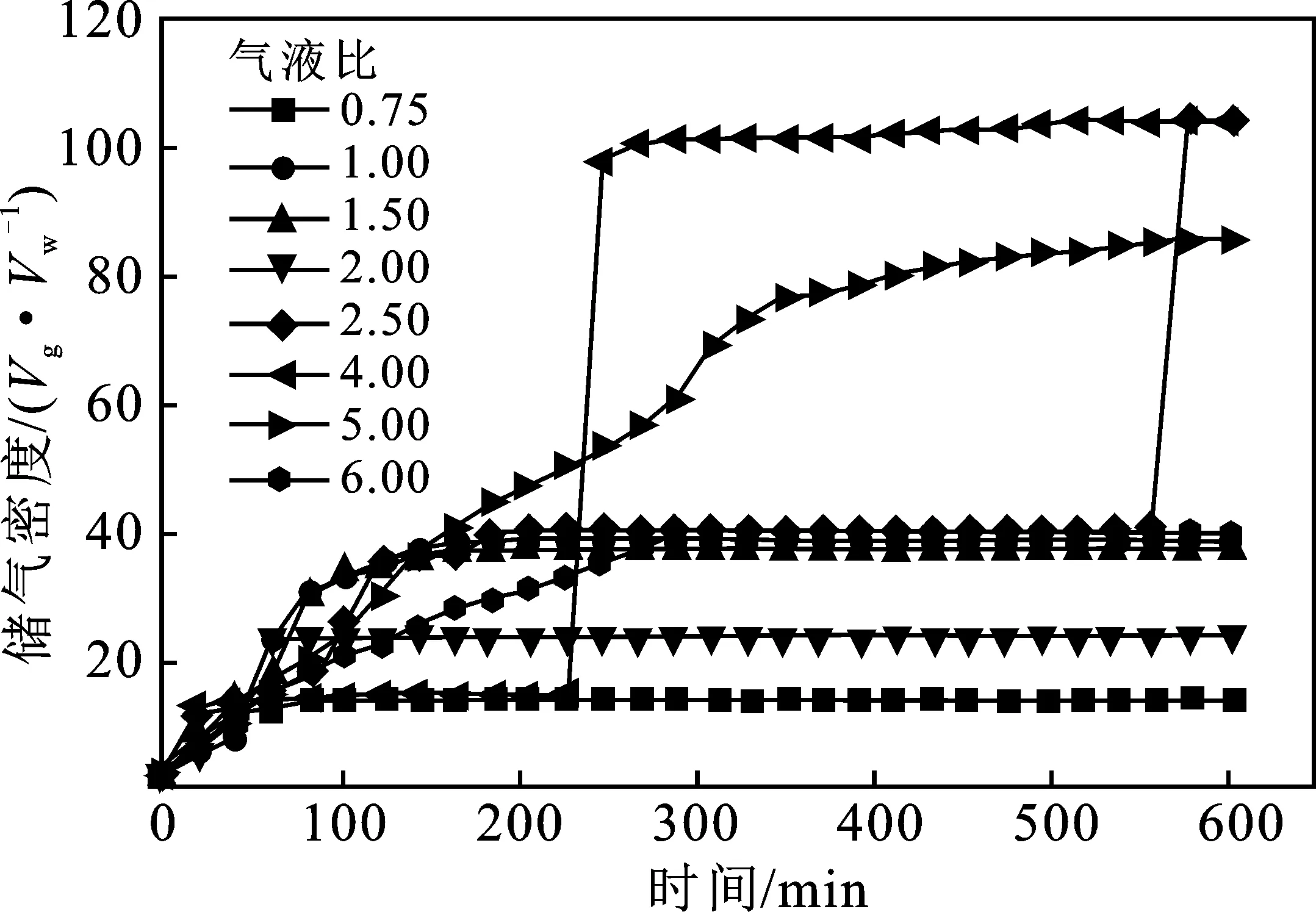
图3 300 mg/L SDS水溶液在不同气液比储气密度变化Fig.3 300 mg/L SDS aqueous solution in different gas-liquid ratio change of gas storage density
由图3可知,气液比为 2.50时促进效果明显,550~600 min釜内压强保持不变,剩余压强为 3.22 MPa,储气密度为104.6(V/V)。
当气液比为0.75和2.00时,压降变化不明显,350 min时储气密度为14.7(V/V)和24.4(V/V),与气液比为2.50相比,可以看出当初始注液量较大时,减弱了SDS的效果,降低了水合物生成量,同时也降低了甲烷水合物的储气能力。
当气液比增大时,水合物生成量逐渐增大,气液比为4.00时促进效果最为明显,由图3可知,350 min 时储气密度最大达到104.6(V/V),与2.50相比虽然生成量和储气密度相等,但是时间缩短了近300 min,说明适当地增大气液比,可以增强SDS表面活性剂的促进效果并提高水合物的生成速率。但与马贵阳等[10]相比储气密度低32%,分析其原因为实验条件的差异:本实验初始压力低于其 0.6 MPa 以及并未使用磁力搅拌器。当气液比为5.00时,水合物生成速率仅次于气液比为4.00的体系,350 min时储气密度达到75.9(V/V)。
由以上可以得出,300 mg/L SDS溶液在低气液比条件下,会减弱SDS的效果,导致水合物生成量较低。相比于低气液比条件,高气液比条件下的水合物体系更利于水合物的生成,但气液比不宜过高,增强气液比至6.00时,水合物生成速率以及生成量都显著下降。这说明最佳气液比时,水合物储气密度较大以生长速率较快。
图4是气液比为0.75,2.00和4.00条件下水合物的生成状况。

图4 气液比为0.75,2.00,4.00体系水合物生成形态Fig.4 Hydrate formation form of system with gas-liquid ratio of 0.75,2.00 and 4.00a.0.75;b.2.00;c.4.00
由图4可知,气液比为0.75和2.00条件下水合物生成效果较差,水合物表面粗糙且结构稀疏。当气液比为4.00时,水合物大量生成以及贴壁生成,表面光滑且致密。因此可以得出结论,压力与温度一定时,表面活性剂溶液超出最佳体积时,表面活性分子过多会延缓水合物的成核速率,阻碍了晶核的形成过程,抑制水合物的生成。
2.2 不同气液比实验体系对APG促进效果的影响
王海秀等[13]在研究APG溶液对天然气水合物储气密度时得出结论:APG溶液在1 200 mg/L时储气密度最大。因此本实验在T=275.15 K,P=6 MPa 条件下,研究了1 200 mg/L APG1214溶液在不同气液比条件下,对促进水合物生成效果的影响。图5是1 200 mg/L APG1214溶液在不同气液比条件下釜内压强变化曲线,图6是1 200 mg/L APG1214溶液在不同气液比条件下水合物储气密度变化曲线。由图5、图6可知,气液比为2.50时对水合物生成效果较好,诱导时间大约350 min,550~600 min釜内压强保持不变,剩余压强为 3.93 MPa,储气密度为80.1(V/V)。
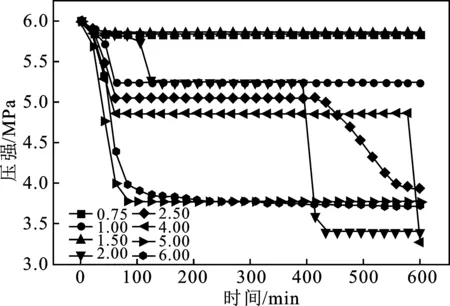
图5 1 200 mg/L APG水溶液在不同气液比条件下釜内压强变化Fig.5 1 200 mg/L APG aqueous solution under different gas-liquid ratio conditions pressure variation in kettle

图6 1 200 mg/L APG水溶液在不同气液比储气密度变化Fig.6 1 200 mg/L APG aqueous solution in different gas-liquid ratio change of gas storage density
气液比为0.75和1.50时,曲线斜率和压降基本不变,400 min时储气密度仅为9.70(V/V)和9.0(V/V),与气液比为2.50相比,可以看出当初始气液比较小时,减弱了APG1214的促进效果,导致甲烷水合物的储气密度与生成量都大幅降低。
当气液比增大时,水合物生成量逐渐增大,气液比为4.00时促进效果最为明显,由图5可知,600 min 时储气密度最大达到102.6(V/V),与气液比2.50体系相比提高了28%,但诱导时间增加了150 min。其次是气液比为2.00的反应条件,水合物生成量仅次于气液比4.00体系,450 min时储气密度达到 98.2(V/V),较气液比2.50体系提高了23%。
当气液比为5.00和6.00时,压降变化明显,100 min时储气密度最大达到85.3(V/V)和 80.4(V/V),与气液比2.50体系相比储气密度相差不大,但反应时间缩短了近450 min。由以上可以得出,在气液比不高于2.00时,APG1214的促进效果会减弱,水合物生成量会降低。高气液比相比于低气液比体系更利于水合物的生成,当气液比增加至6.00时,水合物生成速率大幅提升。这说明适当地增大气液比,能提高APG1214的促进能力以及水合物的生成速率。
图7是气液比为0.75,2.00和4.00条件下水合物的生成状况。

图7 气液比为0.75,2.00,4.00体系水合物生成形态Fig.7 Hydrate formation form of system with gas-liquid ratio of 0.75,2.00 and 4.00a.0.75;b.2.00;c.4.00
由图7可知,气液比为0.75和2.00条件下水合物生成效果较差,水合物结构稀疏,从而在拆卸反应釜时,大部分水合物在排气口处随浆液喷出。与其相比气液比为4.00时,水合物生成量较大且结构致密,反应釜内水合物贴壁生成,中间为空心。与2.1节SDS表面活性剂实验体系做对比,可以得出共同的结论,在压力与温度一定的条件下,选取合适的气液比,会加强APG1214对水合物的促进影响,缩短诱导时间,提升水合物的生成速率以及水合物的储气量,使水合物分布均匀且结构致密。
2.3 不同气液比实验体系对复配溶液促进效果的影响
在T=275.15 K,P=6 MPa条件下,本实验研究了300 mg/L SDS溶液与1 200 mg/L APG1214溶液的复配溶液在不同气液比条件下,对促进水合物生成效果的影响。图8是复配溶液在不同气液比条件下釜内压强变化曲线,图9是复配溶液在不同气液比条件下水合物储气密度变化曲线。
由图8、图9可知,气液比为 2.50时为促进,150~200 min釜内压强保持不变,此时压强为 4.72 MPa,储气密度为51.9(V/V)。
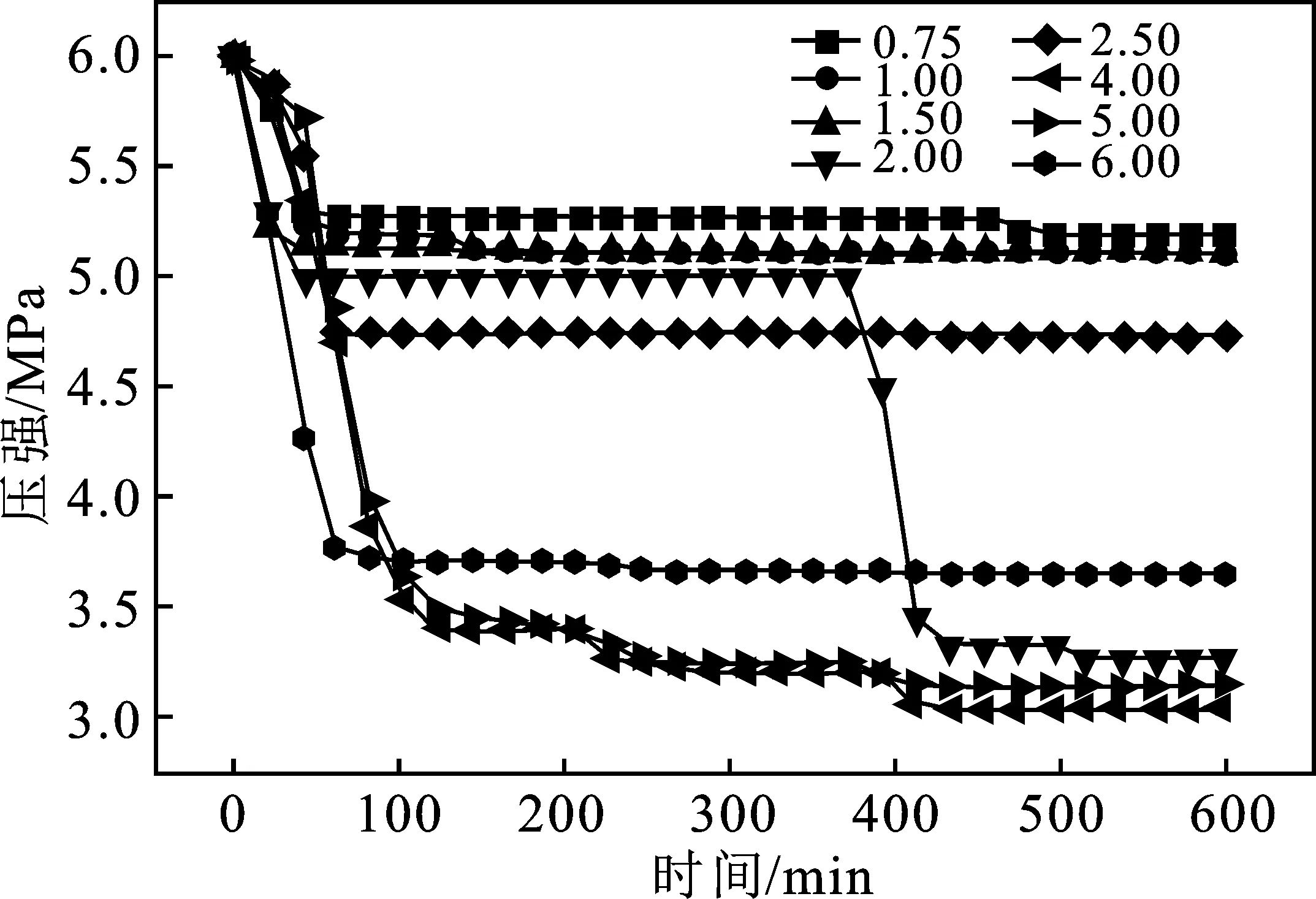
图8 复配溶液在不同气液比条件下釜内压强变化Fig.8 Compound aqueous solution under different gas-liquid ratio conditions pressure variation in kettle
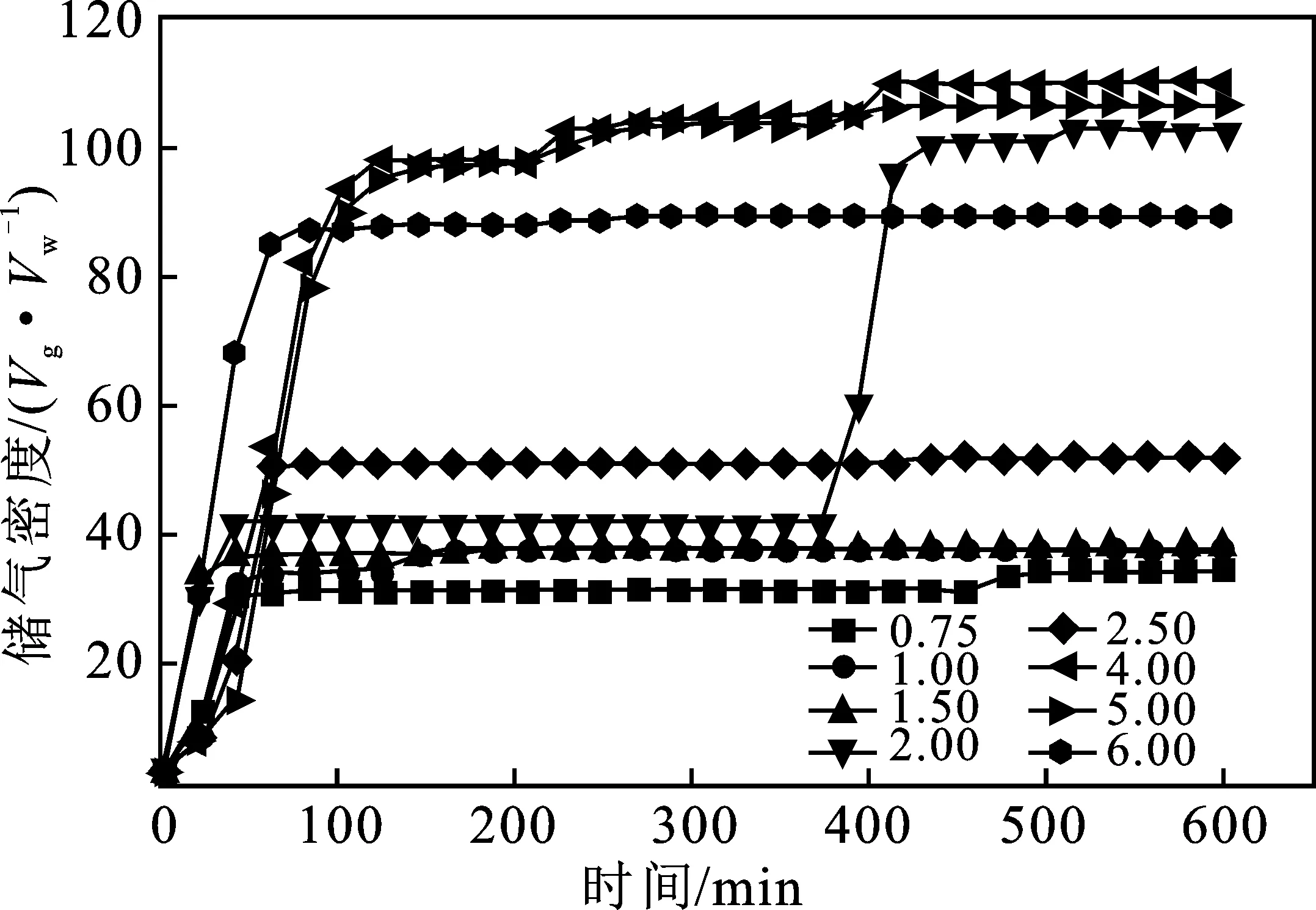
图9 复配溶液在不同气液比条件下储气密度变化Fig.9 Compound aqueous solution in different gas-liquid ratio change of gas storage density
当气液比为0.75和1.50时,压降变化不明显,450 min时储气密度为34.5(V/V)和37.9(V/V),与气液比为2.50相比,可以看出当初始注液量较大时,降低了表面活性剂的效果,但相比于单一的SDS溶液和APG1214溶液,储气密度是有提高的,这表现为复配溶液的全面增效作用。当气液比达到 2.00 时,水合物生成量较大,但诱导大约为 300 min,500~550 min釜内压强保持不变,此时压强为3.26 MPa,储气密度为102.9(V/V)。
当气液比增大时,水合物生成量逐渐增大,气液比为4.00时促进效果最为明显,由图8可知,400 min 时储气密度最大达到110.2(V/V),与气液比2.50体系相比大幅提高。其次是气液比为 5.00的反应条件,压降曲线与4.00体系近似重合,400 min 时储气密度最大达到106.9(V/V)。
当气液比为6.00时,压降变化明显,水合物生成速率大幅提高,50 min时实验基本结束,储气密度最大达到89.7(V/V)。由以上可以得出,复配溶液体系在气液比低于2.00条件下,促进效果较差,仅有少量水合物生成。在气液比高于2.50条件下,促进效果大幅提升,不仅水合物的生成速率得到提高,水合物的储气量也大幅提升。这表明复配溶液体系在高气液比条件下的促进效果要优于低气液比。
图10是气液比为0.75,2.00和4.00条件下水合物的生成状况。

图10 气液比为0.75,2.00,4.00体系水合物生成形态Fig.10 Hydrate formation form of system with gas-liquid ratio of 0.75,2.00 and 4.00a.0.75;b.2.00;c.4.00
由图10可知,气液比为0.75时,水合物生成量较少且结构不稳定,气液比为2.00和4.00水合物大量生成,且中间为空心,可观察到反应釜内泡沫丰富,这是APG1214溶液的性能,水合物形状也与单一APG1214溶液所生成水合物形状类似,因此可以表明,在复配溶液体系中,1 200 mg/L APG1214溶液对水合物形状的作用要优于300 mg/L SDS溶液。
3 机理分析
水合物的生成速率不受水合物的结晶过程所控制,而是受气体从气相主体的传质控制,即水合物生成过程是一个传质现象[14]。高气液比相对于低气液比体系单位体积的溶液所对的天然气的量较多,气液接触更频繁,天然气会在溶液中快速溶解逐渐达到过饱和,促使液相与气相快速形成水合物晶核,使薄弱的水合物笼型结构趋近于稳定,变成稳定的天然气水合物。因此,在APG1214溶液实验中适当地提高气液比,从而提高水合物的生成速率。
水合物的稳定性取决于其笼形孔穴被占有的百分比[15],因此在最佳气液比条件下的水合物较稳定且储气密度较大。当低于最佳气液比时,生成的水合物中会含有空晶核或缝隙水。当高于最佳气液比时,表面活性剂溶液所提供的晶核较少,导致生成量降低。
在实验中发现,在以316不锈钢为材料的反应釜中,SDS溶液和APG1214溶液所生成水合物的位置均在金属壁面上且中间为空心结构。BOTIMER等[16]和GAYET等[17]均在研究SDS溶液对水合物生成影响中发现水合物贴壁生成且做出解释:认为SDS改变了水合物的成核位置,在金属壁面与溶液和甲烷气体三相交界处成核,随着晶核数量的增多,使金属壁面形成了类似多孔介质的环境,SDS溶液由于多孔介质的毛细作用迁移至金属壁面,导致了贴壁生成的现象。
在本实验中使用的APG1214溶液为非离子表面活性剂,由于非离子表面活性剂分子在水中不电离,因此不考虑其与金属壁面的静电作用。但其也会在固-液界面发生吸附现象。对于表面活性剂在固-液界面的吸附等温线可分为三种[18],分别为L型、S型、LS型(图11)。此吸附过程可分为五个阶段,在第一阶段,APG1214分子直接通过范德华力与金属壁面作用被吸附[18]。第二阶段,由于在金属壁面上吸附的APG1214溶液浓度开始增大,吸附APG1214分子的量也开始上升,达到第一平台吸附值。第三阶段,当吸附APG1214溶液浓度略低于其cmc(临界胶束浓度)时,吸附APG1214分子的量急剧上升。第四阶段,在金属壁面上的APG1214分子发生疏水缔合,形成胶束或半胶束从而使吸附量再次上升。第五阶段,当金属壁面吸附APG1214溶液浓度达到其cmc时,溶液中会出现大量胶束,吸附APG1214分子量开始不再变化,吸附过程达饱和状态。此吸附等温线为LS型。
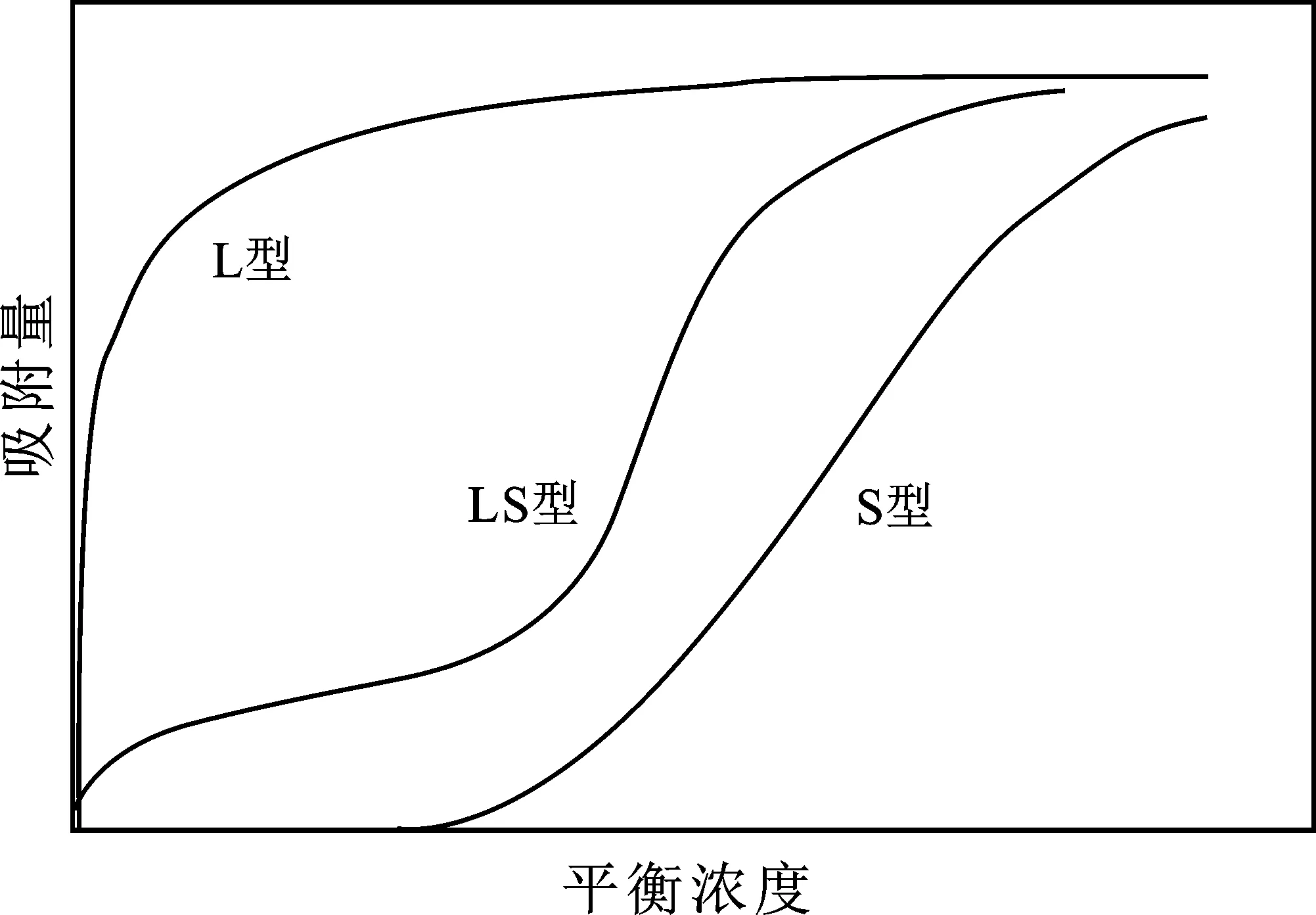
图11 表面活性剂在固液界面吸附等温线的类型Fig.11 Types of adsorption isotherms of surfactants at solid-liquid interface
以SDS与APG1214的复配溶液作为水合剂时,效果强于单一溶液。APG1214溶液与SDS溶液两者复配,溶液中会形成混合胶团,APG1214分子进入混合胶团中会减弱SDS溶液中离子间的作用力[19],而且由于两者疏水链间的缔合会更容易形成胶团,使混合溶液的临界胶束浓度降低。由于SDS与APG1214有良好的配伍性,因此在两者复配时,混合溶液的表面活性会提高,cmc及表面张力会降低[20]。因此会加强气液的传质,表现为全面增效作用。
4 结论
本实验研究了不同气液比下300 mg/L SDS与1 200 mg/L APG1214溶液对生成甲烷水合物的影响,并分析相应的机理,得出以下结论:
(1)SDS溶液在不同气液比下对生成甲烷水合物的影响不同,4.00为最佳气液比,此条件下储气密度最大,约为104.6(V/V)。在压力与温度一定的条件下,当SDS溶液超出最佳体积70 mL(4.00)时,表面活性基团过多会延缓水合物的成核速率,阻碍了晶核的形成过程,抑制水合物的生成。
(2)APG1214溶液在不同气液比下对生成甲烷水合物的影响不同,综合考虑生成速率和气体消耗量,最佳气液比为5.00。适当地增大气液比,会增强APG1214溶液对水合物的促进影响以及提升水合物的生成速率和储气量。
(3)不同气液比条件下复配溶液对生成甲烷水合物的影响不同,4.00为最佳气液比,最大储气密度约为110.2(V/V)。复配溶液体系在同一气液比条件下的促进效果要优于单一的溶液体系,是因为复配降低了溶液的表面张力以及cmc,因此加强气相和液相的传质过程,进而促进甲烷水合物的形成。
(4)在复配溶液体系中,不同单一的表面活性剂溶液对水合物生成的影响有所不同。SDS水溶液体系中,气液比为4.00促进效果最佳。APG1214水溶液体系中,最佳气液比为5.00。在其复配溶液体系中,气液比4.00为最佳。因此从离子的角度来看,在复配溶液体系中,阴离子表面活性剂对水合物的影响要优于非离子表面活性剂。

