固相反应法制备纳米氧化铜及其光催化性能研究
苗征,朱绒霞,栾瑞昕
(空军工程大学 基础部,陕西 西安 710051)
纳米CuO粒子具有大比表面积[1]、表面原子配位不全[2]、粒子表面与内部原子键态[3-5]不同等特点。这令其在光吸收[6]、化学活性[7]和催化剂[8]等方面体现出非比寻常的特性。一直以来,其研究都备受学者关注[9-10]。目前,纳米CuO的制备方法主要有液相法[11]、固相法[12]、电化学法[13]等。其中,以液相法研究较多[14-15]。
本文以CuSO4为原料,采用固相反应法制备纳米CuO,研究纳米CuO粉体在太阳光照射下对有机染料的降解过程。
1 实验部分
1.1 试剂与仪器
硫酸铜、氢氧化钠、无水乙醇、甲基紫均为分析纯;聚乙二醇600(PEG600),化学纯。
JB-3磁力加热搅拌器;YZ-360DB超声清洗器;721可见分光光度计;D/max-3B型X射线衍射仪;HT7800型透射电镜。
1.2 纳米CuO的制备
取NaOH固体5 g,CuSO4·5H2O固体5 g,依次置于玛瑙研钵中,浅蓝色反应物中立即有黑色物质生成。取研杵,充分研磨至其颜色完全变黑。用超声波分散的同时,交替用去离子水与无水乙醇洗涤2次。过滤,烘干,得纳米CuO。
1.3 纳米氧化铜的光催化活性研究
量取10 mg/L甲基紫溶液50 mL,置于烧杯中,加入CuO 0.025 g,设置空白对照组。把磁力搅拌子放入烧杯后用封口胶封口,防止溶液挥发影响浓度变化。将烧杯置于搅拌器上,于暗处反应24 h。取出少量上层溶液,离心,用可见分光光度计在 578 nm 波长下测吸光度,记为C0。剩余溶液接着在太阳光下光照,光照达到5个时间点(1,2,3,4,5 h)时分别取上层清液,在波长578 nm处测吸光度,记为Ca。计算甲基紫的降解率(η)。
η=(C0-Ca)/C0×100%-Cb
式中C0——样品组暗反应后的初始浓度,首次取样浓度,mg/L;
Ca——样品组光照反应后的染料浓度,mg/L;
Cb——光照反应时染料自身降解的降解率,%。
2 结果与讨论
2.1 纳米CuO的制备条件
2.1.1 原料配比的影响 取CuSO4·5H2O 2.5 g(已预先研磨),超声波振荡5 min。分别加入NaOH颗粒1 g(CuSO4·5H2O与NaOH摩尔比1∶2.5,摩尔分数过量25%)和1.4 g(CuSO4·5H2O与NaOH摩尔比1∶3.5,摩尔分数过量75%),按上述方法进行实验。用TEM检测产物,结果见表1。

表1 不同反应配比对产物的影响Table 1 Effect of different reaction ratio on the product
由表1可知,随着CuSO4·5H2O∶NaOH的比例由1∶2.5增至1∶3.5,CuO的分散度改善。由文献[12]可知,最终产物CuO,是由NaOH与Cu盐首先生成Cu(OH)2,由Cu(OH)2脱水生成。反应一开始,CuSO4·5H2O与NaOH溶解,生成少量H2O,并放出热量。这部分热量使Cu(OH)2能够迅速分解(吸热反应)。随着CuSO4·5H2O∶NaOH比例的增大,颗粒间的局部接触不均一增强。
2.1.2 超声波分散时间的影响 取预先研磨的CuSO4·5H2O 2.5 g,NaOH颗粒1.4 g,分别用超声波振荡5,8,10 min。然后进行实验,用TEM检测产物,其结果如下:
开始超声后,随着时间增至8 min,颗粒粒径分散程度有所增加。而时间超过8 min,分散程度增加的趋势越来越小,且分散时间为5 min和10 min的粒径大小几乎相同。可见并不是分散时间越长,颗粒就越散。
据分析[12],产物CuO颗粒间存在着软团聚和硬团聚。软团聚由分子间范德华力和库仑力引起,硬团聚即化学键的作用。通过超声波对产物CuO施加机械能,用来阻止软团聚。随着软团聚减弱,硬团聚仍然存在,这是无法用超声波分散的方法来破坏的。因此,当软团聚的减弱达到临界点后,继续超声分散,颗粒的分散性改变不大。
2.1.3 表面活性剂用量的影响 取预先经过研磨的CuSO4·5H2O 2.5 g,NaOH颗粒1.4 g,分别超声波振荡5 min,放入研钵,依次加入0.01 g、0.02 g (占反应物质量总数的0.5%)、0.03 g聚乙二醇600,按上述实验方法进行实验,用TEM检测产物,结果如下:
加入不同质量百分数的聚二乙醇600后,获得CuO的粒径大小在40~60 nm之间。当其加入量为0.02 g (0.5%)时,产物的粒径最小,约为40 nm。
由上可知,最佳反应物配比为摩尔比n(CuSO4)∶n(NaOH)为1∶3.5,超声波分散时间为8 min,表面活性剂聚乙二醇600的用量为0.5%。
2.1.4 样品的表征与分析 图1为纳米氧化铜产物的XRD图。
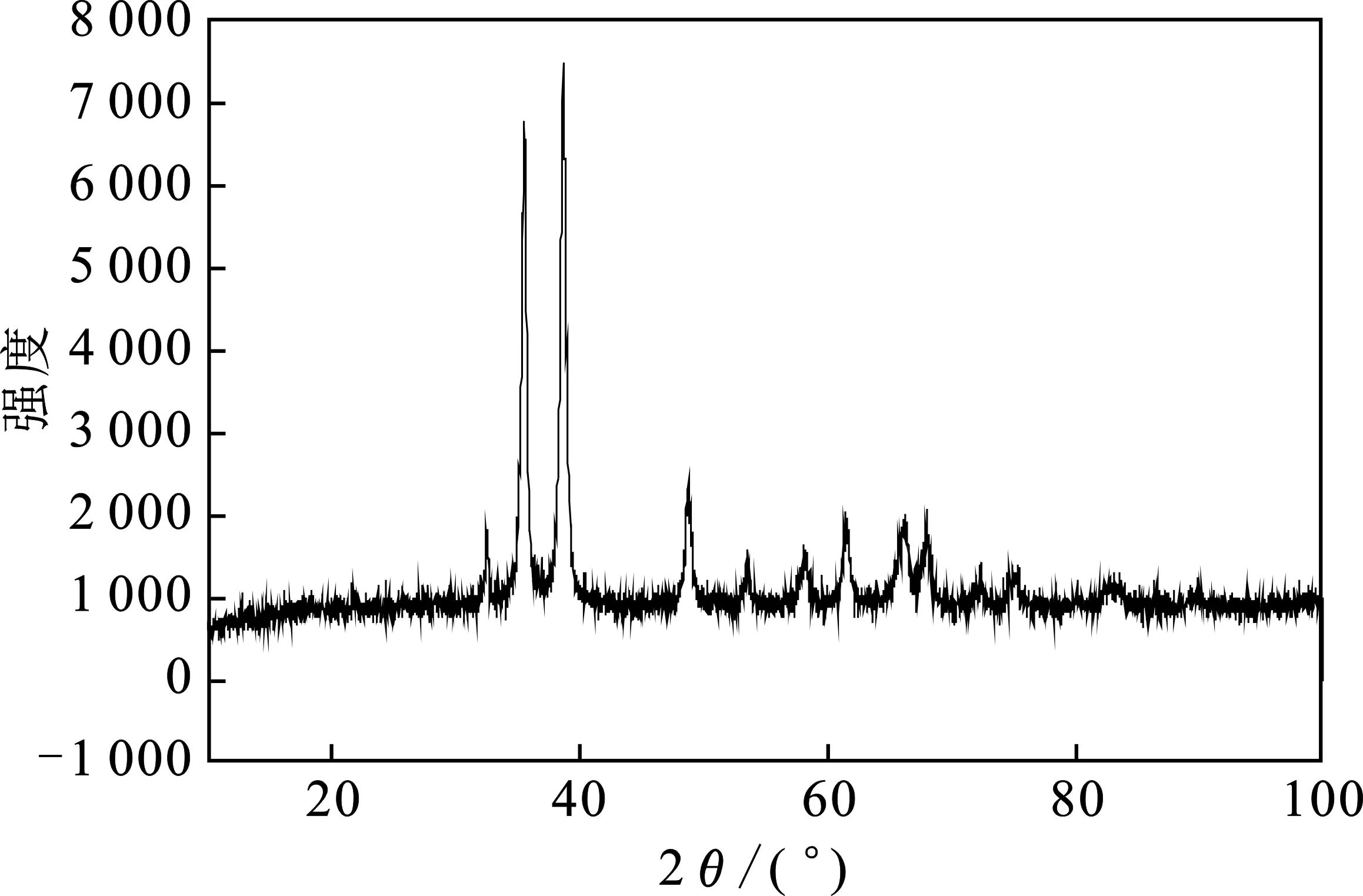
图1 固相反应产物CuO的XRD图Fig.1 XRD diagram of CuO by solid-state reaction
通过与标准CuO的XRD图进行对照分析,证明产物CuO晶形完整。由图1可知,产物衍射峰尖锐,没有出现杂质峰,且宽化明显,表明产物晶形单一,粒径较小,结晶性良好。
2.2 甲基紫的光催化降解
光照条件下,甲基紫与CuO的反应结果见图2。
由图2可知,纳米CuO有较好的光催化活性,对甲基紫的降解率可达70%。
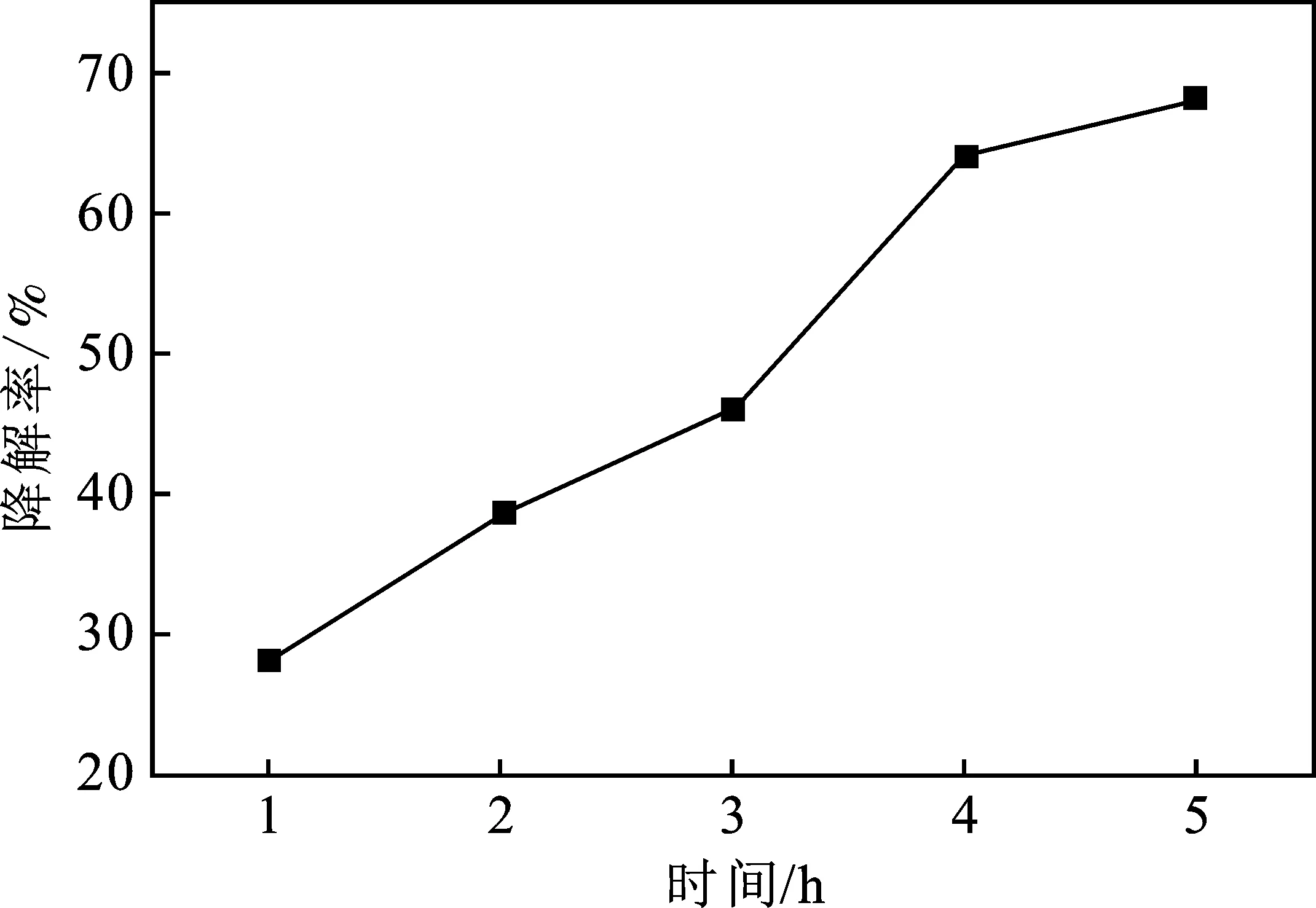
图2 固相反应产物CuO的光催化降解图Fig.2 Photocatalysis degradation of CuO by solid-state reaction
3 结论
(1)采用固相反应法制备纳米CuO的最佳反应条件为:摩尔比n(CuSO4)∶n(NaOH)为1∶3.5,超声波分散时间为8 min、表面活性剂PEG600的用量为0.5%。固相反应法工艺简单,产物粒径均匀,同时,可减少团聚现象。
(2)纳米氧化铜有较好的光催化活性,浓度 10 mg/L 的甲基紫溶液50 mL中,加入CuO 0.025 g在太阳光下光照5 h时,有机染料甲基紫的降解率可达70%。

