肛周胃肠间质瘤1例
王浩,范小华,梁学敏,张思奋
胃肠间质瘤(gastrointestinal stromal tumors,GIST)是一类独立起源于胃肠道原始胃肠道间质干细胞并呈非定向分化的消化道间叶肿瘤,属于消化道间叶性肿瘤[1]。按其在胃肠道发生率高低排序为胃、空肠、回肠、十二指肠、直肠、结肠;发生于肛周的GIST极其罕见,仅占直肠肛门间叶来源肿瘤的3%[2]。我科于2020年7月收治1例肛周GIST患者,穿刺活检明确诊断后行肛周肿瘤切除术+外括约肌吻合术+肛门成型术,手术效果良好,现报道如下。
1 病历资料
患者女性,66岁,因“发现右侧肛周包块1年,排便困难1月”就诊。1年前无明显诱因发现右侧肛周包块,无疼痛等特殊不适,呈进行性增大,未予诊治。1月前开始出现排便困难,遂至门诊就诊并收入院。入院专科检查(膝胸位):(视诊)肛周未见瘘口、裂口,皮肤未见明显异常;(指诊)肛管及直肠下段7~11点位可触及肠壁外一巨大肿块,质韧,直肠肛管明显受压,肛门收缩可,指套无血染。入院查血常规、肝肾功、凝血、CEA、CA19-9、AFP均正常,心电图、胸片、腹部彩超未见明显异常。盆腔MR平扫+增强提示:肛管-会阴右外侧(耻骨直肠肌及肛管外括约肌外侧)局部见范围约6.1 cm×4.4 cm的椭圆形软组织块状影,信号欠均匀,T1W1序列呈等信号,T2W1序列呈等稍高信号,中央见斑片状长短T1长短T2信号影,边缘清晰,并见长T1短T2包膜影,DW1序列呈不均匀,明显高信号,ADC呈低信号改变,增强后较明显,不均匀及延迟强化,临近肛管及周围肌肉受压,盆腔未见肿大淋巴结。后在腰麻下行超声引导穿刺活检,术后病理提示:梭形细胞肿瘤,结合免疫组化,符合胃肠道间质瘤。免疫组化结果:DOG1(+),CD117(+),CD34(+),SMA(-),Desmin(-),S-100(-),Ki67(3%+),SDHB(未见表达缺失),STAT6(-),CK(-)。继续完善胸腹部CT平扫+增强:未见胸腹部肿瘤及转移。完善围手术期准备后在腰麻下行手术治疗,距右侧肛缘作弧形切口;探查见:肿物侵犯右侧坐骨直肠间隙,外括约肌,与直肠壁分界尚清;超声刀离断部分外括约肌,完整切除肿物,放置T管引流,外括约肌重叠U形缝合,逐层缝合切口。术后病理:肿瘤大小6.2 cm×5.3 cm×4.0 cm,GIST亚型为梭形细胞Spindle cell,核分裂>5个/50个高倍视野,灶性坏死,包膜完整;免疫组化示DOG1(+),CD117(+),CD34(+),SMA(-),Desmin(-),S-100(-),SDHB(未见表达缺失),STAT6(-),CK(-),Ki67(约2%+)。提示梭形细胞间叶源性肿瘤,符合胃肠道间质瘤,高危险度。患者术后伤口恢复情况良好,排便通畅,控便能力正常。手术2周后,患者来我科门诊复诊,伤口恢复良好。结合术后病理结果,患者于2020年9月开始口服甲磺酸伊马替尼(剂量为 400 mg/d),继续门诊随访至2021年3月,局部切口愈合良好,肛门控便能力正常。
2 讨论
肛周GIST非常罕见,目前国内外文献多为个案报道[3]。GIST与其它间叶组织来源的肿瘤(平滑肌瘤、平滑肌肉瘤、平滑肌母细胞瘤、神经鞘瘤和神经纤维瘤)的临床表现、形态学、免疫表型相似,并无特异性,鉴别困难。但GIST免疫组化通常为CD117、CD34或DOG1表达阳性[4],其中CD117阳性率为94%~98%,DOG1阳性率为94%~96%[5],CD34阳性率为70%[6]。因此,在临床工作中工作中,推荐联合采用上述3项免疫组化标记物进行诊断。
GIST术前活检的原则[7]:评估手术能够完整切除且不会明显影响相关脏器功能者,可直接行手术切除;如果需要进行术前治疗,应行活检以明确诊断。但活检可能引起肿瘤的破溃、出血,增加肿瘤播散的危险性,应当慎重。尽量通过胃肠腔穿刺,以减少肿瘤针道转移和破裂种植的风险。本例病变活检前无法评估手术效果,故术前进行穿刺活检。考虑肛周或直肠的GIST病灶,推荐经直肠(或肛管)穿刺活检;但对于女性,发生在直肠阴道隔之间的病变,专家共识并无涉及,笔者仍推荐经直肠(或肛管)穿刺活检,采用超声引导下空芯针穿刺,避免直肠阴道瘘及破裂种植;非发生在直肠阴道隔之间的病变,也可在双合诊引导下穿刺,穿刺针避免朝向直肠阴道隔。
肛周GIST经肛门切除是损伤最小的方法之一,但受距齿状线的距离的限制[8]。经骶尾部切除术对直肠后壁 GIST 有效,但术后发病率高,其中 21%的患者可能发生瘘管[9]。据报道,在 肛周GIST中,在R0 和 R1 手术 之间的无复发生存率没有明显差异[10]。 因此,我们应该从保肛的角度选择最合适入路的手术方法。肛周GIST遵循以下手术原则:肿瘤病变局限和最大径线≥2 cm,原则上应手术行完整切除[7]。本例患者病灶孤立,术前检查未见远处肝转移,估计能达到R0切除且手术风险不大(术后证实为R0切除),不会严重影响肛门排便功能,选择手术切除。近年来,随着靶向药物的引入及应用,认为只要考虑到影响功能的问题,就需先行药物治疗,再考虑保留功能的手术,这个原则也成为治疗的总原则。因此,今后保肛手术将越来越多。但并不是所有患者均对药物有效,笔者认为,以下情况仍考虑行经腹会因联合切除术:①药物治疗后肿瘤未见缩小;②肿瘤巨大,距离肛缘5 cm以下,且与直肠壁(或肛管)分界不清;③复发病例,经过一二线药物治疗后未见改善,影响排便时。
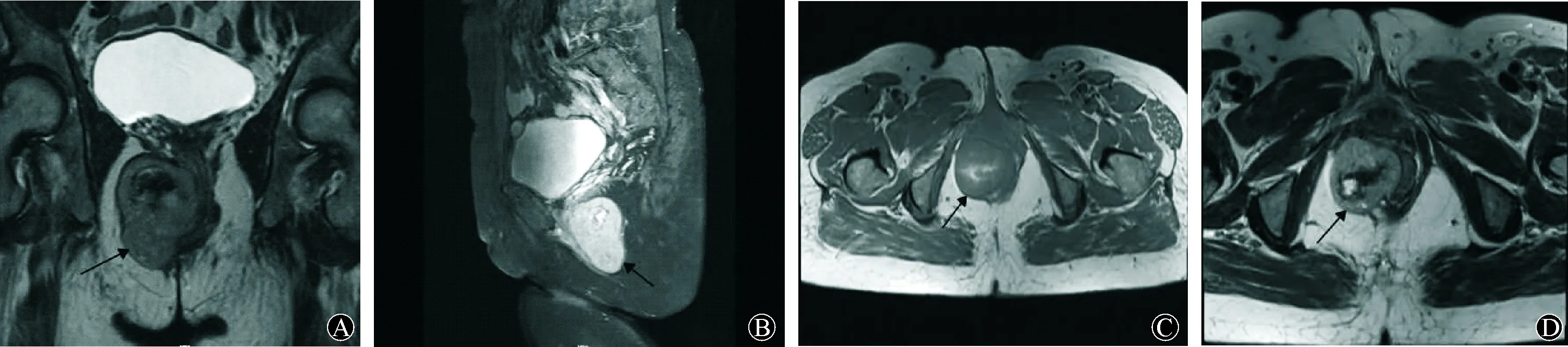
图1 肛周磁共振成像 A冠状位显示肛管-会阴右外侧占位;B:矢状位见占位位于耻骨直肠肌外侧,直肠肛管明显受压;CD:T1W1序列呈等信号,T2W1序列呈等稍高信号,中央见斑片状长短T1长短T2信号影,边缘清晰;增强后不均匀及延迟强化;盆腔未见肿大淋巴结。
GIST大体标本外观多呈粉红色或白色的蕈伞状、环状、分叶状肿块;多呈膨胀性生长,边界清楚,有假包膜,切面灰白色,编织状,质地韧或硬。GIST恶性程度高者质地细腻,鱼肉状,可有或无包膜,常见出血、坏死,并有局部邻近脏器浸润或(和)转移。GIST切面可见肿瘤呈灰红、灰白色,与肌层或黏膜层相交杂。按照原发GIST切除术后危险度分级[11],本例患者肿瘤横径>5 cm,核分裂>5个/50个高倍视野,危险度分级高。根据专家共识意见[12],给予患者甲磺酸伊马替尼(剂量为 400 mg/d,治疗时限:至少3年)术后辅助治疗,随访至今未见复发及转移。
肛周GIST临床罕见,临床表现特异性不强,易漏诊和误诊;以外科手术切除为主的综合治疗是肛周GIST最重要的治疗手段,根据术后危险度分级选择术后辅助治疗及治疗时限,对于所有GIST病人均应建立完整的病例档案,进行全程化管理模式的随访。

