一种基于母血浆的新型冠状病毒核酸检测体系的建立
林彭思远,杨 旭,周世豪,卜秀芬,刘激扬,贺 骏
2019 年12 月始发的由新型冠状病毒(Severe Acute Respiratory Syndrome Related Coronavirus 2,SARS-CoV-2)导致的新型冠状病毒肺炎(Corona‐virus Disease 2019,COVID-19)已成为全球突发公共卫生事件。SARS-CoV-2 隶属于β-冠状病毒属,为有包膜的单股正链RNA 病毒,是迄今为止已发现的可以感染人类的第七种冠状病毒,与严重急性呼吸综合征冠状病毒(Severe Acute Respiratory Syndrome Coronavirus,SARS-CoV)和中东呼吸综合征冠状病毒(Middle East Respiratory Syndrome Coronavirus,MERS-CoV)一样均可引起下呼吸道感染[1]。SARS-CoV 和MERS-CoV 感染的患者在过去20 年里全球累计报道已达1 万余例。相比SARSCoV 和MERS-CoV,SARS-CoV-2 具有更强的传染性,迄今为止全球已报道确诊患者超1 亿,主要传播途径为经呼吸道飞沫和密切接触。孕产妇是冠状病毒的易感人群,已有报道显示孕妇感染SARSCoV 的病死率为25%(普通人群10%),而孕妇感染MERS-CoV的病死率高达37%[2]。
现阶段COVID-19 诊断的首选方法是采集呼吸道标本,采用基于反转录的实时荧光定量PCR(RT-qPCR)技术对SARS-CoV-2 核酸进行检测,除呼吸道样本外,粪便、尿液、血液等多种类型标本中均可检测到SARS-CoV-2 核酸,国内外亦有多项针对血液样本诊断COVID-19的研究报道[3-4]。本研究开发了一种基于胎儿非整倍体无创产前检测(Non-Invasive Prenatal Testing,NIPT)的SARS-CoV-2 核酸检测技术(NIPT-SARS-CoV-2),以期在孕妇进行常规NIPT 检测的同时仅通过一管外周血实现孕妇这一易感人群的SARS-CoV-2筛查。
1 材料和方法
1.1 样本来源 选取2020 年7 月1 日-2020 年9 月30日在长沙市妇幼保健院就诊行NIPT检测的孕妇50 例,其中40 例NIPT 检测正常,10 例NIPT 检测为21、18或13三体。所有孕妇均已签署知情同意书。采集孕妇外周血10 mL,进行血浆分离,分离后的血浆编号立即放入-80 ℃冰箱中保存。将每份血浆平均分成两份,其中一份用于抽提血浆中游离DNA(cell free DNA,cfDNA),另一份用于提取SARS-CoV-2 RNA。从长沙市第一医院收集COV‐ID-19患者的SARS-CoV-2核酸标本,并签署知情同意书。所有标本均在灭活后按三级生物防护要求进行核酸抽提并逆转录储存。
1.2 cfDNA 提取 采用QIAamp Circulating Nucleic Acid Kit(德国Qiagen 公司)提取血浆中的游离DNA,然后采用qubit 核酸定量仪(美国Thermo 公司)进行定量。提取完成的cfDNA 编号后保存于-20 ℃冰箱中。
1.3 SARS-CoV-2 RNA提取与逆转录 采用QIAamp®Viral RNA Mini Kit(德国Qiagen 公司)提取血浆中的RNA,提取完成后采用Fapon RNA-seq cDNA Synthesis Kit(菲鹏生物股份有限公司)对提取的RNA进行逆转录。
1.4 文库制备 文库制备的原始模板通过将孕妇血浆cfDNA 和RNA 逆转录产物等比例混合而成。文库分为三组,正常孕妇组、三体孕妇组和模拟SARS-CoV-2 孕妇组,其中正常孕妇组10 例,由正常孕妇血浆cfDNA 和RNA 逆转录产物混合;三体孕妇组10 例,由NIPT 检测为21、18 或13 三体的孕妇血浆cfDNA 及其RNA 逆转录产物混合;模拟SARS-CoV-2 孕妇组30 例,由正常孕妇血浆cfDNA和COVID-19 患者RNA 逆转录产物混合,同时设置三个不同的病毒浓度梯度:1 400 拷贝/mL,14 000拷贝/mL,140 000拷贝/mL(分别将1 000拷贝病毒、10 000 拷贝病毒和100 000 拷贝病毒加入至700 uL正常孕妇血浆中,混匀后再进行cfDNA 提取和SARS-CoV-2 逆转录),每个浓度梯度各10 例。随后通过末端修复、加接头、PCR扩增、定量等步骤进行各组文库的构建。
1.5 高通量测序与数据分析 所有文库定量后采用DR8600 测序仪进行高通量测序,下机数据去除低质量序列后获得高质量序列,将其与人类参考基因组(hg19)进行比对,获得的BAM文件进行排序后去除PCR重复序列。使用自有NIPT分析软件进行分析,获取21 号染色体、18 号染色体、13 号染色体的Z值,从而判断是否存在21、18、13染色体三体。
与此同时,将下机后获得的高质量序列与新型冠状病毒参考基因组(NC_045512.2)进行比对,去除低比对质量的序列(比对长度不足60),统计新型冠状病毒序列数,从而判断待检样本中是否存在SARS-CoV-2。
1.6 统计学方法 不同方法产生的数据量比较使用配对t检验,数据相关性采用皮尔逊相关系数。配对t检验、皮尔逊相关系数和离散系数均使用R 3.5.1进行统计分析。P<0.05为差异有统计学意义。
2 结果
2.1 胎儿染色体非整倍体检测评估 对正常孕妇组和三体孕妇组的高通量测序数据进行NIPT分析,发现正常孕妇组10例均为阴性,三体孕妇组4例为21三体、4 例为18 三体、1 例为13 三体、1 例为21 三体合并13三体,表1。在长沙市妇幼保健院临床常规NIPT 检测的样本中随机挑选20 例样本,与本研究中的正常孕妇组和三体孕妇组的数据量进行对比分析,发现临床常规NIPT样本与本研究组中的样本检测数据量差异无统计学意义(图1,P>0.05)。
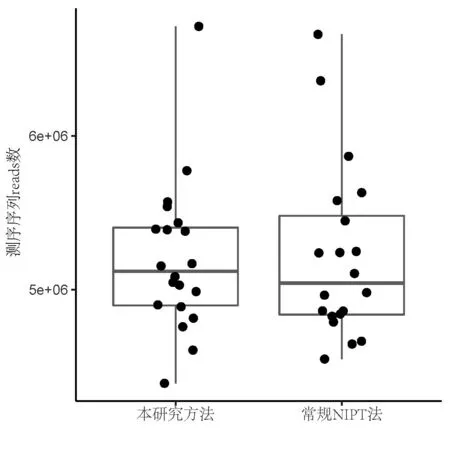
图1 临床常规NIPT样本与本研究组样本数据量对比
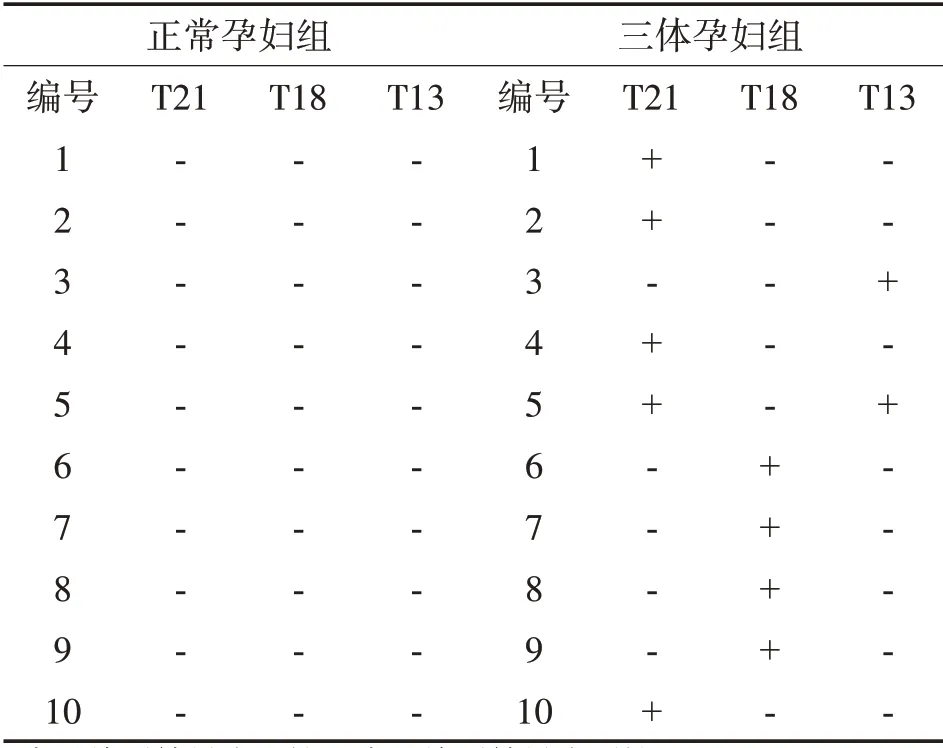
表1 胎儿染色体非整倍分析
2.2 孕妇SARS-CoV-2核酸检测评估 对正常孕妇组和模拟SARS-CoV-2 孕妇组同时进行NIPT 分析和SARS-CoV-2 分析,结果显示,模拟SARS-CoV-2孕妇组的三个浓度梯度均可检测到SARS-CoV-2核酸序列,且该组所有样本NIPT结果均为阴性,表2,正常孕妇组的NIPT 检测和SARS-CoV-2 检测均为阴性。
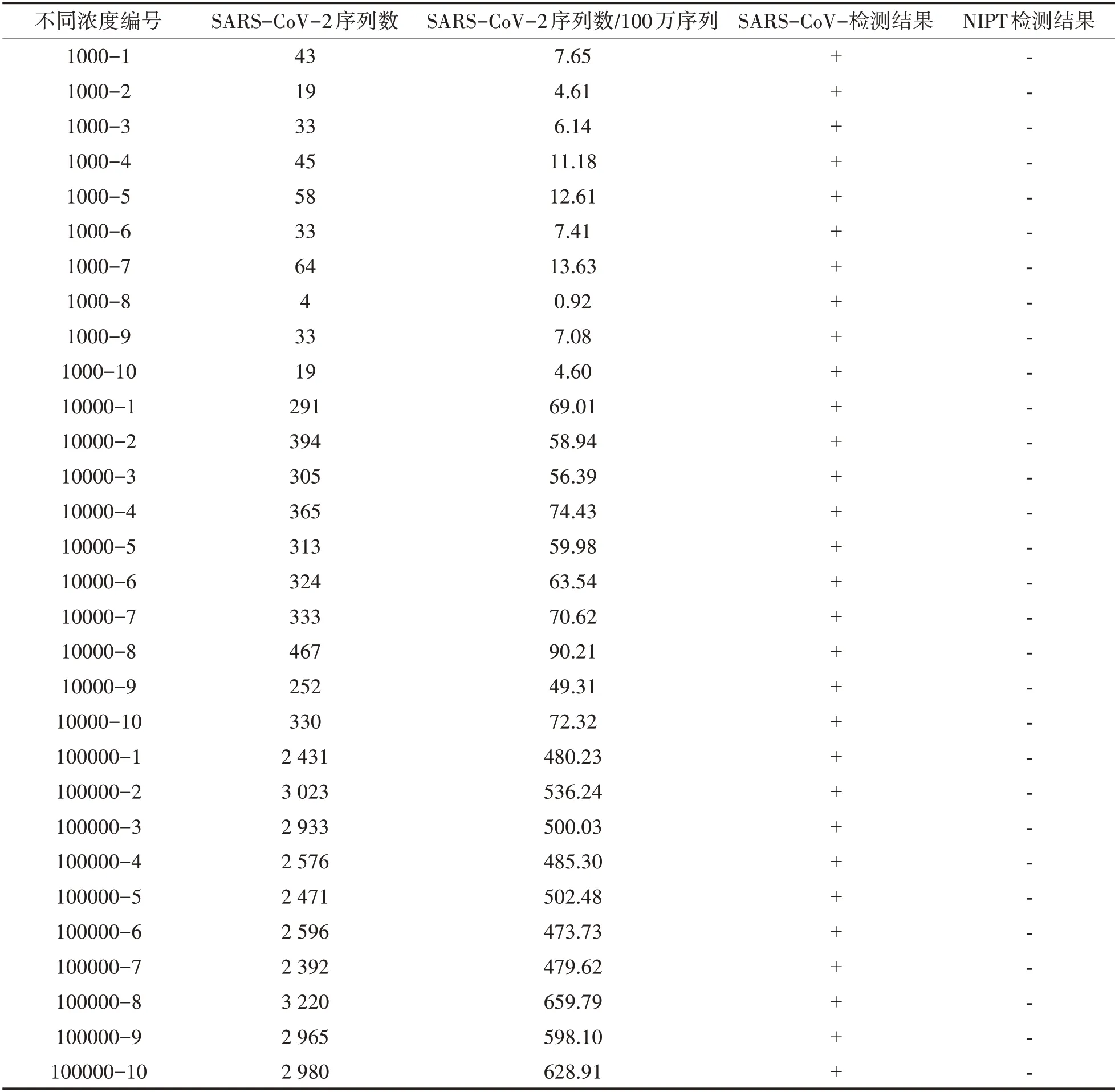
表2 模拟SARS-CoV-2孕妇组SARS-CoV-2检测及NIPT检测
2.3 检测序列数与新型冠状病毒拷贝数相关性分析 为验证该检测方法是否具有用于SARS-CoV-2定量分析的潜力,本研究进一步分析了SARS-CoV-2序列数占比与SARS-CoV-2拷贝数的关系。研究发现,随着SARS-CoV-2拷贝数的减少,病毒序列数的离散系数也随之变大(100 000拷贝组:0.107,10 000拷贝组:0.177,1 000拷贝组:0.522)。随后进一步分析了SARS-CoV-2 序列占比与病毒拷贝数的关系,发现相关系数达到0.977,提示该方法有潜力用于新型冠状病毒的定量或半定量分析,图2。
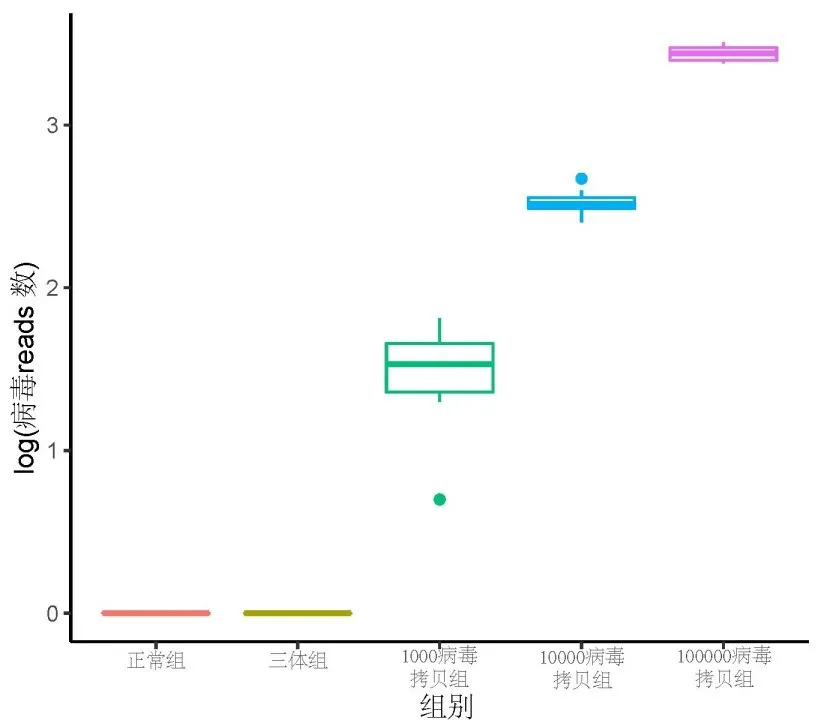
图2 新型冠状病毒序列数与拷贝数的关系
3 讨论
自COVID-19 爆发以来,陆续有无症状感染者报道出来,国家卫健委首次针对这类人群公布的数据显示,截至2020 年4 月14 日,全国累计发现无症状感染者6 764 例[5]。美国疾病控制与预防中心估计,已感染SARS-CoV-2人群中,约35%将不出现症状,且病毒传播往往发生于症状出现之前[6]。目前研究显示,无症状感染者存在传染性,且其病毒载量与COVID-19 患者相似,极有可能成为传染源造成聚集性疫情发生[7-9]。孕产妇是SARS-CoV-2的易感人群,有资料显示感染SARS-CoV-2 的孕妇更易出现并发症[2,10]。美国纽约的一项针对入院待产孕产妇的研究中显示,33 例SARS-CoV-2 检测阳性的孕妇中有高达29 例(87.9%)在入院时并未表现出COVID-19的任何症状[11],另一项针对连续入院分娩的675 名孕产妇的研究显示,10.4%的孕妇SARSCoV-2 核酸检测为阳性,其中78.6%的孕妇未表现出相应症状[10]。因此,对孕产妇这一易感人群实施全面筛查,尽早发现无症状的孕产妇SARS-CoV-2感染者将有利于其得到最优化的管理和救治。
NIPT 是一项用于准确判断孕期胎儿是否罹患染色体非整倍体综合征的产前筛查技术,已在临床广泛推广应用。本研究通过对常规NIPT 方法进行优化改良后开发的NIPT-SARS-CoV-2技术,仅采集一份外周血标本即同时实现NIPT 检测和孕妇SARS-CoV-2核酸检测,达到不额外增加产检项目即实现孕妇群体SARS-CoV-2无症状感染者筛查的目的,从而对SARS-CoV-2 阳性孕妇提前采取干预措施,避免造成潜在的COVID-19 爆发流行。本方法在不增加常规NIPT测序数据量前提下,可以准确的对胎儿染色体非整倍体进行分析,并且可以实现病毒载量为1 400拷贝/mL的SARS-CoV-2核酸检测。
采集呼吸道标本,尤其是肺泡灌洗液等下呼吸道标本诊断COVID-19 的阳性率最高,除呼吸道样本外,粪便、尿液、血液等多种类型标本中亦可检测到SARS-CoV-2 核酸。有研究表明COVID-19 患者发病2~3 d 后即可在血液中检测到SARS-CoV-2 核酸[12],甚至有血液标本SARS-CoV-2 核酸检测阳性,但咽拭子检测阴性的病例报道[13],提示通过血液标本进行SARS-CoV-2 核酸检测是具有可行性的,且有其必要性。人体在病毒感染后,病毒入血形成病毒血症需要一段时间,但病毒死亡和降解的核酸片段极易进入外周血液,本研究结合NIPT具有高通量和高灵敏度的方法进行外周血中SARS-CoV-2核酸的检测,可以在感染早期发现病毒核酸片段,具有早期筛查出SARS-CoV-2携带者的优势。
实时荧光定量PCR(RT-qPCR)是国家卫生健康委员会发布的《新型冠状病毒感染的肺炎诊疗方案》中优先推荐采用的用于COVID-19诊断的方法,该方法可高效、快速完成病毒核酸检测,具有灵敏度高和特异性高的特点。现已注册临床使用的检测试剂盒多以病毒基因组中3 段保守基因序列为检测对象实现SARS-CoV-2 的核酸检测,但不同试剂盒的检测性能存在较大差异[14],假阴性结果常常出现,从而需要待检者反复多次检测,但多次复检仍不能解决病毒变异导致引物和探针不能有效结合而引起的假阴性。最近瑞典报道的宫内感染病例中发现母亲和新生儿感染了同一种病毒,但几天后新生儿体内病毒发生了变异,研究者认为可能与其出生后接触外部环境所引起的,病毒变异之快令人惊讶[15],这也提示对病毒进行基因测序的重要性,以避免由于病毒变异引起核酸检测的假阴性,从而导致不合理的临床处置。本研究开发的NIPTSARS-CoV-2 技术是对病毒的全基因组进行低深度测序,不光可以实现是否感染SARS-CoV-2的检测,理论上还可以发现病毒变异,阻止变异病毒的流行,降低其造成爆发流行的潜在风险。
综上所述,本研究开发的NIPT-SARS-CoV-2 技术可以在孕妇常规产检过程中,采集一管外周血即达到NIPT 检测和孕妇SARS-CoV-2 核酸检测的目的,实现孕产妇这一易感人群的SARS-CoV-2 全面筛查,保证孕妇和新生儿得到最优化的管理与救治。与此同时还有潜力用于病毒变异监测,动态跟踪病毒的变异情况,最大限度阻止变异病毒的传播。

