三色片醇提物抗补体活性物质的UPLC-Q-TOF-MS/MS 研究
秦 艳,陶佳佳,沈 赟,陈 喆,叶岩荣 (复旦大学附属中山医院药剂科,上海 200032)
补体系统是人体重要的免疫防御系统之一,是由30 多种广泛存在于血清、组织液和细胞膜表面的蛋白质组成的,具有精密调控机制的蛋白质反应系统,其主要通过3 种途径激活:经典途径、旁路途径和甘露糖结合凝集素途径。补体系统正常激活,可在靶细胞上形成膜攻击复合物,导致靶细胞的溶解,补体的这一功能在机体的免疫系统中起重要的防御和免疫监视作用,对抵御外来微生物的入侵和维持机体平衡有重要的作用。然而该系统的过度激活将释放炎性过敏毒素C3a 和C5a,具有化学诱导作用的C5a 能趋化嗜中性粒细胞、中核细胞和嗜酸性粒细胞,这些细胞释放蛋白酶和具有趋化作用细胞因子,进一步聚集T、B 淋巴细胞和其他炎性细胞,从而促进炎症反应的发生,引起系统性红斑狼疮、类风湿性关节炎、动脉粥样硬化、肾小球肾炎等[1-2]。近年来已有研究表明[3],补体系统的激活是类风湿性关节炎中慢性滑膜炎的发病因素之一。因此,抑制补体系统的过度激活可能是治疗类风湿性关节炎的重要机制之一。
三色片为复旦大学附属中山医院的院内制剂,由雷公藤、黄芪和丹参三味药材按1∶1∶1 的比例配伍组成,在临床上用于治疗类风湿性关节炎、系统性红斑狼疮、银屑病和湿疹等结缔组织疾病。我院临床医生在长期的医疗实践中总结出来的经验方,效果显著[4]。组方中雷公藤,性味辛寒,有大毒,归肝、肾经,具有清热解毒、活血化瘀、通络止痛、杀虫止痒等功效。现代研究表明,雷公藤内酯醇对大鼠脑皮质内注射β-淀粉酶后补体C1q 和C3 的表达有抑制作用,表明雷公藤对补体系统有抑制作用,目前临床上广泛用于治疗类风湿性关节炎、系统性红斑狼疮、银屑病和湿疹等结缔组织疾病[5]。组方中的黄芪用于脾肺气血或中气下陷之症、卫气虚所致表虚自汗、气虚血滞导致的肢体麻木、关节痹痛等症,可联合治疗类风湿性关节炎[6]。黄芪在治疗2 型糖尿病大鼠的研究中发现其能降低补体C3 的水平,表明其对补体系统具有一定的调节作用[7-8]。丹参是最常用的活血化瘀中药之一,具有祛瘀止痛,养血安神的功效,现代药理学研究表明其还具有保护肝脏的功能[9],可拮抗雷公藤的肝毒性。本研究通过经典途径抗补体活性测定方法筛选出三色片醇提物的乙酸乙酯部位抗补体活性最佳,并采用UPLC-Q-TOF-MS 法对该部位的化学成分进行结构表征,为三色片抗补体活性药效物质基础及治疗补体过度激活相关疾病提供科学依据。
1 仪器、试剂与材料
Tripie TOF5600+型四级杆-飞行时间串联质谱仪,配备电喷雾电离源和CDS 自动校正系统(美国Applied Biosystems 公司);Peak view2.2 和Master view1.1 数据处理系统(美国Applied Biosystems 公司);LC-30A 超高效液相色谱仪,包括高压输液泵,自动进样器,柱温箱和在线脱气机(日本岛津公司);KQ5200E 型超声清洗器(昆山市超声仪器有限公司);甲醇、乙腈(色谱纯,德国Merck 公司);甲酸(色谱纯,美国Sigma-Aldrich 公司); 蒸馏水(娃哈哈集团);三色片提取物由作者自制,现样品存放于复旦大学附属中山医院药剂科(SSP2018);补体、溶血素(自制);毛蕊异黄酮(批号:ST088101),雷公藤甲素(批号:ST020501),雷公藤内酯酮(批号:ST049901),丹参酮II A(ST014601)、黄芪甲苷(ST001601)(纯度≥ 98%,均购自上海斯丹德生物技术有限公司)。
2 方法
2.1 三色片醇提物及各极性部位的制备
雷公藤、黄芪和丹参三味药材按1∶1∶1 配伍,其中,黄芪和丹参加6 倍量的水浸泡2 h 后,煎煮2 次,第一次1.5 h,第二次加水4 倍量煎煮1 h,煎液滤过,合并滤液并浓缩至相对密度为1.10~1.20(70 ℃),加入2 倍量的乙醇,静置沉淀24 h,取上清液备用。雷公藤分别加4 倍量的乙醇加热回流2 次,每次1.5 h,合并提取液,滤过,加入上述备用药液,混匀,回收乙醇至无醇味,浓缩后即得三色片醇提物,经现有的质量标准检验为制备三色片制剂合格的提取物。精密称取三色片醇提物2.0 g,置于100 ml 萃取瓶中,加25 ml 蒸馏水溶解后,用等量的石油醚、乙酸乙酯和正丁醇进行萃取,浓缩干燥后,放冷至室温,得到三色片醇提物的石油醚部位0.36 g,乙酸乙酯部位0.42 g,正丁醇部位0.56 g 和水溶性部位。
2.2 经典途径的抗补体活性测定
取各极性部位样品2 mg 溶于DMSO,采用BBS 缓冲液稀释成不同浓度的样品,并加入临界浓度的补体(1∶80 稀释的豚鼠血清),溶血素和2%绵羊红细胞(SRBC)。37 ℃水浴30 min,离心后取上清液在405 nm 波长下测定吸光度(A)值。同时设置中药对照组(将等量的中药提取物加入BBS缓冲液中,用于测定中药本底A值)、补体组(取临界浓度的补体直接加入适量的BBS 缓冲液、溶血素和2%SRBC,用于测定临界浓度补体所造成红细胞溶血的A值)和全溶血组(将2%SRBC 加入水中使之全溶血,用于观察补体组是否达到或接近全溶血水平),并以肝素作为阳性对照组,计算溶血抑制率。以供试品浓度为横坐标(X),溶血抑制率为纵坐标(Y),计算CH50(经典途径50%抑制溶血所需供试品浓度)。溶血抑制率=1−(A中药−A中药对照)/A全溶血。
2.3 不同浓度的样品色谱与质谱条件
2.3.1 色谱条件
色谱柱为ACQUITY UPLC BEH C18(2.1 mm×100 mm,1.7 μm);流动相0.1%甲酸和水溶液(A)−乙腈(B);梯度洗脱:0~9 min,10%~23% B;9~13 min,23% B;13~28 min,23%~40% B;28~32 min,40%~50% B;32~37 min,50%~100% B;37~42 min,100% B;42~42.1 min,10%B;42.1~50 min,10%B;流速为0.25 ml/min,柱温为35 ℃;进样量为2 μl。
2.3.2 质谱条件
在正/负离子模式,离子源选择电喷雾离子化源(ESI);使用m/z50~1 250 扫描范围;碰撞能量35 eV,碰撞能量叠加(35±15)eV;喷雾电压5 500 V;雾化气温度550 ℃;去簇电压100 V;雾化气和辅助气均为50 psi;气帘气25 psi;数据采集时间50 min;采用母离子触发的子离子(TOF-MS-IDA-MS/MS)扫描方式;多重质量亏损和动态背景扣除为触发二级的条件,满足该条件进行二级扫描。
2.4 对照品溶液的制备
精密称取毛蕊异黄酮、雷公藤甲素、雷公藤内酯酮、丹参酮Ⅱ A 和黄芪甲苷对照品1.0 mg,加甲醇2 ml,溶解,摇匀,即得各对照品溶液。
精密吸取对照品溶液和供试品溶液2 μl,采用“2.1”项下的色谱与质谱条件对样品进行分析,通过正、负离子全扫描,获得正、负离子模式下的总离子流图,见图1。
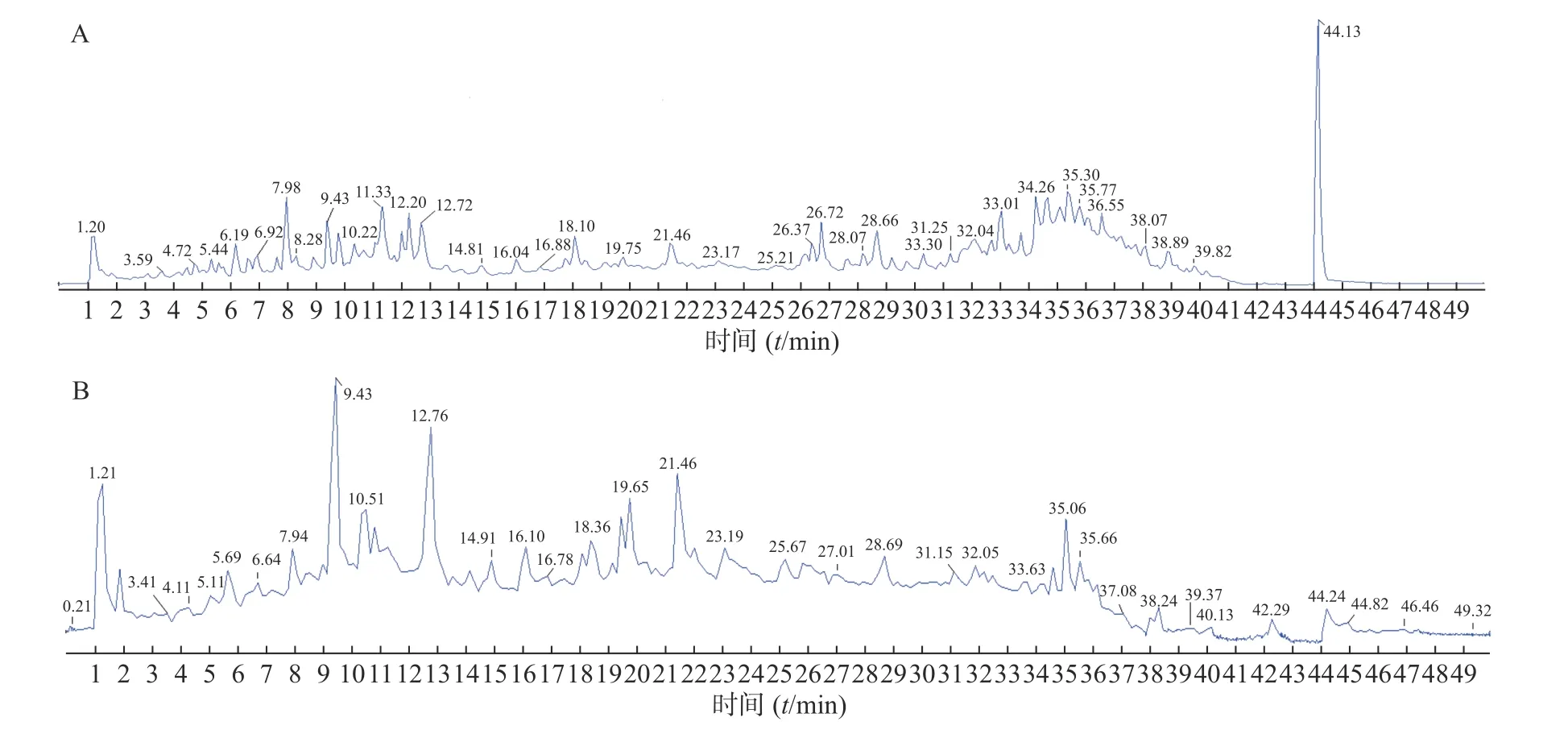
图1 三色片提取物UPLC-Q-TOF-MS 正和负离子模式下的总离子流图
2.5 供试品溶液的制备
取三色片醇提物的乙酸乙酯部位样品0.2 g,置于10 ml 量瓶中,加入70%甲醇5 ml,超声处理(功率250 W,频率40 kHz)30 min,放冷至室温,70%甲醇定容至刻度,摇匀,滤过,取续滤液,即得供试品溶液。
2.6 三色片中化学成分数据库的建立
根据三色片中各药材化学成分研究文献,收集3 种药材所含化合物成分的基本信息,包括化合物名称、分子式、精确分子量、准分子离子峰和碎片离子峰。通过精确分子量匹配,对照品的保留时间,二级谱所得到的离子碎片与文献报道进行比对,最终确定化合物的结构。
3 结果与分析
3.1 三色片醇提物各极性部位的抗补体活性
分别对三色片醇提物的石油醚部位、乙酸乙酯部位和正丁醇部位进行经典途径的抗补体活性测定,以肝素为对照品,结果发现乙酸乙酯部位的抗补体活性最好,其抗补体活性略低于肝素钠,其次是正丁醇部位,结果见表1。

表1 三色片提取物不同部位抗补体活性测定
3.2 三色片醇提物乙酸乙酯部位的UPLC-Q-TOFMS 分析
通过与对照品比对,分子离子峰质谱数据解析,与参考文献比对,共鉴定出三色片醇提物乙酸乙酯部位42 个化合物,结果见表2。
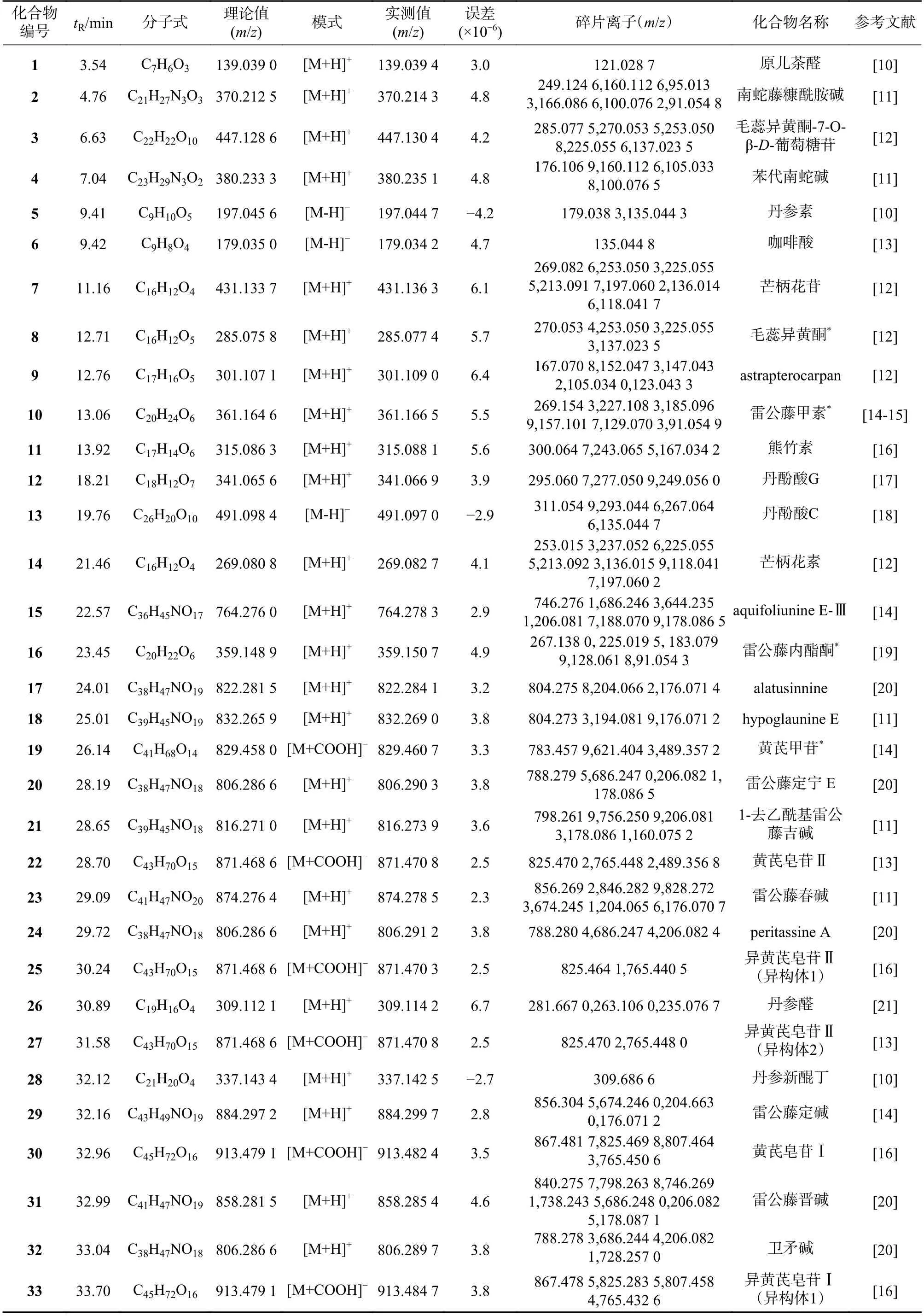
表2 三色片提取物中各成分主要碎片离子及谱峰归属
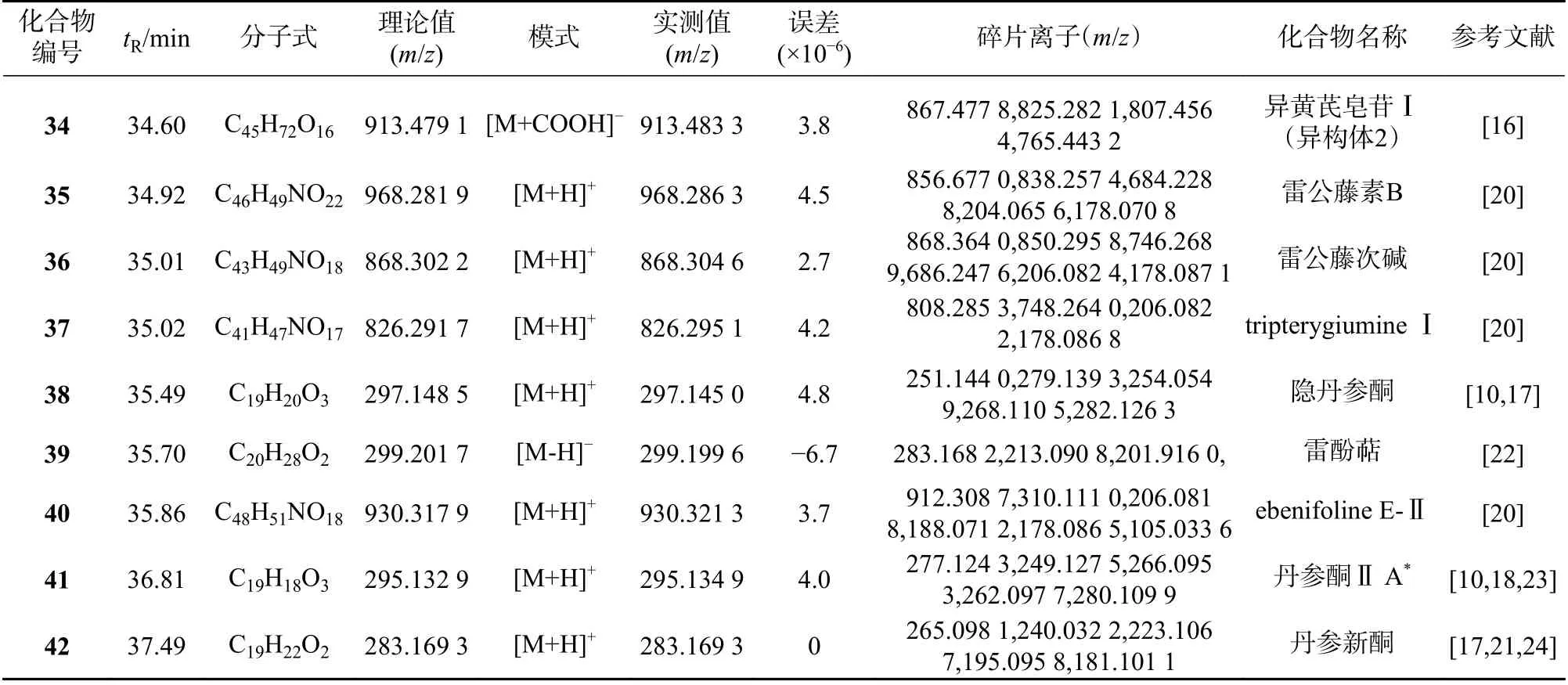
(续表2)
3.2.1 黄酮类化合物结构解析
在乙酸乙酯部位中共鉴定出6 个黄酮类化合物,其中4 个黄酮苷元和2 个黄酮苷,苷元为黄酮、异黄酮和紫檀烷,该类化合物在正离子模式下具有较好的响应。二级质谱中黄酮苷元易发生中性丢失,形成[M+H-H2O]+、[M+H-CO]+、[M+H-CH3]+等碎片离子,如在化合物8 的二级质谱中可见m/z270.053 4 和m/z253.050 3,则为m/z285.077 4 分别脱去-CH3和CH3OH 形成的[M+H-CH3]+和[M+H-CH3OH]+碎片离子峰,m/z225.055 3 是m/z253.050 3 脱去1 分子的CO 形成的碎片离子峰,通过对照品的保留时间和参考文献[12]质谱数据比对确定化合物8 为毛蕊异黄酮,m/z137.023 5 的碎片离子峰为异黄酮母核C 环发生RDA 裂解所产生。黄酮苷类易脱去糖基形成较强的分子离子峰,如化合物3(m/z447.130 4)的二级质谱脱去糖基形成m/z285.077 5 的分子离子峰,并与化合物8(m/z285.077 4)的二级质谱图非常相似,说明化合物3 和化合物8 在结构上是相似的,但化合物3 的分子量多了162(C6H10O5),通过数据库比对和参考文献[12]推测化合物3 则为毛蕊异黄酮-7-O-β-D-葡萄糖苷。化合物9(m/z301.109 0)通过数据库比对发现两种候选化合物分别为astrapterocarpan 和astraisoflavan,二级质谱中主要碎片离子峰为C 环裂解产生的含A 环和B 环片段的碎片离子,其中,m/z167.070 8 为含B 环的碎片离子峰且为基峰,进一步脱甲基形成m/z152.047 3,m/z123.043 3 为含A 环的碎片离子峰,进一步脱水形成m/z105.034 0,m/z147.043 2 为母离子m/z301.109 0 脱去B 环形成的碎片离子峰,根据m/z167.070 8 的碎片离子峰为基峰和含有m/z147.043 2 的碎片离子峰这两个特征,结合参考文献[12]的质谱数据,推测该化合物为astrapterocarpan,其相关裂解途径见图2。
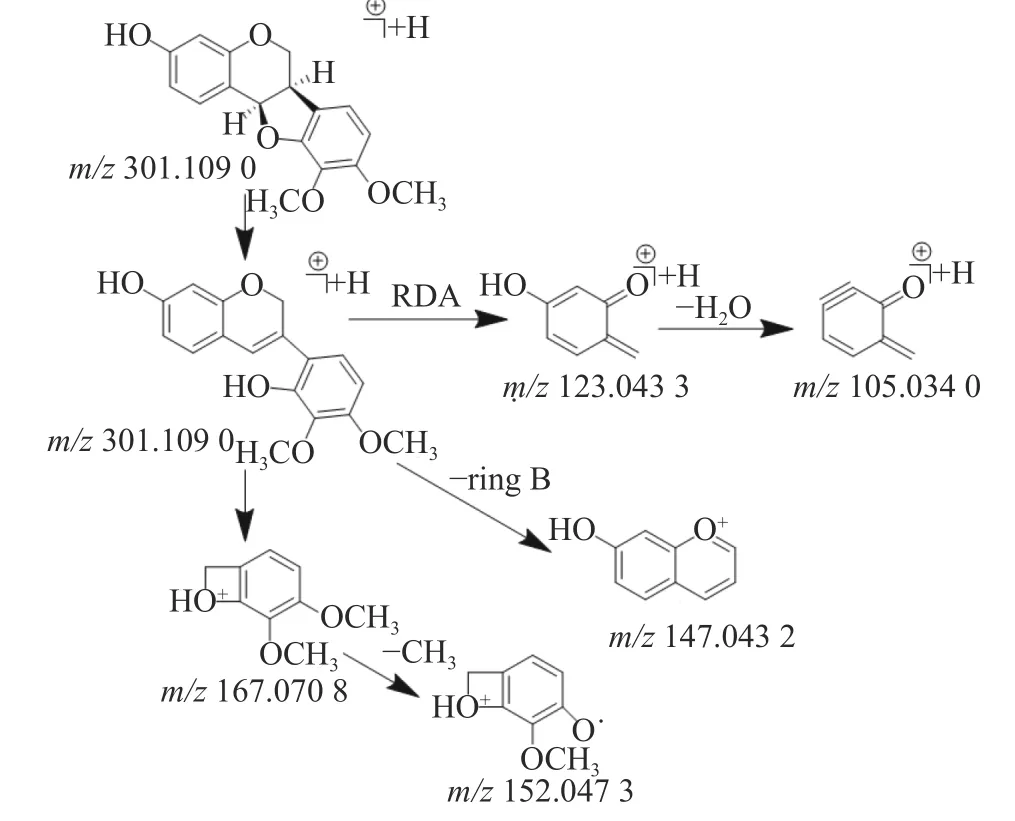
图2 化合物astrapterocarpan 的质谱裂解规律
3.2.2 三萜皂苷类化合物结构解析
在乙酸乙酯部位中鉴定出7 个三萜皂苷类化合物,在负离子模式下均具有较好的响应,一级质谱中产生[M+COOH]−的准分子离子峰,二级质谱中产生较强的[M-H]-碎片离子峰和脱去糖基的较弱的分子离子峰。化合物19 在负离子模式下产生的准分子离子峰为[M+COOH]−(m/z829.458 0),二级质谱中产生m/z783.457 9[M-H]−峰,脱去1 分子六碳糖(C6H10O6)形成m/z621.404 3 的碎片离子峰,m/z489.357 2 则为m/z621.404 3 进一步脱去1 分子五碳糖(C5H6O5)后形成的苷元碎片离子峰,推测其苷元为9,19-环阿尔廷烷,通过对照品的保留时间,参考文献[13]的离子碎片比对确定该化合物为黄芪甲苷。
3.2.3 生物碱类化合物结构解析
三色片提取物中共鉴定出16 个生物碱类化合物,均来自雷公藤药材,在正离子模式下具有较好的响应,一级质谱中产生[M+H]+的准分子离子峰,二级质谱发现该类型的化合物容易脱去H2O、CO 和CH3COOH 等中性小分子而产生碎片离子峰,多数生物碱含有吡啶二羧酸部位的碎片离子峰。如化合物23 在正离子模式下产生m/z874.278 5的准分子离子峰,二级质谱中产生脱去1 分子CO 的m/z846.282 9 的基峰,脱去1 分子H2O 的m/z856.269 2 的碎片离子峰和脱去1 分子HCOOH的m/z828.272 3 的碎片离子峰,m/z674.245 1 峰为m/z846.282 9 脱去C5H4O3侧链和CH3COOH形成的碎片离子峰,m/z204.065 6 峰为大环开裂产生的吡啶二羧酸部分脱水产生的碎片离子,该离子进一步脱羧形成m/z176.070 7 的碎片离子,通过数据库和参考文献[11]质谱数据的比对,推测化合物23 为雷公藤春碱。化合物31 在正离子模式下产生m/z858.285 4 的准分子离子峰,二级质谱中产生脱去1 分子H2O 的m/z840.275 7 的碎片离子峰,准分子离子峰脱去1 分子CH3COOH 形成较强的m/z798.263 8 峰,在进一步脱去1 分子CH3COOH形成738.243 5 峰,准分子离子峰m/z858.285 4 脱去FuOH(C5H4O3)侧链形成的m/z746.269 1 的碎片离子峰,再进一步脱去1 分子CH3COOH,形成m/z686.248 0 的碎片离子,m/z206.082 5 峰为大环开裂产生的吡啶二羧酸部分脱水产生的碎片离子,该离子进一步脱羧形成m/z178.087 1 的碎片离子,通过数据库和参考文献[20]质谱数据的比对,推测化合物31 为雷公藤晋碱。雷公藤晋碱中吡啶二羧酸部分较雷公藤春碱中少一个羟基,故其易产生m/z206.082 5 的碎片离子峰,并通过脱羧产生m/z178.087 1 峰。两种化合物的质谱图见图3。以雷公藤晋碱为例,解析此类化合物的裂解规律,见图4。因此得出吡啶二羧酸部分含有羟基的生物碱会产生m/z204 系列的特征碎片离子峰,不含羟基的生物碱则产生m/z206 系列的特征碎片离子峰。
3.2.4 萜类化合物结构解析
本研究共鉴定出8 种萜类化合物,其中源于丹参药材中的5 种萜类成分,丹参中的萜类化合物因其结构中主要含有羟基,羰基等取代基,所以质谱碰撞中主要丢失H2O,CO 和-CH3等中性分子,产生一系列的碎片离子峰。化合物41 在正离子模式下产生m/z295.134 9 的[M+H]+准分子离子峰,二级质谱中产生脱去1 分子甲基形成的m/z280.109 9的碎片离子峰,在此基础上有丢失1 分子水形成m/z262.097 7 峰,准分子离子峰脱去1 分子H2O 或脱去1 个-CHO 形成m/z277.124 3 峰或m/z266.095 3峰,m/z249.127 5 峰是m/z277.124 3 脱去1 分子H2O 形成的碎片峰,通过对照品的保留时间和参考文献[10,18,23]数据比对,鉴定该化合物为丹参酮Ⅱ A,其质谱裂解规律见图5。
来源于雷公藤药材中的3 种二萜类成分,该类化合物的二级质谱中出现一系列的脱水、脱CO 和异丙基等碎片离子峰。化合物11 在正离子模式下产生m/z361.166 5 的准分子离子峰,脱去2 分子H2O 和2 分子CO 形成m/z269.154 3 的碎片离子峰,m/z227.108 3 为m/z269.154 3 脱去1 分子CH2CHCH3形成的碎片离子,其进一步脱1 分子H2O 和HCHO 形成m/z185.096 9 的碎片离子,通过对照品比对和参考文献[14-15]的质谱数据,确定化合物10 为雷公藤甲素。化合物18 在正离子模式下产生m/z359.148 9 的准分子离子峰,脱去2 分子H2O 和2 分子CO 形成m/z267.138 0 的碎片离子峰,m/z225.019 5 为m/z267.138 0 脱去1 分子CH2CHCH3形成的碎片离子,其进一步脱1 分子H2O 和HCHO 形成m/z183.079 9 的碎片离子,通过对照品比对和参考文献[19]的质谱数据,确定化合物16 为雷公藤内酯酮。化合物39 在负离子模式下产生m/z299.199 6 的准分子离子峰,二级质谱中产生m/z283.168 2 的碎片离子, 提示为丢失1 个-CH3后形成双键产生的碎片离子峰,A 环发生RDA 裂解产生m/z213.090 8 的碎片离子峰,通过数据库比对和参考文献[22]的质谱数据,推测化合物39 为雷酚萜。
3.2.5 酚酸类化合物结构解析
在正负离子模式下共鉴定出乙酸乙酯部位中5 种酚酸类成分,均来自于丹参药材,参考文献[18]报道的丹参中酚酸类成分的裂解规律发现,酚酸类化合物主要含有羰基、羧基和羟基,所以在质谱碰撞中易丢失CO、H2O 和CO2的中性碎片;丹参素和咖啡酸作为基本母核而其他的水溶性酚酸类化合物大多数为这两者的聚合或缩合产物,主要为缩酚酸类的成分,在质谱碰撞中易丢失[M-H-180]−和[M-H-198]−中性碎片;含有羧基的单体化合物在负离子模式下会产生135[C8H7O2]−和179[C9H7O4]−的特征性碎片。化合物5 中,在负离子模式下产生m/z197.044 7 的[M-H]−准分子离子峰,二级质谱进一步产生丢失1 分子H2O 和1 分子CO2,形成的m/z179.038 3 和m/z135.044 3 的碎片离子峰,推测出结构中含有羧基,结合其精确分子量和参考文献[10]质谱数据,推测该化合物为丹参素。化合物12 中,负离子模式下产生m/z491.097 0 的[M-H]−准分子离子峰,二级质谱中产生m/z311.054 9 和m/z293.044 6 的碎片离子峰,分别为[M-H-180]−和[M-H-198]−,m/z267.064 6 峰为m/z311.054 9 脱去1 分子CO2所产生,根据m/z135.044 7 峰推测结构中含有羧基,结合其精确分子量和参考文献[18]质谱数据的比较,推测该化合物为丹酚酸C。化合物1 中,正离子模式下给出m/z139.039 4 的[M+H]+准分子离子峰,脱去1 分子H2O 形成m/z121.028 7的碎片离子峰,通过数据库比对和参考文献[10],推测该化合物1 为原儿茶醛。化合物13 中,在正离子模式下产生m/z341.066 9 的[M+H]+准分子离子峰,脱去1 分子CO2形成m/z295.060 7 的碎片离子峰,m/z277.050 9 和m/z249.056 0 的碎片离子峰是m/z295.060 7 峰分别脱去1 分子H2O 和1 分子CO2形成的,通过数据库比对和参考文献[17]质谱数据,推测该化合物为丹酚酸G。
4 讨论
4.1 色谱与质谱条件考察
本实验流动相考察了乙腈-水系统和甲醇-水系统,结果乙腈-水系统中化合物的分离度较好,加入甲酸可以改善峰形,有助于化合物的离子化,提高质谱的响应,最终选择乙腈-0.1%甲酸水系统作为本次研究的流动相。
4.2 化学成分的定性分析
据以往文献中三色片各化学成分的研究报道,收集各药材的主要化学成分的精确分子量,碎片离子峰等信息,建立相应的化学成分数据库。通过数据库比对,对照品保留时间及参考文献中质谱数据鉴定三色片醇提物乙酸乙酯部位的化学成分。本研究共鉴定出42 个化合物,其中5 个是通过对照品鉴定得出,对无对照品的化合物,通过质谱的裂解特征及参考文献进行结构表征,对同分异构体应结合其在液相色谱中化合物的保留时间及质谱行为,综合对其定性鉴别。
三色片醇提物的乙酸乙酯部位具有较强的抗补体活性,本研究采用UPLC-Q-TOF-MS 法对其中的化学成分进行结构表征,结果发现该部位主要含有生物碱类,萜类,黄酮和酚酸类等化学成分。其中以来源于雷公藤药材中极性中等的生物碱类成分含量较多,这与三色片提取物的制备工艺有关,三色片中雷公藤药材采用乙醇加热回流提取的方式,而黄芪和丹参药材采用水提取醇沉淀的方式。此外,先前的研究发现广藿香中的黄酮和萜类化合物对旁路途径的补体激活具有明显的抑制作用,紫花地丁中的生物碱类成分对旁路途径也有抑制作用(AP50=0.22~0.50 g/L), 牡丹皮和毛七公的抗补体活性成分研究中发现酚羟基决定抗补体活性的存在与否,没食子酰基可改善抗补体活性,甲基则对抗补体活性不利[25-27]。通过本次研究对三色片醇提物的乙酸乙酯部位的化学成分进行了初步表征,为阐明三色片的药效物质基础提供参考依据。研究的不足之处在于,仍有部分化学成分尚未定性鉴定,含量较高的单体成分未进行体外抗补体活性的测定,未来将通过中药化学的方法获得含量较高的单体成分,并进行结构鉴定和抗补体活性测定。

