RGO/PAN 复合材料吸附甲基橙性能的研究
翟江丽,王小薇,杨双花,庞玥鑫,李晓琪
(1.唐山师范学院 化学系,河北 唐山 063000;2.唐山市绿色专用化学品重点实验室,河北 唐山 063000)
合成聚苯胺的方法多样、原料成本低廉,在Mahanta[1]等人首次采用聚苯胺选择性吸附阴离子染料后,聚苯胺在污水处理领域中的应用逐渐增多[2-3],这为聚苯胺的研究开辟了新的领域。石墨烯是一种由sp2杂化的碳原子以六边形排列形成的周期性蜂窝状二维碳质新材料,其理论比表面积非常大,是非常理想的吸附材料,可用来去除水溶液中重金属离子[4-7]和染料[8-10]。在RGO/PAN(简记为GP)的制备中,石墨烯能有效地改善聚苯胺的形貌和物理化学性质[11-13],该复合材料已用于金属离子的吸附研究[14-15],但用于阴离子染料的吸附研究还相对较少。本实验采用化学法制备了还原氧化石墨烯-聚苯胺复合材料,应用于水溶液中阴离子染料甲基橙(MO)的吸附。
1 实验部分
1.1 仪器与试剂
扫描电子显微镜(ZEISS)、傅里叶红外光谱仪(TENSOR37,BRUKER)、UV2550 型紫外可见分光光度计(日本岛津)、85-2A 数显恒温磁力搅拌器(常州澳华仪器有限公司)、SHY-2 型水浴恒温振荡器(江苏金坛环宇科学仪器厂)、PHSJ-4A 数字酸度计(上海精密科学仪器有限公司)、KQ-250E 型超声波清洗器(昆明市超声仪器有限公司),石墨烯(常州第六元素材料科技股份有限公司),苯胺(AR,≥99.5%,使用前经过蒸馏并放入锌粉以去除具有氧化性的杂质,天津市永大化学试剂有限公司),甲基橙(AR,上海埃彼化学试剂有限公司),过硫酸铵(AR,天津市大茂化学试剂厂),盐酸(AR,天津市富宇精细化工有限公司),无水乙醇(AR,天津市永大化学试剂有限公司)。
1.2 石墨烯/聚苯胺复合材料的制备
在2 mg·mL-1的还原氧化石墨烯水分散液中加入1.8 mL 苯胺单体、15.0 mL1 mol·L-1的盐酸,冰水浴中超声分散30 min 后,继续超声中迅速加入0.3 mol·L-1的过硫酸铵盐酸溶液,反应30 min后,离心。将离心所得沉淀用乙醇和去离子水洗涤数次,至滤液无色,真空60 ℃干燥,得到还原氧化石墨烯/聚苯胺复合材料(GP)。用相同的步骤制备不加石墨烯的聚苯胺(PAN)。
1.3 吸附实验
MO 初始浓度为200 mg·L-1。将碘量瓶置于水浴恒温振荡器中震荡,达到平衡后,进行离心分离。上清液中剩余MO 的浓度通过紫外-可见分光光度计在460 nm 的波长下进行测定。单位质量的吸附剂吸附的MO(qe,mg·g-1)由式(1)计算:

式中,c0、ce分别是MO 的初始浓度和平衡浓度(mg·L-1),m为吸附剂的质量(g),V为溶液的体积(L)。
2 结果与讨论
2.1 复合材料的表征
从图1 可以看出,PG 复合材料的谱图与PAN相似,都有聚苯胺醌环和苯环的C=C 伸缩振动吸收峰以及N=Q=N 骨架和苯环N=B=N 骨架吸收峰,但酮环N=Q=N 骨架和苯环N=B=N 骨架的吸收峰分别由1 566 cm-1和1 449 cm-1红移至1 546 cm-1和1 402 cm-1处,这可能是引入的RGO 与聚苯胺骨架之间的π-π 相互作用和氢键作用造成的[16]。由此证明苯胺己经聚合完全[7]。
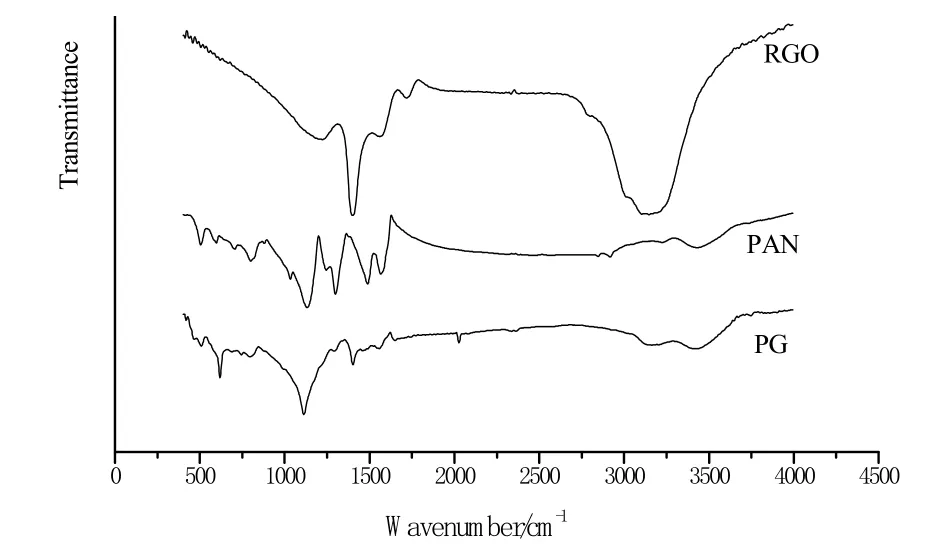
图1 复合材料的红外光谱图
图2 是GP 复合材料的扫描电镜图。由图可见,复合材料中石墨烯片层增厚,聚苯胺在石墨烯表面以毛绒状分布均匀,聚苯胺与石墨烯均未发生明显的团聚,这可能是由于聚苯胺吸附于石墨烯表面增大了石墨烯片层之间的距离,减少了石墨烯的团聚;同时,石墨烯为苯胺聚合提供了均匀的成核位点,使聚苯胺均匀地分散于石墨烯表面。

图2 RGO 和PG 的扫描电镜图片
2.2 GP 对甲基橙的吸附性能
2.2.1 吸附时长的影响
图3 为GP 和PAN 两种材料对MO 的吸附率随时间的变化。从图中可以看出,与PAN 相比,PG 对水溶液中MO 的去除率高,吸附效果好。一方面可能是聚苯胺的表面带正电,吸附剂表面的带正电基团,通过静电引力吸附带负电荷的甲基橙染料;另一方面是由于引入大比表面积石墨烯,增大了聚苯胺原有的比表面积,使复合材料的吸附性能大为提高。
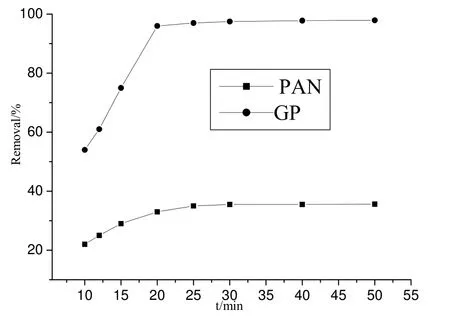
图3 甲基橙吸附率随吸附时长的变化
将不同吸附时长复合材料对甲基橙溶液吸附量的变化进行吸附准一级动力学模型和准二级动力学模型研究,结果如表1 所示。从表1 可以看出,PG 和PAN 两种材料对MO 进行准二阶动力学模型拟合时的相关系数均大于准一级的,且都大于0.99,说明吸附过程更符合准二级动力学吸附模型,为化学吸附[17]。

表1 复合材料吸附的准一阶和准二阶动力学参数
2.2.2 pH 的影响
图4 为pH 对PG 吸附MO 的影响。从图中可以看出,GP 对甲基橙的吸附率先上升后下降,在pH 为7.0 时达到最大。原因可能是在强酸性环境中,大量氢离子会与甲基橙竞争聚苯胺上的吸附活性中心,不利于吸附过程的进行。在pH 为5.0-7.0之间,氢离子的竞争能力减弱,复合材料中聚苯胺上的氨基质子化,可与甲基橙分子中的N 原子形成氢键,并能与甲基橙分子中的SO3-发生静电吸附,因此,此时吸附效果最佳。当pH>7.0 时,复合材料中的聚苯胺链上的氨基发生脱掺杂,与甲基橙骨架中N 原子形成氢键的能力减弱,也不易于发生静电吸附,吸附性能下降。

图4 pH 对PG 吸附MO 的影响
2.2.3 吸附温度的影响
图5 为吸附温度对GP、PAN 吸附甲基橙的影响。从图中可以看出,随着温度的升高,复合材料对甲基橙的吸附率不断增加。原因可能是,随着温度的升高,PG 产生溶胀效应,同时分子热运动加快,使甲基橙分子更容易进入到复合材料内部。当温度适宜,即吸附效果大于解析效果时,吸附会比较顺利地进行。结果表明,PG 和PAN 两种材料吸附甲基橙均为吸热过程。

图5 吸附温度对GP、PAN 吸附甲基橙的影响
为2 为PG 和PAN 复合材料吸附甲基橙的热力学参数。由表可知,PG 吸附甲基橙的ΔG 值均为负值,为自发吸附过程,焓变为正值,说明此吸附为吸热过程,高温对吸附更有利。

表2 PG 和PAN 复合材料吸附甲基橙的热力学参数
2.2.4 甲基橙初始浓度的影响
图6 为室温条件下甲基橙初始浓度对吸附效果的影响。从图中可以看出,随着甲基橙浓度的增加,两种材料的去除率减小。

图6 甲基橙初始浓度对PG、PAN 吸附性能的影响
表3 为PG 和PAN 吸附MO 的Langmuir 和Freundlich 参数(298 K)。由表可知,两种材料的Langmuir 等温吸附模型的相关系数分别都比Freundlich 等温吸附模型的相关系数大,这表明用Langmuir 等温吸附模型能更好地模拟两种吸附材料的吸附过程,可以认为是单层吸附,且PG 复合材料为均质表面。

表3 PG 和PAN 吸附MO 的Langmuir 和Freundlich 参数(298 K)
表4 为不同吸附剂的最大吸附量比较。由表可知,PG 用Langmuir 等温吸附模型计算的最大吸附量为333 mg·g-1,接近于PAN 最大吸附量的3 倍,同时也高于文献报道的其他聚苯胺材料。

表4 不同吸附剂最大吸附量比较
2.3 重复利用性能
表5 为PG 吸附MO 的重复利用效果。

表5 PG 吸附MO 的重复利用
由表可知,将吸附过甲基橙的GP 用乙醇进行解析并干燥,然后再用于吸附甲基橙溶液,重复循环使用5 次,发现随着使用次数增多去除率逐渐下降,但仍在70%以上,说明PG 的再生性能良好,可以循环利用。
3 结论
采用化学合成法制备了还原氧化石墨烯/聚苯胺复合材料,考察了吸附时间、pH、吸附温度、甲基橙浓度对吸附材料吸附甲基橙性能的影响。在20 min 内复合材料对甲基橙的吸附即可达到平衡,符合准二级动力学模型,在pH=7.0 时吸附达到最大;随着吸附温度的升高去除率增大,属于吸热反应;在等温吸附研究中PG 对甲基橙的吸附符合Langmuir 等温吸附模型,最大吸附量可达333 mg·g-1;吸附材料用无水乙醇解附后再次进行吸附,去除率有所下降但仍可达70%以上,这表明该复合材料可以充分利用并可再生,在甲基橙染料废水处理方面具有广阔的应用前景。

