对接受胸腔镜肺癌根治术的患者进行超声引导下菱形肌-肋间肌阻滞的效果探究
刘 奥,董希玮,李 燕,于 海,葛明月,殷姜文
(石河子大学医学院第一附属医院麻醉科,新疆 石河子 832008)
在肺癌的外科治疗中,进行胸腔镜手术虽然较传统的开胸手术能显著减轻患者的手术创伤,但多数患者术后仍会出现中重度的疼痛感。术后若患者的疼痛未得到良好的控制,会引发过度炎症反应,其中约有10% 的患者还可发生慢性疼痛,严重影响其术后的生存质量[1-2]。因此,对肺癌患者进行胸腔镜手术后对其实施良好的镇痛尤为重要。中国胸外科围手术期疼痛管理专家共识(2018 版)[3]推荐采用多种镇痛模式相结合的方式对接受手术后的肺癌患者进行镇痛。菱形肌- 肋间肌阻滞(rhomboid intercostal block,RIB)是一种新型的区域阻滞技术,目前国内相关的研究报道较少。国外的研究指出,RIB 技术可为肋骨骨折患者提供良好的术后镇痛支持[4]。本文主要是探讨对接受胸腔镜肺癌根治术的患者进行超声引导下RIB 的效果
1 资料与方法
1.1 一般资料
本研究为随机对照试验,经石河子大学医学院第一附属医院医学伦理委员会的批准(2019-084-02),选取2019年12 月至2020 年8 月期间在该医院进行全身麻醉下胸腔镜肺癌根治术的92 例患者作为研究对象。其纳入标准是:病情符合原发性肺癌的诊断标准,且经术后病理学检查得到确诊;年龄为18 ~65 周岁;体质指数(body mass index,BMI)为18 ~25 ;美国麻醉医师协会(American Society of Anesthesiologists,ASA)麻醉分级为Ⅰ~Ⅲ级;既往无严重的心血管疾病史、内分泌系统疾病史或肝肾疾病史,无精神类药物、阿片类药物使用史;未长期使用激素类药物或免疫抑制剂进行治疗;未接受过细胞学治疗;无酗酒史;知悉本研究方案,并签署了自愿参与本研究的知情同意书。其排除标准是:有麻醉药物过敏史或对本研究中所用的麻醉药物过敏;注射部位存在局部感染和(或)全身感染;存在凝血功能障碍;合并有消化道溃疡出血;血小板计数<50×109/L ;存在沟通障碍或精神异常。本研究的中止或终止标准是:患者要求退出本研究;术中转为进行开胸手术;在围手术期接受过输血。本研究拟纳入患者92 例,每组各有患者46 例。在研究过程中,观察组患者中有2 例患者术中转为进行开胸手术,有1 例患者自行退出本研究,最终纳入患者43 例;对照组患者中有3 例患者术中转为进行开胸手术,最终纳入患者43 例。在观察组患者中,有男性27 例,女性16 例;其平均年龄为(54.1±9.6)岁,平均的BMI 为(21.6±1.7);其中,ASA 麻醉分级为Ⅰ级、Ⅱ级、Ⅲ级的患者分别有13 例、27 例、3 例;肿瘤分期为Ⅰ期、Ⅱ期的患者分别有28 例、15 例;病理类型为肺鳞状细胞癌(鳞癌)、肺腺癌的患者分别有24 例、19 例。在对照组患者中,有男性29 例,女性14 例;其平均年龄为(56.0±7.7)岁,平均的BMI 为(22.1±1.4);其中,ASA 麻醉分级为Ⅰ级、Ⅱ级、Ⅲ级的患者分别有10 例、31例、2 例;肿瘤分期为Ⅰ期、Ⅱ期的患者分别有25 例、18 例;病理类型为肺鳞癌、肺腺癌、肺大细胞癌的患者分别有28例、14 例、1 例。两组患者的一般资料相比,差异无统计学意义(P>0.05)。详见表1。

表1 两组患者一般资料的比较
1.2 方法
对两组患者均进行胸腔镜肺癌根治术,在T4-T5肋间做一个手术切口,置入胸腔镜和手术器械,术毕在麻醉状态下于腋后线T6-T7肋间放置胸腔闭式引流管。所有胸腔镜手术均由胸外科同一团队完成。两组患者术前均常规禁食8 h、禁饮4 h,进入手术室后监测其血压(blood pressure,BP)、血氧饱和度(blood oxygen saturation,SpO2)、心电图(electrocardiogram,ECG)和脑电双频指数(bispectral index,BIS),为其开放上肢静脉通道,静脉输注乳酸钠林格氏液。对患者进行局部麻醉下桡动脉穿刺置管术和颈内静脉穿刺置管术,监测其有创动脉压和中心静脉压。在麻醉诱导前,对观察组患者进行RIB,方法是:协助其取健侧卧位,确认肩胛骨内侧缘及下缘的位置,将患侧手臂贴于床边垂直放置。对其背部预穿刺部位的皮肤进行常规消毒,将线性超声探头(频率为8 ~12 MHz)置于T5-T6水平肩胛骨内侧缘内侧约1 cm,使探头的长轴位于斜矢状面上。在超声下辨别并确认斜方肌、菱形肌、肋间肌、胸膜和肺后。采用平面内进针技术用一次性无菌神经刺激针在T4-T5的水平处进针,针尖的方向与探头的方向保持平行,逐层进针。当针尖进入菱形肌与肋间肌之间后,向此处注入2 mL的生理盐水,在超声下可见液性暗区。待回抽无血、无气后,确定针尖的位置是否正确。若位置正确,则将局麻药(0.3% 的罗哌卡因40 mL)注入菱形肌与肋间肌之间的深筋膜平面内。当超声图像中可见局麻药在菱形肌与肋间肌之间向头、尾侧扩散,表示注射成功。在阻滞后的30 min 内,每隔10 min 采用针刺的方式测量一次感觉阻滞水平。以上操作均由同一位有经验的麻醉科医师完成。超声引导下RIB的操作图像详见图1。完成上述操作后,由对此试验不知情的另一位麻醉科医生对两组患者进行麻醉诱导,方法是:为其静脉注射咪达唑仑0.02 mg/kg、丙泊酚1.5 ~2.0 mg/kg、舒芬太尼0.5 ~0.6 μg/kg、苯磺顺阿曲库铵0.2 mg/kg。4 min 后对其进行双腔气管插管,使用纤维支气管镜确定蓝套囊的位置。采取容量控制通气(volume control ventilation,VCV)模式对其进行机械通气,将潮气量设为6 ~8 mL/kg,将呼吸频率(respiratory rate,RR)设为12 ~16 次/min,将呼吸比设为1:2,将呼气末正压(positive end-expiratory pressure,PEEP)设为 3 ~5 cmH20,将氧流量设为1.5 L/min,将吸入氧浓度分数(fraction of inspiration oxygen,FiO2)设为80%,将呼气末二氧化碳分压(partial pressure of end-tidal carbon dioxide,PETCO2)设为35 ~45 mmHg。术中持续为患者静脉泵注6 ~10 mg·kg-1·h-1的丙泊酚、0.06 ~0.12 mg·kg-1·h-1的苯磺顺阿曲库铵和0.05 ~0.2 μg·kg-1·min-1的瑞芬太尼进行麻醉维持,将其BIS 维持在40 ~60 之间。术中合理调节瑞芬太尼的泵注剂量,并根据需要为患者补充胶体液,以保持其血压、心率的波动范围不超过基础值的20%,必要时为其静脉注射麻黄碱、去氧肾上腺素、乌拉地尔、阿托品、艾司洛尔等药物。手术结束即刻为患者静脉注射30 mg 的酮咯酸氨丁三醇,并对其实施PCIA(镇痛药物的配置是:酒石酸布托啡诺165 μg/kg,用生理盐水稀释至100 mL;PCIA 泵的各项参数是:背景剂量为2 mL/h,单次剂量为0.5 mL,锁定时间为15 min)。将患者送至胸外科监护室进行复苏,待其意识清醒后拔除双腔气管导管。术后若患者静态下疼痛数字评分法(numerical rating scale,NRS)的评分≥3 分,为其静脉推注30 mg 的酮咯酸氨丁三醇进行补救性镇痛。若注射酮咯酸氨丁三醇后疼痛仍控制不佳,NRS 评分未<3 分,则为其静脉注射5 mg 的地佐辛进行额外补救性镇痛。
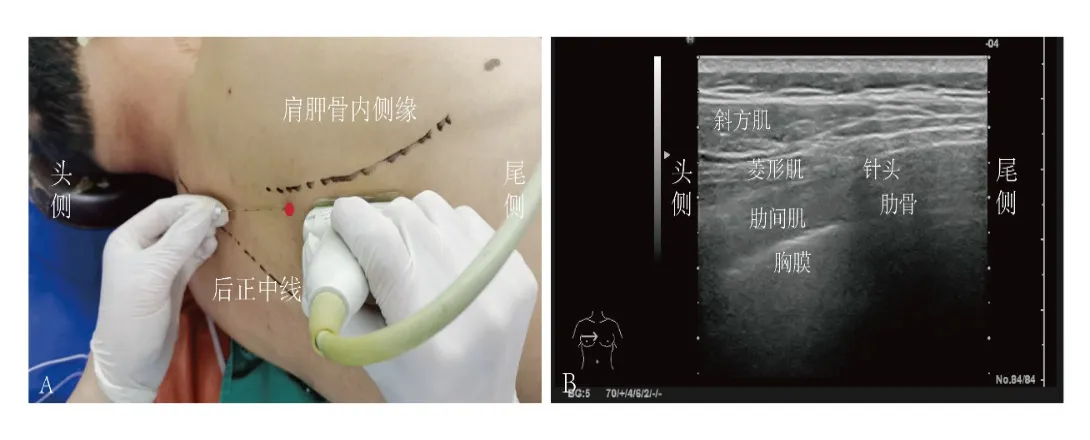
图1 超声引导下RIB 的操作图像
1.3 观察指标
比较两组患者术中的失血量、手术的时间及术中瑞芬太尼的输注量。入室后、切皮时、手术开始后1 h、手术开始后2 h 及手术开始后3 h,比较两组患者的平均动脉压(mean arterial pressure,MAP)及心率(heart rate ,HR)。观察并记录对观察组患者进行RIB 的阻滞范围。术后1 h、6 h、18 h、24 h 及48 h,比较两组患者静态(躺或坐)和动态(翻身或坐起)下的NRS 评分。NRS 的分值为0 ~10 分,患者的评分为0 分、1 ~3 分、4 ~7 分、8 ~10 分,分别表示其无痛、存在轻度疼痛、存在中度疼痛、存在重度疼痛、术后1 h、6 h、18 h、24 h 及48 h,比较两组患者伯格曼舒适度量表(Bruggrmann comfort scale,BCS)的评分。BCS的分值为0 ~4 分。0 分:患者存在持续性疼痛。1 分:患者安静时无痛,深呼吸或咳嗽时疼痛严重。2 分:患者平卧安静时无痛,深呼吸或咳嗽时出现轻微疼痛。3 分:患者深呼吸时亦无痛。4 分:患者咳嗽时亦无痛。比较两组患者术后首次静脉推注酮咯酸氨丁三醇的时间、术后48 h 内静脉推注酮咯酸氨丁三醇的次数、术后24 h 内和48 h 内PCIA的有效按压次数及酒石酸布托啡诺的用量、术后使用地佐辛进行额外补救性镇痛的情况及用药后发生不良反应的情况。所得数据由一位对本研究中分组情况不知情的麻醉科护士评估。
1.4 统计学方法
用SPSS 26.0 软件处理本研究中的数据,计数资料用%表示,组间比较采用χ² 检验;符合正态分布的计量资料用±s表示,组间比较采用成组t检验;偏态分布的计量资料用中位数(四分位数间距)[M(Q1,Q3)] 表示,采用非参数检验,以中位数(四分位数间距)[M(Q1,Q3)]表示,组内比较采用重复测量方差分析,P<0.05 表示差异有统计学意义。
2 结果
2.1 对比两组患者术中的失血量、手术的时间及术中瑞芬太尼的输注量
两组患者术中的失血量及手术的时间相比,差异无统计学意义(P>0.05)。观察组患者术中瑞芬太尼的输注量少于对照组患者,差异有统计学意义(P<0.05)。详见表2。
表2 对比两组患者术中的失血量、手术的时间及术中瑞芬太尼的输注量(± s )

表2 对比两组患者术中的失血量、手术的时间及术中瑞芬太尼的输注量(± s )
术中瑞芬太尼的输注量(μg)观察组(n=43) 169.2±36.6 196.3±12.2 2022.1±290.6对照组(n=43) 165.6±36.0 198.9±11.3 2383.7±294.1 t 值 0.461 -1.024 -5.735 P 值 0.646 0.309 <0.001组别 术中的失血量(mL)手术的时间(min)
2.2 对比两组患者术中各时间点的MAP 及HR
入室后、切皮时、手术开始后1 h、手术开始后2 h 及手术开始后3 h,两组患者的MAP 及HR 相比,差异无统计学意义(P>0.05)。详见表3。
表3 对比两组患者术中各时间点的MAP 及HR(± s )

表3 对比两组患者术中各时间点的MAP 及HR(± s )
注:1F 组间=0.053,1F 组内=103.640,1F 交互=4.509;2F 组间=0.304,2F 组内=209.755,2F 交互=0.340。
指标 组别 入室后 切皮时 手术开始后1 h 手术开始后2 h 手术开始后3 h MAP1(mmHg) 观察组(n=43) 98.7±7.9 87.4±4.4 83.3±5.9 85.1±5,3 87.6±3.6对照组(n=43) 95.5±12.0 88.1±7.0 85.4±6.9 86.7±6.8 87.8±5.9 t 值 1.455 -0.552 -1.492 -1.256 -0.154 P 值 0.149 0.582 0.139 0.213 0.878 HR2(次/min)观察组(n=43) 76.1±9.3 66.8±8.1 65.6±9.3 64.6±8.6 64.7±7.1对照组(n=43) 76.9±8.9 68.0±7.1 66.0±7.6 65.4±7.5 66.0±7.5 t 值 -0.39 -0.778 -0.215 -0.454 -0.841 P 值 0.697 0.438 0.403 0.651 0.403
2.3 对观察组患者进行RIB 的阻滞范围
对观察组患者进行RIB 后,采用针刺法测量其感觉神经阻滞的范围,结果显示,其中有31 例患者的阻滞范围为T3-T7肋间神经外侧支及胸神经后支支配区域,另外12 例患者的阻滞范围为T3-T8肋间神经外侧支及胸神经后支支配区域。
2.4 对比两组患者术后不同时间点的NRS 评分及BCS 评分
术后6 h、18 h 及24 h,观察组患者静态和动态下的NRS 评分均低于对照组患者,差异有统计学意义(P<0.05)。术后1 h 及48 h,两组患者静态及动态下的NRS 评分相比,差异无统计学意义(P>0.05)。术后6 h、18 h 及24 h,观察组患者的BCS 评分均高于对照组患者,差异有统计学意义(P<0.05)。术后1 h 及48 h,两组患者的BCS 评分相比,差异无统计学意义(P>0.05)。详见表4。

表4 对比两组患者术后不同时间点的NRS 评分及BCS 评分[分,M(Q1,Q3)]
2.5 对比两组患者术后使用镇痛药物的情况
与对照组患者相比,观察组患者术后首次静脉推注酮咯酸氨丁三醇的时间更晚,其术后48 h 内静脉推注酮咯酸氨丁三醇的次数更少,其术后24 h 内和48 h 内PCIA 的有效按压次数和酒石酸布托啡诺的用量均更少,差异有统计学意义(P<0.05)。详见表5。术后,对照组患者中有2例患者采用地佐辛进行额外补救性镇痛,观察组患者中无患者采用地佐辛进行额外补救性镇痛。术后,观察组患者与对照组患者采用地佐辛进行额外补救性镇痛的比率分别为4.65%(2/43)与0%(0/43),二者相比差异无统计学意义(P>0.05)。
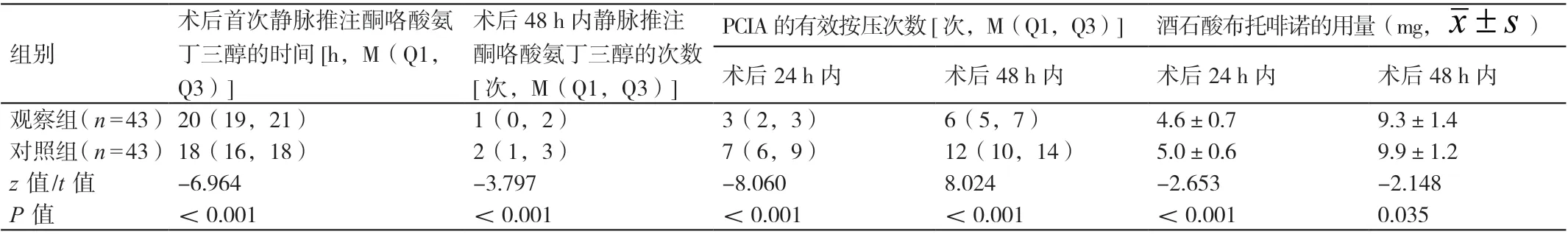
表5 对比两组患者术后使用镇痛药物的情况
2.6 对比两组患者不良反应的发生率
用药后,两组患者恶心呕吐、便秘、皮肤瘙痒的发生率相比,差异无统计学意义(P>0.05)。详见表6。术后48 h 内,观察组患者均未出现阻滞后低血压和(或)心动过缓、气胸等并发症。

表6 对比两组患者不良反应的发生率[例(%)]
3 讨论
与对肺癌患者进行开胸手术相比,对其实施胸腔镜肺癌根治术能有效地减轻其术后的应激反应,但术中仍会损伤其肋间肌肉及神经,导致其术后出现较为强烈的疼痛感,故术后需要为其提供有效的镇痛措施[5]。阿片类药物在术后镇痛方面具有独特的优势,但易引起呕吐、痛觉过敏、呼吸抑制等不良反应[6]。此外,阿片类药物可使淋巴细胞、炎症细胞的数量失衡,降低自然杀伤细胞的活性[7]。近年来随着多模式镇痛理念的发展及完善,术后镇痛方式、镇痛药物的选择不断优化,少阿片或无阿片类药物镇痛的相关研究逐渐成为主要的研究方向[8-9]。Elsharkawy 等[4]于2016 年首次提出RIB,其镇痛原理是通过局麻药在菱形肌与肋间肌平面内的扩散,阻滞肋间神经外侧支和胸神经后支,进而减轻该神经支配区域的疼痛感。对人类尸体进行相关的实验表明,将25 mL 的亚甲蓝注入尸体的菱形肌与肋间肌平面内,可观察到染料向头侧、尾侧、后正中线扩散,扩散的范围可达T2-T8[4]。Elsharkawy 等[4]对一名多发肋骨骨折患者使用0.25% 的布比卡因25 mL 进行RIB,其感觉水平阻滞的范围为T2-T9。Altıparmak 等[10]对两例接受开胸手术的患者术前实施RIB(所用局麻药为0.25% 的布比卡因30 mL),其感觉阻滞范围在T3-T10之间。本研究对观察组患者进行RIB 时使用的局麻药为0.3% 的盐酸罗哌卡因40 mL,患者的感觉阻滞范围达到T3-T8。布比卡因与罗哌卡因的镇痛效果相似,但Altıparmak 等报道中所用局麻药的浓度及容量均低于本研究。本研究与上述报道中获得的阻滞范围大致相同,且均完全覆盖手术切口及引流管放置区域,这一情况的发生可能与两项研究中患者的体型、进针角度、注药速度等存在差异有关。本研究的结果显示,观察组患者术后6 h、18 h、24 h 静态和动态下的NRS 评分及BCS 评分均优于对照组患者。有报道称,进行RIB 可抑制神经动作电位的产生,减少痛觉信号由外周神经向中枢神经的传递,进而可达到镇痛的目的[11]。本研究中观察组患者术后24 h 静态、动态下的NRS 评分均高于术后6 h、18 h,且本组患者术后首次静脉推注酮咯酸氨丁三醇时间约为20 h。导致这一情况出现的原因可能是进行单次RIB 后随着时间的推移,局麻药物会逐渐代谢,难以控制因活动导致的急性疼痛。在本课题组的后续研究中,考虑若使用相同剂量的罗哌卡因,可以术后20 h 为分割点超前追加非甾体类抗炎药或将此类药物作为术后镇痛的基础用药为患者阶段性连续输注。本研究中,术后1 h 两组患者的NRS评分及BCS 评分相近。这可能与术中进行麻醉诱导时舒芬太尼的用量偏大,术后早期药物代谢不完全,且患者在转运前、未清醒时连接进行PCIA 等有关。由于进行RIB 可减少患者术中及术后阿片类药物的用量,故本研究中观察组患者恶心呕吐、皮肤瘙痒、便秘等不良反应的发生率均低于对照组患者,但组间相比差异无统计学意义(P>0.05)。这与Altıparmak 等[12]的研究结果相似。究其原因可能是本研究存在选择性偏移、样本量较小等情况。在进行胸腔镜肺癌根治术时,对患者实施胸段硬膜外麻醉阻滞的效果确切,但存在易误穿破蛛网膜下隙、患者循环波动明显等缺点[13]。进行前锯肌阻滞具有操作简单、安全性高等优点,但存在阻滞的时间较短、穿刺部位靠近手术操作区域等缺点[14]。国外的相关报道称,将RIB 技术应用于女性缩胸手术[15]、肩胛区纤维瘤切除手术[16]、小儿胸科手术[17]中均能取得良好的术后镇痛效果,且未观察到患者出现明显的不良反应。尽管进行RIB 存在对自主神经系统阻滞不充分的情况,但通过与阿片类药物、非甾体类药物等镇痛药联合使用,可发挥多模式镇痛的优势,弥补对内脏感觉神经阻滞不足的缺点。本研究的结果显示,对观察组患者进行RIB 未导致其术中的MAP、HR 出现明显波动,提示进行该操作的安全性较高。本研究存在以下不足之处:1)未采用恢复量表等工具评估患者术后恢复的情况。2)本研究仅针对手术患者,未纳入危重症患者。本课题组在后续的相关研究中考虑进行多中心、大样本的研究,完善各项评价指标,并适当纳入危重症患者,以进一步证实本研究的结论。
综上所述,对接受胸腔镜肺癌根治术的患者进行超声引导下RIB 能减少其术中及术后镇痛药物的用量,减轻其术后疼痛的程度,提高其术后的舒适度,且用药较为安全。

