甲氨蝶呤结合腹腔镜保守术在输卵管妊娠患者中的实施效果
吴松珊,杨 岚
(廉江市人民医院妇科, 广东 廉江 524400)
输卵管妊娠(Tubal pregnancy)属于临床最常见异位妊娠之一,其中,以壶腹部较为常见[1]。患者可表现为阴道不规律流血、腹痛、痛经等,若治疗不及时,可造成输卵管妊娠破裂,导致患者腹腔大量出血,有生命危险[2]。输卵管妊娠发病率较高,主要表现为停经、腹痛、阴道不规则出血,如果错过了最佳治疗时机,妊娠囊容易破裂,影响生育功能。腹腔镜保守术是临床治疗输卵管妊娠的常用手段,其可最大程度地保留患者输卵管,减轻对其生育能力的影响。但此种治疗方式难以充分将绒毛组织去除,术后易出现持续异位妊娠[3]。甲氨蝶呤(methotrexate)属于抗叶酸类药,可阻止滋养细胞生长,可抑制DNA的生物合成,可以抑制叶细胞持续增生,促使绒毛细胞受到破坏,合成拮抗核酸,对绒毛组织产生破坏作用,促进胚胎脱落,抑制细胞中二氢叶酸转向四氢叶酸,从而降低持续性异位妊娠发生风险[4]。为进一步证实在输卵管妊娠治疗中甲氨蝶呤与腹腔镜保守术的联合应用价值,现对本院76例输卵管妊娠患者展开研讨。
1 资料与方法
1.1 一般资料
选择2019年4月-2020年12月我院接收的76例输卵管妊娠患者,按照随机摸球法分成甲组与乙组,各38例。甲组:初产妇与经产妇各为21例、17例;年龄范围22~36岁,平均年龄(28.15±2.37)岁;输卵管妊娠部位:伞端5例(占比13.16%),峡部6例(占比15.79%),壶腹部27例(占比71.05%)。孕次1次至4次,平均孕次(2.23±0.32)次。乙组:初产妇与经产妇各为19例、19例;年龄范围22~37岁,平均年龄(28.17±2.34)岁;输卵管妊娠部位:伞端4例(占比10.53%),峡部7例(占比18.42%),壶腹部27例(占比71.05%)。孕次1次至4次,平均孕次(2.25±0.33)次。两组患者以上数据相比均无明显差异(P>0.05),可对比。
纳入标准:(1)经症状分析、妇科检查及辅助检查确诊为输卵管妊娠;(2)能积极配合研究;(3)患者、家属均了解且同意本次研究,并经医院医学伦理委员会批准。排除标准:(1)腹腔、卵巢、宫颈等部位妊娠者;(2)具有腹腔镜手术禁忌症或对甲氨蝶呤过敏者;(3)存在与本研究无关危急重症者;(4)精神疾病者;(5)合并恶性肿瘤的患者;(6)凝血功能障碍者。
1.2 方法
甲组给予腹腔镜保守术治疗:全麻条件下,协助患者摆放头低臀高仰卧位,在腹腔镜作用下确定输卵管妊娠最突出位置并施以线性切开,待将妊娠物取出后,进行反复冲洗。而后,予以双极电凝止血,间断缝合创面。
乙组在甲组基础上,加用甲氨蝶呤注射液(2mL∶50mg,Pfizer Australia Pty Ltd,批号EC8098)。治疗:在电凝止血后,于病灶近端输卵管系膜周围注射40mg甲氨蝶呤。术后第一天复查绒毛膜促性腺激素(human chorionic gonadotrophin,HCG),出院后每周复查HCG至HCG转阴。
1.3 观察指标
(1)观察两组输卵管妊娠患者手术相关指标,包含术中、术后出血量、住院时间。
(2)观察两组输卵管妊娠患者患侧输卵管状况及持续性异位妊娠发生情况。术后3月,实施四维超色造影观察输卵管通畅状况。当注射造影剂时无显著阻力、无反流,且造影剂可沿输卵管伞端弥散到盆腔即为通畅,反之则不通畅。术后随访3月,统计两组持续性异位妊娠发生率。
(3)观察两组输卵管妊娠患者组间β-HCG、盆腔包块直径、血清孕酮。
(4)观察两组输卵管妊娠患者的术后激素水平,包含促排卵激素(Follicle stimulating hormone,FSH)、促黄体生成激素(luteinizing hormone,LH)。取静脉血5毫升,分离血清后,使用放射免疫测定法进行测量,使用上海科苑生物工程技术中心提供的试剂盒进行测量。
1.4 统计学方法
两组输卵管妊娠患者的数据以统计学软件SPSS 24.0处理,计数资料(患侧输卵管通畅、持续性异位妊娠)采用(%)表示,差异性应用卡方检验;计量资料(术中、术后出血量、住院时间、β-HCG、盆腔包块直径、血清孕酮、FSH、LH)应用均数±标准差表示,差异性应用t检验。若具有统计学意义则P<0.05。
2 结果
2.1 比较两组手术相关指标
与甲组相比,乙组术中、术后出血量较低(P<0.05)具有统计学意义,两组输卵管妊娠患者的住院时间相比,无明显差异(P>0.05),详细数据见表1。

表1 比较两组手术相关指标
2.2 比较两组患侧输卵管通畅率、持续性异位妊娠率
较甲组,乙组患侧输卵管通畅率较高,持续性异位妊娠发生率较低(P<0.05),详细数据见表2。

表2 比较两组患侧输卵管通畅率、持续性异位妊娠率[n(%)]
2.3 比较两组输卵管妊娠患者组间β-HCG、盆腔包块直径、血清孕酮
两组输卵管妊娠患者组间β-HCG、盆腔包块直径、血清孕酮治疗前无明显差异,(P>0.05)无统计学意义。详细数据见表3,与甲组相比,乙组治疗后的β-HCG、盆腔包块直径、血清孕酮小于甲组,(P<0.05)。
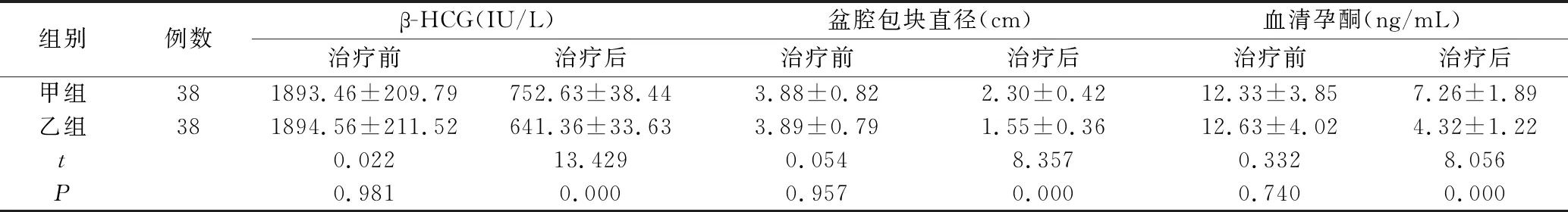
表3 两组输卵管妊娠患者组间β-HCG、盆腔包块直径、血清孕酮
2.4 比较两组输卵管妊娠患者的术后激素水平
两组输卵管妊娠患者治疗后1个月、治疗后3个月的激素水平(FSH、LH)无明显差异(P>0.05)。详细数据见表4。

表4 两组输卵管妊娠患者组间β-HCG、盆腔包块直径、血清孕酮(mIU/mL)
3 讨论
输卵管妊娠是常见的妇产科急腹症,是导致孕妇死亡的重要原因。据调查发现,输卵管妊娠与输卵管发育功能异常、慢性输卵管炎、盆腔子宫内膜异位等具有密切联系。据大数据调查显示,输卵管妊娠患病率逐渐上升,输卵管妊娠的临床治疗方式得到妇产科的重点关注,通过腹腔镜保守手术治疗可以有效的改善患者预后,达到治疗效果。有研究认为,在异位妊娠保守治疗过程中,血清β-HCG水平越高,成功率越低,治疗时间与恢复时间越长。
腹腔镜保守术为临床常用输卵管妊娠治疗手段,与输卵管切除术相比,其能最大程度地保留患者生育能力,因此,受到诸多具有生育要求患者的青睐[5]。但手术期间,难以完全将滋养细胞清除,而遗留的滋养细胞易造成持续性异位妊娠[6-7]。因此,如何有效预防持续性异位妊娠已成为提升输卵管保守治疗质量的关键。临床研究发现,腹腔镜保守手术治疗后患者持续异位妊娠的发生率较高,若出现持续性异位妊娠,不仅会对患者造成较大的身体伤害,还会导致患者出现较大的心理负担,还容易引发医患纠纷。腹腔镜保守术成功关键在于胚胎卓床的位置止血和预防处理方式,通过减少输卵管损伤来保质症患者术后的康复。为了降低腹腔镜保守术对患者输卵管的伤害,多采用正压冲洗法将妊娠物去除,避免输卵管刮伤。为了降低患者术后持续异位妊娠的发生率,通过轻刮妊娠位置来去除残留绒毛。在腹腔镜保守术治疗中,采用注射甲氨蝶呤方式,可以降低对输卵管的过度伤害,有利于降低术后持续异位妊娠的发生率。甲氨蝶呤属于叶酸还原酶抑制剂,可通过阻止二氢叶酸还原酶的生成,抑制增殖细胞与肿瘤细胞生成[8]。另外,甲氨蝶呤还可降低绒毛活性,阻碍滋养细胞发育生成,使妊娠组织脱离、坏死,促妊娠物自输卵管管壁脱离,从而降低术后创面出血,避免反复电凝止血而对输卵管造成二次损伤,起到保护输卵管功能作用。甲氨蝶呤对机体DNA的合成和细胞倍增会产生一定的干扰效果,为叶酸还原剂抑制药物,但是,药物治疗只适用于早期的异位妊娠患者,且要求患者无盆腔炎症史、无血液系统疾病、肝功能正常。腹腔镜手术治疗的可以在保留患者输卵管的基础上,保护卵巢和相关组织,可以降低并发症,安全性较高。根据本研究中术后患侧输卵管通畅观察,乙组较甲组通畅率明显提高,故甲氨蝶呤在腹腔镜输卵管保守手术中,显著增加患侧输卵管通畅率。甲氨蝶呤对输卵管妊娠的治疗具有显著的临床效果,但单使用该药物治疗需要较长的治疗时间,患者恢复缓慢,胚胎死亡,吸收速度缓慢,可导致输卵管局部阻塞或粘连,影响妊娠。药物治疗可能发生在输卵管妊娠组织清除不完全,可导致持续性输卵管妊娠的发生。腹腔镜保守性手术治疗未破裂输卵管妊娠,有利于对病变部位的清晰观察,彻底有效地清除病变部位的血栓和绒毛,防止输卵管妊娠的持续发生,同时有利于减少盆腔粘连,恢复输卵管的正常解剖位置,减少输卵管的狭窄和堵塞,提高输卵管通畅率,有效减少器官暴露,减少手套敷料和组织接触,降低腹部感染的可能性。
张晶晶等[9]文献中报道,甲氨蝶呤能改善机体HCG水平,促使附件包块吸收,帮助患侧输卵管通畅,预防持续性异位妊娠。张华[10]研究中关于在腹腔镜保守治疗中甲氨蝶呤的应用价值展开探讨,结果显示:观察组持续性异位妊娠率(3.33%)与对照组异位妊娠率(26.67%)相比,显著较低。本研究中,乙组持续性异位妊娠发生率(5.26%)与甲组持续性异位妊娠发生率(23.68%)相比,明显较低。这与上述研究结果相一致,均说明甲氨蝶呤联合腹腔镜保守术治疗能降低持续性异位妊娠率。
综上所述,甲氨蝶呤结合腹腔镜保守术在输卵管妊娠治疗中的应用,提高患侧输卵管通畅率,降低持续性异位妊娠发生率。

