生物医用抗凝血性材料的研究进展
苏瑞,闫莉华,代庆海,徐健,曹宇,蒋贝,于美丽(通信作者)
天津市第二人民医院肝病医学研究所 (天津 300192)
生物医用材料是一种与生物系统接触,对生物体病损组织、器官进行诊断,治疗、修复及诱导再生或增强其功能的高新技术材料[1-2]。生物医用材料可用于治疗心血管疾病患者,为其提供人工心脏或人工血管;还可用于控制药物和生物活性物质的释放;也能用于骨和牙齿等硬组织的更替和修复[3-4]。按照材料功能性,生物医用材料分为可降解材料、组织工程材料与人工器官、齿科材料、控释材料、仿生智能材料、临床诊断及生物传感器等[5-6]。最初生物医用材料的研究需满足治疗疾病的目的,而现在着重于改善材料生物相容性,从而减少并发症的发生,提高患者生命质量及医院医疗水平[7-8]。尽管功能性机械心脏瓣膜、血管支架、血液充氧器和血泵已经在临床上被广泛使用,但合成材料与血液之间产生的影响,如破坏红细胞、血小板,吸附血液中的蛋白和电解质,造成血栓形成和血栓栓塞事件,成为临床需要解决的难点[9-12]。
1 与血液接触的生物医用材料的安全性能要点
在临床应用和生物技术中,多数生物医用材料会涉及到与血液接触,如冠状动脉支架、生物心脏瓣膜、血液透析器、人工肺、导管等。这些材料与血液接触后可能会产生一系列安全问题,例如诱导血栓形成,引起感染或其他并发症。因此,涉及与血液接触的生物医用材料,需要重点关注材料的安全性能,主要包括抗菌性能、生物相容性、血液相容性等。
1.1 抗菌性
抗菌性是生物医用材料应用过程中重要的安全性能评估标准[13]。与血液接触的材料可能会被细菌、真菌和微生物感染,其中内毒素是细菌的常见污染物,忽视其存在,可能引发并发症,甚至导致患者死亡,同时还会使生物医用材料无法发挥其真正的生物学作用[14]。随着生物医用材料的广泛应用,越来越多的人面临着以医用材料为主的感染。因此,生物医用材料的低毒性和抗菌活性变得尤为重要。从以下三个方面着手可以减少以生物医用材料为主的感染:(1)对生物医用材料进行灭菌处理;(2)使用生物医用材料时按医嘱服用抗生素;(3)提高生物医用材料的抗菌性能。
1.2 生物相容性
生物相容性是指生命体组织与生物医用材料之间相互作用产生的影响,包括组织相容性和血液相容性。其中分为两种原则:生物安全性原则和生物功能性原则。生物医用材料不是完全的惰性材料,对于机体生物医用材料是抗原,会产生刺激,还可能会激发机体进行免疫应答反应,所以生物医用材料不仅要满足临床治疗目的,将性能发挥到最大,而且还要具备与接触的组织和整个身体的良好生物安全性,同时对专业人员和环境无任何影响[15]。根据国标GB/T16886《医疗器械生物学评价标准》,生物相容性包括细胞毒性、全身毒性、迟发型超敏反应试验、刺激与皮肤致敏试验、与血液相互作用试验选择等,确定了生物医用材料的适用性,确保接触生物医用材料的患者人身安全。
1.3 血液相容性
血液相容性是对血管内血液形成血栓能力的影响,包括对血液的溶血现象,血小板黏附作用,白细胞数量和功能以及补体激活等血液生理功能的影响。血液相容性是与血液接触生物医用材料关键检测指标,其限制了血液接触生物医用材料的临床适用性[16]。血液是一个复杂的“器官”,由血浆、红细胞、白细胞、血浆蛋白、细胞因子和血小板组成[17]。因此,应着重研究分析生物医用材料与血液之间的不良相互作用,以防止血液成分的活化和破坏。吸附在生物医用材料表面上的纤维蛋白质层主要触发不良反应,如激活内在途径激活凝血系统,促进凝血因子与血小板相互作用,激活凝血酶,最终聚集形成血栓。
2 抗凝剂的临床作用及抗凝机制
凝血过程是一个复杂的生物防御系统,平衡抗凝和促凝过程才能保持血液的流动性,同时又能阻止受损血管出血[18]。血液与异物接触会涉及一期止血-血小板止血和二期止血-凝血级联反应。首先,一期止血包括白细胞表面黏附作用诱导血栓形成,血小板活化对诱导炎症反应的作用,以及补体、血小板和与血液接触的生物材料表面之间的作用[19-20]。二期止血包括外源性和内源性途径,其中内源性途径中Ⅻ因子被激活促进凝血酶原复合物形成,从而激活凝血酶原形成凝血酶,最后形成纤维蛋白凝块;外源性途径中Ⅶ因子被激活促进纤维蛋白的生成[21-24]。因此,探索医用生物材料如何激活这些先天系统和如何控制或防止这些作用的发生成为解决血液相容性问题的关键[25],见图1[16]。
除补体系统外,内源性和外源性凝血途径均可被激活。凝血激活导致血纤蛋白网络产生。此外,血小板可以黏附并聚集在表面上。白细胞的黏附和激活可导致多形核弹性蛋白酶和组织因子的释放,并导致外源性途径的激活。
Wendel和Defraigne与Pincemail等[26-27]研究发现血液与体外各种人工合成表面会导致非特异性的灌注后综合征,为减少副作用,可利用肝素涂层降低补体和白细胞活性,减少炎症介质引起的脑部并发症,有效改善材料的血液相容性。Bito等[28]认为第一代药物洗脱支架导致晚期支架血栓形成和支架内皮化,由2-甲基丙烯酰氧基乙基磷酰胆碱和微模式化氢化非晶碳等组成的药物释放平台可以有效地支持人脐静脉内皮细胞增殖,抑制血小板黏附,延缓心脏支架表面内皮化,为支架抗凝提供有效的屏障,抵抗血栓形成,同时Bito等[29]还发现类金刚石碳与用碱性成纤维细胞生长因子浸渍后的2-甲基丙烯酸氧基磷酸胆碱形成聚合物不仅能精准控制药物释放速率,还有效降低血小板黏附数量和增强细胞相容性。相关研究[30-32]表明通过测定全血凝固时间、凝血酶原时间和活化部分凝血活酶时间,具有高度疏水作用的纳米纤维膜表现出抗凝血作用,可降低血小板黏附,溶血率极低;也有研究[33-34]通过表面图案化技术证明天然多酚成分单宁酸表面丰富的没食子酰基,可以诱导与纤维蛋白原分子的强氢键相互作用,抑制纤维蛋白原构象发生变化,使被吸附的纤维蛋白原更接近天然构象,且α和γ链高度失活,从而更好地减少血小板的黏附作用。也有文献指出修饰惰性亲水基团或者将生物活性部分附加到目标表面等不同策略可减少血小板对材料的黏附作用,见表1。
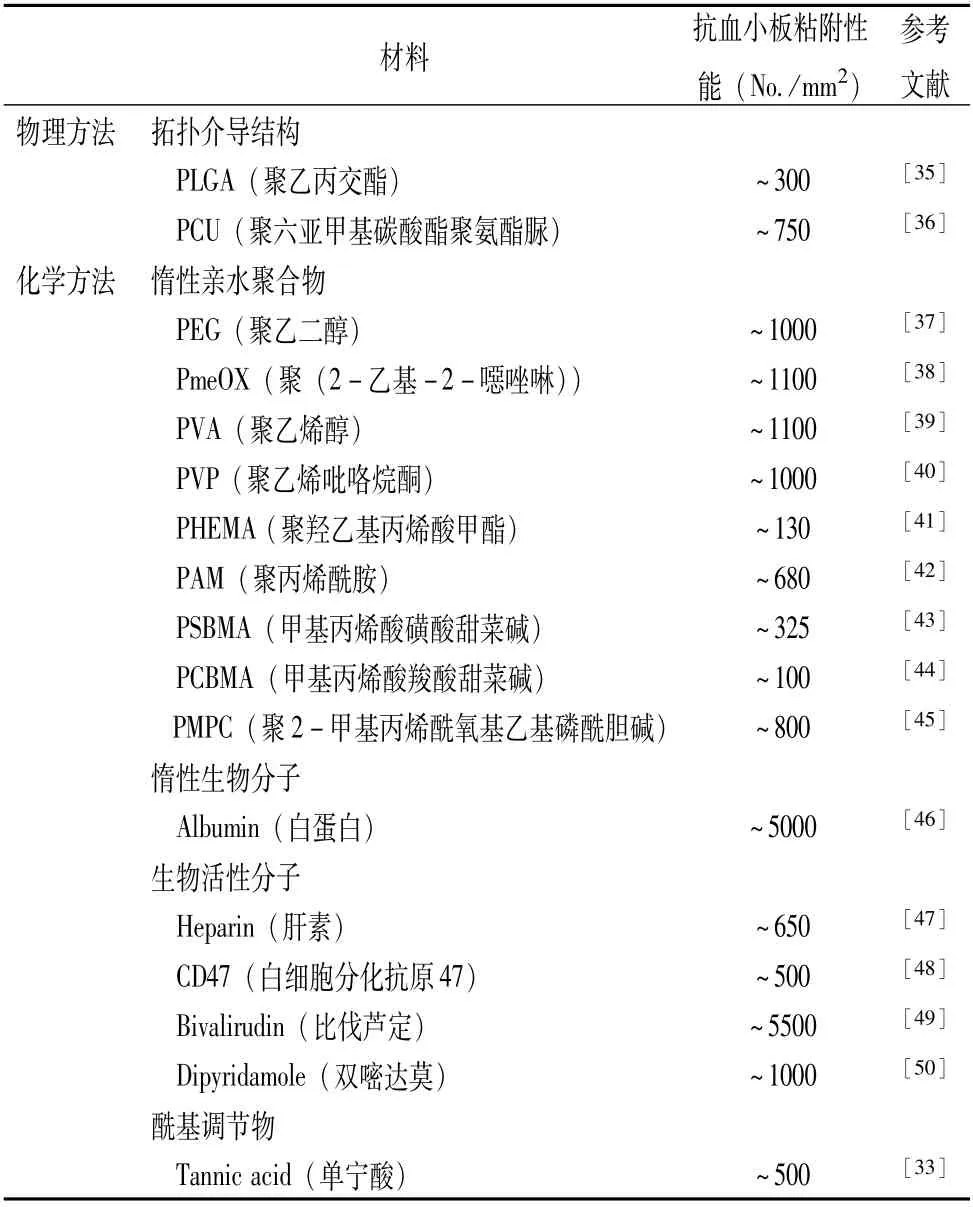
表1 当前减少血小板黏附的方法
3 展望
在我国,重症肝病、肾功能不全患者都要经历接受血浆置换或血液滤过等治疗手段,血液需由体内引出经过置换装置或透析膜才能达到疗效。目前还没有成功研制出抗凝血透析膜,但是血液在体外接触透析膜会诱发凝血机制导致治疗无法进行,临床医师会根据患者情况输注抗凝血药物,重症肝病及肾功能不全患者自身抗凝血功能已经很差,如果继续输注抗凝药物,可能会导致患者因出血而死亡。因此,临床对抗凝血性的生物医用透析膜的需求十分紧迫,结合多年来抗凝血材料的研究发展,这一问题将会最终得到解决,为提高患者生命质量和保障患者健康发挥重大作用。

