2型糖尿病肾病患者尿外泌体足细胞标志蛋白、二肽基肽酶Ⅳ与尿白蛋白/尿肌酐相关性
刘 洋,赵 锦,胡翠宁,杨 阳,刘 丹
锦州市中心医院1.内分泌糖尿病足亚专科;2.内分泌科;3.肿瘤科,辽宁 锦州 121000;4.南京医科大学附属老年医院 内分泌科,江苏 南京 210009
糖尿病肾病作为糖尿病的严重并发症,是增加糖尿病患者心血管疾病、终末期肾病乃至死亡风险的重要因素,患者需要以透析、肾移植等方式维持生命[1]。糖尿病肾病早期肾损害较为隐匿,通过常规的尿蛋白定量定性检查及患者的临床症状很难获得明显的发病证据,这对糖尿病肾病患者的早期诊断和治疗十分不利。近年来,细胞外泌体所携带的标志miRNA或蛋白质已被证实能够准确反映细胞的病理生理状况,且稳定的双层膜结构使其反馈的结果更加稳定和真实[2-3]。本研究旨在探讨2型糖尿病肾病患者尿外泌体足细胞标志蛋白(exosome podocyte marker protein,exosome-PCX)、二肽基肽酶Ⅳ(exosome dipeptidyl peptidase Ⅳ,exosome-DPP4)与尿白蛋白/尿肌酐(urine albumin creatine ratio,UACR)的相关性。现报道如下。
1 对象与方法
1.1 研究对象 选取锦州市中心医院自2018年9月至2019年9月收治的180例2型糖尿病肾病患者为研究对象。纳入标准:符合2型糖尿病肾病诊断标准[4];体质量指数20~30 kg/m2。排除标准:其他类型糖尿病,如1型糖尿病、成人迟发性糖尿病、妊娠糖尿病、继发性糖尿病等;合并糖尿病急性并发症,如酮症酸中毒、高渗昏迷、低血糖昏迷等;合并原发性肾-泌尿疾病,如肾小球或肾小管间质疾病、尿路感染等;应激性血糖升高,如心肌梗死、急性创伤、酒精性胃出血、各类感染等;近4周内应用过可能引起肾毒性的药物。按照UACR分级将患者分入A1组(UACR<30 mg/g)、A2组(UACR 30~300 mg/g)、A3组(UACR≥300 mg/g),每组各60例。另将同期60例健康体检志愿者纳入X组。4组研究对象均签署知情同意书。本研究经医院伦理委员会批准。
1.2 研究方法
1.2.1 实验室指标检测 嘱研究对象禁食热量8 h以上,晨起抽取静脉血并留取两管晨尿以备研究检测。血液样本经离心、沉淀后,以血清检测患者肌酐、糖化血红蛋白、空腹血糖等指标。
1.2.2 exosome-PCX和exosome-DPP4检测
1.2.2.1 透射电镜和纳米示踪技术 通过液压透析滤过法对新鲜尿液样本中的细胞外泌体进行分离和富集,以透射电镜进行外泌体的外在形态特征鉴定。根据考马斯亮蓝蛋白定量结果选取10 μg左右的细胞外囊泡,1∶1 000比例PBS稀释,通过纳米示踪技术进行外泌体的颗粒直径和浓度统计。
1.2.2.2 蛋白免疫印迹法 在富集细胞外囊泡的样本中加入5×loading buffer(上样缓冲液),5 min沸水浴(每个槽上样本量蛋白为4 μg,加缓冲液至40 μl)。加入10% SDS-PAGE凝胶电泳将蛋白分离后,用Bio-Rad电泳仪转移槽将凝胶蛋白条转移至PVDF膜上,封闭3 h后洗膜3次,浸入含有肾足细胞标志蛋白(podocyte marker protein,PCX)单克隆抗体和二肽基肽酶Ⅳ(dipeptidyl peptidase Ⅳ,DPP4)单克隆抗体的抗体缓冲液中,经过一抗和二抗之后,洗膜加入曝光液,取出滤干后定影扫描。
1.2.2.3 酶联免疫吸附法 将所需板条取出,将各浓度的标准品及待测样本置于相应的孔中,在37℃箱内孵育60 min后甩尽孔内液体,按照酶联免疫吸附法说明书进行洗涤和孵育后,每孔加入90 μl显色液,继续37℃孵育15 min后,加入50 μl终止液,随即在酶标仪上读取出样本数值。
2 结果
2.1 4组研究对象一般资料比较 与X组比较,A1组、A2组、A3组收缩压、舒张压、体质量指数、糖化血红蛋白、空腹血糖升高,差异有统计学意义(P<0.05)。A1组糖尿病病程最短,A2组长于A1组,A3组最长,差异有统计学意义(P<0.05);且随着糖尿病病程增加,收缩压、舒张压、肌酐、UACR逐渐升高,差异有统计学意义(P<0.05)。见表1。
表1 4组研究对象一般资料比较
2.2 4组研究对象exosome-PCX和exosome-DPP4表达水平比较 X组、A1组、A2组、A3组exosome-PCX分别为(1.18±0.37)ng/ml、(2.00±1.05)ng/ml、(2.41±1.13)ng/ml、(3.30±1.78)ng/ml,组间两两比较,差异均有统计学意义(P<0.05)。X组、A1组、A2组、A3组exosome-DPP4分别为(0.77±0.32)ng/ml、(1.55±0.22)ng/ml、(1.80±0.18)ng/ml、(2.69±0.75)ng/ml,组间两两比较,差异均有统计学意义(P<0.05)。
2.3 exosome-PCX、exosome-DPP4与UACR的相关性分析 exosome-PCX、exosome-DPP4与UACR呈正相关(r=0.873、0.805,P<0.05)。
2.4 exosome-PCX、exosome-DPP4、UACR对2型糖尿病肾病诊断价值 exosome-PCX ROC曲线下面积为0.673(95%可信区间0.585~0.756,P<0.05),exosome-DPP4 ROC曲线下面积为0.667(95%可信区间0.579~0.761,P<0.05),UACR ROC曲线下面积为0.669(95%可信区间0.573~0.752,P<0.05)。见图1。
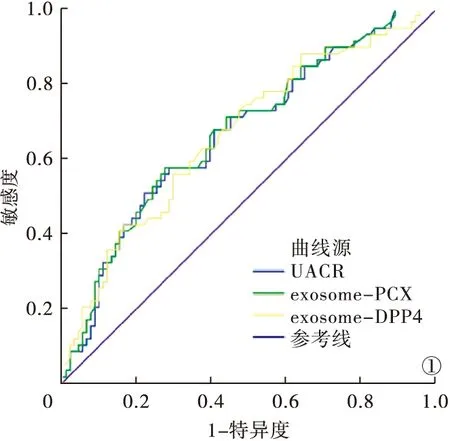
图1 exosome-PCX、exosome-DPP4、UACR对2型糖尿病肾病诊断价值ROC曲线
3 讨论
糖尿病肾病是糖尿病患者的常见慢性并发症,危害性极高。糖尿病肾病患者体内糖原反应物随着病程延长而不断蓄积,有20%~40%的糖尿病肾病患者会走向终末期肾病[5]。糖尿病肾病的理化检查样本以尿液为主,临床上通常选择尿蛋白、肾小球滤过率、UACR及炎症因子等作为肾损伤的标志物。但当肾功能(肾小球功能为主)出现较为显著的障碍时,肌酐才会出现异常改变;尿中白蛋白含量升高时,肾小球滤过率通常早已低于正常水平。因此,将单纯的尿蛋白定性定量检测作为糖尿病肾病的早期诊断指标存在一定的滞后性[6-7]。
随着分子生物学的飞速发展,外泌体逐渐成为疾病早期预防、诊断及治疗的研究热点。外泌体双层膜结构的隔离作用可防止RNA酶及蛋白酶水解,使细胞释放的信息保存更完整。尿中外泌体成分较为复杂,24 h新鲜尿液可发现尿外泌体约1 400种,且外泌体的种类和数目是动态的,与机体状态密切相关[8]。有研究报道,糖尿病肾病早期肾小球基底膜会出现增厚、扩张等改变,足细胞作为构成肾小球滤过屏障的重要组成部分,对大分子的渗透性作用大幅减弱,足细胞及其碎片(通常认为是exosome-PCX)会随着尿液排出,因此,exosome-PCX是早期肾损害的标志物之一[9]。DPP4作为一种高度保守的外肽酶,分布在血液、尿液等体液中,能够通过刺激多种因子表达而刺激肾系膜增殖、膜外基质蓄积,从而导致肾基底膜增厚,引起肾功能障碍。有研究发现,糖尿病患者尿exosome-DPP4表达显著升高,且在短时间内结构稳定,是较好的动态监测糖尿病疗效的指标[10]。因此,本研究选取exosome-PCX和exosome-DPP4作为观察指标。本研究结果显示:X组、A1组、A2组、A3组exosome-PCX、exosome-DPP4表达水平呈逐渐升高趋势,组间两两比较,差异均有统计学意义(P<0.05);且exosome-PCX、exosome-DPP4与UACR呈正相关(r=0.873、0.805,P<0.05)。这提示,尿外泌体可反映糖尿病肾病患者的疾病发展程度。在肾活检仍是肾病诊断“金标准”的背景下,UACR在肾疾病发生、发展中扮演重要角色,但其存在的滞后性,可能对糖尿病肾病早期诊断造成不利影响。本研究通过绘制ROC曲线得知exosome-PCX、exosome-DPP4的ROC曲线下面积与UACR相仿,这表明,尿exosome-PCX、exosome-DPP4与UACR一样对于2型糖尿病肾病有着较强的诊断价值。
综上所述,exosome-PCX、exosome-DPP4表达水平与UACR密切相关,具有与UACR相近的2型糖尿病肾病诊断作用,可预测早期2型糖尿病肾病的发生和发展。外泌体作为一种新型生物学非侵入性疾病诊断方法,有望代替肾组织病理活检,给糖尿病肾病患者带来新的诊疗希望。

