O-C3N4/Ag2O p-n异质结光催化剂增强可见光降解有机物
李 雪,刘婷婷,陶喜洋,田 飞,武占省
(西安工程大学 环境与化学工程学院,陕西 西安 710048)
0 引 言
随着科技的发展,难降解的废水已成为关注的焦点,目前常见的处理方法有物理吸附法[1]、生物法[2]、芬顿法[3]等,但是都具有一定的局限性,而光催化技术由于价格低廉、制备工艺简单、处理较为彻底而广泛应用于有机物的降解[4]。光催化剂在一定频率的光源照射下受激产生电子-空穴对,随后通过一系列化学变化诱导生成可降解污染物的活性自由基[5-6]。因此,当光源一定时,随着半导体催化剂的带隙值变窄,激发了更多的光生电子-空穴对[7-8],然而因存在光生电子-空穴对快速复合的缺点,极大地限制其光催化活性。前人通过离子掺杂[9]、异质结构建[10]等方法对单一半导体催化剂进行改性来提高载流子分离效率,从而提高对污染物的降解效率。
石墨氮化碳(g-C3N4)是一种n型聚合物半导体,因其具有吸收可见光波段的能带结构,抗化学腐蚀和高温能力强,而被应用于光催化领域;然而,g-C3N4电子-空穴对复合率高,对可见光利用率低,影响了其催化活性。采用金属或非金属掺杂[11-12]、形貌控制[13-14]、与其他半导体复合[10]等方法对g-C3N4进行改性以提高其光催化性能,其中与其他半导体构建异质结可提高光生电子-空穴对的分离效率,减少电子空穴复合,从而提高光催化效率[15]。前人利用窄带隙p型半导体催化剂Ag2O与g-C3N4之间的能带匹配形成p-n异质结[10,16-17]。与传统复合光催化剂相比,p-n异质结有助于光生电子和空穴的转移,但仍存在载流子复合效率高等问题。因此提高复合光催化剂的可见光响应,同时降低载流子复合效率是光催化实际应用的一大挑战[10]。
因环糊精具有特殊的腔体结构,将其固定到载体表面,继而用于污染物的去除研究[18]。CHEN等以微波辅助一步法合成了Ag和β-环糊精共掺杂的二氧化钛/活性炭并用于光催化降解萘[19]。迟悦等采用分步合成法成功制备出β-环糊精修饰的磁性纳米材料(Fe3O4-CD),并对水中甲基橙分子的吸附去除效果进行探究[20]。虽然前人利用环糊精在一定程度上提高了复合光催化剂的性能,但仍存在光生电子-空穴对复合率高等问题。
本文以三聚氰胺和β-环糊精为原料制备了O-C3N4,以O-C3N4为前驱体,通过原位沉积法制备不同质量比的O-C3N4/Ag2O复合光催化剂,表征单一及复合催化剂的结构和光学性质,并通过在可见光下降解甲基橙、诺氟沙星测试其光催化性能。
1 实 验
1.1 试剂和仪器
1.1.1 试剂 β-Cyclodextrin(β-CD,Admas);三聚氰胺(C3H6N6,Admas);氢氧化钠(NaOH,GENRAL-REAGENT);硝酸银(AgNO3,天津市科密欧化学试剂有限公司);以上试剂均为分析纯。去离子水(实验室自制)。
1.1.2 仪器 紫外可见分光光度计(UV-2600,日本岛津);X射线衍射仪(XRD,Mini Flex600,Japan);场发射扫描电镜(SEM,FlexSEM1000,日本日立公司);透射电子显微镜(TEM,Tecnai G2 F20,美国FEI公司);傅里叶变换红外光谱仪(FTIR,NICOLET 5700,美国尼高力公司);X射线光电子能谱(XPS,250XIESCA,美国赛默飞世尔科技公司);紫外可见漫反射(UV-Vis DRS,U-3310,日本日立公司)。
1.2 O-C3N4光催化剂的制备
O-C3N4的合成参考课题前期的制备方法[18]。以三聚氰胺和β-环糊精为原料,利用煅烧法制备O-C3N4。同时,采用相同方法在未添加β-环糊精的条件下制备g-C3N4。
1.3 O-C3N4/Ag2O复合光催化剂的制备
在0.15 g O-C3N4中加入60 mL蒸馏水,超声分散0.5 h,向上述悬浊液中加1 g NaOH并磁力搅拌1 h后缓慢滴加浓度为0.1 mol/L的不同体积的AgNO3。所得到的沉淀物经离心、洗涤、干燥(30 ℃下)制得不同质量比的O-C3N4/Ag2O复合光催化剂(1∶1、1∶4、1∶8、4∶1)。在上述相同条件下不添加O-C3N4制备纯Ag2O[10]。
1.4 光催化性能测试
将所制备的20 mg催化剂(g-C3N4、O-C3N4、Ag2O、不同质量比的O-C3N4/Ag2O)置于反应器中,分别加入100 mL甲基橙(30 mg/L)、诺氟沙星(10 mg/L)溶液,超声分散5 min后在暗中磁力搅拌30 min以达到吸附-解析平衡。将悬浮液置于可见光下(300 W,光源距溶液的高度为13 cm),间隔固定时间后取样,离心样品并对上清液进行分析。利用紫外-可见分光光度计测上清液吸光度,并计算出有机污染物的去除率。去除率(η)和拟一级动力学模型的计算公式分别为
(1)
(2)
式中:C0为污染物的初始浓度;Ct为可见光照射t时间后的浓度;K为速率常数。
1.5 循环实验
每次做完降解实验后将反应器和离心后的溶液离心洗涤后收集,以备循环实验使用。
2 结果与分析
2.1 表征分析
2.1.1 SEM和TEM分析 质量比1∶1的O-C3N4/Ag2O、Ag2O、g-C3N4和O-C3N4的扫描电镜见图1。图1(a)中,层状的O-C3N4表面上附着Ag2O纳米粒子,这可能归因于表面粗糙的O-C3N4纳米片为Ag2O纳米粒子的生长提供了条件,使O-C3N4和Ag2O能够紧密结合并形成p-n异质结。图1(b)是Ag2O纳米粒子的形貌[18]。由图1(c)可以看到g-C3N4的皱纹形态是由薄片堆积形成且表面具有丰富的孔洞[10],由图1(d)可以看出O-C3N4和g-C3N4的形貌基本一致,只是比g-C3N4具有更多的缺陷,这为O-C3N4和Ag2O的结合及异质结的形成提供了可能。1∶1 O-C3N4/Ag2O的TEM见图1(e),所有的Ag2O颗粒都附着在O-C3N4的表面,从1∶1 O-C3N4/Ag2O的HRTEM图1(f)中可以看出,制备的复合光催化剂Ag2O和g-C3N4之间形成紧密界面,可促进异质结的形成,这有利于分离光生电子-空穴对,提高量子效率。

(a) 1∶1 O-C3N4/Ag2O (b) Ag2O

(c) g-C3N4 (d) O-C3N4
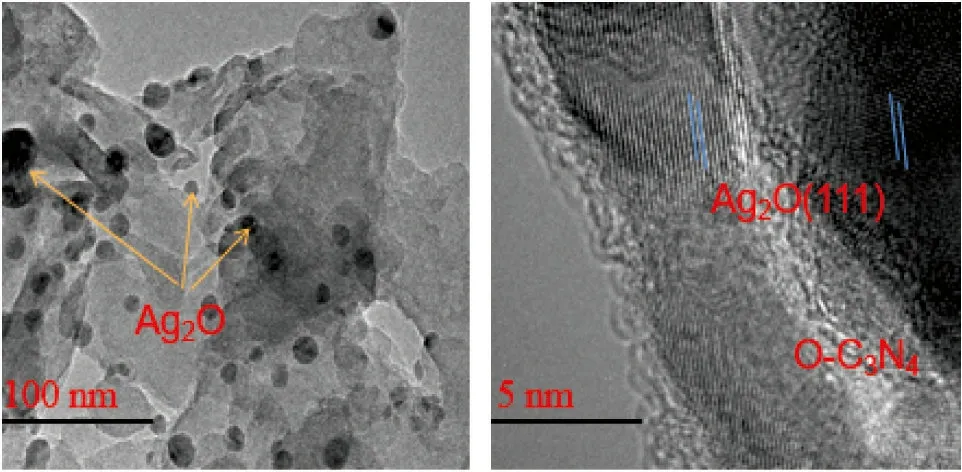
(e) 1∶1 O-C3N4/Ag2O (f) 1∶1 O-C3N4/Ag2O TEM HRTEM图 1 SEM图、TEM图和HRTEM图Fig.1 SEM、TEM and HRTEM
2.1.2 XRD分析 所制备样品的XRD图谱如图2所示。图2中,27.7°和12.8°处的衍射峰分别对应g-C3N4片层与片层堆叠形成的(002)晶面和片层内3-s-三嗪环重复堆叠形成的(100)晶面[10,18],与PDF标准卡片 (JCPDS-87-1526) 相对应。 O-C3N4在27.7°处的衍射峰较g-C3N4的衍射峰更尖锐,说明β-环糊精与C3N4共热解后所得的样品具有更好的结晶性。32.9°、38.1°、55.0°、65.9°和68.8°处的衍射峰分别指向Ag2O立方晶相的(111)、(200)、(220)、(311)和(222)面[10,16]。随着O-C3N4和Ag2O的质量比从1∶8提高到4∶1,g-C3N4典型的衍射峰逐渐出现且没有发现其他衍射峰。上述结果表明,Ag2O和O-C3N4共存,在制备复合光催化剂过程中没有形成杂质。
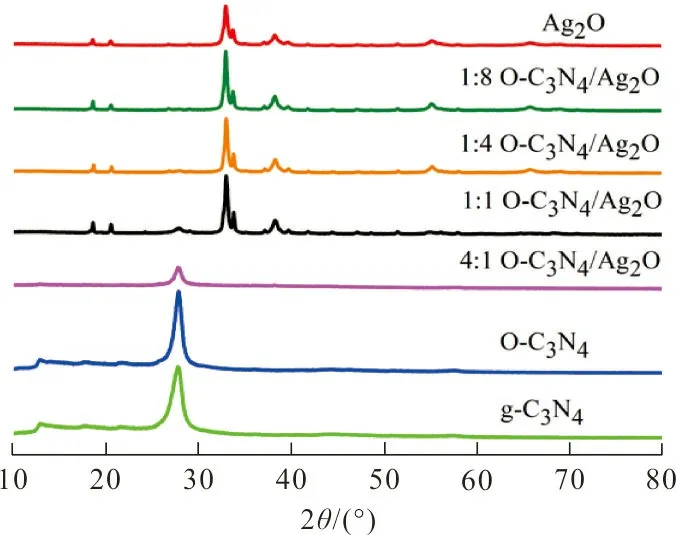
图 2 样品的XRD衍射谱图Fig.2 XRD spectrum of the samples
2.1.3 FTIR分析 通过FTIR研究了g-C3N4、O-C3N4和O-C3N4/Ag2O复合光催化剂的表面官能团。傅里叶变换红外光谱如图3所示。从图3可以看出,纯的g-C3N4样品有3个主要吸收区域:在3 000~3 500 cm-1处的宽峰对应H2O分子和未缩合的氨基;在808 cm-1处的特征峰归属于g-C3N4三嗪结构的呼吸震动[15]; 在1 240 cm-1、 1 360 cm-1、 1 410 cm-1、1 540 cm-1、1 640 cm-1处的特征峰归因于g-C3N4结构中C—N杂环的拉伸振动[21]。O-C3N4的特征峰与g-C3N4基本一致。对于纯Ag2O,在3 500 cm-1附近观察到的宽峰和1 661 cm-1处的峰归属于O—H的拉伸振动,而在1 388 cm-1处的峰属于表面吸附的水分子H—O—H的弯曲振动[10]。此外,在615 cm-1附近的宽吸收峰与Ag—O键的振动有关[16]。O-C3N4和Ag2O的特征峰重叠,在808 cm-1处峰的强度值随Ag2O含量的增加而减小。
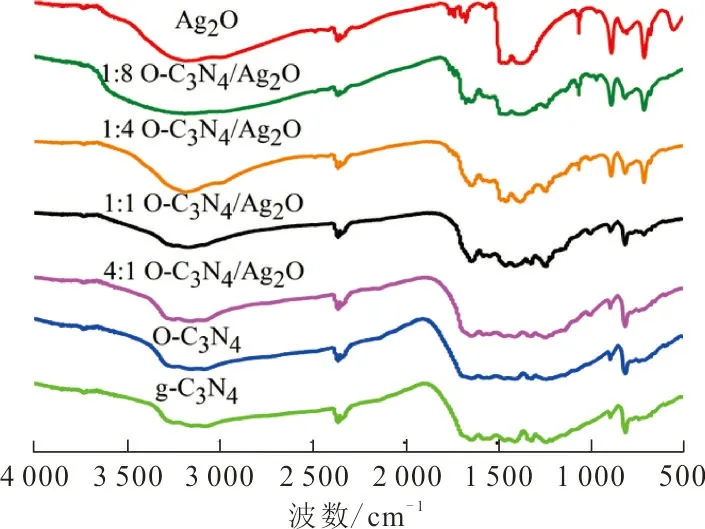
图 3 傅里叶变换红外光谱Fig.3 Fourier transform infrared spectrum

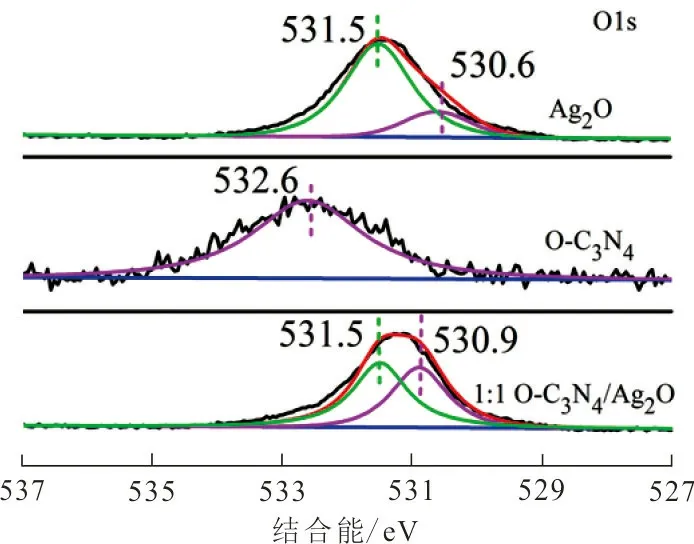
(d) O1s谱
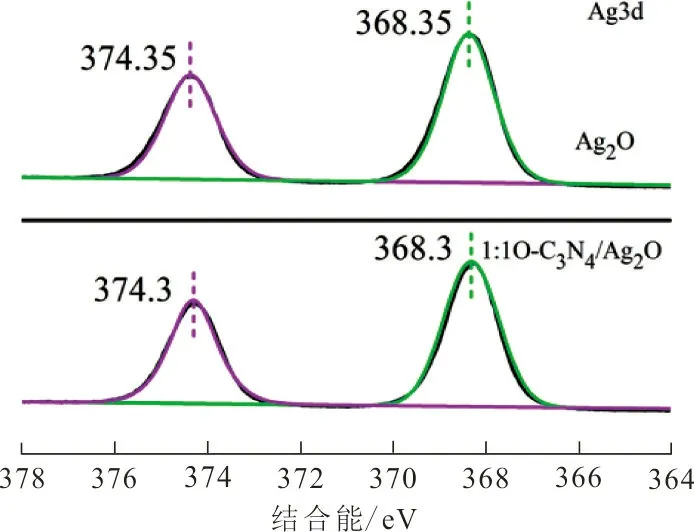
(e) Ag3d谱图 4 XPS谱和高分辨XPS图谱Fig.4 XPS spectrum and high-resolution XPS spectrum
2.1.5 UV-Vis分析 采用紫外-可见漫反射技术研究了Ag2O、g-C3N4、O-C3N4和1∶1 O-C3N4/Ag2O复合光催化剂的光吸收性能。由图5可知,与纯g-C3N4相比,β-环糊精对g-C3N4进行掺杂改性并在其表面引入Ag2O纳米粒子后,复合光催化剂的吸收范围发生红移,这可能是由于Ag2O本身具有较窄的禁带宽度,与O-C3N4能带匹配后增强其对可见光的吸收[25-26]。Ag2O样品在200~800 nm的紫外-可见范围内有较强的光吸收性能,使其具备优异的光催化活性[10]。紫外-可见漫反射研究结果表明,制备异质结复合光催化剂可大大提高光吸收性能,提高太阳光的利用效率,有利于提高光催化活性。
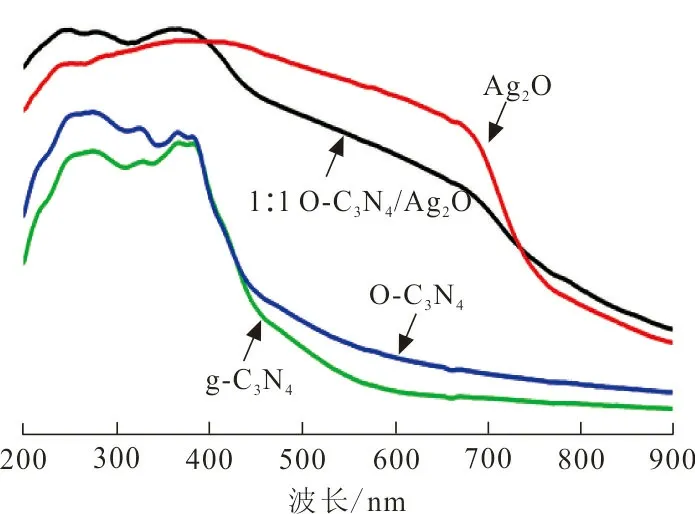
图 5 紫外可见漫反射光谱Fig.5 UV-Vis diffuse reflectance absorbance spectrum
2.1.6 PL分析 PL光谱用于分析半导体材料中光生电子和空穴对,以此来表明其转移和复合规律。图6是制备的样品的光致发光(PL)谱图。纯g-C3N4在400~800 nm范围内具有较强的峰值,β-环糊精掺杂后峰强度有所下降,Ag2O二次修饰后强度再次降低,表明掺杂与修饰均有效抑制了电子-空穴对的复合[27-28]。PL峰强度与半导体内电子-空穴对的复合有关,结果证明在1∶1 O-C3N4/Ag2O复合光催化剂中光生电子-空穴对可以在异质结的界面上有效地转移,从而增强其光催化活性[18]。
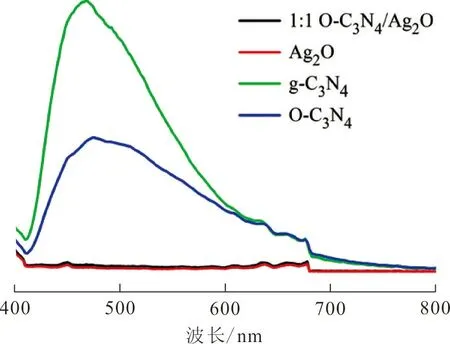
图 6 光致发光谱图Fig.6 Photoluminescence spectrum
2.2 光催化性能

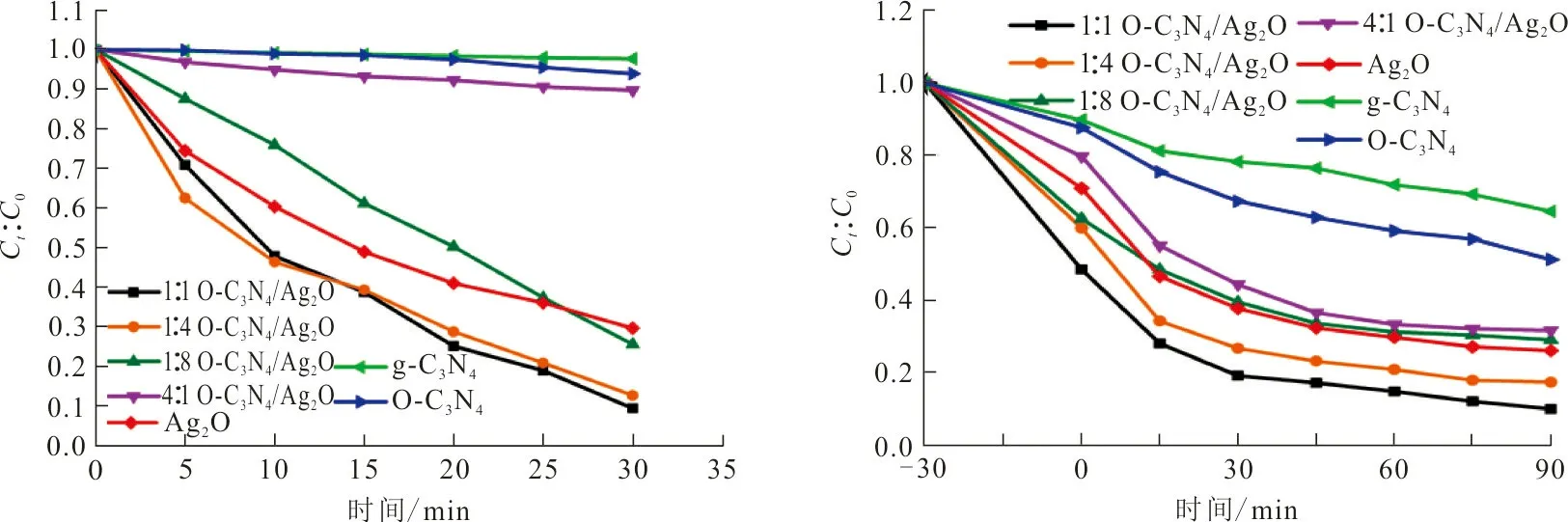
(a) 甲基橙降解 (b) 诺氟沙星降解
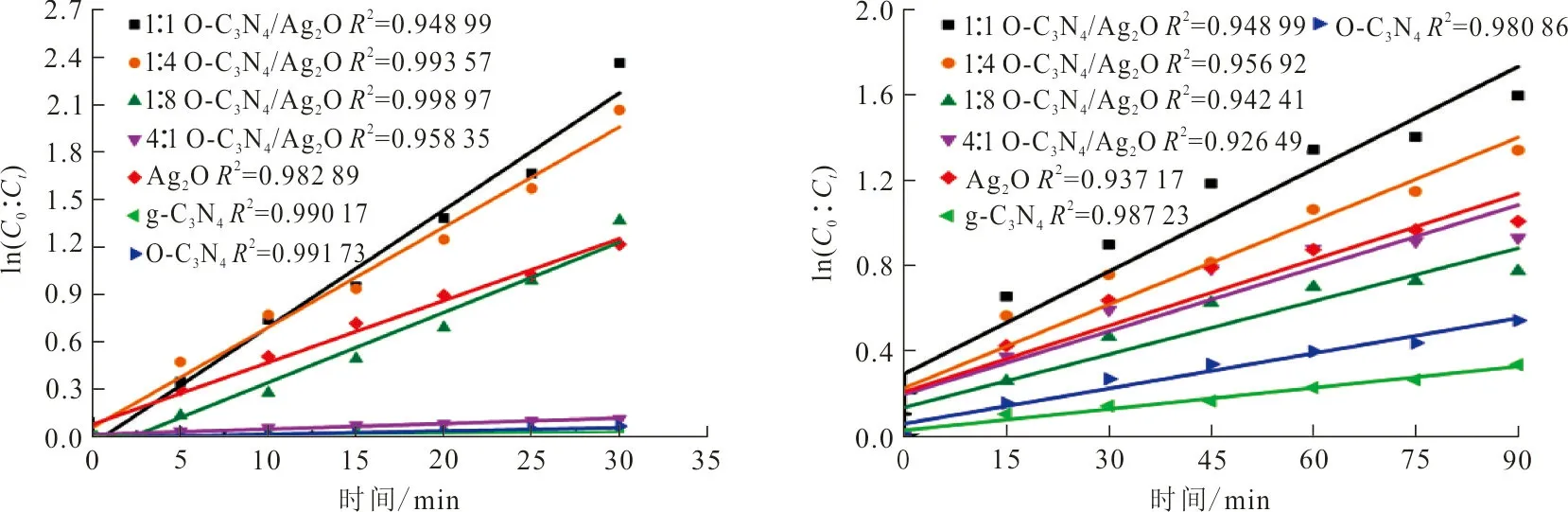
(c) 甲基橙降解一级动力学 (d) 诺氟沙星降解一级动力学图 7 可见光下甲基橙和诺氟沙星的降解及一级动力学Fig.7 Degradation and first order kinetics of methyl orange and norfloxacin under visible light
2.3 光催化机理分析
图8是添加乙醇(EA)、叔丁醇(TBA)和对苯醌(BQ)分别作为h+,·OH和自由基清除剂时,可见光下1∶1 O-C3N4/Ag2O对诺氟沙星的降解效果。
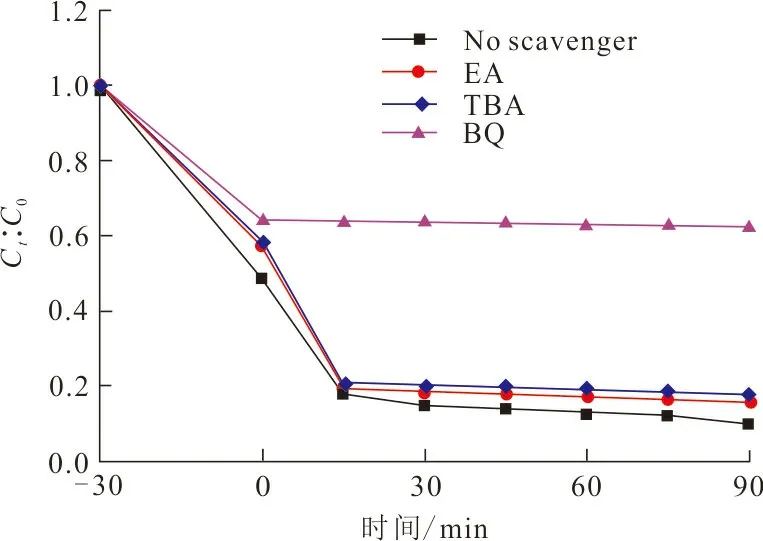
图 8 样品自由基清除实验Fig.8 Free radical scavenging experiment of samples
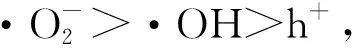
通过上述表征分析和降解性能实验可以推断出光催化的降解机理,如图9所示。
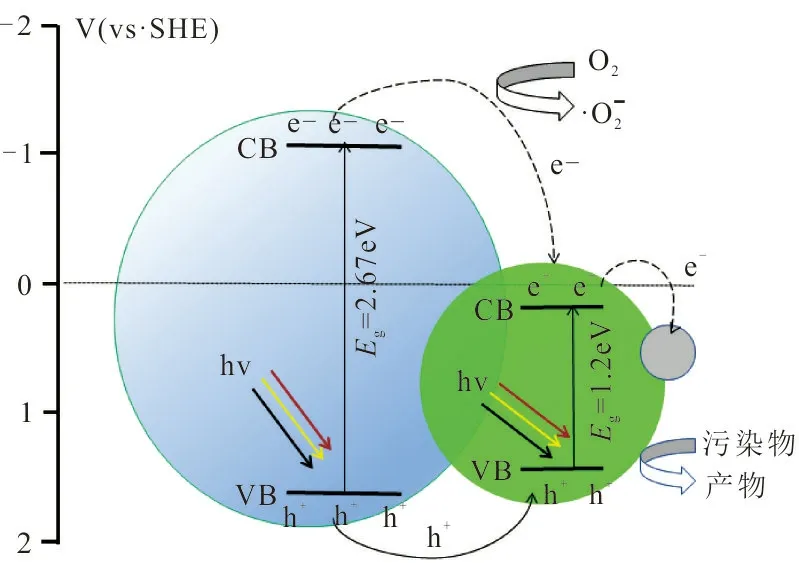
图 9 机理推测Fig.9 Mechanism speculation
图9可以看出,Ag2O纳米颗粒分散到O-C3N4的表面可以形成p-n异质结,在可见光照射下,Ag2O和 O-C3N4被激发产生光生电子-空穴对, 随后 O-C3N4导带位置上的空穴迁移至Ag2O的导带,价带上的电子迁移至Ag2O的价带位。在Ag2O价带和导带位置上的电子和空穴与溶液中O2和水分子进一步反应生成超氧自由基和羟基,并与目标污染物进行反应将其降解为无毒无害的小分子污染物。另一方面,O-C3N4(-1.02 V) 的导带 (CB) 比 Ag2O(0.19 V)更负,O-C3N4(1.65 V)的价带(VB)比Ag2O(1.41 V)更正[17],由于受内部电场和能带结构的影响,限制了复合光催化剂的电子转移,但加速了空穴的转移,有利于光生电子和空穴的有效分离。可见光激发产生的光生电子可以传输到Ag2O表面,而Ag2O可部分还原为金属Ag,这样也有利于电子迁移从而抑制光生电子-空穴对的复合[16]。因此,在O-C3N4/Ag2O异质结光催化体系中,光生电子-空穴对可以有效分离,从而比纯O-C3N4和Ag2O具有更优异的光催化活性。上述结果表明,O-C3N4/Ag2O的光催化活性增强不仅可归因于Ag2O的分散性和粒径的改善,O-C3N4和Ag2O之间异质结引起的光吸收性能的改善,而且还可归因于其内部电场和匹配能带结构的协同效应引起的光生电荷载流子的有效分离[17]。
3 结 语
用化学沉积法合成了不同质量比O-C3N4/Ag2O异质结光催化剂,并通过一系列表征手段对复合光催化剂的结构和物理性能进行分析,通过降解实验测定光化学特性。光降解甲基橙和诺氟沙星的实验表明,O-C3N4和Ag2O的质量比对可见光催化活性有着显著影响;质量比为1∶1 O-C3N4/Ag2O复合光催化剂在30 min对甲基橙的降解率为90.58%,在90 min对诺氟沙星的降解率为90.14%;UV-Vis证明O-C3N4和Ag2O复合后增大了对可见光的吸收范围;PL结果表明O-C3N4和Ag2O复合后提高了光生电子和空穴分离效率。环糊精掺杂石墨氮化碳使其表面具有更多的缺陷,更有利于形成异质结,而异质结的形成提高了光生电子-空穴对的分离效率,增强了O-C3N4/Ag2O复合光催化剂的光催化活性,所制备的光催化剂在可见光照射下具有相对稳定性,这也为制备高效、经济的异质结结构光催化剂提供了新的思路。

