微生物制备L-苹果酸的研究进展
袁 恺,周卫强,唐 堂,孙浩轩,杨 硕,彭 超,陈 博,卢宗梅,周 勇,李 义,3,周 哲,3,徐 晴,佟 毅,3
(1.中粮营养健康研究院有限公司 营养健康与食品安全北京市重点实验室 老年营养食品研究北京市工程实验室,北京 102209;2.中粮生物科技股份有限公司,安徽 蚌埠 233010;3.玉米深加工国家工程研究中心,吉林 长春 130033;4.南京师范大学 食品与制药工程学院,江苏 南京 210046)
L-苹果酸(L-malic acid,L-羟基丁二酸)是细胞代谢途径的必需中间物,也是一种重要的四碳二元羧酸,因其具有较好的酸度和口感,被广泛用作食品、饮料行业的酸化剂和增味剂,更被认为是传统酸化剂柠檬酸的替代品。2004年,美国能源部将L-苹果酸列为十二大基础化学品之一。作为潜在的C4平台化合物,L-苹果酸又可以进一步转化为多种用于纺织业、农业和医药行业领域的化学品[1]。L-苹果酸全球市场需求量已经达到6万t,并且保持4%的年增长率,而L-苹果酸的年产量仅为4万t[2]。
目前工业上主要以苯为原料,通过化学合成法生产DL-苹果酸,然后经分离纯化获得L-苹果酸。随着公众对全球变暖、环境污染和原油短缺的关注日益增加,通过微生物发酵法转化可再生资源生产各类有机物已经实现了工业化,而微生物发酵法生产L-苹果酸仍处于实验室研究阶段。本文中,笔者从菌株种类和合成代谢途径分析了微生物发酵产L-苹果酸的优势,并分别从可再生资源菌株的获得、外部环境胁迫条件、合成代谢途径改造和转运能力提高4个方面详细介绍了L-苹果酸的优化工艺,希望这些研究方法和改进措施能够为微生物发酵法合成L-苹果酸的工业化提供理论指导。
1 微生物法产L-苹果酸研究现状
1.1 L-苹果酸生产方式
L-苹果酸的获得方法主要有4种:直接提取法[3-4]、化学合成法[5]、酶转化法[6]和直接利用微生物转化糖质或非糖质原料的微生物发酵法[7]。由于这4种生产方式之间的优劣差异(表1),目前工业上主要以化学合成法和酶转化法生产L-苹果酸。微生物发酵法成本低廉,依赖可再生资源,可以减少对石油储备的依赖和CO2的排放,鉴于这些优势,国内已有生物制造企业开始进行尝试,如安徽丰原年产3万t L-苹果酸的微生物发酵生产线正在建设中。

表1 L-苹果酸不同生产方式的优缺点
1.2 L-苹果酸生产菌株
选择合适的菌株是实现微生物发酵法生产L-苹果酸的基础。细菌、酵母和丝状真菌都可以用作微生物发酵法生产L-苹果酸的开发平台[8-9]。Zhang等[10]通过基因敲除将产琥珀酸的大肠杆菌KJ060改造成产L-苹果酸大肠杆菌XZ658,发酵3 d后L-苹果酸产量达到33.9 g/L。2008年,Zelle等[11]以酿酒酵母为平台,过表达自身的丙酮酸羧化酶、苹果酸脱氢酶和异源表达裂殖酵母的苹果酸通透酶将L-苹果酸产量从出发菌株的12 g/L提高到59 g/L,葡萄糖转换率达到42%。
丝状真菌作为“微生物工厂”,因其天然优势常被用于大规模生产工业酶、有机酸和抗生素等物质。20世纪60年代,黄曲霉被发现可以用于合成L-苹果酸,并且产量达到58.4 g/L[7]。Battat等[12]将L-苹果酸发酵产量提高到113 g/L,产率约为0.59 g/(L·h)。尽管黄曲霉在生产L-苹果酸上有巨大产量优势,但是因为其自身会合成致癌物质黄曲霉毒素,所以无法满足食品行业的要求[13-14]。于是被认为是安全生产菌株[15]的黑曲霉和米曲霉受到关注。Knuf等[16]发现,野生型米曲霉NRRL 3485和NRRL 3488在正常情况下的L-苹果酸合成产量分别能够达到23.1和38.8 g/L,野生型米曲霉DSM1863的L-苹果酸合成产量能够达到43.47 g/L[17]。黑曲霉ATCC 9029、ATCC 9142和ATCC 10577同样具有L-苹果酸合成能力[18]。除了曲霉属外,青霉属的草酸青霉[19]、葡萄青霉[20-21]和菌核青霉[22]等也被发现可以用于L-苹果酸生产。
与其他种类的微生物相比,曲霉属微生物在 L-苹果酸合成能力方面优势更大,而且曲霉属微生物的基因序列注释完整,转化和基因敲除方法、诱变方法、高通量筛选方法成熟,有较好的底物适应性和pH适应性[23-24]。同时,它自身能够表达水解生物质的酶,实现木质纤维素等廉价生物质资源的高值化转化[25]。此外,工业上已经实现了使用曲霉类微生物生产柠檬酸、α-淀粉酶的工艺开发,这为开发微生物产L-苹果酸工艺奠定了基础。
1.3 L-苹果酸合成代谢途径
分析L-苹果酸的合成代谢途径,为微生物发酵菌种的选择和合成代谢途径的改造提供了理论指导。L-苹果酸合成代谢途径主要有4条(图1)。途径1:草酰乙酸还原途径。真菌中丙酮酸在丙酮酸羧化酶作用下转化为草酰乙酸。细菌中磷酸烯醇式丙酮酸在磷酸烯醇式丙酮酸羧化酶作用下转化为草酰乙酸,随后草酰乙酸经苹果酸脱氢酶作用还原为L-苹果酸。该途径中生成草酰乙酸时会固定CO2[26],所以每消耗1 mol葡萄糖生成L-苹果酸的最大理论产量是2 mol。同时这条途径还实现了能量ATP的守恒。途径2:三羧酸循环(TCA循环)途径。草酰乙酸与乙酰CoA缩合生成柠檬酸后进入TCA循环氧化生成L-苹果酸。由于在该途径中会有CO2释放,所以通过这条途径每消耗1 mol葡萄糖生成L-苹果酸的最大理论产量为1 mol。途径3:乙醛酸环形途径。异柠檬酸在异柠檬酸裂解酶作用下生成乙醛酸和琥珀酸,乙醛酸和乙酰CoA在苹果酸合酶作用下生成L-苹果酸。由于需要丙酮酸氧化脱羧生成乙酰CoA,所以这条途径每消耗1 mol葡萄糖生成L-苹果酸的最大理论产量为1 mol。途径4:涉及乙醛酸环形途径酶的非环形途径,此途径需通过丙酮酸的转化来补充草酰乙酸,所以每消耗1 mol葡萄糖生成L-苹果酸最大理论产量为1.33 mol。

Glu—葡萄糖;G-6-P—6-磷酸葡萄糖;PEP—磷酸烯醇式丙酮酸;PA—丙酮酸;OAA—草酰乙酸;MA—L-苹果酸;Acetyl-CoA—乙酰CoA;CA—柠檬酸;ISA—异柠檬酸;SA—琥珀酸;FA—富马酸;GA—乙醛酸;PEPC—磷酸烯醇式丙酮酸羧化酶;PYC—丙酮酸羧化酶;MDH—苹果酸脱氢酶;CS—柠檬酸合酶;ICL—异柠檬酸裂解酶;MS—苹果酸合酶;FUM—富马酸酶;C4T318—L-苹果酸转运酶;MAE1—L-苹果酸转运酶图1 L-苹果酸生物合成代谢途径Fig.1 Biosynthesis pathways of L-malic acid
从理论产量和能量守恒方面考虑,途径1最适用于L-苹果酸的积累。在真菌、细菌中草酰乙酸的不同转化途径为后期L-苹果酸合成代谢改造提供了理论指导;在途径2中,L-苹果酸的高浓度积累会造成琥珀酸、富马酸等杂酸富集,不利于下游L-苹果酸的分离纯化;对于途径3和途径4,它们仅仅是微生物胞内L-苹果酸合成代谢的补充途径。
2 微生物发酵法产L-苹果酸研究策略
2.1 利用可再生资源生产L-苹果酸
从依赖化石燃料转向利用可再生资源,尤其是一些工业副产物,是实现微生物发酵法生产L-苹果酸的首要任务。例如,生物柴油行业主要副产物粗甘油在2020年达到450亿L,其中甘油占比高达67%[27]。同样,国内生物燃料乙醇产能在2018年已经达到320万t,其生产过程中的副产物稀釜馏物中甘油成分占比达到17%。将粗甘油转化为L-苹果酸,不但有利于新能源的生产、减少化石燃料的使用,而且还可提高副产物的附属价值[28-31]。Iyyappan等[32-33]通过适应性进化获得的黑曲霉MTCC 281 mutant,在25 ℃条件下以未经处理的粗甘油为底物发酵192 h,L-苹果酸产量从出发菌株的70.32 g/L提高到92.64 g/L。West[18]则发现,黑曲霉ATCC 9142和10577可以直接利用稀釜馏物中的甘油成分生产L-苹果酸,利用率超过95%。这表明来自工业的副产物粗甘油可以直接用于L-苹果酸的微生物发酵生产,这必将大大降低L-苹果酸的生产成本。
玉米是我国第一大粮食作物,年产量超过2.5亿t,其中玉米粒已被完全开发为淀粉、纤维饲料、蛋白饲料及玉米胚芽油等商品,但是玉米秸秆、玉米芯等木质纤维素资源丰富、利用度却很低[34],是微生物发酵法生产L-苹果酸的理想原料。Deng等[35]直接利用粉碎的玉米秸秆作为发酵原料,通过嗜热单胞菌发酵5 d后,L-苹果酸产量达到21.47 g/L。玉米芯可以通过酸或酶水解成微生物可以利用的五碳糖或六碳糖,为了削弱玉米芯水解期间生成的糠醛、甲酸和乙酸等副产物对微生物的生长毒害作用,Zou等[36]采用适应性进化的方式提高了出芽短梗霉对玉米芯水解副产物的耐受性,经过9批次发酵后,L-苹果酸的产量和产率分别达到38.6 g/L和0.40 g/(L·h),高于第一批的27.6 g/L和0.29 g/(L·h)。
通过菌株筛选或驯化获得可以利用粗甘油、木质纤维素等可再生资源的菌株,是实现微生物发酵法生产L-苹果酸工业化生产的第一步。在此基础上,通过对发酵过程的优化和对合成代谢途径的改造,能够再次提高L-苹果酸的发酵产量。
2.2 利用外部环境胁迫积累L-苹果酸
外部环境胁迫是所有微生物积累有机酸的常见方式,而控制氮源种类可以直接影响微生物碳通量流向。对出芽短梗霉而言,酵母粉有利于生物量的积累,(NH4)2SO4有利于L-苹果酸积累[36];而在嗜热单孢菌中,酵母粉和(NH4)2SO4的效果恰恰相反[37]。Knuf等[16]发现在米曲霉NRRL 3488的基因序列中存在类似于酵母转录因子Msn2/4的结合位点,在不同氮源胁迫下,基因出现不同程度的表达,从而决定是否将碳通量导向L-苹果酸的合成。这表明合适的氮源有利于L-苹果酸的积累。

2.3 改造合成代谢途径增强L-苹果酸的积累
增强微生物体内原有的L-苹果酸合成代谢途径是提高微生物生产能力的直接方法。Peleg等[41]通过13C示踪法发现,曲霉主要通过草酰乙酸还原途径积累L-苹果酸,其中关键步骤是丙酮酸的羧化和草酰乙酸的还原[42]。在米曲霉NRRL 3488中,Brown等[43]和Liu等[44]过量表达丙酮酸羧化酶和苹果酸脱氢酶,将两者表达量分别提升了4.8倍和2.1倍,L-苹果酸产量达到154 g/L,比出发菌株产量提高了26.23%,其中L-苹果酸产率达到0.94 g/(L·h),葡萄糖对L-苹果酸的转化率达到最大理论值的69%。
除了增强L-苹果酸合成代谢途径外,构建新的合成代谢途径同样可以促进L-苹果酸积累。在途径1中,真菌和细菌的草酰乙酸来源不同。嗜热单孢菌muC缺少丙酮酸羧化酶,由磷酸烯醇式丙酮酸羧化酶负责将磷酸烯醇式丙酮酸转化为草酰乙酸,于是Deng等[35,45]将谷氨酸棒杆菌ATCC 13032中的pyc基因引入嗜热单孢菌muC中,获得可以同时表达丙酮酸羧化酶和磷酸烯醇式丙酮酸羧化酶的工程菌株嗜热单孢菌muC-16,结果发现,经过改造后的菌株L-苹果酸产量达到62.76 g/L。与嗜热单孢菌muC相反,米曲霉依靠丙酮酸羧化酶催化生成草酰乙酸[46],于是Liu等[44]将细菌中的磷酸烯醇式丙酮酸羧化酶引入到米曲霉NRRL 3488中,构建了将磷酸烯醇式丙酮酸和丙酮酸同时转化为草酰乙酸的联合途径,解决了米曲霉NRRL 3488胞内草酰乙酸浓度低的问题,结果发现,L-苹果酸产量提高至58.5 g/L,比出发菌株提高了38.3%。
在正常情况下,苹果酸酶只具有催化L-苹果转化为丙酮酸的正向催化能力,而Dong等[47]发现来自拟南芥的苹果酸酶具有微弱的催化丙酮酸生成L-苹果酸的反向催化能力,并且L-苹果酸的最大理论产量同样为2 mol(式(1))。
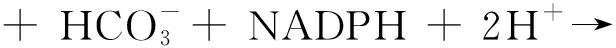
(1)
Dong等[47]对来自拟南芥的苹果酸酶进行了定点突变,并在大肠杆菌中构建了直接催化丙酮酸生成L-苹果酸的新途径,L-苹果酸的终产量约为3.62 g/L,比出发菌株产量提高了83.7%。经过分子手段[48]削弱胞内L-苹果酸向富马酸的转化和提高胞内NADPH的供应后,L-苹果酸产量最终达到21.65 g/L。尽管经过改造后L-苹果酸产量依然无法和曲霉类微生物相比,但是这种对酶的改造工艺和在微生物体内重新构建新的合成代谢途径的思路为菌株改造提供了新的改造方向(表2)。

表2 菌株合成代谢途径改造
2.4 通过改善细胞转运能力提高L-苹果酸的产量
在微生物发酵过程中,代谢物的积累往往会引起产物反馈抑制。在导致代谢产物无法大量积累的同时还会抑制细胞生长,甚至最终导致细胞破碎死亡[49]。细胞内L-苹果酸的积累会抑制TCA循环、糖酵解途径和ABC型转运系统[17,44],阻碍L-苹果酸合成代谢的正向进行和高浓度积累。
除简单扩散外[50],酵母内还存在负责L-苹果酸分泌的二羧酸转运蛋白MAE1[51-52]。Yang等[53]以炭曲霉ITEM 5010菌株为出发菌株考察二羧酸转运蛋白对炭曲霉合成L-苹果酸能力的影响,结果发现,当炭曲霉ITEM 5010胞内二羧酸转运蛋白表达量提高33倍时,L-苹果酸的产量也从出发菌株的0.4 g/L提高到32 g/L。Liu等[44]同时在米曲霉NRRL 3488菌株中过量表达了自身和来自酵母的编码二羧酸转运蛋白的基因c4t318、mae1,在两种二羧酸转运蛋白共同作用下,L-苹果酸产量提高至89.5 g/L,比出发菌株产量提高了52.5%。这些结果都表明,可以通过提高生产菌株中二羧酸转运蛋白的表达量,增加胞内L-苹果酸的胞外转运,碳通量持续流向L-苹果酸合成,最终实现L-苹果酸的高浓度积累。
除了提高ABC型蛋白转运能力外,还可以通过提高细胞膜通透性促进胞内L-苹果酸的胞外分泌来达到积累L-苹果酸的目的。在其他微生物发酵中提高细胞膜通透性主要有两个方法:一个是通过EDTA结合细胞外膜上彼此连接脂多糖的Ca2+和Mg2+,使脂多糖无法稳定细胞外膜,从而提高细胞膜通透性[54];第二个是通过在发酵液中添加Tween-80、Triton X-100等表面活性剂来抑制磷脂合成,造成细胞膜磷脂不足,导致细胞膜通透性增加[55]。
利用微生物生产聚L-苹果酸,再水解成L-苹果酸单体是这两年新兴的研究方向。首先,聚L-苹果酸不会对细胞的代谢和生长产生负面影响,能够实现胞内高浓度积累。其次,水解后的L-苹果酸纯度可以达到100%,减少了杂酸分离纯化的工艺操作和成本支出[56-59]。例如,Feng等[57]利用细胞固定化后的出芽短梗霉CCTCC M2012223进行发酵,聚L-苹果酸产量约为123.7 g/L,水解后L-苹果酸产量达到144.2 g/L,产率达到0.74 g/(L·h)。由此可见,采用微生物发酵法生产聚L-苹果酸再水解成为L-苹果酸单体为工业上获得高产量、高纯度的L-苹果酸提供了可能性。
3 结论与展望
随着环境污染加重、化石燃料消耗,化学合成法和酶转化法生产L-苹果酸将逐渐被微生物发酵法替代。但是目前利用微生物发酵法产L-苹果酸依然存在诸多障碍。例如:曲霉类微生物的人工载体稳定性差、转化率低、拷贝数低、表达水平低;发酵副产物中延胡索酸、富马酸等杂酸多等。在实验室条件下,通过筛选或适应性进化获得利用可再生资源的菌株、改造菌株原有的合成代谢途径等方式提高L-苹果酸发酵产量取得了一定成效,为加快实现微生物发酵法工业生产L-苹果酸提供了参考。

