芳香环修饰的5-苯基-2,4-戊二烯酰哌啶的合成和活性研究*
余丽丽,秦 兰,2,王成斌,田利娜,秦 蓓,2
(1.西安医学院 药学院,药物研究所,陕西 西安710021;2.成都医学院 药学院,四川 成都610500)
天然产物的结构研究和基于天然产物的结构修饰,是发现具有生物活性的化合物的重要研究基础[1-4]。生物碱是一类含有氮的天然有机化合物,具有类似于碱的性质。生物结构种类繁琐,按照其基本结构进行分类可分为约60类[5]。哌啶类生物碱就是其中的一类,该类生物碱被研究者们广泛研究,并证实其中多数具有一定的生物学活性[6-8]。此外,文献调研发现,一些通过共轭烃基连接芳香环、哌啶环或者脂肪胺的生物碱或者生物碱衍生物具有良好的生物学活性。例如,Min Han等[9]合成了芳香环修饰的肉桂酰胺类化合物,并且验证了其具有良好的抗抑郁活性。Natarajan等[10]合成了通过长共轭结构连接芳香环和哌啶环的生物碱衍生物,并验证了其良好的NF-kB的抑制作用、细胞迁移抑制作用。朱美玲[11]合成了芳香环修饰的阿魏酰哌啶类化合物,并证实该类化合物具有良好的抗氧化活性。
据此,本研究合成了通过长共轭酰胺键连接芳香环和哌啶环的4种生物碱类似物,并对其结构进行了表征。同时初步探讨了化合物4d对α-葡萄糖苷酶的抑制活性。
1 实验部分
1.1 原料与试剂
二氯甲烷(DCM)、乙酸乙酯(EA)、四氢呋喃(THF),均为分析纯,天津市恒兴化学试剂制剂有限公司;二甲基亚砜(DMSO)(AR天津市富宇精细化工有限公司);巴豆酸(98%)、哌啶盐酸盐(98%)、草酰氯(98%)、2,4-二甲氧基苯甲醛(98%)、3,4-二甲氧基苯甲醛(98%)、4-甲氧基苯甲醛(98%)、对氯苯甲醛(98%),萨恩化学技术(上海)有限公司;对硝基苯基-α-D-葡萄糖苷(PNPG)(98%),百灵威;α-葡萄糖苷酶(500000U·mL-1),上海金穗;Na2HPO4·12H2O、NaH2PO4·2H2O均为分析纯,西陇科学;Na2CO3(AR天津红岩试剂)。
AVANCEⅢ型400MHz核磁共振波谱仪(德国-瑞士Bruker公司);1260-6460A型三重四级杆液-质联用仪(美国安捷伦公司);JHX-4B型显微熔点测定仪(上海佳航仪器仪表有限公司);ZF-7N型智能暗箱式三用紫外分析仪(上海嘉鹏科技有限公司);HJ-2A型磁力加热搅拌器(常州国华电器有限公司);UV-2102 PCS型紫外可见分光光度计(尤尼柯(上海)仪器有限公司);Multiskan FC型自动全波长酶标仪(赛默飞世尔科技(中国)有限公司);Sybyl软件(2.1.1美国Tripos公司)。
1.2 合成方法

图1 芳香环修饰的5-苯基-2,4-戊二烯酰哌啶的合成Fig.1 Synthesis of 5-phenyl-2,4-pentadienylpiperidine modified by aromatic ring
1.2.1 巴豆酰氯(2)的制备 取巴豆酸(1.13g,13.17mmol)于100mL圆底烧瓶中,加入5mL无水DCM,超声分散,加入草酰氯1.1mL(31.7mmol),常温搅拌。反应完成后,浓缩,即得巴豆酰氯(2)。
1.2.2 巴豆酰哌啶(3)的合成 向100mL圆底烧瓶加入哌啶盐酸盐(1.69g,13.86mmol)、8mL四氢呋喃(THF)和10mL的1M NaOH溶液,0℃下。将上述制得的巴豆酰氯溶于3mL无水THF溶液,并将其缓慢滴加至反应液中,0℃下反应2h后,用乙酸乙酯萃取(10mL×3),合并有机层,分别用1M的HCl溶液、1M NaOH溶液和饱和NaCl洗涤1次,无水Na2SO4干燥,减压蒸馏,得淡黄色液体1.46g,产率为73%。
1.2.3 芳香环修饰的5-苯基-2,4-戊二烯酰哌啶(4a~4d)的合成 取2,4-二甲氧基苯甲醛(1.30g,7.8mmol)于100mL圆底烧瓶中,加入5mL DMSO,超声分散溶解,加入巴豆酰哌啶(1.19g,7.8mmol),搅拌同时加入1mL 50% KOH溶液,室温反应1h。用20mL H3PO4(30%)淬灭反应,加入20mL DCM进行萃取,水洗3次后用无水Na2SO4干燥,浓缩得到黄色固体产物(4a)1.41g,产率为60.0%。
用对氯苯甲醛(1.10g,7.8mmol)、4-甲氧基苯甲醛(7.8mmol,1.06g)、2,3-二甲氧基苯甲醛用量为(1.30g,7.8mmol)为原料分别合成4b、4c、4d,产率分别为63.0%、54.2%、58.1%。
1.3 分子对接
利用Sybyl 2.1.1中的Surflex-Dock模块对化合物和α-葡萄糖苷酶进行分子对接。
小分子准备 在Sybyl中建立化合物结构数据库,并对每个小分子进行加氢、加电荷(Gasteiger-Hückel),并选择Tripos力场进行能量优化(优化次数10000,能量收敛标准0.005kcal/mol·A),建立相关表单;
大分子准备和对接 从蛋白质数据库中(http://www.rcsb.org/pdb)下载α-葡萄糖苷酶晶体结构(1UOK),并采用Sybyl 2.1.1软件对蛋白结构进行准备。对接时选取蛋白结构中的文献报道的活性口袋为活性中心[12],每个化合物生成20个对接构象,并计算经验参数。
1.4 α-葡萄糖苷酶抑制剂的活性测定
参照文献[13]方法,按表1依次加入0.1mol·L-1磷酸盐缓冲液(PBS,pH值6.8)、抑制剂溶液和PNPG底物,混合均匀,于37℃孵育15min,取出加入37℃预热的酶溶液;混匀,于37℃水浴反应30min,加入Na2CO3溶液终止反应,实验设3个平行组。在405nm测定吸光度并按照下式计算抑制率:


表1 反应物添加量(μL)Tab.1 Adding amount of reactants
2 结果与讨论
2.1 巴豆酰哌啶的合成和表征
实验以巴豆酸为原料,先通过与草酰氯酰氯化制得巴豆酰氯(图1),再与哌啶盐酸盐在碱性环境下酰胺化合成巴豆酰哌啶。整个过程中应使用无水溶剂,保证实验仪器干燥,且由于酰氯的活泼性较高,中间产物巴豆酰氯需现制现用。
1H NMR(400MHz,Chloroform-d)δ6.84(dtd,J=14.7,7.7,7.3,6.3Hz,1H),6.28(dq,J=15.0,1.5Hz,1H),3.55(s,4H),1.88(dt,J=6.8,1.3Hz,4H),1.70~1.63(m,2H),1.58(ddd,J=9.5,4.7,2.7Hz,4H)。
2.2 芳香环修饰的5-苯基-2,4-戊二烯酰哌啶(4a-4d)的合成和表征
实验通过巴豆酰哌啶与3,4-二甲氧基苯甲醛、对氯苯甲醛、4-甲氧基苯甲醛、2,3-二甲基苯甲醛在碱性环境的羟醛缩合-消除反应合成芳香环修饰的5-苯基-2,4-戊二烯酰哌啶(4a~4d)。实验通过核磁共振氢谱和质谱对化合物的结构进行了表征。
4a:ESI-MS:M/Z=301.09;1H NMR(400MHz,CDCl3):δ7.52~7.39(m,2H),7.12(d,J=15.6Hz,1H),6.89(dd,J=15.7,11.1Hz,1H),6.52~6.45(m,2H),6.42(d,J=14.6Hz,1H),3.89~3.84(m,6H),3.60(s,4H),1.68(d,J=5.3Hz,2H),1.61(d,J=5.7Hz,3H)。
4b:ESI-MS:M/Z=274.99;1H NMR(400MHz,CDCl3):δ7.48~7.30(m,5H),6.97~6.76(m,2H),6.52(d,J=14.7Hz,1H),3.61(s,4H),1.74~1.66(m,2H),1.62(ddt,J=11.0,7.7,4.0Hz,5H)。
4c:ESI-MS:M/Z=271.35;1H NMR(400MHz,CDCl3):δ7.41(d,J=8.8Hz,3H),6.90(dd,J=9.2,3.0Hz,2H),6.81(d,J=8.2Hz,2H),6.45(d,J=14.6Hz,1H),3.85(d,J=0.9Hz,3H),3.61(s,4H),1.69(d,J=4.9Hz,3H),1.61(dd,J=7.0,4.0Hz,5H)。
4d:ESI-MS:M/Z=302.1;1H NMR(400MHz,CDCl3):δ7.47(ddt,J=14.4,10.0,4.8Hz,1H),7.09~6.95(m,2H),6.94~6.75(m,3H),6.48(d,J=14.7Hz,1H),3.98~3.88(m,6H),3.61(s,4H),1.68(s,3H),1.65~1.59(m,5H)。
2.3 计算机模拟筛选

表2 化合物与α-葡萄糖苷酶的对接结果Tab.2 Docking results of compounds withα-glucosidase
实验通过SYBYL软件中的Surflex-Dock对化合物与α-葡萄糖苷酶进行对接。对接打分分别有Total Score、D Score、PMF Score、G Score、Chem-Score、C Score[12]。起关键作用的是Total Score和C Score,其中Total Score标志了受体和配体之间的亲和力,打分越高,亲和力越大[12];C Score是其他5种打分的综合考量,其分值上线为5,该值越高表示配体和受体的对接构象越接近于实际分子的构象[12],通常认为C Score大于等于4才有意义。因此,在满足C Score大于等于4前提下,Total Score越大越好。表2为对接结果的经验打分,由表2可见,化合物4d的Total Score值最高。
本文对文献[12]报道的关键残基5A内形成的活性口袋与化合物进行了对接,图2为化合物4d与α-葡萄糖苷酶的对接图。根据文献报道,α-葡萄糖苷酶的活性口袋为深椭圆形,其边缘及内部存在一些极性区域[14],此外,文献报道该口袋为疏水性口袋[12,14],因此,本实验的化合物的结构中设计了长的疏水链段和疏水性的取代基,以期望提高化合物与α-葡萄糖苷酶的结合力,从而提高化合物的潜在活性。
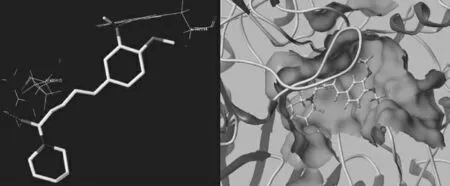
图2 化合物4d与α-葡萄糖苷酶的对接图Fig.2 Docking diagram of compound 4d withα-glucosidase
由图2可知,化合物4d能够很好地深入到α-葡萄糖苷酶的活性口袋中,并与活性口袋中的部分氨基酸残基形成氢键作用。其中,化合物4d结构上酰胺键的氧原子与氨基酸残基ARG415形成氢键,苯环上3位上的甲氧基中的氧原子可与氨基酸残基TRP294形成氢键。由此可见,化合物4d能结合于α-葡萄糖苷酶的活性口袋,且氢键和疏水作用是化合物与α-葡萄糖苷酶主要作用方式。
2.4 化合物4d对α-葡萄糖苷酶的抑制和酶动力学研究
为了验证化合物4d的活性,本实验对该化合物的α-葡萄糖苷酶的抑制作用进行了初步验证,结果见图3。
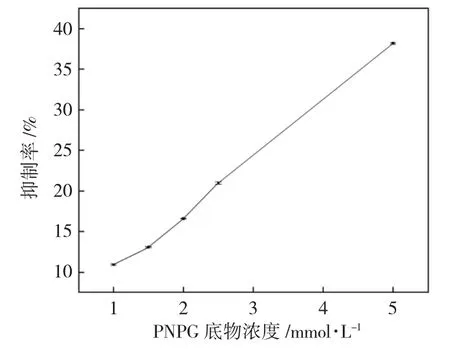
图3 4d对α-葡萄糖苷酶的抑制(±SD)Fig.3 Inhibition ofα-glucosidase by 4d
由图3可见,化合物4d对α-葡萄糖苷酶的抑制作用比较显著,在一定浓度范围内(1~5mmol·L-1),随着化合物4d的浓度水平的提高,抑制率显著提高。其中在浓度为5mmol·L-1时,化合物4d对α-葡萄糖苷酶的抑制率可达38.2%。
3 结论
实验通过酰氯化反应、酰胺化反应、羟醛缩合反应,合成了4种苯环修饰的胡椒碱衍生物,并对其结构进行了表征,该研究为芳香环修饰的5-苯基-2,4-戊二烯酰哌啶类化合物的系列化合成奠定了合成基础,为该类化合物后续的活性研究提供了化合物。计算机模拟分子对接实验筛选出化合物4d与α-葡萄糖苷酶具有相互作用,化合物与活性点位之间的作用主要依靠于氧原子与氨基酸残基之间的氢键以及分子与活性口袋之间的疏水作用。实验对化合物4d的α-葡萄糖苷酶抑制活性进行了初步探讨,验证了其具有抑制α-葡萄糖苷酶的作用。

