临床、细胞学和超声指标在不同病变程度甲状腺肿瘤患者价值分析
张汉新 边毅 李小宁 罗希
(宝鸡市中医医院,(1.外四科;(2.脑病二科;(3.超声科,陕西 宝鸡 721000)
甲状腺肿瘤是常见的头颈部肿瘤之一,其种类较多,可分为良性[滤泡型甲状腺腺瘤(FA)和乳头型腺瘤(PTA)]和恶性肿瘤(乳头状癌、滤泡状癌、髓样癌和未分化癌)。滤泡性甲状腺病变包括滤泡性甲状腺腺瘤和滤泡状甲状腺癌(FTC),且不同亚型之间存在固有的细胞学相似性,细胞学区分良性和恶性病变的能力受到限制,且受观察者重现性的显著影响。细针穿刺(FNA)结果具有较高的不确定性,需手术确定病变是否为恶性肿瘤。基于此患者常遭受不良干预,如良性病变的甲状腺全切除或恶性结节叶切除后的甲状腺全切除。以往的研究为了提高术前甲状腺滤泡良恶性病变的鉴别,试图描述其临床、影像学和细胞学特征,大多数研究局限于一种或两种亚型滤泡性甲状腺病变,不包括临床、超声和细胞学特征[1-2]。本文主要探讨通过检查良性滤泡状腺瘤和甲状腺滤泡状癌的临床特征来确定恶性甲状腺肿瘤的预测因素。
1 资料与方法
1.1一般资料 对2014年至2018年在我院接受甲状腺手术并确诊的362例甲状腺病变患者数据进行回顾性分析,患者均签订知情同意书。排除细胞学和/或成像结果不能相互对应或数据缺失的患者,剩下302例患者包含216例良性(FAs)和86例恶性(77例FVPTCs和9例FTCs)。记录结果包括以下内容:人口统计学资料(性别、年龄、种族),临床特征(表现症状、甲状腺癌家族史、头颈部放疗史、甲状腺共患病、结节一致性和移动性、多结节状态、胸骨下扩张、气管偏斜及术前喉镜检查结果),细胞学诊断,超声指标特征,外科治疗类型,病理结果。
1.2统计学方法 采用Stata13进行方差分析(正态分布变量)、Kruskal-Wallis(非正态分布变量)、χ2、单变量和多变量逻辑回归分析。将单变量分析P值<0.1的变量纳入多变量分析。细针穿刺存在固有的风险分层,超声数据部分丢失,所以细针穿刺和超声特征被排除在最终模型之外。为使结果更符合临床应用,使用同一逻辑回归模型运行两次:首先恶性肿瘤,然后是良性结节。P<0.05为差异有统计学意义。
2 结 果
2.1人口统计学数据 滤泡性甲状腺病变在女性中得发生率明显多于男性(P<0.001),女性的平均年龄显著低于男性(P<0.001)。滤泡状癌患者表现相对较年轻。其他人口统计学无显著差异。见表1。

表1 滤泡性肿瘤患者的人口学特征[n(%)]
2.2临床结果 有103例(48%)滤泡型腺瘤和65例(76%)滤泡状癌无症状(P<0.001)。无症状者随后表现为:良性,吞咽困难(50例,23%)、压迫感(51例,24%)、嘶哑(30例,14%);恶性滤泡性肿瘤,颈部肿胀或肿块(11例,13%),嘶哑或吞咽困难(4例,5%)、压迫感(4例,5%)。与有症状患者相比,无症状患者更有可能发生恶性肿瘤(14% VS 37%,P<0.001)。滤泡型腺瘤组与滤泡状癌组症状数无显著性差异,良性组和恶性组的大多数症状患者都只表现出一种症状(分别为76%和74%,P=0.79)。伴有甲状腺功能亢进的患者更容易产生良性病变(32% VS 8%,P=0.003)。滤泡状癌患者比滤泡型腺瘤患者更有可能具有甲状腺癌阳性家族史(14% VS 2%,P<0.001)或头颈部放疗阳性史(14% VS 7%,P= 0.004)。大部分患者表现出异常体检结果,体检异常患者更可能出现滤泡型腺瘤(76% VS 20%,P< 0.001)。体检异常者中,大多数结节为单发(56%)、活动型(87%)、软的(93%)和非触痛的(99%)。滤泡型腺瘤在多发结节患者[84% VS 65%(单发结节患者),P<0.001]、胸骨下结节患者[90% VS 70%(无胸骨下扩展),P<0.001]、气管偏斜患者[87% VS 71%(无气管偏斜),P= 0.01]中更为常见。
2.3细胞学结果 良性滤泡型腺瘤更可能与良性或不确定细胞学相关(86%),而滤泡状癌更可能与不确定、可疑或恶性细胞学相关(94%,P<0.001)。5例(2%)最终诊断为滤泡型腺瘤的患者最初细针穿刺报告为可疑恶性(4例,2%)或恶性(1例,<1%),而5例(6%)滤泡状癌患者最初的细针穿刺报告为良性。见表2。
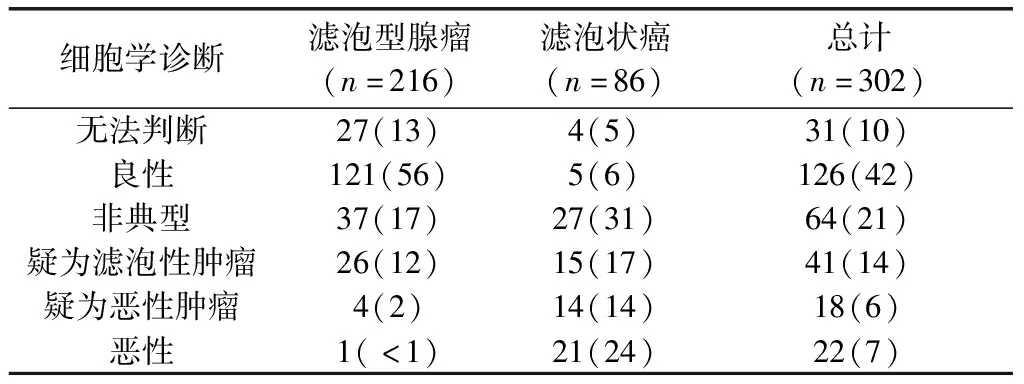
表2 根据甲状腺细胞病理学的细胞学诊断结果[n(%)]
2.4超声结果 对114例现有超声报告的患者(74例滤泡型腺瘤,40例滤泡状癌)回顾性分析表明,两组患者除钙化外的所有超声特征均相似(P>0.05)。大多数结节为实性(75%),同质的(58%),等回声(63%),边缘规则(96%),无晕(96%)或内部出血(67%)。超声检查发现钙化患者更容易发生甲状腺滤泡状癌(48% VS 33%,P=0.03)。
2.5手术方式 滤泡状癌患者最常见的手术方式是甲状腺全切除(38例,44%)和甲状腺全切除加淋巴结切除(27例,31%),滤泡型腺瘤患者最常见的手术方式是甲状腺全切除(149例,69%)和甲状腺小叶切除(29例,13%)。
2.6病理结果 滤泡型腺瘤的中位结节大小明显大于滤泡状癌(2.6 cm, 1.4~4.1 cm VS 1.6 cm, 1.1~2.8 cm;P<0.001)。结节大小分为≤2 cm、>2 cm且≤4 cm、>4 cm。结节尺寸≤2 cm的有36%为恶性(2 cm<结节≤4 cm,25%;结节>4 cm,10%;P<0.001)。多结节性甲状腺肿患者更容易出现滤泡型腺瘤(81% VS 55%,P<0.001)。桥本式甲状腺炎患者更有可能发生滤泡状癌(40% VS 25%,P=0.007)。甲状腺功能减退与Graves疾病无显著相关性(P>0.05)。见表3。

表3 良性和恶性滤泡病变基于结节大小的分布
2.7单变量分析 结果显示,性滤泡状癌的几率稍高于女性(P<0.05)。甲状腺癌家族史呈阳性,头颈部放射史,超声钙化与滤泡状癌的发生率显著增高相关(P均<0.05)。与良性细针穿刺结果相比,非良性细针穿刺与更高的肿瘤发生率显著相关(P均<0.05)。年龄>45岁,有症状患者、吞咽困难、压迫感或声音嘶哑与滤泡型腺瘤的几率增加相关(P均<0.05)。甲状腺功能亢进症患者出现滤泡型腺瘤的几率更高(P<0.05),体检异常患者、多发结节、气管偏移、胸骨下扩张、结节>4 cm或病理检查为多结节性甲状腺肿均与滤泡型腺瘤的几率增加相关(P均<0.05)。见表4。
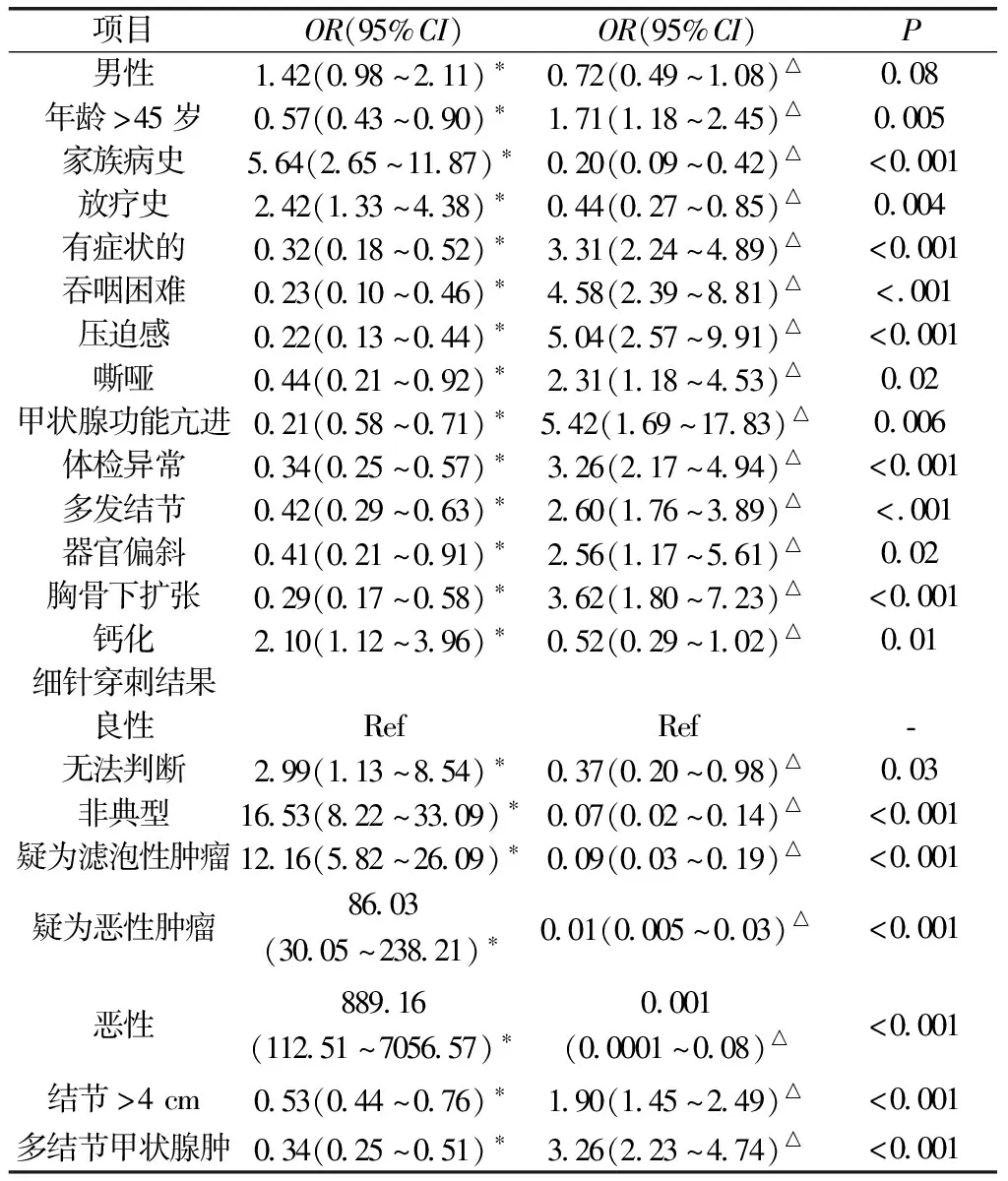
表4 滤泡状癌或滤泡型腺瘤相关因素的单因素分析
2.8多变量分析 结果显示,男性和甲状腺癌家族史患者患滤泡状癌的几率明显更高。有头颈部放疗史的患者患滤泡状癌的可能性是正常人的两倍。年龄>45岁的患者发生滤泡型腺瘤的几率增加。在出现的症状中,吞咽困难和压迫感与滤泡型腺瘤相关。结节≥4 cm更有可能是良性的。与预期一样,伴随甲状腺功能亢进的患者(7%的患者)更有可能出现滤泡型腺瘤。见表5。
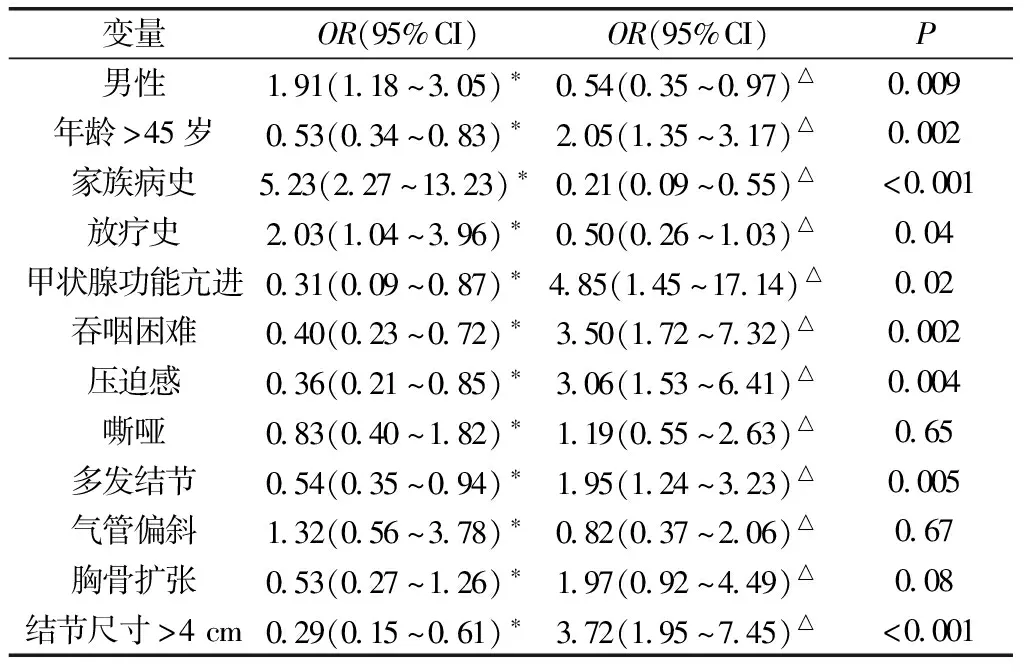
表5 滤泡状癌或滤泡型腺瘤相关因素的多因素分析
3 讨 论
研究[2-3]表明滤泡型腺瘤和恶性滤泡状癌的患者在单因素分析中表现出不同的临床特征。在控制了所有潜在的混杂因素后,其中一些差异不再显著。如声音嘶哑、多发结节、气管偏移或胸骨后扩张最初与良性滤泡病变相关,但在多因素分析中无显著相关性。在单因素分析中,性别不是恶性肿瘤的显著预测因子,但在多因素分析中,性别却成为滤泡状癌的预测因子,再次证实了以前的研究结果,即男性与甲状腺恶性肿瘤相关。
甲状腺滤泡状癌的其他预测因子是甲状腺癌家族史和头颈部放疗史。阳性家族史已被报道为分化型甲状腺癌的危险因素,与甲状腺乳头状癌患者有较强的相关性[4]。头颈部放疗是所有类型甲状腺癌的危险因素,接触放疗5~20年后会受影响[5]。滤泡型腺瘤和滤泡状癌的超声特征非常相似。本研究中单因素分析中唯一的预测滤泡状癌的超声因素是钙化。由于只有小部分患者(114/302)具有超声结果,不能将超声纳入多变量模型。曾经有报道钙化为滤泡性甲状腺结节滤泡状癌的超声指标[6-7]。最初表现为吞咽困难或压感症状的患者更可能出现良性滤泡甲状腺病变。可能是由于术前多年增长的良性滤泡病变的压力效应。另外,年龄>45岁与病理结果为良性的几率显著相关。可能是因为老年患者甲状腺结节的总体患病率较高,其中大多数是良性[8]。
本研究多因素分析显示,多发结节是滤泡型腺瘤的预测因子。结节>4 cm更有可能是良性的组织病理学。以往的研究大多认为恶性滤泡病变更大[2,8-9]。这种差异可能是由于研究设计不同,如研究人群和研究标准不同。恶性甲状腺结节比良性甲状腺结节生长更快,更多可能在细针穿刺结果后手术切除。而良性结节更可能在手术前被随访更长时间。良性滤泡性甲状腺病变的另一个独立预测因子是伴有甲状腺功能亢进。目前没有一项研究显示伴有甲状腺功能亢进是良性滤泡性甲状腺肿瘤的独立预测因子,因为功能亢进的甲状腺结节更有可能是良性的热结节[10]。
综上所述,临床独立预测因子可有助于术前鉴别良性和恶性滤泡甲状腺肿瘤。预测因子与细针穿刺和分子结果的结合可有助于改善对滤泡性甲状腺病变患者的临床管理。

