沙丁胺醇人工抗原的制备及ic-ELISA方法的建立
崔芳微,郭东光,李文明,朱艳平,李 鹏,孙国鹏,岳 锋,王选年*
(1.新乡学院生物技术研究中心,河南新乡 453000;2.郑州大学,河南郑州 450000)
沙丁胺醇(salbutamol,SAL)别名为舒喘宁,化学名被称为4-羟基-5-羟甲基苯基-α(叔丁胺)甲基苯乙醇胺[1],是人工合成的肾上腺素药物,具有β2-受体激动剂的作用,为白色结晶性粉末(图1)。SAL与“瘦肉精”克仑特罗促生长效果相同[2],其性质及检测方法的研究相对较少,检测手段也较滞后,因而逐步取代盐酸克仑特罗成为不法分子谋取暴利的新手段,造成的不良影响和危害也日趋严重,也越来越引起人们的重视。

图1 SAL化学结构式
目前,检测沙丁胺醇的方法有高效液相色谱法(HPLC)[3-5]、气相色谱-质谱联用法(GC-MS)、液相色谱-质谱联用法(LC-MS)[6]和酶联免疫吸附法(enzyme-linked immunosorbent assay,ELISA)[7]等。虽然GC-MS、HPLC和LC-MS方法准确可靠,但样品前处理繁琐,对仪器设备以及操作过程的要求较高,不适于生产、基层单位及现场检测,而SAL的快速检测对SAL监督起着至关重要的作用[8-9]。因此,针对当前SAL使用现状,建立快速、灵敏、方便的检测技术,对食品中SAL残留物的检测及防控具有重要的现实意义。免疫分析技术是一种常用的快速检测技术,特别是近年来在食品分析中得到越来越广泛的运用,其中ELISA法具有操作简便、快速、特异性和灵敏度高,费用低等优点,能够用于SAL检测的定性及定量测定,是当前应用最为广泛的兽药残留的检测方法[10]。
因此,本研究通过制备沙丁胺醇完全抗原,获得针对SAL的多克隆抗体,以此为基础通过对反应条件的优化建立了检测SAL的间接竞争ELISA(ic-ELISA)检测方法,为进一步开发快速检测SAL试剂盒和胶体金免疫层析试纸条奠定基础。
1 材料与方法
1.1 材料
1.1.1 主要试剂 沙丁胺醇(salbutamol,SAL)、特布他林(terbutaline,TBL)、西马特罗(cimaterol,CIM)、盐酸克仑特罗(clenbuterol hydrochloride,CLB)、盐酸齐帕特罗(zilpaterol hydrochloride,ZIL)、盐酸多巴胺(3-hydroxytyramine hydrochloride,DH)、莱克多巴胺(ractopamine,RAC)、达氟沙星(danofloxain,DAN)、泰乐菌素(tylosin,TYL)标准品,德国Dr.Ehrenstorfer GmbH公司产品;牛血清白蛋白(bovine albumin,BSA)、弗氏完全佐剂(Freund's complete adjuvant,FCA)、鸡卵清白蛋白(ovalbumin,OVA)、弗氏不完全佐剂(Freund's incomplete adjuvant,FIA),德国Sigma公司产品;琥珀酸酐、三硝基苯磺酸、HRP-羊抗兔IgG,北京索莱宝生物科技有限公司产品。
1.1.2 实验动物 新西兰大白兔体重约1.5 kg,由新乡学院生物技术研究中心提供。
1.1.3 主要仪器 多功能酶标仪(Enspire),美国Bio-Rad公司产品;加热磁力搅拌器(CMAGHS4),德国IKA公司产品;紫外可见分光光度计(UV-3010),日本Hitachi公司产品;透析袋(MD25),北京索莱宝生物科技有限公司产品。
1.2 方法
1.2.1 SAL完全抗原的制备及鉴定 用琥珀酸酐法先将SAL的羟甲基与琥珀酸酐发生醇解反应,生成琥珀酸衍生物(SAL-HS)(图2)。用混合酸酐法,以三乙胺作为催化剂,将SAL-HS与BSA载体蛋白偶联,合成SAL-BSA完全抗原[11](图3)。参考史晓亚等人的方法[12],用活化酯法,将SAL-HS与OVA载体蛋白偶联,合成SAL-OVA完全抗原(图4)。使用Bradford蛋白浓度测定试剂盒检测人工抗原SAL-BSA和SAL-OVA的浓度,并用SDS-PAGE法和紫外光谱扫描法鉴定是否偶联成功。根据Torres等所述[13],利用三硝基苯磺酸(2,4,6-trinitrobenzene sulfonic acid sol,TNBS)法检测SAL-BSA与SAL-OVA的偶联比。

图2 SAL-HS合成过程
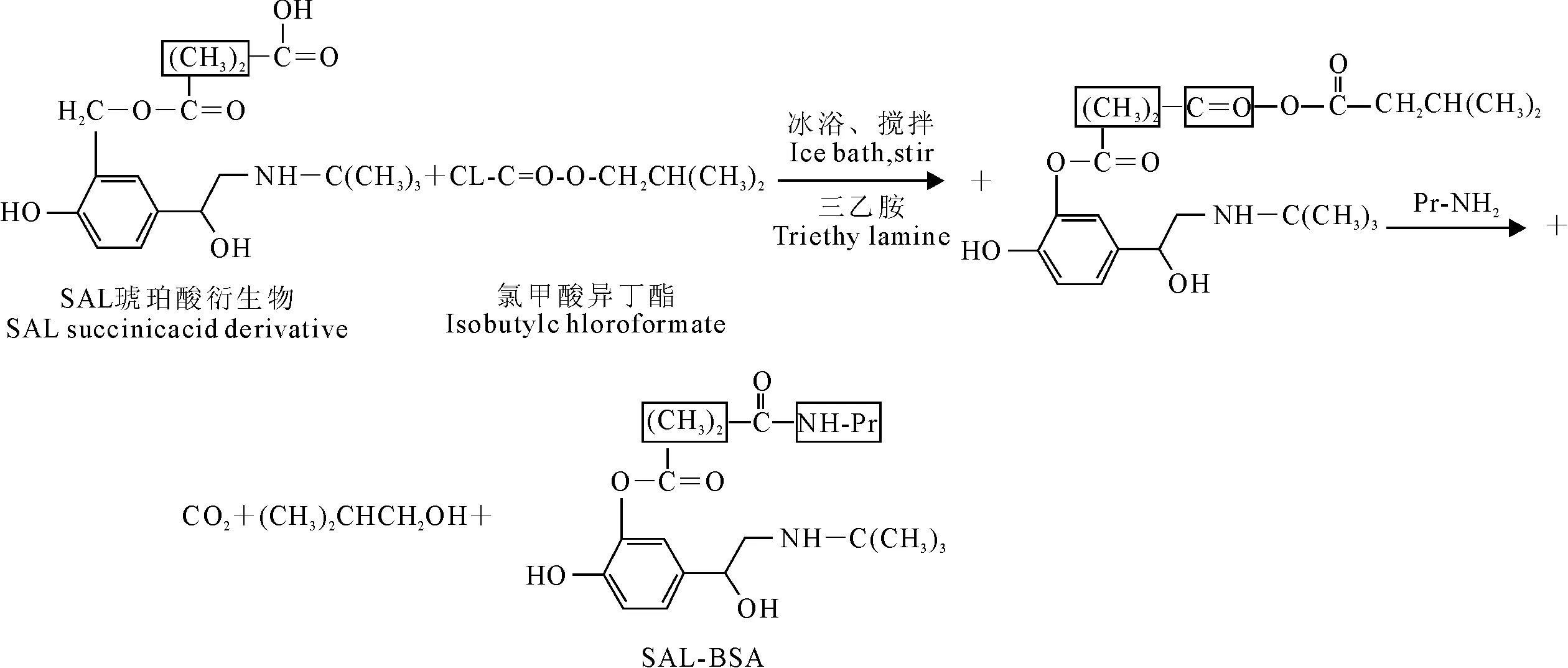
图3 完全抗原SAL-BSA合成过程

图4 完全抗原SAL-OVA合成过程
1.2.2 多克隆抗体的制备 选择健康的新西兰大白兔3只,体重1.5 kg左右,免疫剂量为500 μg/只,1 mL/只,用等体积的弗氏佐剂进行乳化,乳化完全后进行背部皮下多点注射。首免后每隔20 d进行下一次免疫,免疫剂量、方法同首免。第3次、第4次免疫后10 d,耳缘静脉取血2 mL,37℃放置2 h后,4℃过夜,6 000 r/min离心5 min,吸取血清,用于检测抗血清效价。7 d后进行心脏釆血,37℃放置2 h后,4℃过夜,6 000 r/min离心5 min,得到SAL抗血清,分装后置-20℃保存[14]。
1.2.3 ic-ELISA的基本步骤
(1)包被:将检测原(SAL-OVA)用包被缓冲液稀释到合适浓度,100 μL/孔加入96孔酶标板中,4℃包被过夜。
(2)封闭:甩去孔内液体,PBST-50 g/L脱脂奶粉洗涤5次,每次3 min;每孔加入200 μL封闭液,于37℃恒温箱中孵育2 h,甩干孔内液体,洗涤5次。
(3)竞争反应:将0.5 μg/mL的标准品稀释成系列浓度,50 μL/孔加入到已固定抗原的酶标板中;再向板中加入稀释至合适浓度的抗体50 μL/孔,37℃反应30 min,洗涤5次,甩干。
(4)加酶标二抗:每孔加入100 μL 10 000倍稀释的HRP-羊抗兔IgG,37℃反应30 min,洗涤5次,甩干。
(5)显色:每孔加显色液100 μL,室温避光显色15 min,每孔加入50 μL终止液终止反应。
(6)测定:酶标仪测定各孔在450 nm处的吸光值(OD)。
(7)计算:使用Origin 9.0软件中的四参数拟合函数对数据进行拟合,以标准品浓度的对数值为横坐标,以吸光值B/B0作为纵坐标绘制标准曲线,计算其最大吸光值Amax和半数抑制浓度IC50。综合考虑Amax、IC50和Amax/IC50,确定ic-ELISA的最佳反应条件。Amax/IC50的比值越大,说明该方法的灵敏度越高。其中抑制率的计算公式如下:抑制率%=(SAL抗血清效价-SAL抗血清抑制)/SAL抗血清效价×100%。
1.2.4 ic-ELISA条件的优化[15]
(1)最佳包被原浓度和抗体稀释倍数的确定:利用棋盘法,确定合适的包被原浓度和抗体稀释倍数。将包被原稀释成浓度为1 μg/mL、3 μg/mL、5 μg/mL和7 μg/mL的浓度包被酶标板,抗体按1∶400~1∶25 600梯度进行倍比稀释,按照步骤1.2.3测定,测定0 μg/L和0.5 μg/mL的SAL标准品在OD 450 nm处的吸光值,选择OD 450 nm在1.0~1.5之间的包被原浓度和抗体稀释倍数组合绘制抑制曲线。对比不同组合的Amax和IC50及其两者的比值,确定最佳的包被原浓度和抗体稀释倍数。
(2)最佳标准品稀释液的确定:在上述最佳反应条件下,分别用PBS、PBST-50 g/L脱脂奶和PB 3种稀释液稀释标准品,按步骤1.2.3测定,对比不同种类的标准品稀释液Amax和IC50及其两者的比值,确定最佳的标准品稀释液。
(3)最佳竞争反应时间的确定:在上述最佳反应条件下,将标准品与SAL抗血清的竞争反应时间设定为30 min、45 min、60 min、90 min,按步骤1.2.3测定,对比不同竞争反应时间Amax和IC50及其两者的比值确定最佳的竞争反应时间。
(4)最佳二抗反应时间的确定:在上述最佳反应条件下,设置二抗反应时间为15 min、30 min、60 min和90 min,按步骤1.2.3测定,对比不同二抗反应时间Amax和IC50及其两者的比值,确定最佳的二抗反应时间。
(5)最佳二抗稀释度的确定:在上述最佳反应条件下,将二抗稀释倍数按1∶3 000、1∶5 000、1∶7 000和1∶9 000共4个梯度进行倍比稀释,按步骤1.2.3测定,对比不同稀释浓度Amax和IC50及其两者的比值确定最佳的二抗稀释度。
(6)最佳显色时间的确定:在上述最佳反应条件下,设定四组显色时间,分别是5 min、8 min、10 min和15 min,按步骤1.2.3测定,对比不同显色时间Amax和IC50及其两者的比值,确定最佳的显色时间。
1.2.5 ic-ELISA标准曲线的建立 根据上述确定的最佳ic-ELISA反应条件,按步骤1.2.3测定,绘制其标准曲线。以标准品对抗原抗体特异性结合的抑制率达到50%时对应的标准品浓度作为半数抑制浓度,以标准品对抗原抗体特异性结合的抑制率达到20%~80%时所对应的标准品浓度作为标准曲线的检测范围,以标准品对抗原抗体特异性结合的抑制率达到10%时对应的标准品浓度作为最低检测限[15]。
1.2.6 方法特异性 选取CLB、ZIL、RAC、DAN、CIM、TBL、DH和TYL作为抑制物,评价该方法的特异性。按步骤1.2.3测定,绘制标准曲线,计算相对应的交叉反应率。公式:CR%=IC50(标准品)/IC50(结构类似物)×100%。
1.2.7 精密度试验 选择3个标准品SAL质量浓度(2.5 μg/L、25 μg/L和250 μg/L),将每个浓度重复测定3次,计算变异系数(CV)。变异系数(CV)%=标准差/平均值×100%。
1.2.8 回收率 称取SAL标准品添加到尿样中,分别配成2.5 μg/L、25 μg/L和250 μg/L浓度的溶液,用已建立的ic-ELISA方法进行回收试验,计算回收率。计算公式如下:回收率%=实际测定的浓度/添加的浓度×100%。
2 结果
2.1 完全抗原的鉴定
2.1.1 SDS-PAGE法鉴定 采用Bradford蛋白浓度测定试剂盒检测SAL-BSA和SAL-OVA的浓度分别为1.95 mg/mL和2.2 mg/mL。将制备得到的SAL-BSA和SAL-OVA完全抗原,经SDS-PAGE电泳分析(图5,图6)。SAL-BSA和SAL-OVA的条带明显高于BSA和OVA的条带,表明SAL与BSA、OVA偶联成功。

M.蛋白分子质量标准; 1,3.BSA载体蛋白; 2,4.SAL-BSA偶联产物

M.蛋白分子质量标准; 1.OVA载体蛋白; 2.SAL-OVA偶联产物
2.1.2 紫外光谱扫描法鉴定 将小分子(SAL)、载体蛋白(BSA、OVA)及偶联物(SAL-BSA、SAL-OVA)进行紫外光谱扫描鉴定(图7A,7B)。载体蛋白BSA和OVA分别在276 nm和278 nm处出现了最高吸收峰,小分子SAL在225 nm和277 nm处各出现了最高吸收峰,SAL-BSA和SAL-OVA分别在274 nm和275 nm处出现了最高吸收峰,相比于载体蛋白,由于助色团的作用,偶联物均发生了蓝移,形成了一种新的共轭结构,导致其紫外吸收光谱发生了改变[16]。因此可以判断完全抗原制备成功。

A.SAL-BSA紫外光谱扫描;B.SAL-OVA紫外光谱扫描
2.1.3 偶联比的测定 根据TNBS法建立标准曲线[15],测得SAL-BSA的偶联比为17∶1,SAL-OVA的偶联比为6.4∶1。由此说明该完全抗原具有良好的免疫原性,能够产生高特异性抗体。
2.2 抗血清的评价
经过4次免疫,最终得到的血清作为抗血清,在优化好的条件下测定抗体效价,抗体的效价可达1∶102 400(表1)。
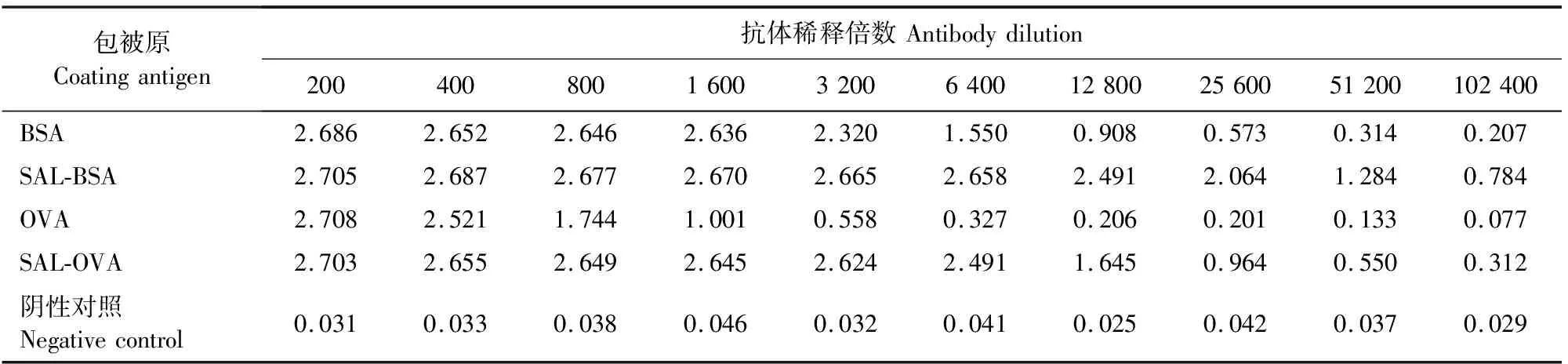
表1 SAL抗血清评价结果
2.3 抗原、抗体最适工作浓度的确定
根据实际ic-ELISA检测的经验,当0 μg/L的标准液OD 450 nm值为1.2~1.8,最高浓度标准液(0.5 μg/mL)的OD 450 nm值在0.1~0.3之间时,绘制标准曲线的梯度和线性关系良好。综合考虑最大吸光值(Amax)、半数抑制浓度(IC50)和两者之间的比值来选择最佳反应条件,IC50值低、Amax/IC50值高所对应的反应条件为最佳反应条件(表2)。因此最佳包被原浓度为3 μg/mL,SAL抗血清最佳稀释度为1∶12 800。

表2 包被原浓度与抗体稀释倍数的确定
2.4 优化标准品稀释液、竞争反应时间、二抗反应时间与稀释倍数、显色时间
不同标准品稀释液条件的比较(图8A),经过优化,最终选择PBST-50 g/L脱脂奶作为标准品稀释液;在以上确定最佳条件的基础上,其他条件的比较情况如图8B~8E所示,最终确定最佳竞争反应时间为1 h(图8B);最佳二抗反应时间为30 min(图8C);最佳二抗稀释倍数为1∶5 000(图8D);最佳显色时间为10 min(图8E)。

A.标准品稀释液; B.竞争反应时间; C.二抗反应时间; D.二抗稀释倍数; E.显色时间
2.5 ic-ELISA方法的建立及标准曲线的绘制
按照上述ELISA条件优化的结果,得到SAL ic-ELISA方法的最佳反应条件。以SAL标准品浓度的对数值为横坐标(x),以吸光值B/B0为纵坐标(y),应用Origin 9.0软件中的四参数拟合竞争标准曲线,在上述最优条件下建立ic-ELISA的标准曲线(图9)。其曲线的回归方程为y=A2+(A1-A2)/(1+(x/x0)∧p),相关系数R2为0.967 2,IC50为24.84 μg/L,最低检测限(IC10)为0.78 μg/L,线性范围IC20-IC80为3.16 μg/L~80.1 μg/L。

图9 ic-ELISA检测SAL标准曲线
2.6 特异性分析
SAL抗血清与侧链上含有叔丁基官能团的结构类似物有较强的交叉反应,例如与CLB、TBL的交叉反应率均在100%左右,与其他小分子的交叉反应率均<0.1%(表3)。

表3 SAL抗血清与结构类似物的交叉反应率检测
2.7 精密度检测
精密度以样品测定值的变异系数来表示。选取3个SAL标准品浓度(2.5 μg/L、25 μg/L和250 μg/L),将每个浓度反复测定3次,计算CV。3个标准品浓度所对应的CV分别为5.37%、7.61%和5.45%,其平均CV为6.14%。CV<10%,表明该方法精密度较好。
2.8 回收率的测定
ic-ELISA方法准确度以回收率表示,选择2.5 μg/L、25 μg/L、250 μg/L 3个添加水平进行SAL添加回收试验,将每个浓度反复测定3次,最终确定为猪尿中样品的平均回收率在98%~110%之间(表4),证明了检测方法的可靠性,适用于实际样品中SAL的检测。

表4 SAL抗血清在猪尿样品中的回收率
3 讨论
偶联物中的偶联比对于刺激机体产生高特异性抗体有一定影响,偶联率太低容易引起无关的免疫应答;过高易诱导低特异性抗体的产生,Erlanger[17]认为偶联比一般在5∶1~25∶1较为合适。因SAL半抗原本身没有可以直接与载体蛋白上的氨基偶联的活性基团,需要将其改造成含有氨基、羧基等基团的衍生物,然后再与载体蛋白偶联[18]。由于免疫系统一般对远离载体端的结构识别能力较强,对连接端识别能力较弱,文献中通常选择远离待测物特征结构的官能团作为连接臂的结合位点[19]。而SAL主要含有的活性基团是羟基,含有羟基的半抗原衍生物的制备方法有一氯醋酸法、对氨基苯甲酸法和琥珀酸酐法;琥珀酸酐法的优点在于用琥珀酸酐将SAL酰化后,会形成一个含4个碳的间隔臂的中间产物,这样就突出了SAL半抗原决定簇的特征结构,有助于制备出特异性强的抗SAL抗体[20]。因此,本研究中选择琥珀酸酐法制备SAL琥珀酸衍生物,再利用混合酸酐法和活化酯法分别制备SAL-BSA和SAL-OVA完全抗原,进一步保证了机体免疫系统对所制备的完全抗原具有良好的识别能力。本研究结果显示,将偶联成功的SAL-BSA免疫新西兰大白兔,SAL-OVA用于检测免疫效果,四免后的兔血清效价可达到102 400,且抗血清对SAL的IC50为24.84 μg/L,成功获得了效价良好的抗SAL多抗。
虽然已有不少文献报道制备出了抗SAL单抗并建立了类似的检测方法,例如,胡颖[1]成功制备了抗SAL单克隆抗体,并且与CLB的交叉反应率只有38%,而与其他结构类似物均无交叉反应;李春生[21]的结果也显示了制备出的抗SAL单克隆抗体只与CLB有交叉反应,其交叉反应率为26.09%,而与其它结构类似物没有交叉反应,说明单克隆抗体相比于多克隆抗体其特异性高,比较稳定,但是制备周期长,过程复杂,容易造成污染。而多克隆抗体制备周期短,并且能识别多个抗原表位,即使有个别抗原表位被破坏,试验结果影响也不大,但是多克隆抗体很难避免非特异性反应。在本研究中,我们发现所制备的抗SAL多抗血清也存在非特异性反应现象,与CLB和TBL的交叉反应率分别为108.57%和95.14%。经过分析发现,有如此高的交叉反应率是因为在三者的侧链上都具有相同的叔丁基官能团,下一步将通过寻求新的半抗原改造方法避免此种现象的发生。但是这种交叉反应的存在也为后期应用该抗体建立同时检测多残留物的方法奠定了研究基础。
在建立ic-ELISA的过程中,ic-ELISA条件优化对方法敏感性至关重要,因抗体和标准品在不同缓冲体系中分散能力不同,所以需要找到抗体和标准品最适合的溶剂,经试验验证,最终选择PBST-50 g/L脱脂奶作为标准品稀释液。此外,反应时间长短决定抗原抗体是否充分结合,所以要优化竞争反应时间达到最佳反应程度。蛋白性质不同,抗原抗体反应所需最佳浓度、缓冲体系、离子浓度、反应时间等参数也有所差异[22];针对各种因素,本研究设置了标准品稀释液、竞争反应时间、二抗反应时间与稀释倍数、显色时间共5组条件进行优化,最终建立了检测SAL的ic-ELISA检测方法。
综上所述,本研究以合成SAL人工抗原为基础获得抗SAL的多抗,成功建立了检测SAL的ic-ELISA检测方法,为建立同时检测多残留物的快速检测方法奠定了基础。

