急性心肌梗死介入治疗患者发生慢性心力衰竭状况及其影响因素分析
张 亮
(龙川县人民医院,广东 河源517300)
急性心肌梗死(acute myocardial infarction,AMI)具有发病急、病情重、病死率高等特点,以剧烈而持久的胸骨后疼痛为主要临床特征,若未得到及时救治,将严重危及患者生命安全。目前,经皮冠状动脉介入(PCI)为治疗AMI 患者的重要方法,通过患者冠状动脉尽快再通,恢复血流,改善心肌的血流灌注,减轻心肌缺氧、缺血,降低病死率。但受多种因素影响介入治疗后部分患者可能会发生不良心血管事件,以慢性心力衰竭(Congestive heart failure,CHF)较为常见,严重影响疾病预后。基于此,本研究旨在分析AMI 介入治疗患者CHF 的发生状况及影响因素,现报道如下。
1 资料与方法
1.1 一般资料
经我院医学伦理委员会批准,选取2019 年8 月至2020 年8 月我院接收的60 例AMI 患者为研究对象,其中男性31 例,女性29 例;年龄<60 岁30例,≥60 岁30 例。
纳入标准:(1)符合AMI 相关诊断标准[1];(2)发病后12h 内接受PCI 治疗;(3)自愿签署知情同意书。
排除标准:(1)合并先天性心脏病;(2)合并器质性病变;(3)认知功能异常。
1.2 方 法
所有患者入院后均接受PCI 治疗,统计术后1个月内CHF 发生情况,CHF 判定标参照《中国心力衰竭诊断和治疗指南2018》[2]中相关标准进行判定。根据评估结果将发生CHF 的患者纳入发生组,将未发生CHF 的患者纳入未发生组。
1.3 观察指标
记录两组性别、年龄、发病至闭塞血管开通时间、左心室射血分数(LVEF)、无复流状况。
1.4 统计学方法
2 结 果
2.1 CHF 发生状况
本研究60 例患者中,有17 例患者发生CHF,占28.33%(17/60);43 例 患 者 未 发 生CHF,占71.67%(43/60)。
2.2 影响AMI 介入治疗患者发生CHF 的单因素分析
经单因素分析显示,性别与AMI 介入治疗患者发生CHF 无关,差异无统计学意义(P>0.05);年龄、发病至闭塞血管开通时间、LVEF、无复流状况均与AMI 介入治疗患者发生CHF 有关,差异有统计学意义(P<0.05)。见表1。
2.3 多因素Logistic 回归分析
将AMI 介入治疗患者CHF 发生状况作为因变量(1=发生,0=未发生),将年龄、发病至闭塞血管开通时间、LVEF、无复流状况作为自变量,变量说明见表2;经多因素Logistic 回归分析显示,年龄≥60岁、发病至闭塞血管开通时间长、LVEF<57%、无复流均为AMI 介入治疗患者CHF 发生的影响因素(OR>1,P<0.05)。见表3。
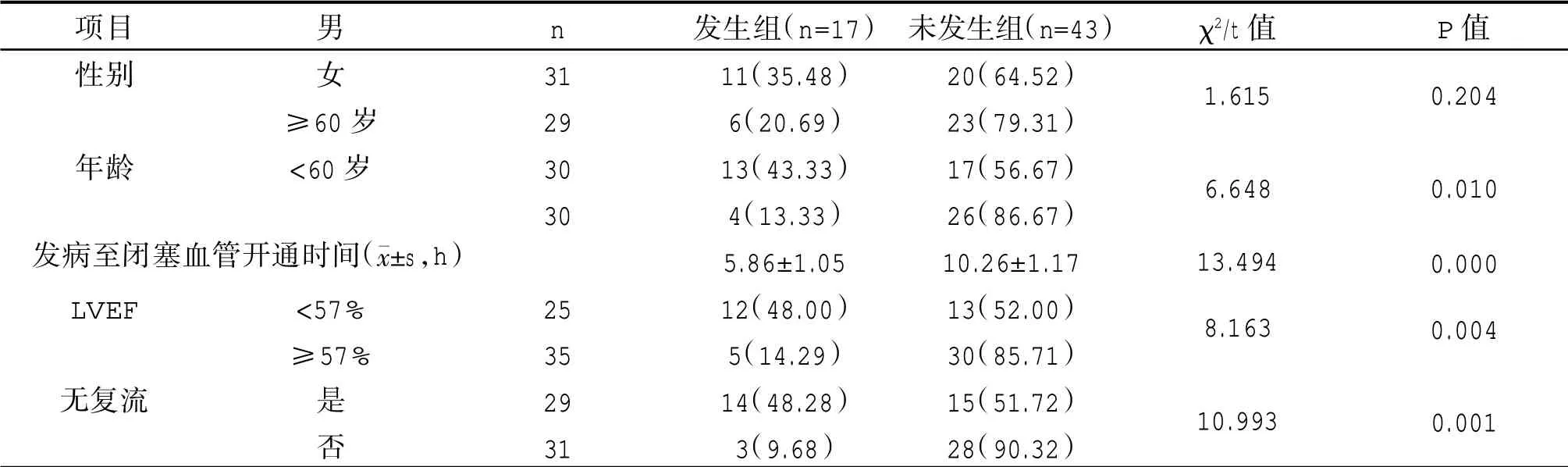
表1 影响AMI 介入治疗患者发生CHF 的单因素分析[n(%)]

表2 自变量说明

表3 影响AMI 介入治疗患者发生CHF 的多因素Logistic 回归分析
3 讨 论
PCI 治疗AMI 患者可有效挽救生命,但PCI 术后发生CHF 已成为严重的并发症问题。本研究60例患者中,有17 例患者发生CHF,发生率为28.33%,提示AMI 介入治疗患者CHF 发生率较高。因此,积极研究AMI 介入治疗患者发生CHF 的影响因素具有重要意义。
本研究经多因素Logistic 回归分析显示,年龄≥60 岁、发病至闭塞血管开通时间长、LVEF<57%、无复流均为AMI 介入治疗患者CHF 发生的影响因素。分析其原因在于:(1)高龄对AMI 介入治疗患者发生CHF 的影响机制尚未具体明确,但多认为可能与高龄患者组织灌注低、术后心肌细胞恢复能力差等因素有关[3]。因此,临床在治疗高龄患者时,应积极采取预防措施进行干预。(2)研究指出,冠脉闭塞20-30min 后仅小部分心肌细胞坏死,闭塞3h后约60%心肌细胞坏死,闭塞6h 后约70%心肌细胞坏死[4]。因此,发病至闭塞血管开通时间越长,罪犯血管闭塞时间也越长,梗死面积会逐渐增加,故介入治疗后CHF 发生风险性越高。因此,尽早、快速疏通梗死血管可有效降低介入治疗后CHF 发生率。(3)LVEF 水平越高,心功能越好,发生CHF 的几率越低,反之则发生CHF 的几率越高[5]。因此,LVEF水平低为介入治疗后发生CHF 的影响因素,建议临床可依据介入治疗后患者的LVEF 水平,采取措施积极改善心功能。(4)无复流指罪犯血管疏通后心肌组织无灌注现象,其病理生理机制较为复杂,可能与缺血再灌注损伤、患者自身对微循环损伤的敏感性、远端动脉栓塞等有关,一旦发生,将会明显加重心肌缺血程度、促进心室重构、增加梗死面积,进而引发CHF[6]。因此,一旦患者发生无复流现象,不仅要改善无复流,同时应实施可预防CHF 发生的措施。
综上所述,AMI 介入治疗患者CHF 发生率较高,高龄、发病至闭塞血管开通时间长、LVEF 低、无复流均为其影响因素,临床可据此积极采取措施干预,以降低患者CHF 发生率。

