超声刀联合腋窝皮肤外固定在乳腺癌改良根治术中的应用及安全性分析
郑振忠
南阳张仲景医院,河南省南阳市 473000
乳腺癌是女性最常见的恶性肿瘤之一,现阶段,保留胸大、小肌的改良根治术是主要应用术式,因由于胸大、小肌的支撑作用,术后腋下形成圆锥形“空洞”,导致引流量增多或拔管后腋窝积液,进而引起皮下积液,延长住院时间,增加患者痛苦[1]。超声刀具有切割、分离、止血三大功能,在乳癌改良根治术中的应用逐渐增多,被认为可有效预防皮下积液。随着对胸肌神经、肋间臂神经解剖及功能的认知逐渐加深,保留上述神经的手术已在临床开展,可有效预防术后胸肌萎缩及上臂内侧皮肤感觉异常[2]。目前,关于超声刀、电刀在游离并保护胸肌神经、肋间臂神经方面的对照研究临床报道较少。另外,手术创伤对患者术后应激及免疫功能的影响仍是不可忽视的问题[3]。基于此,本研究探究了超声刀联合腋窝皮肤外固定在保护胸肌神经及肋间臂神经、应激及免疫功能等方面的应用效果。报道如下。
1 资料与方法
1.1 一般资料 选取我院2019年1月—2020年2月乳腺癌改良根治术患者126例,根据手术方案不同分为两组,各63例。两组年龄、体质量指数(BMI)、TNM分期、病理类型、肿瘤直径均衡可比(P>0.05),见表1。

表1 两组一般资料比较
1.2 选择标准 纳入标准:(1)均经病理学检查确诊;(2)均为单侧、单病灶;(3)患者及家属知情同意。排除标准:(1)凝血功能异常;(2)接受放化疗治疗;(3)伴精神疾病或认知功能异常;(4)术前无术区及上肢疼痛、感觉异常。
1.3 方法
1.3.1 手术方法:两组均行乳腺癌改良根治术,常规切口标记,电刀完成皮瓣分离与乳房切除,暴露腋静脉。观察组采用超声刀清扫腋窝淋巴结,仅结扎直径>3mm的腋静脉分支。清扫完成后,冲洗创腔,用纱布卷将腋窝正中处皮肤和背阔肌肌腱前缘缝合固定,术后于胸壁和腋窝处放置引流管负压吸引,皮瓣弹力胸带加压包扎。对照组采用电刀行腋窝淋巴结清扫,腋窝皮肤外固定同观察组。两组术中均保留胸肌神经及肋间臂神经。
1.3.2 检测方法:抽取外周静脉血5ml,离心(半径8cm,3 500r/min,9min),取血清,应激指标[C反应蛋白(CRP)、白介素6(IL-6)、IL-10]采用酶联免疫吸附法测定,北京安迪华泰科技有限公司试剂盒;免疫指标(CD3+、CD4+、CD4+/CD8+)采用FACS Aria型流式细胞仪(美国BD公司)检测。
1.4 观察指标 (1)手术相关指标(腋窝手术时间、术中出血量、术后引流量、拔管时间、清扫淋巴结数目)。(2)并发症。(3)术前、术后1d、术后3d应激指标(CRP、IL-6、IL-10)水平。(4)术前、术后1d、术后3d免疫指标(CD3+、CD4+、CD4+/CD8+)水平。(5)术后3个月、6个月患侧腋部及上臂内侧皮肤感觉情况。(6)术后3个月、6个月胸大肌厚度。

2 结果
2.1 两组手术相关指标对比 观察组腋窝手术时间、拔管时间短于对照组,术中出血量、术后引流量低于对照组(P<0.05);两组清扫淋巴结数目无显著差异(P>0.05),见表2。
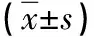
表2 两组手术相关指标对比
2.2 两组并发症发生情况对比 观察组并发症发生率为3.17%,显著低于对照组的19.05%(χ2=8.036,P=0.005<0.05)。见表3。

表3 两组并发症对比[n(%)]
2.3 两组应激指标水平对比 术后1d、3d观察组血清CRP、IL-6、IL-10水平低于对照组(P<0.05)。见表4。
2.4 两组免疫指标对比 术前、术后1d、术后3d两组血清CD3+、CD4+、CD4+/CD8+水平无显著差异(P>0.05),见表5。
2.5 两组胸大肌厚度对比 术后3个月两组患侧、健侧胸大肌厚度无显著差异(P>0.05);术后6个月观察组患侧、健侧胸大肌厚度无显著差异(P>0.05),对照组患侧胸大肌厚度低于健侧(P<0.05)。见表6。
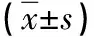
表4 两组应激指标水平对比
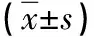
表5 两组血清T淋巴细胞亚群对比
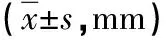
表6 两组胸大肌厚度对比
2.6 两组患侧腋部及上臂内侧皮肤感觉情况对比 术后3个月、术后6个月时观察组患侧腋部及上臂内侧皮肤感觉异常发生率低于对照组(P<0.05)。见表7。

表7 两组患侧腋部及上臂内侧皮肤感觉情况对比[n(%)]
3 讨论
目前,乳腺癌改良根治术仍是大部分乳腺癌患者标准手术方式的选择,但皮下积液等并发症一直是制约患者术后恢复的重要因素[4]。乳腺癌患者术后皮下积液发生率为15%~20%,延长患者住院时间,并影响术后放疗、化疗的实施[5]。目前,乳腺癌改良根治术中,腋窝淋巴脂肪组织清除普遍应用高频单极电刀,电刀的微血管凝固作用替代了淋巴管、血管结扎,但淋巴管断端暴露,结痂脱落而导致淋巴漏;且电凝高温(150~400℃)可引起周围正常组织损伤,脂肪坏死液化,导致引流量较多。超声刀通过超声波产生机械振动,而引起组织内水分子汽化、蛋白质氢键断裂,进而引起细胞崩解,实现组织凝固或分离、血管闭合,达到切割与止血目的[6]。与传统电刀相比,超声刀具有热损伤小、止血效果好、无电刺激等优点。本研究数据显示,超声刀联合腋窝皮肤外固定应用于乳腺癌改良根治术患者,可缩短手术时间,减少术中出血、术后引流量及并发症发生,与既往研究一致[7-8]。考虑与超声刀对局部刺激损伤较小,淋巴管、血管闭塞效果好有关。且两组清扫淋巴结数目无显著差异(P>0.05),提示两种术式均可达根治目的。
研究发现,乳腺癌改良根治术中,尽管肋间臂神经、胸肌神经保留,部分患者术后仍发生不同程度腋窝及上臂内侧皮肤疼痛或感觉异常、胸大肌萎缩[9]。这与本研究结论一致,考虑与手术器具(超声刀、电刀等)导致神经损伤有关。本研究结果显示,术后3个月、术后6个月时观察组患侧腋部及上臂内侧皮肤感觉异常发生率低于对照组(P<0.05);术后6个月观察组患侧、健侧胸大肌厚度无显著差异(P>0.05),对照组患侧胸大肌厚度低于健侧(P<0.05)。提示超声刀应用于乳腺癌改良根治术患者,可更好地保护肋间臂神经、胸肌神经。分析原因在于,超声刀对周围组织不产生电击灼伤,且切割时不产生烟雾,术野清晰,可灵活、准确地在肋间臂神经、胸肌神经等神经附近操作,减少副损伤。
手术创伤可使机体产生应激反应,CRP、IL-6、IL-10均为常用炎性应激指标,研究证实,其水平升高程度与手术创伤大小有关[10]。本研究数据显示,术后1d、3d观察组血清CRP、IL-6、IL-10水平低于对照组(P<0.05),提示超声刀联合腋窝皮肤外固定应用于乳腺癌改良根治术患者,可减轻应激反应,这与超声刀对周围组织的创伤较小直接相关。免疫抑制是手术常见并发症,与手术损伤、应激反应等均有关。本研究发现,术前、术后1d、术后3d两组血清CD3+、CD4+、CD4+/CD8+水平无显著差异(P>0.05),提示两种术式对机体免疫功能均无显著影响,可能与两种器械对机体的创伤均较轻有关。
综上可知,超声刀联合腋窝皮肤外固定应用于乳腺癌改良根治术患者,可减轻应激反应,缩短手术时间,减少术中出血、术后引流量及并发症发生,并可更好地保护肋间臂神经、胸肌神经,减少术后神经功能异常发生。

