PI模型在肝细胞肝癌根治术后辅助性TACE治疗中的应用价值
哈丽达·夏尔甫哈孜,冯娟,范晓棠,石绣江,陈兰,克拉热·阿合买提,阿丽亚·热哈提
(新疆医科大学第一附属医院 肝病科,新疆 乌鲁木齐 830054)
肝细胞肝癌(hepatocellular carcinoma,HCC)是最常见的恶性肿瘤之一,发病率位居全球恶性肿瘤第6,病死率位居癌症相关死亡第2。全球每年新增HCC病例超过75 万,其中近55%的病例发生在中国[1-4]。目前根治HCC的最有效手段仍然是外科手术,随着早癌筛查的开展和外科技术的成熟,世界范围内接受HCC根治性手术治疗的患者比例逐渐增加,但术后较高的复发率和转移率仍然制约着患者的远期生存和预后,文献报道HCC术后50%~90%的死亡原因与肿瘤复发转移有关[5-6],因此,正确有效的辅助治疗对预防HCC术后复发转移具有非常重要的临床意义,术后辅助性TACE治疗为目前临床上应用最广的预防HCC术后复发和转移的肝内局部治疗方法[7-8],然而是否所有HCC患者术后都能进行TACE治疗,是否能使所有患者术后生存获益,目前尚缺乏循证医学证据和大样本前瞻性随机对照研究。本研究基于多因素Cox回归模型建立HCC根治术后5年生存情况的预测指数(predictive index,PI)模型,并评价PI模型在HCC根治术后辅助性TACE治疗的应用价值,为HCC术后TACE治疗的合理应用提供新的循证医学证据。
1 资料和方法
1.1 研究对象
收集2010年10月至2014年12月期间在新疆医科大学第一附属医院普通外科接受根治性手术切除的201例HCC患者的临床病例资料。
纳入标准:临床病例资料完整,一般情况较好,无明显重要脏器器质性病变;肝功能储备分级为A级或B级;所有患者均为慢性乙型肝炎患者,慢性乙型肝炎诊断符合中华医学会2015年制定的《慢性乙型肝炎防治指南》中的诊断标准[9]。根治性切除的标准为:肿瘤完整切除;余肝、切缘无残癌;肿瘤数目≤3个;门静脉、肝总管、肝静脉主干及一级分支无癌栓;下腔静脉无癌栓;无全身淋巴结及远处转移。
排除标准:合并有其他肝炎或肝病患者;合并失代偿期肝硬化;肝功能储备分级为C级;合并有重大基础疾病(心脑血管、呼吸系统、肾脏疾病等);心肺功能无法耐受手术者;病例资料不全者。
1.2 研究方法
随访采用电话、门诊复查相结合的方式,观察时间以首次在本院行手术治疗为起点,截止时间为2019年12月。转归包括生存和死亡,记录患者首次入院行手术治疗时的一般情况(年龄、性别、吸烟史、饮酒史等),围术期的血常规、生化、凝血、免疫检查,腹部CT血管造影(CTA),手术情况,病理结果,免疫组化以及辅助性TACE治疗情况,具体变量赋值见表1。
1.3 统计学分析
运用SPSS 22.0软件进行统计分析,对所有指标先进行Cox回归单因素分析,然后将单因素分析中有统计学意义的指标代入Cox风险比例回归模型进行多因素校正,采用向前逐步回归,经3步回归,得出独立预测因子和回归系数,根据独立预测因子结合其回归系数建立PI模型,运用ROC获得PI模型临界值以及AUROC,根据PI模型临界值将所有纳入观察的患者分为高、低危组;将PI值代入Cox风险比例回归模型进行单因素分析和多因素校正,生存分析曲线分别比较高危组和低危组不同TACE治疗各阶段累计生存率变化情况,用以评估PI模型在术后TACE治疗的临床应用价值,P<0.05表示具有统计学意义。

表1 HCC围手术期的相关影响因素及赋值
2 结果
2.1 患者一般情况
201例患者中男130例(64.7%),女71例(35.3%),年龄38~69岁,平均(52±7)岁,生存时间为7~60个月,5年内死亡81例(40.3%),存活120例(59.7%)。HCC根治术后,接受术后辅助性TACE治疗112 例(55.7%),未接受辅助性TACE治疗89例(44.3%)。
2.2 单因素Cox回归分析
9 个指标在回归模型中有统计学差异,对生存预后有显著性影响,分别为乙肝病毒DNA载量、前白蛋白、凝血酶原活动度、中性粒细胞/淋巴细胞比值(neutrophil-to-lymphocyte ratio,NLR)、微血管侵润(microvascular invasion,MVI)、肿瘤最大直径(the maximum size of tumor,MTS)、肿瘤数目(the amount of tumor,AT)、肿瘤分化程度(histological grade,HG)、血管内皮生长因子(vascular endothelial growth factor,VEGF)基因表达,说明这9个因素可能对此类患者生存情况以及预后有影响(P<0.05)见表2。
2.3 多因素Cox回归分析
将单因素分析中有统计学意义的指标代入多因素Cox模型进行分析,校正和控制混杂变量后,筛选出对预后有显著性影响的独立预测因子有6个:NLR(β=0.32,OR1.38)、MTS(β=0.53,OR1.69)、HG(β=0.39,OR1.47)、VEGF(β=0.92,OR2.50)、MVI(β=0.73,OR2.08)、AT(β=0.46,OR1.58),其中NLR每增加1个单位5年内死亡的风险将增加38%,而HG每降低1个等级5年内死亡的风险将增加47%(P<0.05)。见表3。
2.4 TACE治疗的单因素分析和多因素校正
对TACE治疗这一指标进行单因素分析以及多因素校正(校正指标为单因素分析中有统计学意义的指标),分析结果显示:在校正的Cox回归模型中,TACE治疗进入到了最后的回归模型,对生存预后具有显著性影响,其校正后的OR值为0.51,提示术后未行TACE治疗的患者术后5年内死亡的风险是行TACE治疗的1.96倍(P<0.05)。见表4。
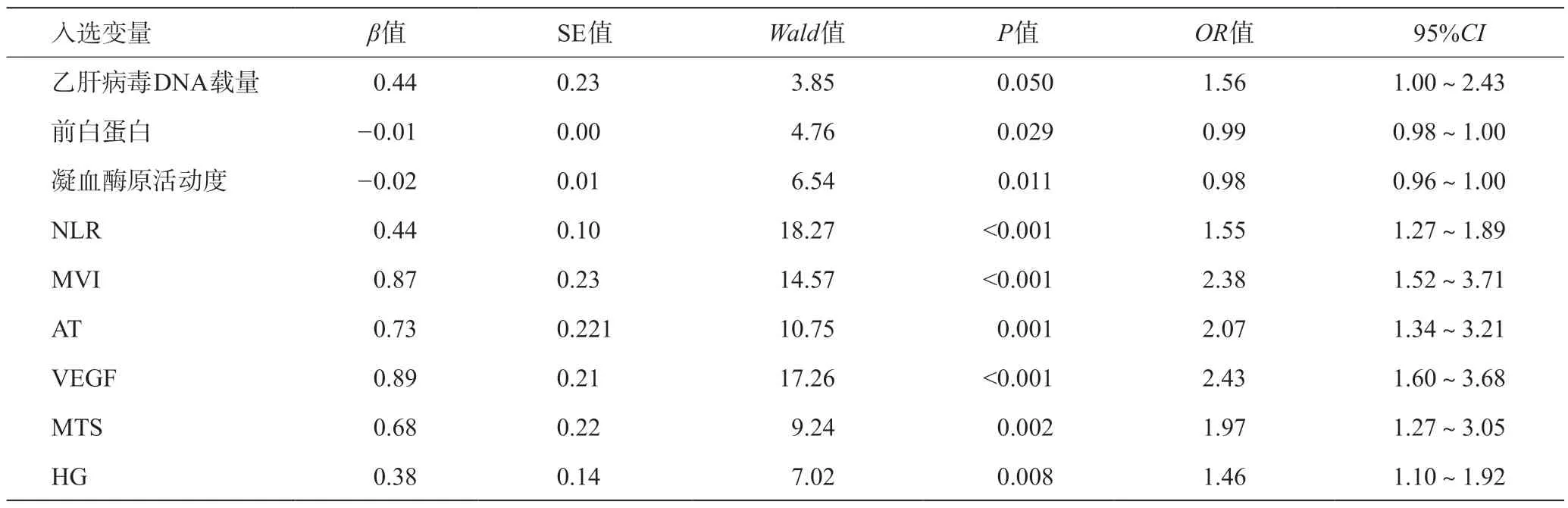
表2 Cox回归单因素分析
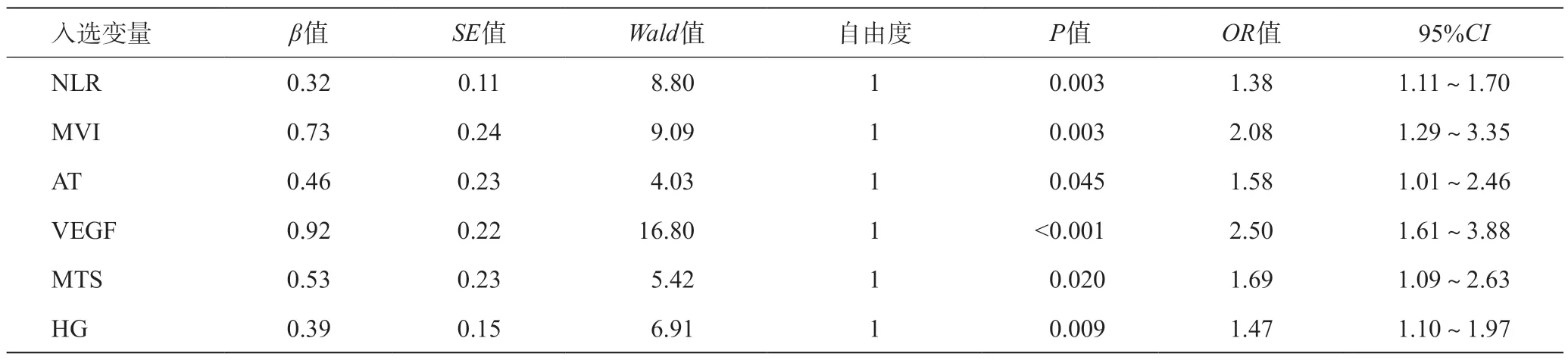
表3 Cox回归多因素分析

表4 术后TACE辅助性治疗的单因素分析和多因素校正
2.5 PI模型的建立以及验证
根据独立预测因子以及其回归系数建立PI模型:PI=0.32×NLR+0.39×HG(高=1,中=2,低=3)+0.92×VEGF(高表达=1,低表达=0)+0.87×MVI(是=1,否=0)+0.73×AT(单发=0,多发=1)+0.53×MTS(≥5 cm=1,<5 cm=0),PI值的范围在0.72~4.78之间,PI值越大,表示术后5 年内死亡风险越高,图1显示了PI模型预测术后5 年生存情况的ROC曲线,AUROC为0.841,敏感性为81.2%,特异性89.4%,总体准确度为85.6%,并采用Bootstrap自抽样法对PI模型进行内部验证,对所有样本重复抽样1 000次,得到PI模型的一致性指数(C-Index)为0.842(95%CI0.763~0.912),提示模型的预测能力较好,准确性较高,通过ROC曲线获得PI临界值为2.75,以PI值>2.75作为判断此类患者5内死亡的标志,记为高危组,PI值≤2.75作为判断此类患者5年内存活的标志,记为低危组,将PI值代入Cox风险回归模型进行单因素分析和多因素校正,多因素校正的指标为单因素分析中有统计学意义的指标,在校正相关因素后,PI值成为独立预测因子,PI值每增加1个单位代表5年内死亡的风险将增加1.72倍(P<0.05)。见表5。
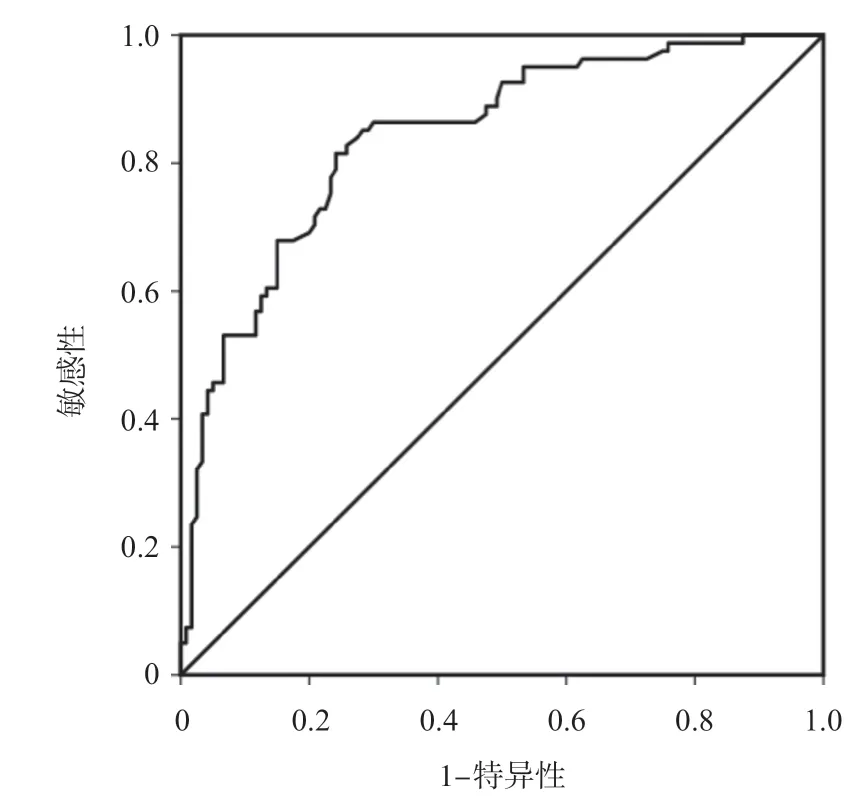
图1 PI模型预测HCC术后5年生存率的ROC曲线
2.6 Kaplan-Meier生存分析
低危组:TACE亚组与未行TACE亚组术后1年、3年、5年累计生存率比较,无统计学差异(TACE亚组:97.6%、95.2%、90.5%,无TACE亚组:95.2%、85.5%、83.9%,P>0.05);高危组:TACE治疗≥3次、TACE治疗<3次和未行TACE治疗三个亚组进行两两比较,其生存曲线和各阶段累计生存率都具有统计学差异;TACE治疗≥3 次亚组术后1、3、5 年累计生存率(100%、80.0%、53.3%),显著高于TACE治疗<3 次组(81.8%、40.9%、36.4%,P<0.05);而TACE治疗<3次亚组各阶段累计生存率(81.8%、40.9%、36.4%),显著高于未行TACE治疗组(73.3%、13.3%、13.3%,P<0.05)。见图2、图3。

表5 PI模型的单因素分析和多因素校正
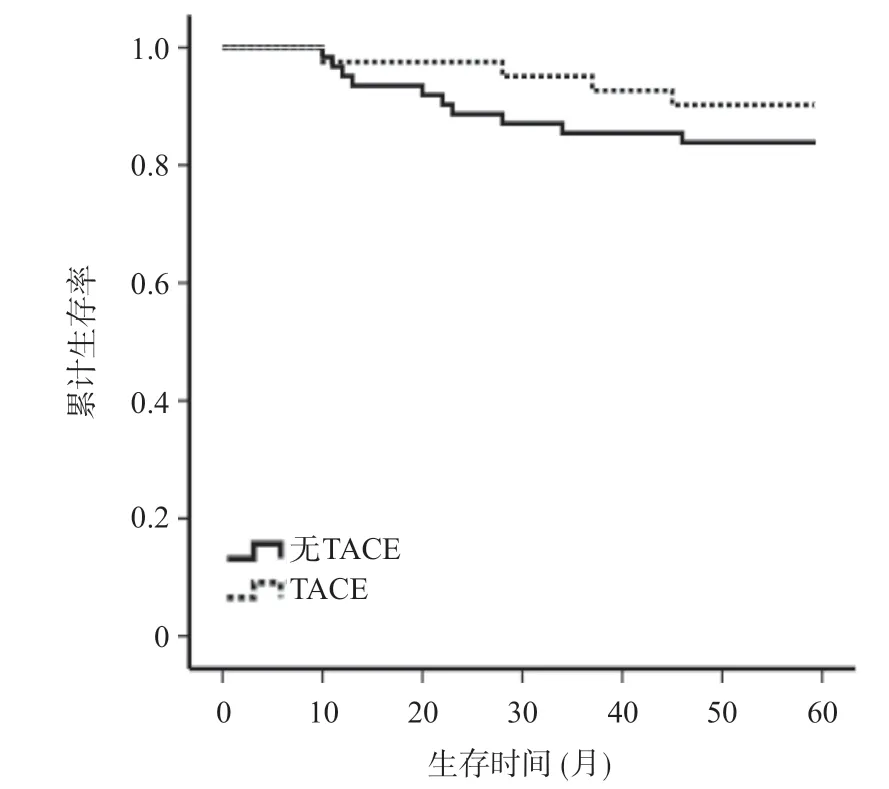
图2 低危组TACE和无TACE治疗累计生存率比较
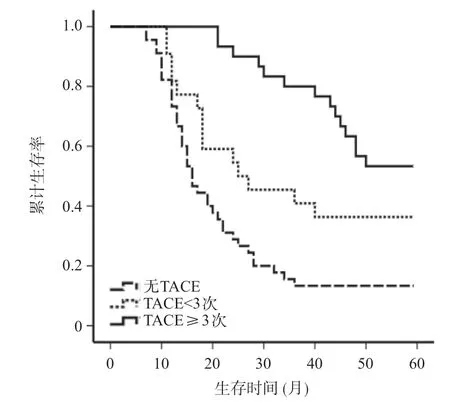
图3 高危组不同TACE治疗次数累计生存率比较
3 讨论
HCC血供丰富,侵袭血管能力强,故早期就容易侵犯肝血窦,并经门静脉系统的微血管系统造成肝内播撒和转移,因而微血管侵犯常被认为是影响HCC术后复发以及发生肝内转移的主要危险因素[10-15]。在一些报道中,微血管侵犯还是影响HCC术后肿瘤早期复发的危险因素和预测因子[16]。对于HCC术后病理结果显示微血管侵犯阳性的患者予以辅助性TACE治疗,主要目的是阻断肿瘤血供和侧支循环的建立,杀灭或抑制残留的肿瘤细胞以及早期复发灶或癌前病变组织,从而达到降低早期复发和转移的风险,延长患者无瘤生存期和总生存期。
尽管有一些循证医学证据显示HCC肿瘤大小和数目与术后的复发和转移无关,但总体的循证医学证据和文献报道还是认为肿瘤大小和数目是影响术后复发和转移的一个重要因素和预测因子[17-21]。肿瘤大小和数目影响复发的主要原因在于它反映肿瘤的侵袭程度,大肿瘤,尤其是5 cm以上的肿瘤,可显著增加术后复发的风险,单纯手术不易达到根治,有研究显示5 cm以上肿瘤其发生肝内转移及门静脉血管侵犯的几率显著增高[22],且肿瘤越大,其术后复发的时间也越早[23]。
VEGF通过在体内诱导血管内皮细胞分裂增殖,促进肿瘤血管的形成和生长,从而成为影响肿瘤的转移、复发及扩散的关键因素。近年来,以VEGFVEGFR轴为靶点在HCC生物免疫治疗中的作用也成为研究的热点。国外研究报道,VEGF高表达患者HCC根治术后无病生存率与总生存率明显低于VEGF低表达患者,提示VEGF的表达水平与HCC术后存活率降低和复发率增加呈正相关,VEGF表达水平可作为预测HCC患者术后生存情况的辅助诊断指标之一[24]。本研究多因素分析结果显示,VEGF高表达者HCC术后5 年内死亡的风险是VEGF低表达者的2.5倍,再次证实了以上结论。
术后TACE治疗的目的在于消灭残肝内微小残癌或癌前病变组织,以期达到预防余肝新生肿瘤的目的,减少术后肿瘤的复发与转移的几率,进而改善手术疗效,提高患者生存期。本研究中TACE治疗也作为独立预测因素进入最后的Cox多因素回归模型,对HCC患者术后的生存情况有显著性影响。但现阶段对HCC术后是否需要接受TACE治疗仍存在很大争议,主要原因是目前国内外尚无HCC术后辅助性TACE治疗的明确指南推荐以及制定出适合不同病情的术后TACE治疗方案,为解决以上问题,我们结合了最后进入模型的独立预测因子及其回归系数建立了PI模型,将PI模型代入Cox回归模型进行多因素校正,也具有统计学差异,且PI预测值每增加1个单位术后5年内死亡的风险将增加1.72倍,对结局事件的影响和贡献最强,预测价值最高,具有前瞻性。Kaplan-Meier生存曲线提示PI>2.75的高危患者将受益于术后辅助性TACE治疗,明显增加术后总生存时间,并且予以3次以上辅助性TACE治疗对预后的改善最显著,生存获益最明显;而在PI≤2.75的低危患者中,TACE组术后1、3、5年累计生存率虽高于未行TACE组,但总体无统计学差异,造成这种情况的原因可能是这些低危患者可能存在1或2种侵袭性危险因素,手术不易达到根治,而术后TACE治疗可帮助消灭术后残癌灶或癌前病变组织,减少余肝新生肿瘤的几率,提高这类患者的总生存率,因此推荐这些伴有危险因素的低危患者在术后接受1~2次TACE治疗,多次的TACE治疗会加重术后肝脏负担,损害肝功能,使机体免疫受抑制,刺激新生肿瘤细胞生长,得到适得其反的效果;而对于不伴有危险因素的低危患者,推荐定期随访,不进行TACE治疗。
综上所述,本研究团队从临床病理角度探讨影响HCC患者术后5年生存情况的相关危险因素并建立PI模型,为临床HCC术后辅助性TACE治疗提供了借鉴,通过评估HCC患者的PI值可以预测术后辅助性TACE治疗效果,有助于优化辅助性TACE治疗,并且制定出与患者个体化相适宜、易实施的TACE治疗方案。