长链非编码核糖核酸与冠心病的研究进展
——从发病机制到诊断与治疗
杨环莞,刘昱圻,陈韵岱
(解放军总医院第一医学中心心血管内科,北京 100853)
心血管疾病是全球范围造成死亡的最主要原因,包括冠心病、高血压、心律失常、瓣膜性心脏病等。动脉粥样硬化是冠心病的主要病理基础,在动脉粥样硬化基础上,易损斑块破裂和侵蚀继发血栓形成是引起急性心血管事件的主要原因。除了传统的胆固醇学说,最近发表的CANTOS研究[1]进一步为动脉粥样硬化的炎症假说提供了有力的试验证据,提示了全身及局部炎症、免疫活化在斑块易损性中的作用。然而尽管经皮冠状动脉介入(percutaneous coronary intervention,PCI)联合药物治疗不断进展,急性冠状动脉综合征的死亡率仍居高不下,其中缺血再灌注损伤及梗死后心脏重构或发挥重要作用。
长链非编码核糖核酸(long non-coding RNA,lncRNA)是转录本长度超过200 nt的核糖核酸(RNA),几乎无蛋白质编码功能。其大多位于细胞的胞核或胞浆中,在转录及转录后水平调控基因表达[2]。根据其在基因组中的位置,分为正义、反义、双向、基因内及基因间lncRNA[3]。最近的研究表明,lncRNA在动脉粥样硬化、急性心肌梗死、微血管功能障碍、心脏重构及心力衰竭等发生、发展过程中起着重要的调节作用[4-6]。本文将对lncRNA的生物学功能,在心血管疾病发生、发展及诊断和治疗中的作用进行概述。
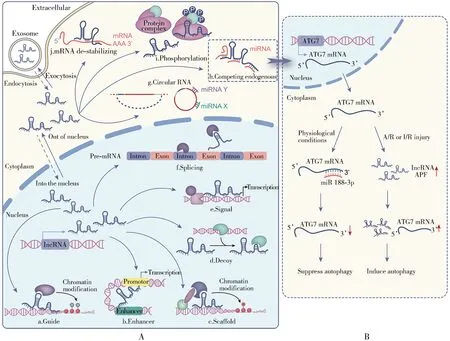
图1 lncRNA的生物学作用模式
1 lncRNA的生物学作用模式
1.1 转录水平调节
定位在胞核中的lncRNA主要在转录水平对基因表达进行调控。lncRNA可作为分子诱饵来诱导特定蛋白(如转录因子),并与之结合,该作用能使其序列下游的转录反应受到阻碍[7];引导型lncRNA通过与DNA或者蛋白质结合,可将特定的复合体引导到特定的染色体位置上,可通过顺式或反式作用调控基因的表达[7];增强子lncRNA转录自增强子区域,可通过顺式作用促进增强子原件与启动子区域结合,从而促进下游的蛋白质编码基因的表达[8];lncRNA还可以作为蛋白质复合物的骨架把表观修饰的酶联合在一起[7],从而调控DNA甲基化、组蛋白修饰或染色质重构,使基因沉默或激活。通过与剪切因子相互作用,影响mRNA前体的剪切,lncRNA可调控靶基因产生不同的转录本,进而被翻译成不同的蛋白质构体。此外,lncRNA还可担任信号分子的角色,在受到特定刺激后,能表现出时间特异性及组织特异性,使其具有作为生物标志物的潜力[7]。
1.2 转录后调节
定位在胞浆中的lncRNA主要在转录后水平影响基因的表达。lncRNA可通过影响蛋白的转运以及磷酸化或去磷酸化影响细胞信号转导,进而影响功能蛋白的表达[9,10]。lncRNA还可通过与信使核糖核酸(messenger RNA, mRNA)结合影响mRNA的稳定性,并以竞争性内源性核糖核酸(competing endogenous RNA, ceRNA)的形式,通过竞争性结合同种微小核糖核酸(microRNA, miRNA) 来调控各自的表达水平,从而影响细胞的功能[11]。详见图1[12]。
2 lncRNA与冠心病
2.1 lncRNA与动脉粥样硬化和急性心肌梗死
动脉粥样硬化是一种复杂的病理生理过程,其最终导致斑块形成及动脉壁的炎症,既与遗传相关,也有环境因素参与。lncRNAs在内皮细胞功能障碍、平滑肌细胞增殖、表型转化及胆固醇代谢中发挥重要作用。其中lncRNA H19被发现与中国人群的冠心病和缺血性卒中相关[13]。最初在人类及啮齿类动物粥样硬化斑块的平滑肌细胞中发现H19重复表达[14],其以分子海绵的形式与miRNA let-7a相互作用进而上调细胞周期蛋白D(cyclin D)的表达,从而促进血管平滑肌细胞的增殖[15]。而最近的研究也表明,lncRNA H19通过抑制STAT3信号通路影响内皮细胞的衰老[16]。此外,Cremer等[17]在小鼠模型与人群中检验了lncRNA MALAT1对动脉粥样硬化的作用。实验发现,ApoE(-/-)MALAT1(-/-)的动脉粥样硬化小鼠模型与对照组相比斑块体积更大,且斑块中CD45+炎症细胞浸润较多;同时发现将MALAT1小鼠的骨髓移植给对照组小鼠后,对照组小鼠的斑块体积增大。体外实验表明,MALAT1小鼠中分离的骨髓细胞与血管内皮细胞的黏附性增加,且表达更多的炎症因子。进一步在人群中检验MALAT1对动脉粥样硬化的作用,发现动脉狭窄较重的人群较狭窄较轻的人群MALAT1表达下调,且有症状人群较无症状人群的MALAT1表达亦下调,随访研究表明MALAT1越低其预后越差。
一项大规模病例对照研究发现lncRNA MIAT与急性心肌梗死相关[18]。该研究发现MIAT基因位点的6个单核苷酸多态性与急性心肌梗死风险增加有关。进一步的体外实验证实,第5号外显子的单核苷酸多态性显著增加MIAT转录[18]。功能实验证实,lncRNA MIAT以ceRNA的形式与 miR-150-5p相互作用,参与内皮生长因子表达的调控及病理性血管生成[19]。
2.2 lncRNA与心脏重构
急性心肌梗死后心脏重构的发生是导致心肌梗死后心力衰竭发生的主要机制,影响患者的长期预后,其中纤维化过程起着重要作用。Piccoli等[20]通过体内及体外实验证实,lncRNA Meg3可通过调节基质金属蛋白酶-2(matrix metalloproteinase-2, MMP-2)促进心肌纤维化,影响心脏舒张功能。Kumarswamy等[4]发现,与心肌梗死后无心脏重构的人群相比,急性心肌梗死后心脏重构人群的血液样本中线粒体lncRNA LIPCAR表达在早期明显下调,而在心肌梗死后1、3、12个月后表达上调。另一独立队列研究进行3年随访后发现,在矫正年龄、性别、缺血病因及糖尿病后, LIPCAR水平升高与心血管死亡率增加显著相关(OR=1.42, 95%CI: 1.02~2.01;P=0.04)。Micheletti等[21]发现,心脏成纤维细胞显著表达lncRNA Wisper在心肌损伤后心脏纤维化过程中发挥重要作用。在心肌梗死小鼠模型及患者中均发现,Wisper表达量与心脏纤维化程度呈显著相关。体外细胞实验发现,Wisper可影响成纤维细胞的增殖、迁移及存活,并且可通过影响T细胞细胞内抗原1(T-cell intracellular antigen 1, TIA1)表达影响成纤维细胞前体的表型,进而影响细胞外胶原的沉积与交联,促进心肌细胞外基质的沉积及心脏重构。
3 lncRNA在冠心病诊断与治疗中的作用
lncRNA在循环中多以外泌体的形式存在,其易被获得且在不同的贮存条件、理化条件及体液中稳定存在,可作为新型生物标志物。然而,仅有少量研究关注循环lncRNA在冠心病诊断中的作用。最近的一项研究表明,lncRNA UCA1可作为急性心肌梗死的新型标志物。与健康对照相比,在急性心肌梗死后12 h,血浆UCA1的水平明显下降,72 h后上升[22]。Zhang等[23]发现,与对照组相比,lncRNA MYHEART在急性心肌梗死人群中表达上升,且其表达量与心肌损伤标志物肌钙蛋白T呈显著正相关。此外,有研究发现lncRNA CoroMarker和lncPPARδ 在冠心病人群中特征性表达上调且验证队列显示具有较好的诊断效能,受试者工作特征曲线下面积分别为0.920和0.727[24,25]。另外,联合不同的lncRNA或lncRNA与传统标志物提高疾病诊断效能也是未来发展的一个方向。
近年来基于lncRNA的药物治疗不断进展。动物实验表明,通过转基因(如lncRNA MHRT)或药物抑制(如lncRNA CHAST),人为干预lncRNA可有效阻止或逆转疾病的进程[26,27]。反义寡核苷酸药物、病毒载体、纳米材料及显微注射等方法的发展也使靶向lncRNA的治疗成为可能。然而,其依然存在以下问题:(1)许多lncRNA在物种间并不具有高度保守性,因此对基于动物水平的机制研究很难顺推于人类;(2)由于目前的研究多在啮齿类动物中完成,在临床转化中面临的问题,如基于载体的靶向治疗在大型哺乳动物中是否有效?特定lncRNA在动物和人体中的作用机制是否一致?靶向的准确性、脱靶率、安全性及潜在的副作用如何?
4 结论与展望
lncRNA的发现使人们对心血管疾病调控机制有了全新的理解,架起了基础研究与临床转化之间的桥梁。目前的研究已证明,lncRNA在动脉粥样硬化、急性心肌梗死、心脏重构等病理过程中发挥重要作用,部分lncRNA更是在疾病诊断中表现出了良好的灵敏度与特异度,有望成为新型生物标志物,实现疾病的早期诊断。纳米材料及显微注射等技术的发展也使未来靶向lncRNA治疗冠心病成为可能。而优化分离纯化方法、标准化流程、提高不同检测平台间的一致性和准确性及消除技术和分析方法的偏倚,是得到可靠性和可重复性高的检测结果的必要前提。在治疗方面,也需要开展更多的基础研究和大型临床试验以进一步验证其安全性和有效性。

